Ti、Na、Mg、C、N、O、Fe等元素的研究一直在进行中,其单质及化合物在诸多领域都有广泛的应用。回答下列问题
(1)钠在火焰上灼烧的黄光是一种___________ (填字母)。
A.吸收光谱 B.发射光谱
钠元素原子核外最外层电子的排布图是___________ ;能量最高的电子有___________ 个,其电子云形状为___________ 。
(2)下列Mg原子的核外电子排布式中,能量最高的是___________ ,能量最低的是___________ (填序号)。
a. b.
b.
c. d.
d.
(3) 所含的化学键类型:
所含的化学键类型:___________ ;属于___________ 分子(填极性或非极性)
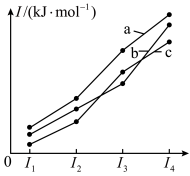
(4)磷及其化合物与人类生产、生活密切相关。如图表示碳、硅、磷元素的四级电离能(失去第四个电子)变化趋势,其中表示磷的曲线是___________ (填标号)。
(1)钠在火焰上灼烧的黄光是一种
A.吸收光谱 B.发射光谱
钠元素原子核外最外层电子的排布图是
(2)下列Mg原子的核外电子排布式中,能量最高的是
a.
 b.
b.
c.
 d.
d.
(3)
 所含的化学键类型:
所含的化学键类型:(4)磷及其化合物与人类生产、生活密切相关。如图表示碳、硅、磷元素的四级电离能(失去第四个电子)变化趋势,其中表示磷的曲线是

更新时间:2024-04-03 22:41:25
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】回答以下关于常见元素及其化合物的问题。
(1)碘元素在元素周期表中位置_____ ,碘基态原子价电子的电子排布式为_____ 。价电子共占据_____ 个轨道。
(2) 是一种与
是一种与 性质相似的气体,在
性质相似的气体,在 中C显
中C显 价,N是
价,N是 价,氮元素显负价的原因
价,氮元素显负价的原因_____ 。该分子中每个原子都达到了8电子稳定结构,写出 的电子式
的电子式_____ 。
(3)请比较氮元素与氧元素的非金属性强弱:N_____ O(填“>”、“<”或“=”),用一个化学方程式说明强弱关系_____ 。
(4)在常压下,甲醇的沸点(65℃)比甲醛的沸点(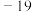 ℃)高。主要原因是
℃)高。主要原因是_____ 。
(5)一定条件下,向 溶液中滴加碱性
溶液中滴加碱性 溶液,溶液中的
溶液,溶液中的 (B元素的化合价为
(B元素的化合价为 )与
)与 反应生成纳米铁粉、
反应生成纳米铁粉、 和
和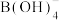 ,其离子方程式为
,其离子方程式为_____ 。
(1)碘元素在元素周期表中位置
(2)
 是一种与
是一种与 性质相似的气体,在
性质相似的气体,在 中C显
中C显 价,N是
价,N是 价,氮元素显负价的原因
价,氮元素显负价的原因 的电子式
的电子式(3)请比较氮元素与氧元素的非金属性强弱:N
(4)在常压下,甲醇的沸点(65℃)比甲醛的沸点(
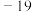 ℃)高。主要原因是
℃)高。主要原因是(5)一定条件下,向
 溶液中滴加碱性
溶液中滴加碱性 溶液,溶液中的
溶液,溶液中的 (B元素的化合价为
(B元素的化合价为 )与
)与 反应生成纳米铁粉、
反应生成纳米铁粉、 和
和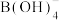 ,其离子方程式为
,其离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】根据所学知识,回答下列问题:
(1)Cu的简化电子排布式为___________ 。Fe2+的价电子轨道表示式为___________ 。
(2)乙炔分子中σ键与π键个数之比为___________ 。
(3)吡啶( )是一种常用的有机溶剂。已知吡啶中所有原子共面,且分子中含有与苯类似的
)是一种常用的有机溶剂。已知吡啶中所有原子共面,且分子中含有与苯类似的 大π键,由此可知,吡啶中N原子的价层孤电子对占据
大π键,由此可知,吡啶中N原子的价层孤电子对占据___________ 轨道。
(4)NH3、PH3、AsH3按照沸点由高到低排序,依次为___________ 。
(5)BF3、SiF4、NF3按照键角由大到小排序,依次为___________ 。
(6)科学家合成了一种新型离子化合物NH5,其所有原子最外层都符合相应稀有气体原子电子层结构,该物质遇水会发生水解,生成一种一元弱碱和一种单质气体。该反应的化学方程式为___________ 。
(1)Cu的简化电子排布式为
(2)乙炔分子中σ键与π键个数之比为
(3)吡啶(
 )是一种常用的有机溶剂。已知吡啶中所有原子共面,且分子中含有与苯类似的
)是一种常用的有机溶剂。已知吡啶中所有原子共面,且分子中含有与苯类似的 大π键,由此可知,吡啶中N原子的价层孤电子对占据
大π键,由此可知,吡啶中N原子的价层孤电子对占据(4)NH3、PH3、AsH3按照沸点由高到低排序,依次为
(5)BF3、SiF4、NF3按照键角由大到小排序,依次为
(6)科学家合成了一种新型离子化合物NH5,其所有原子最外层都符合相应稀有气体原子电子层结构,该物质遇水会发生水解,生成一种一元弱碱和一种单质气体。该反应的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】I.有下列几种物质:①CH4②N2③CO2④CH3CH3⑤C2H4⑥H2O2。请按要求回答下列问题(填写编号):
(1)只有σ键的有____ ,既有σ键又有π键的有____ 。
(2)已知CO和CN-与N2结构相似,CO分子内σ键与π键个数之比为___ 。
II.2019年1月3日,嫦娥四号探测器翩然落月,首次实现人类飞行器在月球背面的软着陆。其所搭载的“玉兔二号”月球车,通过砷化镓(GaAs)太阳能电池提供能量进行工作。回答下列问题:
(3)基态Ga原子价电子排布式为____ ,核外电子占据最高能级的电子云形状为____ ;基态As原子最高能层上有___ 个电子。
(4)镓失去电子的逐级电离能(单位:kJ•mol-1)的数值依次为577、1985、2962、6192,由此可推知镓的主要化合价为____ 和+3,砷的第一电离能比镓___ (填“大”或“小”)。
(5)第四周期元素中,与基态As原子核外未成对电子数目相同的元素符号为____ 。
(6)砷化镓可由(CH3)3Ga和AsH3在700℃制得,其中AsH3分子的VSEPR模型为____ 。
(7)与砷同主族的氮容易形成三键,但砷却难以形成三键的原因是___ 。
(1)只有σ键的有
(2)已知CO和CN-与N2结构相似,CO分子内σ键与π键个数之比为
II.2019年1月3日,嫦娥四号探测器翩然落月,首次实现人类飞行器在月球背面的软着陆。其所搭载的“玉兔二号”月球车,通过砷化镓(GaAs)太阳能电池提供能量进行工作。回答下列问题:
(3)基态Ga原子价电子排布式为
(4)镓失去电子的逐级电离能(单位:kJ•mol-1)的数值依次为577、1985、2962、6192,由此可推知镓的主要化合价为
(5)第四周期元素中,与基态As原子核外未成对电子数目相同的元素符号为
(6)砷化镓可由(CH3)3Ga和AsH3在700℃制得,其中AsH3分子的VSEPR模型为
(7)与砷同主族的氮容易形成三键,但砷却难以形成三键的原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】已知和碳元素同主族的X元素位于周期表中的第1个长周期,短周期元素Y原子的最外层电子数比内层电子总数少3,它们所形成化合物的分子式是XY4。试回答:
(1)X元素的原子基态时电子排布式为__________ ;Y元素原子最外层电子的电子排布图为__________ 。
(2)若X、Y两元素电负性分别为2.1和2.85,则XY4中X与Y之间的化学键为__________ (填“共价键”或“离子键”)。
(3)该化合物的立体构型为__________ ,中心原子的杂化类型为__________ ,分子为__________ (填“极性分子”或“非极性分子”)。
(1)X元素的原子基态时电子排布式为
(2)若X、Y两元素电负性分别为2.1和2.85,则XY4中X与Y之间的化学键为
(3)该化合物的立体构型为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】金属钠及其化合物在人类生产生活中起着重要作用。回答下列问题:
(1)基态Na原子的价层电子轨道表示式为___________ 。
(2)NaCl熔点为800.8℃,工业上采用电解熔融NaCl制备金属Na。电解反应方程式如下: ,加入
,加入 的目的是
的目的是___________ 。
(3) 的电子式为
的电子式为___________ 。在25℃和101kPa时,Na与 反应生成1mol
反应生成1mol 放热510.9kJ,写出该反应的热化学方程式:
放热510.9kJ,写出该反应的热化学方程式:___________ 。 可作供氧剂,写出
可作供氧剂,写出 与CO2反应的化学方程式
与CO2反应的化学方程式___________ 。若有1mol 参加反应则转移电子的物质的量为
参加反应则转移电子的物质的量为___________ mol。
(4)采用空气和Na为原料可直接制备 。空气与熔融金属Na反应前需依次通过
。空气与熔融金属Na反应前需依次通过___________ 、___________ (填序号)。
a.浓硫酸 b.饱和食盐水 c.NaOH溶液 d. 溶液
溶液
(5)向酸性KMnO4溶液中加入 粉末,观察到溶液褪色,发生如下反应: ______MnO
粉末,观察到溶液褪色,发生如下反应: ______MnO +_____H++_____Na2O2=_____Mn2+_____O2↑+_____H2O+_____Na+,配平该离子方程式:
+_____H++_____Na2O2=_____Mn2+_____O2↑+_____H2O+_____Na+,配平该离子方程式:___________ ,该反应说明 具有
具有___________ 性(选填“氧化”,“还原”或“漂白”)。
(6)钠的某氧化物晶胞如下图,图中所示钠离子全部位于晶胞内。由晶胞图判断该氧化物的化学式为___________ 。

(7)天然碱的主要成分为 ,1mol
,1mol 经充分加热得到
经充分加热得到 的质量为
的质量为___________ g。
(1)基态Na原子的价层电子轨道表示式为
(2)NaCl熔点为800.8℃,工业上采用电解熔融NaCl制备金属Na。电解反应方程式如下:
 ,加入
,加入 的目的是
的目的是(3)
 的电子式为
的电子式为 反应生成1mol
反应生成1mol 放热510.9kJ,写出该反应的热化学方程式:
放热510.9kJ,写出该反应的热化学方程式: 可作供氧剂,写出
可作供氧剂,写出 与CO2反应的化学方程式
与CO2反应的化学方程式 参加反应则转移电子的物质的量为
参加反应则转移电子的物质的量为(4)采用空气和Na为原料可直接制备
 。空气与熔融金属Na反应前需依次通过
。空气与熔融金属Na反应前需依次通过a.浓硫酸 b.饱和食盐水 c.NaOH溶液 d.
 溶液
溶液(5)向酸性KMnO4溶液中加入
 粉末,观察到溶液褪色,发生如下反应: ______MnO
粉末,观察到溶液褪色,发生如下反应: ______MnO +_____H++_____Na2O2=_____Mn2+_____O2↑+_____H2O+_____Na+,配平该离子方程式:
+_____H++_____Na2O2=_____Mn2+_____O2↑+_____H2O+_____Na+,配平该离子方程式: 具有
具有(6)钠的某氧化物晶胞如下图,图中所示钠离子全部位于晶胞内。由晶胞图判断该氧化物的化学式为

(7)天然碱的主要成分为
 ,1mol
,1mol 经充分加热得到
经充分加热得到 的质量为
的质量为
您最近一年使用:0次
【推荐1】回答下列问题
(1)①写出小苏打的化学式___________ ;
②写出Fe2+的价电子排布式___________ 。
(2)实验室用软锰矿和浓盐酸制氯气,写出该反应的化学方程式___________ 。
(3)在常温下,0.1mol/LCH3COONa溶液的pH=9,则溶液中由水电离出来的c(OH-)=___________
(4)火箭发射可以用肼(N2H4,液态)作燃料,NO2作氧化剂,两者反应生成N2和水蒸气。
已知:N2(g)+2O2(g)=2NO2(g) ΔH1=+66.4kJ/mol
N2H4(l)+O2(g)=N2(g)+2H2O(g) ΔH2=-534kJ/mol
请写出N2H4(l)与NO2反应的热化学方程式___________
(5)下表列出了某短周期元素R的各级电离能数据(用I1、I2……表示)。
关于元素R的下列推断中,正确的是___________ (用相应的编号填写)
①R元素基态原子的电子排布式为1s22s2
②R元素位于元素周期表中第ⅡA族
③R元素的最高正化合价为+2价
④R元素的第一电离能高于同周期相邻元素的第一电离能
(1)①写出小苏打的化学式
②写出Fe2+的价电子排布式
(2)实验室用软锰矿和浓盐酸制氯气,写出该反应的化学方程式
(3)在常温下,0.1mol/LCH3COONa溶液的pH=9,则溶液中由水电离出来的c(OH-)=
(4)火箭发射可以用肼(N2H4,液态)作燃料,NO2作氧化剂,两者反应生成N2和水蒸气。
已知:N2(g)+2O2(g)=2NO2(g) ΔH1=+66.4kJ/mol
N2H4(l)+O2(g)=N2(g)+2H2O(g) ΔH2=-534kJ/mol
请写出N2H4(l)与NO2反应的热化学方程式
(5)下表列出了某短周期元素R的各级电离能数据(用I1、I2……表示)。
| 元素 | 电离能/(kJ·mol-1) | |||||
| I1 | I2 | I3 | I4 | I5 | …… | |
| R | 740 | 1500 | 7700 | 10500 | 13630 | …… |
①R元素基态原子的电子排布式为1s22s2
②R元素位于元素周期表中第ⅡA族
③R元素的最高正化合价为+2价
④R元素的第一电离能高于同周期相邻元素的第一电离能
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】试用原子结构的知识解释下列实验事实。
(1)在第2周期元素中,氖的第一电离能最大。_______
(2)磷的第一电离能比硫的第一电离能大。_______
(3)在化学反应中,镁原子通常失去两个电子,形成镁离子( )。
)。_______
(4) 是离子化合物,
是离子化合物, 是共价化合物。
是共价化合物。_______
(1)在第2周期元素中,氖的第一电离能最大。
(2)磷的第一电离能比硫的第一电离能大。
(3)在化学反应中,镁原子通常失去两个电子,形成镁离子(
 )。
)。(4)
 是离子化合物,
是离子化合物, 是共价化合物。
是共价化合物。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】以铁、硫酸、柠檬酸、双氧水、氨水等为原料可制备柠檬酸铁铵【(NH4)3Fe(C6H5O7)2】。
(1)Fe2+基态核外电子排布式为___ ;NO 的空间构型为
的空间构型为___ (用文字描述)。
(2)NH3分子中氮原子的轨道杂化类型是___ ;C、N、O元素的第一电离能由大到小的顺序为___ 。
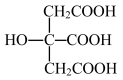
(3)柠檬酸的结构简式见图。1mol柠檬酸分子中碳原子与氧原子形成的σ键的数目为=__ mol。
(4)利用键能数据计算反应的ΔH(请写出解题过程):N2(g)+3H2(g)=2NH3(g)。___
(1)Fe2+基态核外电子排布式为
 的空间构型为
的空间构型为(2)NH3分子中氮原子的轨道杂化类型是
(3)柠檬酸的结构简式见图。1mol柠檬酸分子中碳原子与氧原子形成的σ键的数目为=

(4)利用键能数据计算反应的ΔH(请写出解题过程):N2(g)+3H2(g)=2NH3(g)。
| 化学键 | H—H | N—H | N≡N |
| 键能/(kJ·mol-1) | 436 | 393 | 946 |
您最近一年使用:0次



