下列事实中,不能比较氢硫酸与亚硫酸的酸性强弱的是
| A.氢硫酸不能与碳酸氢钠反应,而亚硫酸可以与碳酸氢钠反应生成二氧化碳 |
| B.氢硫酸的导电能力低于相同浓度的亚硫酸 |
C. 的氢硫酸和亚硫酸的 的氢硫酸和亚硫酸的 分别为4.5和 分别为4.5和 |
| D.氢硫酸与亚硫酸混合时有黄色沉淀产生 |
更新时间:2024-03-24 06:26:51
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】向酸化的Fe(NO3)3溶液中逐渐通入H2S气体,可能发生反应的离子方程式正确的是( )
A.3S2-+2NO +8H+=2NO+3S↓+4H2O +8H+=2NO+3S↓+4H2O |
B.Fe3++3NO +5H2S+2H+=3NO+5S↓+Fe2++6H2O +5H2S+2H+=3NO+5S↓+Fe2++6H2O |
C.Fe3++7NO +10H2S+8H+=7NO+10S+Fe2++14H2O +10H2S+8H+=7NO+10S+Fe2++14H2O |
D.S2-+2NO +4H+=2NO2↑+S↓+2H2O +4H+=2NO2↑+S↓+2H2O |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列说法正确的是
| A.根据反应5Fe2++MnO4-+8H+=5Fe3++Mn2++4H2O可知:用酸性KMnO4溶液可检验绿矾(FeSO4·7H2O)是否变质 |
| B.根据反应H3PO3+2NaOH(足量)===Na2HPO3+2H2O可知:H3PO3属于三元酸 |
| C.根据反应3Fe+8HNO3===3Fe(NO3)2+2NO↑+4H2O可知:反应中HNO3表现酸性和氧化性 |
| D.根据反应CuSO4+H2S===CuS↓+H2SO4可知:H2S的酸性比H2SO4强 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列有关说法正确的是
| A.复分解型离子反应的实质是离子间重新组合使某些离子的浓度或数目减少 |
| B.电解质与非电解质的本质区别在于是否在溶于水后能否导电 |
| C.CO2 、NH3的水溶液均能导电,所以CO2 、NH3是电解质 |
| D.H++OH-=H2O可以表示所有强酸与强碱反应的离子方程式 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列说法正确的是( )
①SO2的水溶液能导电,故SO2是电解质;②将pH=5的硫酸溶液稀释1000倍后,溶液中的SO42-与H+浓度的比值约为1:20; ③在0.10mol·L-1CH3COOH溶液中加水稀释或加入少量CH3COONa晶体,溶液pH均增大;④将稀氨水逐滴加入稀硫酸中,当溶液的pH=7时,c(NH4+)>c(SO42-);⑤ 体积相同、pH相同的盐酸和醋酸溶液分别与锌粒反应,醋酸生成的氢气较多。
①SO2的水溶液能导电,故SO2是电解质;②将pH=5的硫酸溶液稀释1000倍后,溶液中的SO42-与H+浓度的比值约为1:20; ③在0.10mol·L-1CH3COOH溶液中加水稀释或加入少量CH3COONa晶体,溶液pH均增大;④将稀氨水逐滴加入稀硫酸中,当溶液的pH=7时,c(NH4+)>c(SO42-);⑤ 体积相同、pH相同的盐酸和醋酸溶液分别与锌粒反应,醋酸生成的氢气较多。
| A.①②③④⑤ | B.②③④ | C.③④⑤ | D.②③④⑤ |
您最近半年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】有一包固体粉末,由NaOH、Na2SO3、MgCl2、CaCO3、Ba( NO3)2、FeSO4中的几种组成,取少量样品进行如下实验:
①将样品加入水中,得到白色不溶物a和无色溶液
②向①中加入足量稀盐酸,产生气体,仍存在不溶物
该固体粉末一定含有的是
①将样品加入水中,得到白色不溶物a和无色溶液
②向①中加入足量稀盐酸,产生气体,仍存在不溶物
该固体粉末一定含有的是
| A.CaCO3、Ba( NO3)2 | B.CaCO3、Na2SO3 |
| C.Na2SO3、Ba( NO3)2 | D.CaCO3、Na2SO3、Ba( NO3)2 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】实验I和实验II中,均有气体产生。
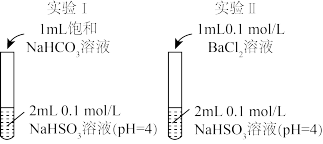
下列分析不正确的是

下列分析不正确的是
A.NaHSO3溶液中:c(SO )>c(H2SO3) )>c(H2SO3) | B.I中有CO2生成 |
| C.II中产生白色沉淀 | D.I和II中溶液的pH均增大 |
您最近半年使用:0次
单选题
|
适中
(0.65)
【推荐3】宏观辨识与微观探析是化学学科核心素养之一。下列反应的离子方程式书写正确的是
A.将NH3通入稀硝酸中: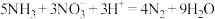 |
B.向FeCl3溶液中加入KSCN溶液: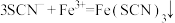 |
C.将Na2SO3溶液与酸性高锰酸钾溶液混合: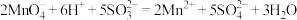 |
D.Mg(OH)2溶于NH4Cl溶液中: |
您最近半年使用:0次


 BaS+4CO↑
BaS+4CO↑


