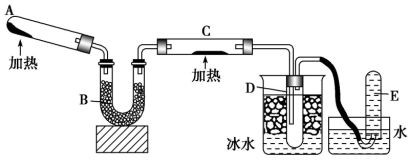
已知氨气具有还原性,可以与灼热的氧化铜反应生成两种单质和水,用下图中的装置可以实现该反应.
回答下列问题:
(1)A中加入的物质是两种固体,A中反应的化学方程式为____________ 。
(2)仪器B可以用仪器_________ 代替(填名称).B中加入的物质是_______ (单选,填标号)。
a.碱石灰 b.无水氯化钙 c.无水硫酸铜 d.五氧化二磷
(3)实验时在C中观察到得现象是___________ ,发生反应的化学方程式为______________________ 。
(4)D中收集到的物质是_________ (选填“液氨”或“氨水”);将酚酞溶液滴到该物质中,出现的现象是_________ ,用电离方程式解释出现该现象的原因__________________ 。
(5)金属镁在E中收集到的气体中燃烧的化学方程式为_____________ ,产物名称为__________ 。

回答下列问题:
(1)A中加入的物质是两种固体,A中反应的化学方程式为
(2)仪器B可以用仪器
a.碱石灰 b.无水氯化钙 c.无水硫酸铜 d.五氧化二磷
(3)实验时在C中观察到得现象是
(4)D中收集到的物质是
(5)金属镁在E中收集到的气体中燃烧的化学方程式为
更新时间:2024/04/03 19:42:55
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】碱式氯化铜 为绿色或墨绿色的结晶性粉末,难溶于水,溶于稀酸和氨水,在空气中十分稳定。
为绿色或墨绿色的结晶性粉末,难溶于水,溶于稀酸和氨水,在空气中十分稳定。
Ⅰ.模拟制备碱式氯化铜。
向 溶液中通入
溶液中通入 ,同时滴加稀盐酸,调节
,同时滴加稀盐酸,调节 至5.0~5.5,控制反应温度于70-80℃,实验装置如题图所示(部分夹持装置已省略)。
至5.0~5.5,控制反应温度于70-80℃,实验装置如题图所示(部分夹持装置已省略)。________ 。
(2)实验室利用装置B制备 ,圆底烧瓶中盛放的固体药品可能是
,圆底烧瓶中盛放的固体药品可能是_______ (填名称)。
(3)反应结束后,将装置A中反应容器内的混合物过滤,经提纯得产品无水碱式氯化铜;从滤液中还可以获得的副产品是________ (填化学式)。
Ⅱ.无水碱式氯化铜组成的测定。
(4)铜的测定。
称取产品6.435g,加稀硝酸溶解,并加水定容至250mL,得到待测液。取100mL待测液,加入足量的氢氧化钠,经过滤,洗涤,低温烘干,称量得到的蓝色固体质量为2.352g。则称取的样品中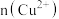 为
为________ mol。
(5)采用沉淀滴定法测定氯。
请补充完整的测定氯的实验过程:准确量取25.00mL待测液于锥形瓶中,①________ ,记录消耗 溶液的体积
溶液的体积 ,②
,②________ ,记录滴加 标准溶液体积
标准溶液体积 ,重复上述实验2~3次。已知:①
,重复上述实验2~3次。已知:① (白色沉淀),当
(白色沉淀),当 与
与 共存时,
共存时, 与
与 优先反应;②聚乙烯醇可以覆盖在
优先反应;②聚乙烯醇可以覆盖在 表面,阻止
表面,阻止 与
与 的转化。[须使用试剂:0.2molL
的转化。[须使用试剂:0.2molL 溶液、0.010mol/L
溶液、0.010mol/L 标准溶液、
标准溶液、 溶液、聚乙烯醇]
溶液、聚乙烯醇]
 为绿色或墨绿色的结晶性粉末,难溶于水,溶于稀酸和氨水,在空气中十分稳定。
为绿色或墨绿色的结晶性粉末,难溶于水,溶于稀酸和氨水,在空气中十分稳定。Ⅰ.模拟制备碱式氯化铜。
向
 溶液中通入
溶液中通入 ,同时滴加稀盐酸,调节
,同时滴加稀盐酸,调节 至5.0~5.5,控制反应温度于70-80℃,实验装置如题图所示(部分夹持装置已省略)。
至5.0~5.5,控制反应温度于70-80℃,实验装置如题图所示(部分夹持装置已省略)。
(2)实验室利用装置B制备
 ,圆底烧瓶中盛放的固体药品可能是
,圆底烧瓶中盛放的固体药品可能是(3)反应结束后,将装置A中反应容器内的混合物过滤,经提纯得产品无水碱式氯化铜;从滤液中还可以获得的副产品是
Ⅱ.无水碱式氯化铜组成的测定。
(4)铜的测定。
称取产品6.435g,加稀硝酸溶解,并加水定容至250mL,得到待测液。取100mL待测液,加入足量的氢氧化钠,经过滤,洗涤,低温烘干,称量得到的蓝色固体质量为2.352g。则称取的样品中
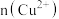 为
为(5)采用沉淀滴定法测定氯。
请补充完整的测定氯的实验过程:准确量取25.00mL待测液于锥形瓶中,①
 溶液的体积
溶液的体积 ,②
,② 标准溶液体积
标准溶液体积 ,重复上述实验2~3次。已知:①
,重复上述实验2~3次。已知:① (白色沉淀),当
(白色沉淀),当 与
与 共存时,
共存时, 与
与 优先反应;②聚乙烯醇可以覆盖在
优先反应;②聚乙烯醇可以覆盖在 表面,阻止
表面,阻止 与
与 的转化。[须使用试剂:0.2molL
的转化。[须使用试剂:0.2molL 溶液、0.010mol/L
溶液、0.010mol/L 标准溶液、
标准溶液、 溶液、聚乙烯醇]
溶液、聚乙烯醇]
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
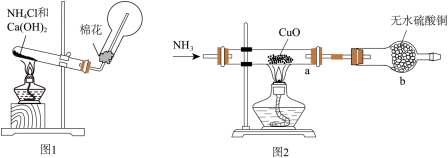
【推荐2】人类的农业生产离不开氮肥,几乎所有的氮肥都以氨为原料,某化学兴趣小组利用图1装置制备氨气,图2装置探究其相关性质。
(1)图1装置中生成 的化学方程式为
的化学方程式为___________ 。检验圆底烧瓶中已收集满氨气的方法是___________ 。
II.探究氨气与氧化铜的反应,验证氨气的性质及部分反应产物。
(2)无水硫酸铜的作用是___________ ;有同学认为需要在无水硫酸铜的后面再接一个装有 固体的球形干燥管,这样做的目的是
固体的球形干燥管,这样做的目的是___________ 。
(3)该实验缺少尾气吸收装置。如图中能用来吸收尾气的装置是___________ (填字母)。 粉末变红,b中无水硫酸铜变蓝,并收集到一种单质气体。则该反应的化学方程式为
粉末变红,b中无水硫酸铜变蓝,并收集到一种单质气体。则该反应的化学方程式为___________ ,证明氨气具有___________ (填“氧化”或“还原”)性。
(1)图1装置中生成
 的化学方程式为
的化学方程式为II.探究氨气与氧化铜的反应,验证氨气的性质及部分反应产物。
(2)无水硫酸铜的作用是
 固体的球形干燥管,这样做的目的是
固体的球形干燥管,这样做的目的是(3)该实验缺少尾气吸收装置。如图中能用来吸收尾气的装置是
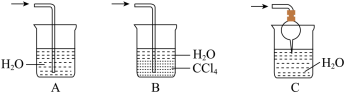
 粉末变红,b中无水硫酸铜变蓝,并收集到一种单质气体。则该反应的化学方程式为
粉末变红,b中无水硫酸铜变蓝,并收集到一种单质气体。则该反应的化学方程式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】人类的农业生产离不开氨肥,几乎所有的氮肥都以氨为原料生产,某化学兴趣小组利用如图装置制备氨气并探究相关性质。

(1)实验装置A中制备 的化学方程式为
的化学方程式为___________ 。
(2)B装置中盛放的试剂可能是___________ ,装置D中盛放无水硫酸铜仪器的名称是___________ 。
(3)实验开始时先点燃的酒精灯为___________ (填“A”或“C”),目的是___________ ,该反应装置的缺陷是___________ 。
(4)实验发现C中固体完全变红,D中无水硫酸铜变蓝,还产生一种单质气体。实验后取C中红色固体于试管中,加入过量稀硫酸。
已知:Cu和 均为红色固体,
均为红色固体, 。
。
①若溶液不变蓝,C中发生的总反应方程式为:___________ 。
②若溶液变蓝,证明红色固体中___________  (填“有”或“没有”),经称量反应前C中
(填“有”或“没有”),经称量反应前C中 质量为
质量为 ,反应后C中红色固体质量为
,反应后C中红色固体质量为 ,则红色固体中金属铜的质量分数为
,则红色固体中金属铜的质量分数为___________ %(保留小数点后两位)。

(1)实验装置A中制备
 的化学方程式为
的化学方程式为(2)B装置中盛放的试剂可能是
(3)实验开始时先点燃的酒精灯为
(4)实验发现C中固体完全变红,D中无水硫酸铜变蓝,还产生一种单质气体。实验后取C中红色固体于试管中,加入过量稀硫酸。
已知:Cu和
 均为红色固体,
均为红色固体, 。
。①若溶液不变蓝,C中发生的总反应方程式为:
②若溶液变蓝,证明红色固体中
 (填“有”或“没有”),经称量反应前C中
(填“有”或“没有”),经称量反应前C中 质量为
质量为 ,反应后C中红色固体质量为
,反应后C中红色固体质量为 ,则红色固体中金属铜的质量分数为
,则红色固体中金属铜的质量分数为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】某校兴趣小组设计实验探究SO2与新制Cu(OH)2悬浊液反应的产物。按图连接好装置(夹持装置省略),打开磁搅拌器,先往20 mL 1.0 mol·L-1的CuCl2 溶液中加入20 mL 2.0 mol·L-1的NaOH溶液,再通入一定量SO2,三颈烧瓶中生成大量白色沉淀X。
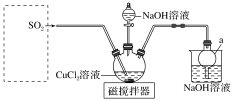
回答下列问题:
(1)以亚硫酸钠和浓硫酸为原料制取SO2,虚框中应选用_______ (填“A”或“B”)装置,写出该装置制备SO2的化学方程式_______ 。实验室制备SO2一般选择70%的浓硫酸,不选择98.3%的浓硫酸的理由是_______ 。

(2)仪器a的名称为_______ ,烧杯中发生反应的离子方程式为_______ 。
(3)据SO2是酸性氧化物,推测X可能为_______ 。取少量X加入稀硫酸进行验证,观察到_______ ,说明该推测错误。
(4)根据实验验证X为CuCl,写出生成X的离子方程式为_____ 。说明SO2具有_____ 。

回答下列问题:
(1)以亚硫酸钠和浓硫酸为原料制取SO2,虚框中应选用

(2)仪器a的名称为
(3)据SO2是酸性氧化物,推测X可能为
(4)根据实验验证X为CuCl,写出生成X的离子方程式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】化学兴趣小组的同学们设计了如图装置来验证乙醇催化氧化的产物(加热仪器、夹持装置已略去)。
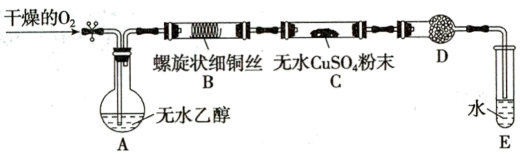
已知:乙醇的沸点为78℃,易溶于水;乙醛的沸点为20.8℃,易溶于水。
(1)实验时上述装置需要加热,其中应该先加热的是______ (填标号),为使装置A中的乙醇成为稳定的蒸气,适宜的加热方法是______ 。
(2)实验开始后,装置B中能观察到的现象是_______ ;装置C中无水硫酸铜的作用是______ ,观察到的实验现象为______ 。
(3)乙醇催化氧化反应的化学方程式是_____ 。
(4)装置D中的药品是______ (填名称),其作用是______ 。
(5)装置E的作用是_______ 。

已知:乙醇的沸点为78℃,易溶于水;乙醛的沸点为20.8℃,易溶于水。
(1)实验时上述装置需要加热,其中应该先加热的是
(2)实验开始后,装置B中能观察到的现象是
(3)乙醇催化氧化反应的化学方程式是
(4)装置D中的药品是
(5)装置E的作用是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】某学习小组为探究 与
与 的酸性强弱开展下列实验,所用装置如图所示。回答下列问题:
的酸性强弱开展下列实验,所用装置如图所示。回答下列问题:
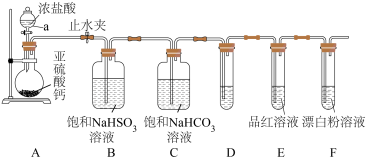
(1)仪器 的名称为
的名称为_____ 。
(2)装置 的作用是
的作用是_____ 。
(3)装置D中盛放的试剂是_____ (填“酸性 溶液”“
溶液”“ 溶液”或“
溶液”或“ 溶液”),该装置的作用是
溶液”),该装置的作用是_____ ,发生反应的离子方程式为_____ 。
(4)通过装置E、F中的现象:_____ 可证明 的酸性强于
的酸性强于 ,用
,用 试纸测定等浓度的
试纸测定等浓度的 溶液和
溶液和 溶液的
溶液的 ,
,_____ (填“能”或“不能”)判断 与
与 的酸性强弱。
的酸性强弱。
(5)由石灰乳与 反应制备漂白粉,发生反应的化学方程式为
反应制备漂白粉,发生反应的化学方程式为_____ ,若标准状况下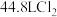 制得了
制得了 漂白粉,则漂白粉的产率为
漂白粉,则漂白粉的产率为_____  (保留两位有效数字)。
(保留两位有效数字)。
 与
与 的酸性强弱开展下列实验,所用装置如图所示。回答下列问题:
的酸性强弱开展下列实验,所用装置如图所示。回答下列问题:
(1)仪器
 的名称为
的名称为(2)装置
 的作用是
的作用是(3)装置D中盛放的试剂是
 溶液”“
溶液”“ 溶液”或“
溶液”或“ 溶液”),该装置的作用是
溶液”),该装置的作用是(4)通过装置E、F中的现象:
 的酸性强于
的酸性强于 ,用
,用 试纸测定等浓度的
试纸测定等浓度的 溶液和
溶液和 溶液的
溶液的 ,
, 与
与 的酸性强弱。
的酸性强弱。(5)由石灰乳与
 反应制备漂白粉,发生反应的化学方程式为
反应制备漂白粉,发生反应的化学方程式为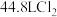 制得了
制得了 漂白粉,则漂白粉的产率为
漂白粉,则漂白粉的产率为 (保留两位有效数字)。
(保留两位有效数字)。
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】某化学兴趣小组以海带为原料获得少量碘水,并以 为萃取剂将碘从碘水中提取出来,具体过程如下:
为萃取剂将碘从碘水中提取出来,具体过程如下:

请回答:
(1)步骤③用到的玻璃仪器有烧杯、玻璃棒和________ 。
(2)步骤④可用酸化的 溶液氧化碘化钾,写出该反应的离子方程式
溶液氧化碘化钾,写出该反应的离子方程式________ 。
(3)步骤⑤中萃取剂也可用苯,理由是________ 。
 为萃取剂将碘从碘水中提取出来,具体过程如下:
为萃取剂将碘从碘水中提取出来,具体过程如下:
请回答:
(1)步骤③用到的玻璃仪器有烧杯、玻璃棒和
(2)步骤④可用酸化的
 溶液氧化碘化钾,写出该反应的离子方程式
溶液氧化碘化钾,写出该反应的离子方程式(3)步骤⑤中萃取剂也可用苯,理由是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐2】硒(Se)、碲(Te)的单质和化合物在化工生产等方面具有重要应用。
(1)下列关于硒、碲及其化合物的叙述不正确的是_______ 。
A.Te 位于周期表的第五周期 Ⅵ A 族
B.Se 的氧化物通常有SeO2和SeO3
C.H2TeO4的酸性比H2SO4的酸性强
D.热稳定性H2Se比H2S弱,但比HBr强
(2)25℃ 时,硒酸的电离H2SeO4=H+ +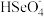 ;
;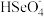 ⇌H+ +
⇌H+ + Ka2 = 1×10-3,则0.1 mol·L-1NaHSeO4溶液的pH约为
Ka2 = 1×10-3,则0.1 mol·L-1NaHSeO4溶液的pH约为________ ;NaHSeO4溶液中的物料守恒表达式为____________ 。
(3)TeO2微溶于水,易溶于较浓的强酸和强碱。工业上常用铜阳极泥(主要含TeO2,还含有少量Ag、Au)为原料制备单质碲,其工艺流程如图:

①铜阳极泥在碱浸前需烘干、研成粉末,目的是____________ ;
②“碱浸”时TeO2发生反应的化学方程式为_____________ ;
③“沉碲”时控制溶液的 pH 为 4.5~5.0,生成TeO2沉淀,酸性不能过强的原因是__________ ;
④“还原”得到固态碲为粗碲,对粗碲进行洗涤,判断洗涤干净的实验操作和现象是________ 。
(1)下列关于硒、碲及其化合物的叙述不正确的是
A.Te 位于周期表的第五周期 Ⅵ A 族
B.Se 的氧化物通常有SeO2和SeO3
C.H2TeO4的酸性比H2SO4的酸性强
D.热稳定性H2Se比H2S弱,但比HBr强
(2)25℃ 时,硒酸的电离H2SeO4=H+ +
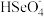 ;
;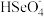 ⇌H+ +
⇌H+ + Ka2 = 1×10-3,则0.1 mol·L-1NaHSeO4溶液的pH约为
Ka2 = 1×10-3,则0.1 mol·L-1NaHSeO4溶液的pH约为(3)TeO2微溶于水,易溶于较浓的强酸和强碱。工业上常用铜阳极泥(主要含TeO2,还含有少量Ag、Au)为原料制备单质碲,其工艺流程如图:

①铜阳极泥在碱浸前需烘干、研成粉末,目的是
②“碱浸”时TeO2发生反应的化学方程式为
③“沉碲”时控制溶液的 pH 为 4.5~5.0,生成TeO2沉淀,酸性不能过强的原因是
④“还原”得到固态碲为粗碲,对粗碲进行洗涤,判断洗涤干净的实验操作和现象是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐3】由钛精矿(主要成分为TiO2)制备钛(Ti)的工艺流程示意图如下:

回答下列问题:
(1)与Ti元素未成对电子数相同的同周期主族元素还有_______ (填写元素名称);基态O原子的核外电子排布图是_______ 。
(2)钛精矿、焦炭和氯气高温反应制取粗TiCl4过程中产生CO和CO2,若产生CO和CO2物质的量之比为2:1,则该步反应的化学方程式为_______ 。
(3)实验室进行蒸馏提纯时所用的玻璃仪器有蒸馏烧瓶、酒精灯、牛角管、锥形瓶、_______ 、_______ 。
(4)用金属镁还原TiCl4过程中需要保护气,下列气体可作为保护气的是_______ 。
a.Cl2 b.N2 c.Ar d.CO2
(5)有同学认为用金属镁制取钛生产成本较高,若采用电解TiCl4的方法制取金属钛可降低生产成本。你是否认同该同学的设想?_______ (填“是”或“否”)。你的理由是_______ 。

回答下列问题:
(1)与Ti元素未成对电子数相同的同周期主族元素还有
(2)钛精矿、焦炭和氯气高温反应制取粗TiCl4过程中产生CO和CO2,若产生CO和CO2物质的量之比为2:1,则该步反应的化学方程式为
(3)实验室进行蒸馏提纯时所用的玻璃仪器有蒸馏烧瓶、酒精灯、牛角管、锥形瓶、
(4)用金属镁还原TiCl4过程中需要保护气,下列气体可作为保护气的是
a.Cl2 b.N2 c.Ar d.CO2
(5)有同学认为用金属镁制取钛生产成本较高,若采用电解TiCl4的方法制取金属钛可降低生产成本。你是否认同该同学的设想?
您最近一年使用:0次



