钴(Co)在化学上称为铁系元素,其化合物在生产生活中应用广泛。以甲醇为溶剂,Co2+可与色胺酮分子配位结合形成对DNA具有切割作用的色胺酮钴配合物(合成过程如图所示),下列说法错误的是
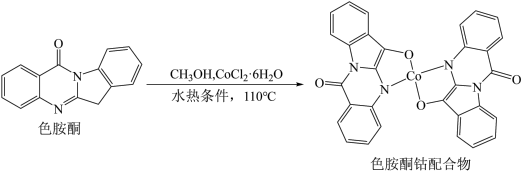

| A.色胺酮分子中所含元素第一电离能由大到小的顺序为N>O>H >C |
| B.色胺酮分子中N原子杂化类型不同 |
| C.色胺酮钴配合物中钴的配位数为4 |
| D.X射线衍射分析显示色胺酮钴配合物晶胞中还含有一个CH3OH分子,CH3OH是通过配位键作用与色胺酮钴配合物相结合 |
更新时间:2024-03-25 15:48:51
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】CO与 在催化剂作用下可生成
在催化剂作用下可生成 与
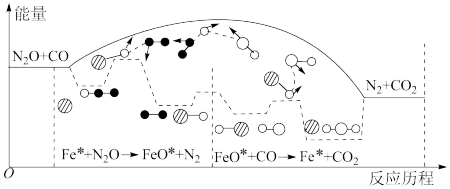
与 减少环境污染。其中在铁催化剂表面进行的反应可分为两步反应,其相对能量与反应历程的关系如下图所示,下列说法错误的是
减少环境污染。其中在铁催化剂表面进行的反应可分为两步反应,其相对能量与反应历程的关系如下图所示,下列说法错误的是
 在催化剂作用下可生成
在催化剂作用下可生成 与
与 减少环境污染。其中在铁催化剂表面进行的反应可分为两步反应,其相对能量与反应历程的关系如下图所示,下列说法错误的是
减少环境污染。其中在铁催化剂表面进行的反应可分为两步反应,其相对能量与反应历程的关系如下图所示,下列说法错误的是
A. 分子的中心原子N和 分子的中心原子N和 分子的中心原子C的杂化类型不相同 分子的中心原子C的杂化类型不相同 |
| B.基态原子的第一电离能:N>O>C>Fe |
C.该过程的决速步反应为 |
| D.Fe*为反应的催化剂,FeO*为反应的中间产物 |
您最近半年使用:0次
单选题
|
适中
(0.65)
【推荐2】EDTA(乙二胺四乙酸)结构简式如图所示,关于化合物 的说法正确的是
的说法正确的是
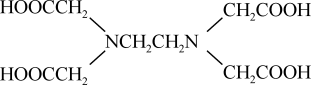
 的说法正确的是
的说法正确的是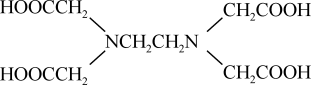
| A.1 mol EDTA中含4mol π键 |
B.EDTA中碳原子的杂化轨道类型为 、 、 、 、 |
C.EDTA组成元素的第一电离能顺序为 |
D. 中所含的化学键有离子键、共价键、配位键和氢键 中所含的化学键有离子键、共价键、配位键和氢键 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】固体A的化学式为NH5 , 它的所有原子的电子层结构都跟该原子同周期的稀有气体原子一样,NH5能跟水反应,化学方程式为:NH5+H2O=NH3•H2O+H2↑.则下列说法中,不正确的是( )
| A.NH5跟水的反应中,H2既是氧化产物又是还原产物 |
| B.NH5中既有共价键,又有离子键,属于离子化合物 |
| C.NH5跟水的反应是氧化还原反应 |
| D.1molNH5中有5NA个N﹣H键(NA为阿伏伽德罗常数的值) |
您最近半年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】尿素是一种易溶于水的氮肥,分子的结构简式如图,下列有关尿素分子的说法错误的是


| A.该分子是一种极性分子 |
B.该分子中的N原子采用 杂化 杂化 |
C.该分子中 键和 键和 键的个数比为 键的个数比为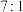 |
| D.该分子中的所有原子都在同一平面上 |
您最近半年使用:0次
单选题
|
适中
(0.65)
【推荐1】设 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是A.30g甲醛分子其中心原子的价层电子对数为 |
B.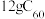 和12g金刚石均含有 和12g金刚石均含有 个碳原子 个碳原子 |
C.标准状况下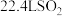 与 与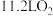 充分反应后的分子总数为 充分反应后的分子总数为 |
D.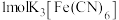 中含有 中含有 键数目为 键数目为 |
您最近半年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】反应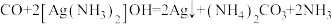 可用于检验微量CO的存在。下列说法正确的是
可用于检验微量CO的存在。下列说法正确的是
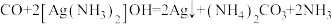 可用于检验微量CO的存在。下列说法正确的是
可用于检验微量CO的存在。下列说法正确的是| A.NH3是非极性分子 | B. 的空间构型为三角锥形 的空间构型为三角锥形 |
C. 中存在 中存在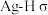 键 键 | D.电负性大小: |
您最近半年使用:0次
【推荐3】已知[Co(H2O)6]2+呈粉红色,[CoCl4]2-呈蓝色,[ZnCl4]2-为无色。现将CoCl2溶于水,加入浓盐酸后,溶液由粉红色变为蓝色,存在以下平衡:[Co(H2O)6]2++4Cl- [CoCl4]2-+6H2O ΔH,用该溶液做实验,溶液的颜色变化如下:
[CoCl4]2-+6H2O ΔH,用该溶液做实验,溶液的颜色变化如下:

以下结论和解释错误的是
 [CoCl4]2-+6H2O ΔH,用该溶液做实验,溶液的颜色变化如下:
[CoCl4]2-+6H2O ΔH,用该溶液做实验,溶液的颜色变化如下:
以下结论和解释错误的是
| A.由实验①可推知ΔH>0,实验②平衡逆向移动 |
| B.等物质的量的[Co(H2O)6]2+和[CoCl4]2-中σ键数之比为9:2 |
| C.由实验③可知配离子的稳定性:[ZnCl4]2->[CoCl4]2- |
| D.以上离子涉及的元素的电负性顺序为 Zn<Co<H<Cl<O |
您最近半年使用:0次

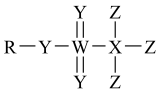
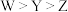
 元素形成的单质晶体中,原子的杂化类型均相同
元素形成的单质晶体中,原子的杂化类型均相同


