2022年北京冬季奥运会场馆建设使用了大量不锈钢材质,不锈钢属于铁碳合金,常含铬(Cr)、镍(Ni)等元素。回答下列问题:
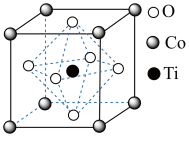
(1)某钛酸盐晶体结构模型如图所示。该晶体的化学式是_______ ,在晶体中1个Co原子周围距离最近的O原子数目为_______ 个,钛离子配位数为_______ 。
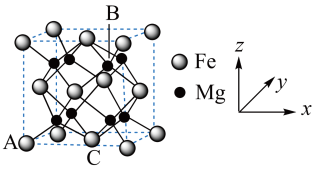
(2)铁合金用途广泛,某种铁镁合金储氢效率很高,其晶胞如图所示。晶体中每个镁原子周围距离最近的铁原子有_______ 个,该铁镁合金中原子个数比Fe:Mg=_______ ;原子坐标参数可以表示晶胞内部各原子的相对位置,其中原子坐标参数A为 ,C为
,C为 ,B点坐标参数为
,B点坐标参数为_______ 。
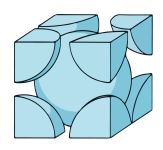
(3)金属铬晶胞如图,已知其密度为a g∙cm-3,阿伏加德罗常数的值为NA,则晶体中铬原子的半径为_______ cm(用含NA的表达式表示)。
(1)某钛酸盐晶体结构模型如图所示。该晶体的化学式是

(2)铁合金用途广泛,某种铁镁合金储氢效率很高,其晶胞如图所示。晶体中每个镁原子周围距离最近的铁原子有
 ,C为
,C为 ,B点坐标参数为
,B点坐标参数为
(3)金属铬晶胞如图,已知其密度为a g∙cm-3,阿伏加德罗常数的值为NA,则晶体中铬原子的半径为

更新时间:2024-03-27 14:59:59
|
相似题推荐
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】硼(B)及其化合物在化学中有重要的地位。请回答下列问题:
(1)基态B原子中能量最高的电子所在的原子轨道的电子云在空间上有______ 个伸展方向,原子轨道呈______ 形。 分子中,与N原子相连的H呈正电性(
分子中,与N原子相连的H呈正电性(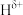 ),与B原子相连的H呈负电性(
),与B原子相连的H呈负电性(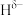 ),H、B、N电负性大小顺序是
),H、B、N电负性大小顺序是______ 。
(2)硼酸( )是白色片状晶体(层状结构如图),有滑腻感,在冷水中溶解度很小,加热时溶解度增大。
)是白色片状晶体(层状结构如图),有滑腻感,在冷水中溶解度很小,加热时溶解度增大。______ 。
②加热时,硼酸的溶解度增大,主要原因是______ 。
③硼酸是一元弱酸,在水中电离时,硼酸结合水电离出的 而呈酸性。写出硼酸的电离方程式:
而呈酸性。写出硼酸的电离方程式:______ 。
(3)硼氢化钠( )是有机化学中的一种常用还原剂,在热水中水解生成硼酸钠和氢气,用化学方程式表示其反应原理:
)是有机化学中的一种常用还原剂,在热水中水解生成硼酸钠和氢气,用化学方程式表示其反应原理:______ 。
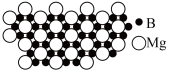
(4)硼化镁晶体在39K时呈超导性。在硼化镁晶体中,镁原子和硼原子是分层排布的,如图是该晶体微观结构的透视图,图中的硼原子和镁原子投影在同一平面上。则硼化镁的化学式为______ 。
(1)基态B原子中能量最高的电子所在的原子轨道的电子云在空间上有
 分子中,与N原子相连的H呈正电性(
分子中,与N原子相连的H呈正电性(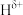 ),与B原子相连的H呈负电性(
),与B原子相连的H呈负电性(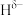 ),H、B、N电负性大小顺序是
),H、B、N电负性大小顺序是(2)硼酸(
 )是白色片状晶体(层状结构如图),有滑腻感,在冷水中溶解度很小,加热时溶解度增大。
)是白色片状晶体(层状结构如图),有滑腻感,在冷水中溶解度很小,加热时溶解度增大。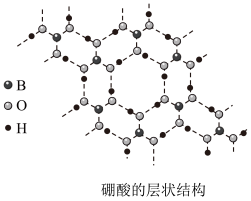
②加热时,硼酸的溶解度增大,主要原因是
③硼酸是一元弱酸,在水中电离时,硼酸结合水电离出的
 而呈酸性。写出硼酸的电离方程式:
而呈酸性。写出硼酸的电离方程式:(3)硼氢化钠(
 )是有机化学中的一种常用还原剂,在热水中水解生成硼酸钠和氢气,用化学方程式表示其反应原理:
)是有机化学中的一种常用还原剂,在热水中水解生成硼酸钠和氢气,用化学方程式表示其反应原理:(4)硼化镁晶体在39K时呈超导性。在硼化镁晶体中,镁原子和硼原子是分层排布的,如图是该晶体微观结构的透视图,图中的硼原子和镁原子投影在同一平面上。则硼化镁的化学式为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐2】硼及其化合物是用途广泛的化工原料,硼可以与多种元素形成化合物。
回答下列问题:
(1)硼酸的化学式为B(OH)3,是一元弱酸。
①硼酸具有弱酸性是由于B与水中的OH-形成配位键,在该键中由____ 原子提供空轨道。
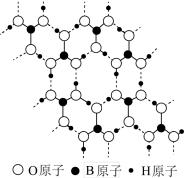
②硼酸晶体是片层结构,其中一层的结构如图所示。硼酸晶体在冷水中的溶解度很小,但在热水中较大,可能的原因是____ 。
(2)砷化硼和硼化镁均可做高温超导材料,其晶胞结构分别如图所示。
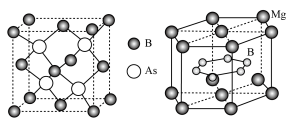
①砷化硼属于____ 晶体,B原子的杂化轨道类型是____ 。
②硼化镁的化学式是____ 。
回答下列问题:
(1)硼酸的化学式为B(OH)3,是一元弱酸。
①硼酸具有弱酸性是由于B与水中的OH-形成配位键,在该键中由
②硼酸晶体是片层结构,其中一层的结构如图所示。硼酸晶体在冷水中的溶解度很小,但在热水中较大,可能的原因是

(2)砷化硼和硼化镁均可做高温超导材料,其晶胞结构分别如图所示。

①砷化硼属于
②硼化镁的化学式是
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】重金属汞的泄露易造成污染。
(1)如遇液态汞泄露,应采用硫粉处理,发生反应的化学方程式是___________ 。汞泄露后主要以蒸气形态经呼吸道进入人体引起中毒现象,含巯基(―SH)的有机化合物二巯丙醇(结构如图I所示)是一种汞的解毒剂。

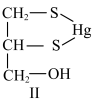
药理作用:金属汞进入体内后与细胞酶系统的巯基(―SH)结合,抑制酶的活性,出现中毒现象,药物的两个巯基可与金属汞结合,形成不易离解的无毒性化合物(结构如图Ⅱ所示)由尿排出。
(2)基态硫原子价层电子排布式是___________ 。
(3)比较 、
、 的沸点,并说明理由
的沸点,并说明理由___________ 。
(4)化合物Ⅲ也是一种汞解毒剂,下列说法正确的是___________ 。

a.在Ⅰ中S原子采取 杂化
杂化
b.在Ⅱ中S元素的电负性最大
c.在Ⅲ中存在离子键与共价键
d.化合物Ⅰ与化合物Ⅲ相比,化合物Ⅰ水溶性较好
(5)经理论计算,汞可与锗(Ge)和锑(Sb)可形成一种潜在的拓扑绝缘材料,晶胞结构如下图所示。
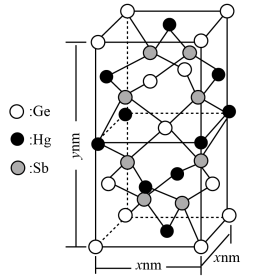
①已知Ge分别位于晶胞的顶点、面上和体心处,该晶胞中与Hg距离最近的Sb的数目为___________ ,该晶胞中的粒子个数比为Hg∶Ge∶Sb=___________ 。
②若该物质最简式的相对分子质量为M,则该晶体的晶胞密度为___________ 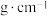 。
。
(1)如遇液态汞泄露,应采用硫粉处理,发生反应的化学方程式是

药理作用:金属汞进入体内后与细胞酶系统的巯基(―SH)结合,抑制酶的活性,出现中毒现象,药物的两个巯基可与金属汞结合,形成不易离解的无毒性化合物(结构如图Ⅱ所示)由尿排出。

(2)基态硫原子价层电子排布式是
(3)比较
 、
、 的沸点,并说明理由
的沸点,并说明理由(4)化合物Ⅲ也是一种汞解毒剂,下列说法正确的是

a.在Ⅰ中S原子采取
 杂化
杂化b.在Ⅱ中S元素的电负性最大
c.在Ⅲ中存在离子键与共价键
d.化合物Ⅰ与化合物Ⅲ相比,化合物Ⅰ水溶性较好
(5)经理论计算,汞可与锗(Ge)和锑(Sb)可形成一种潜在的拓扑绝缘材料,晶胞结构如下图所示。

①已知Ge分别位于晶胞的顶点、面上和体心处,该晶胞中与Hg距离最近的Sb的数目为
②若该物质最简式的相对分子质量为M,则该晶体的晶胞密度为
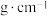 。
。
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】某种水性钠离子电池电极材料属于配位化合物,使用过程中电极 嵌入或脱嵌,变化如下:格林绿
嵌入或脱嵌,变化如下:格林绿 普鲁士蓝
普鲁士蓝 普鲁士白,格林绿、普鲁士蓝、普鲁士白均为立方晶胞,省略
普鲁士白,格林绿、普鲁士蓝、普鲁士白均为立方晶胞,省略 的晶胞示意图如图1,嵌入和脱嵌过程中
的晶胞示意图如图1,嵌入和脱嵌过程中 均填充在小立方体的体心。X为上述三种晶体中的其中一种,如果不考虑
均填充在小立方体的体心。X为上述三种晶体中的其中一种,如果不考虑 ,所有微粒都只有一种化学环境,从X中切出的部分结构如图2所示。
,所有微粒都只有一种化学环境,从X中切出的部分结构如图2所示。

回答下列问题:
(1)从结构上分析基态 、
、 ,
,_______ 相对更稳定,原因是_______ 。
(2)配位化合物X中,N原子的杂化类型是_______ , 的配位数是
的配位数是_______ ,X中 键和
键和 键的数目之比为
键的数目之比为_______ 。
(3)格林绿、普鲁士蓝、普鲁士白的化学式可用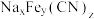 表示,后两者的化学式依次是
表示,后两者的化学式依次是_______ 、_______ 。
 嵌入或脱嵌,变化如下:格林绿
嵌入或脱嵌,变化如下:格林绿 普鲁士蓝
普鲁士蓝 普鲁士白,格林绿、普鲁士蓝、普鲁士白均为立方晶胞,省略
普鲁士白,格林绿、普鲁士蓝、普鲁士白均为立方晶胞,省略 的晶胞示意图如图1,嵌入和脱嵌过程中
的晶胞示意图如图1,嵌入和脱嵌过程中 均填充在小立方体的体心。X为上述三种晶体中的其中一种,如果不考虑
均填充在小立方体的体心。X为上述三种晶体中的其中一种,如果不考虑 ,所有微粒都只有一种化学环境,从X中切出的部分结构如图2所示。
,所有微粒都只有一种化学环境,从X中切出的部分结构如图2所示。
回答下列问题:
(1)从结构上分析基态
 、
、 ,
,(2)配位化合物X中,N原子的杂化类型是
 的配位数是
的配位数是 键和
键和 键的数目之比为
键的数目之比为(3)格林绿、普鲁士蓝、普鲁士白的化学式可用
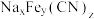 表示,后两者的化学式依次是
表示,后两者的化学式依次是
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】卤素化学丰富多彩,能形成卤化物、卤素互化物、多卤化物等多种类型的化合物。
(1)基态溴原子的价电子排布式为__ 。
(2)卤素互化物如IBr、ICl等与卤素单质结构相似、性质相近。则Cl2、IBr、ICl的沸点由高到低的顺序为__ 。
(3)气态氟化氢中存在二聚分子(HF)2,这是由于__ 。
(4)互为等电子体的微粒相互之间结构相似。I3+属于多卤素阳离子,根据VSEPR模型推测I3+的空间构型为___ ,中心原子杂化类型为__ 。
(5)铁在元素周期表中的位置___ (用“周期”和“族”来描述)。
(6)简述三价铁比二价铁稳定的原因___ 。
(7)如图所示为卤化物冰晶石(化学式为Na3AlF6)的晶胞。图中●位于大立方体顶点和面心,○位于大立方体的12条棱的中点和8个小立方体的体心,▽是图中●、○中的一种。图中●、○分别指代哪种粒子__ 、__ ;大立方体的体心处▽所代表的是__ 。

(1)基态溴原子的价电子排布式为
(2)卤素互化物如IBr、ICl等与卤素单质结构相似、性质相近。则Cl2、IBr、ICl的沸点由高到低的顺序为
(3)气态氟化氢中存在二聚分子(HF)2,这是由于
(4)互为等电子体的微粒相互之间结构相似。I3+属于多卤素阳离子,根据VSEPR模型推测I3+的空间构型为
(5)铁在元素周期表中的位置
(6)简述三价铁比二价铁稳定的原因
(7)如图所示为卤化物冰晶石(化学式为Na3AlF6)的晶胞。图中●位于大立方体顶点和面心,○位于大立方体的12条棱的中点和8个小立方体的体心,▽是图中●、○中的一种。图中●、○分别指代哪种粒子

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐3】Ⅰ.氯化钠是一种典型且极具魅力的晶体,我们通过学习氯化钠可以更好地了解其他类似物质的结构。已知氯化钠的晶胞如图1所示。___________ 。
(2)已知NaCl的密度为 ,NaCl的摩尔质量为
,NaCl的摩尔质量为 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,则在NaCl晶体里
,则在NaCl晶体里 和
和 的最短距离为
的最短距离为___________ pm。
(3)下列关于氯化钠的说法不正确的是___________。
(4)用离子方程式表示氯碱工业反应原理___________ 。
Ⅱ.我国某研究所于2022年研制出一种新型离子液体[CPMIm]Cl(如图2)可弥补该电池表面的 和
和 缺陷,进一步提高该电池的性能。
缺陷,进一步提高该电池的性能。___________ (填选项字母)。
A.离子键 B.共价键 C.氢键
(6)离子液体[CPMIm]Cl中不同杂化方式的碳原子个数比: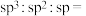
___________ 。
(7)相较于传统液态有机溶剂,该离子液体具有难挥发的优点,原因是:___________ 。
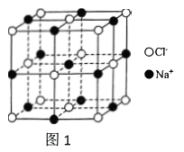
(2)已知NaCl的密度为
 ,NaCl的摩尔质量为
,NaCl的摩尔质量为 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,则在NaCl晶体里
,则在NaCl晶体里 和
和 的最短距离为
的最短距离为(3)下列关于氯化钠的说法不正确的是___________。
A.基态 的电子有5种空间运动状态 的电子有5种空间运动状态 |
B.第三周期离子半径最大的是 |
C.第三电离能大小: |
| D.每个氯离子周围与它最近且等距的氯离子有12个 |
Ⅱ.我国某研究所于2022年研制出一种新型离子液体[CPMIm]Cl(如图2)可弥补该电池表面的
 和
和 缺陷,进一步提高该电池的性能。
缺陷,进一步提高该电池的性能。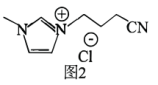
A.离子键 B.共价键 C.氢键
(6)离子液体[CPMIm]Cl中不同杂化方式的碳原子个数比:
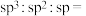
(7)相较于传统液态有机溶剂,该离子液体具有难挥发的优点,原因是:
您最近一年使用:0次
【推荐1】氢能被视为21世纪最具发展潜力的清洁能源。
(1)水是制取H2的常见原料,下列有关水的说法正确的是______ .
a.水分子是一种极性分子,水分子空间结构呈直线型
b.1个H2O分子中有2个由s轨道与sp3杂化轨道形成的σ键
c.水分子间通过H﹣O键形成冰晶体
d.冰晶胞中水分子的空间排列方式与干冰晶胞类似
(2)氢气的安全贮存和运输是氢能应用的关键。
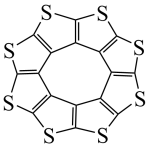
①最近尼赫鲁先进科学研究中心借助ADF软件对一种新型环烯类储氢材料(C16S8)进行研究,从理论角度证明这种分子中的原子都处于同一平面上(如图1所示),每个平面上下两侧最多可存10个H2分子.分子中C原子的杂化轨道类型为______ ,C16S8中σ键与π键之比为______ ,C16S8与H2微粒间的作用力是______ 。
②氨硼烷化合物(NH3BH3)是最近密切关注的一种新型化学氢化物储氢材料.请画出含有配位键(用“→”表示)的氨硼烷的结构式_____ ;与氨硼烷互为等电子体的有机小分子是___ (写结构简式)。
③某种具有储氢功能的铜合金晶体具有立方最密堆积的结构,晶胞中Cu原子处于面心,Au原子处于顶点位置,氢原子可进入到由Cu原子与Au原子构成的四面体空隙中.若将Cu原子与Au原子等同看待,该晶体储氢后的晶胞结构与CaF2(晶胞结构如图)的结构相似,该晶体储氢后Cu:Au:H为______ 。
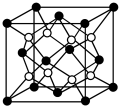
④MgH2是金属氢化物储氢材料,其晶胞如图所示,已知该晶体的密度ag·cm-3,则晶胞的体积为______________ cm3(用含a、NA的代数式表示,NA表示阿伏加 德罗常数)。

(1)水是制取H2的常见原料,下列有关水的说法正确的是
a.水分子是一种极性分子,水分子空间结构呈直线型
b.1个H2O分子中有2个由s轨道与sp3杂化轨道形成的σ键
c.水分子间通过H﹣O键形成冰晶体
d.冰晶胞中水分子的空间排列方式与干冰晶胞类似
(2)氢气的安全贮存和运输是氢能应用的关键。
①最近尼赫鲁先进科学研究中心借助ADF软件对一种新型环烯类储氢材料(C16S8)进行研究,从理论角度证明这种分子中的原子都处于同一平面上(如图1所示),每个平面上下两侧最多可存10个H2分子.分子中C原子的杂化轨道类型为

②氨硼烷化合物(NH3BH3)是最近密切关注的一种新型化学氢化物储氢材料.请画出含有配位键(用“→”表示)的氨硼烷的结构式
③某种具有储氢功能的铜合金晶体具有立方最密堆积的结构,晶胞中Cu原子处于面心,Au原子处于顶点位置,氢原子可进入到由Cu原子与Au原子构成的四面体空隙中.若将Cu原子与Au原子等同看待,该晶体储氢后的晶胞结构与CaF2(晶胞结构如图)的结构相似,该晶体储氢后Cu:Au:H为

④MgH2是金属氢化物储氢材料,其晶胞如图所示,已知该晶体的密度ag·cm-3,则晶胞的体积为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐2】钠和铜的单质及其化合物在社会实际中有着广泛的应用。
(1)NaCl晶体的晶胞结构如图所示,每个NaCl的晶胞中含有的阴离子的个数为______ ,阳离子周围最近且等距离得阴离子的个数为________ 。
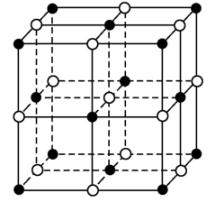
(2)碘化钠溶液和硫酸铜溶液能反应生成一种铜的碘化物A(白色沉淀),A的晶胞如图所示,则A的化学式是______ ,A中铜元素的化合价为________ 。

(3)向硫酸铜溶液中滴加氨水会生成蓝色沉淀,再滴加氨水到沉淀刚好全部溶解可得到深蓝色溶液,继续向其中加入极性较小的乙醇可以生成深蓝色的[Cu(NH3)4]SO4·H2O沉淀,请写出该沉淀中金属微粒的电子式________ ,并用示意图画出其内界的配位键_____ 。
(1)NaCl晶体的晶胞结构如图所示,每个NaCl的晶胞中含有的阴离子的个数为

(2)碘化钠溶液和硫酸铜溶液能反应生成一种铜的碘化物A(白色沉淀),A的晶胞如图所示,则A的化学式是

(3)向硫酸铜溶液中滴加氨水会生成蓝色沉淀,再滴加氨水到沉淀刚好全部溶解可得到深蓝色溶液,继续向其中加入极性较小的乙醇可以生成深蓝色的[Cu(NH3)4]SO4·H2O沉淀,请写出该沉淀中金属微粒的电子式
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐3】磷酸亚铁锂(LiFePO4)可用作锂离子电池正极材料,具有热稳定性好、循环性能优良、安全性高等特点,文献报道可采用FeCl3、NH4H2PO4、LiCl和苯胺等作为原料制备。回答下列问题:
(1)在周期表中,与Li的化学性质最相似的邻族元素是________ ,该元素基态原子核外M层电子的自旋状态_________ (填“相同”或“相反”)。
(2)FeCl3中的化学键具有明显的共价性,蒸汽状态下以双聚分子存在的FeCl3的结构式为________ ,其中Fe的配位数为_____________ 。
(3)苯胺 )的晶体类型是
)的晶体类型是__________ 。苯胺与甲苯(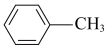 )的相对分子质量相近,但苯胺的熔点(-5.9℃)、沸点(184.4℃)分别高于甲苯的熔点(-95.0℃)、沸点(110.6℃),原因是
)的相对分子质量相近,但苯胺的熔点(-5.9℃)、沸点(184.4℃)分别高于甲苯的熔点(-95.0℃)、沸点(110.6℃),原因是___________ 。
(4)NH4H2PO4中,电负性最高的元素是______ ;P的_______ 杂化轨道与O的2p轨道形成_______ 键。
(5)NH4H2PO4和LiFePO4属于简单磷酸盐,而直链的多磷酸盐则是一种复杂磷酸盐,如:焦磷酸钠、三磷酸钠等。焦磷酸根离子、三磷酸根离子如下图所示:
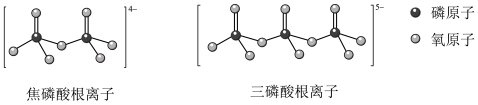
这类磷酸根离子的化学式可用通式表示为____________ (用n代表P原子数)。
(1)在周期表中,与Li的化学性质最相似的邻族元素是
(2)FeCl3中的化学键具有明显的共价性,蒸汽状态下以双聚分子存在的FeCl3的结构式为
(3)苯胺
 )的晶体类型是
)的晶体类型是 )的相对分子质量相近,但苯胺的熔点(-5.9℃)、沸点(184.4℃)分别高于甲苯的熔点(-95.0℃)、沸点(110.6℃),原因是
)的相对分子质量相近,但苯胺的熔点(-5.9℃)、沸点(184.4℃)分别高于甲苯的熔点(-95.0℃)、沸点(110.6℃),原因是(4)NH4H2PO4中,电负性最高的元素是
(5)NH4H2PO4和LiFePO4属于简单磷酸盐,而直链的多磷酸盐则是一种复杂磷酸盐,如:焦磷酸钠、三磷酸钠等。焦磷酸根离子、三磷酸根离子如下图所示:

这类磷酸根离子的化学式可用通式表示为
您最近一年使用:0次



