高铁酸钾(K2FeO4)是一种既能杀菌消毒、又能净水的处理剂。工业制备高铁酸钾的反应离子方程式为Fe(OH)3+ClO-+OH-→FeO +Cl-+H2O(未配平),下列有关说法不正确的是
+Cl-+H2O(未配平),下列有关说法不正确的是
 +Cl-+H2O(未配平),下列有关说法不正确的是
+Cl-+H2O(未配平),下列有关说法不正确的是| A.ClO-参与反应转移3mol电子可生产1molK2FeO4 |
| B.高铁酸钾中铁元素显+6价 |
| C.上述反应中氧化剂和还原剂的物质的量之比为2∶3 |
D.由上述反应可知,Fe(OH)3的氧化性弱于FeO |
更新时间:2024-03-30 21:43:07
|
相似题推荐
单选题
|
较易
(0.85)
解题方法
【推荐1】下图是铜及部分含铜粒子的价荷图。下列推断合理的是
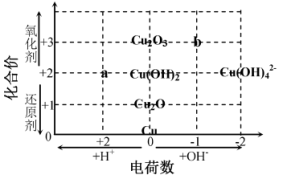

| A.Cu变成a可以加稀氨水 |
B.Cu (OH) 的中心原子Cu采取sp3杂化,离子构型为正四面体 的中心原子Cu采取sp3杂化,离子构型为正四面体 |
C.如果将高铜酸根离子(CuO ) 填入坐标,应该填在b的位置 ) 填入坐标,应该填在b的位置 |
| D.在酸性环境中,Cu2O生成a必须加氧化剂 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】下列物质转化需要加入还原剂的是
A.SO →SO2 →SO2 | B.Cl2→Cl- | C.Na→Na+ | D.SO2→S |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐3】铋(Bi)是第ⅤA族元素,+3价时较稳定,铋酸钠(NaBiO3)溶液呈无色。现取一定量的硫酸锰(MnSO4)溶液,依次滴加下列溶液,对应现象如下表所示:(已知I2能使淀粉碘化钾试纸变蓝)
在上述实验条件下,下列结论正确的是
| 加入溶液 | ①适量铋酸钠溶液 | ②过量双氧水 | ③适量KI-淀粉溶液 |
| 实验现象 | 溶液呈紫红色 | 溶液紫红色消失,产生气泡 | 溶液缓慢变成蓝色 |
| A.H2O2被高锰酸根离子还原成O2 |
| B.KI-淀粉溶液中滴加铋酸钠溶液,溶液出现蓝色 |
C.实验②的离子方程式为 |
D.氧化性强弱顺序: |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐1】短程稍化-厌氧氨氧化工艺的目的是将氨氮废水中的NH 转变为N2脱除,其机理如图.下列说法中错误的是
转变为N2脱除,其机理如图.下列说法中错误的是

 转变为N2脱除,其机理如图.下列说法中错误的是
转变为N2脱除,其机理如图.下列说法中错误的是
A.O2氧化性大于NO |
B.参与Ⅰ中反应的n(NH ):n(O2)=2:3 ):n(O2)=2:3 |
C.此工艺中被氧化的含氮微粒是NH |
| D.标准状况下,当Ⅱ中转移6mol电子时生成氮气22.4L |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】A元素原子得电子变成阴离子释放出的能量比B元素原子得电子变成阴离子释放出的能量大,则
| A.氧化性A->B- | B.还原性 A->B- | C.氧化性 A>B | D.还原性A>B |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐1】下列有关氧化还原反应的说法正确的是
A.3SiO2+6C+2N2 Si3N4+6CO该反应中氧化剂和还原剂个数比为3∶1 Si3N4+6CO该反应中氧化剂和还原剂个数比为3∶1 |
| B.在氧化还原反应中,氧化剂与还原剂不可能是同一种物质 |
| C.KClO3+6HCl=KCl+3Cl2↑+3H2O反应中,转移的电子数为6e- |
| D.CaH2+2H2O=Ca(OH)2+2H2↑反应中,Ca(OH)2既不是氧化产物也不是还原产物 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】 气体与足量
气体与足量 溶液完全反应后,再加入
溶液完全反应后,再加入 溶液,发生如下反应:
溶液,发生如下反应:
①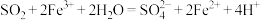
②
下列有关说法不正确 的是
 气体与足量
气体与足量 溶液完全反应后,再加入
溶液完全反应后,再加入 溶液,发生如下反应:
溶液,发生如下反应:①
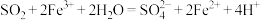
②

下列有关说法
A.反应①中 发生氧化反应 发生氧化反应 |
B.反应②中 被氧化 被氧化 |
C.反应②中每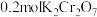 参加反应,转移电子的数目约为 参加反应,转移电子的数目约为 |
D.若有 (标准状况)参加反应,则最终消耗 (标准状况)参加反应,则最终消耗 |
您最近一年使用:0次




