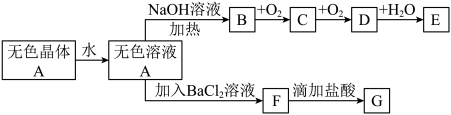
氨对人类生产、生活有重要影响。回答下列问题:
(1)合成氨是工业上人工固氮的重要方法,写出该反应的化学方程式:__________ 。
(2)氨气的制备
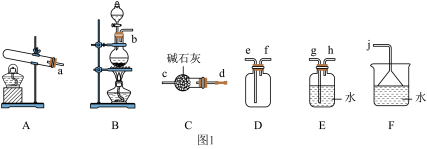
①氨气的发生装置可以选择图1中的__________ (填字母),反应的化学方程式为__________ 。
②欲收集一瓶干燥的氨气,选择图1中的装置,其连接顺序为:发生装置→__________ (按气流方向,用小写字母表示)。
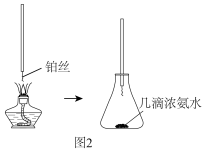
(3)氨的催化氧化:已知NH3在Pt催化和加热条件下与氧气反应,如图2是探究氨的催化氧化简易装置,观察到锥形瓶中铂丝保持红热,有红棕色气体或白烟产生。红棕色气体成分是___________ (填化学式,下同),白烟的成分是____________ 。
(1)合成氨是工业上人工固氮的重要方法,写出该反应的化学方程式:
(2)氨气的制备


①氨气的发生装置可以选择图1中的
②欲收集一瓶干燥的氨气,选择图1中的装置,其连接顺序为:发生装置→
(3)氨的催化氧化:已知NH3在Pt催化和加热条件下与氧气反应,如图2是探究氨的催化氧化简易装置,观察到锥形瓶中铂丝保持红热,有红棕色气体或白烟产生。红棕色气体成分是
更新时间:2024-04-08 17:44:47
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
【推荐1】1913年,合成氨问世,氨催化氧化法生产硝酸开始进入工业化阶段,氨及硝酸都是重要的化工原料,回答下列问题:
(1)用NH4Cl和Ca(OH)2制备NH3的化学方程式为___________ ,反应发生、气体干燥、气体收集和尾气处理装置依次为___________ (填写字母)。
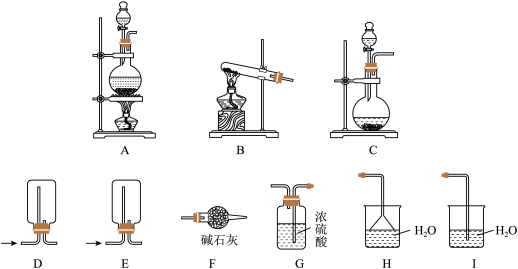
(2)按下图装置进行NH3性质实验。
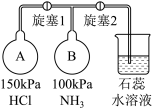
①先打开旋塞1,B瓶中的现象是___________ ,原因是___________ ,稳定后,关闭旋塞1。
②再打开旋塞2,B瓶中的现象是___________ 。
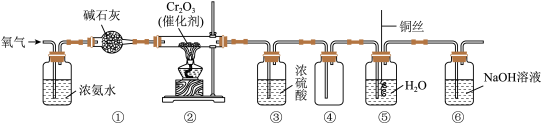
(3)化学小组模拟氨催化氧化的实验装置如图所示,装置②中氨催化氧化的化学方程式为___________ ,装置③中浓硫酸的作用是___________ ,装置⑤中溶液变为蓝色的原因是___________ (用离子方程式表示)。
(4)若足量铜与一定量浓硝酸反应,得到硝酸铜溶液和NO、NO2的混合气体,这些气体与1.12 LO2(标准状况下)混合后通入水中,所有气体完全被水吸收生成硝酸。若向所得硝酸铜溶液中加入4 mol·L-1NaOH溶液至Cu2+恰好完全沉淀,则消耗NaOH溶液的体积是___________ mL。
(1)用NH4Cl和Ca(OH)2制备NH3的化学方程式为

(2)按下图装置进行NH3性质实验。

①先打开旋塞1,B瓶中的现象是
②再打开旋塞2,B瓶中的现象是
(3)化学小组模拟氨催化氧化的实验装置如图所示,装置②中氨催化氧化的化学方程式为

(4)若足量铜与一定量浓硝酸反应,得到硝酸铜溶液和NO、NO2的混合气体,这些气体与1.12 LO2(标准状况下)混合后通入水中,所有气体完全被水吸收生成硝酸。若向所得硝酸铜溶液中加入4 mol·L-1NaOH溶液至Cu2+恰好完全沉淀,则消耗NaOH溶液的体积是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】喷泉是一种常见的现象,其产生的原理是存在压强差。

试回答下列问题:
(1)实验室制取氨气的化学方程式为________ 。
①用图A装置进行喷泉实验,上部烧瓶已充满干燥的氨气,引发喷泉的操作是_______ 。
②利用图B装置引发喷泉的操作是___________ 。
(2)利用图C装置,在锥形瓶中分别加入足量的下列物质,反应后可能产生喷泉的有______ 。
A. 与稀盐酸 B.
与稀盐酸 B. 与稀硫酸
与稀硫酸
C. 与稀硝酸 D.
与稀硝酸 D. 溶液与
溶液与 溶液
溶液
(3)在图D装置的锥形瓶中加入乙醇,瓶外放一水槽,水槽中加入冷水后,再加入足量的下列物质,结果也形成了喷泉,水槽中加入的物质可能是_____ 。
A 浓硫酸 B 食盐 C 硝酸钾 D 硫酸铜
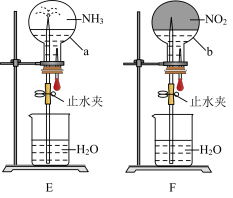
(4)同温同压下,两个等体积的干燥圆底烧瓶中分别充满 和
和 ,进行喷泉实验如图E、F所示,经充分反应后,发现烧瓶a中充满液体,b中有
,进行喷泉实验如图E、F所示,经充分反应后,发现烧瓶a中充满液体,b中有 体积的液体,则两烧瓶内溶质的物质的量浓度的关系是
体积的液体,则两烧瓶内溶质的物质的量浓度的关系是_______ 。
A.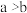 B.
B. C.
C. D.不能确定
D.不能确定

试回答下列问题:
(1)实验室制取氨气的化学方程式为
①用图A装置进行喷泉实验,上部烧瓶已充满干燥的氨气,引发喷泉的操作是
②利用图B装置引发喷泉的操作是
(2)利用图C装置,在锥形瓶中分别加入足量的下列物质,反应后可能产生喷泉的有
A.
 与稀盐酸 B.
与稀盐酸 B. 与稀硫酸
与稀硫酸C.
 与稀硝酸 D.
与稀硝酸 D. 溶液与
溶液与 溶液
溶液(3)在图D装置的锥形瓶中加入乙醇,瓶外放一水槽,水槽中加入冷水后,再加入足量的下列物质,结果也形成了喷泉,水槽中加入的物质可能是
A 浓硫酸 B 食盐 C 硝酸钾 D 硫酸铜
(4)同温同压下,两个等体积的干燥圆底烧瓶中分别充满
 和
和 ,进行喷泉实验如图E、F所示,经充分反应后,发现烧瓶a中充满液体,b中有
,进行喷泉实验如图E、F所示,经充分反应后,发现烧瓶a中充满液体,b中有 体积的液体,则两烧瓶内溶质的物质的量浓度的关系是
体积的液体,则两烧瓶内溶质的物质的量浓度的关系是
A.
 B.
B. C.
C. D.不能确定
D.不能确定
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】Ⅰ.实验室常见的几种气体发生装置如图A、B、C所示:

(1)实验室可以用B或C装置制取氨气,如果用B装置制取氨气其化学反应方程式为_______ 。
(2)气体的性质是选择气体收集方法的主要依据。下列性质与收集方法无关的是_______ (填序号,下同)。
①密度 ②颜色 ③溶解性 ④热稳定性 ⑤与氧气反应
(3)若用A装置与D装置相连制取并收集X气体,则X可以是下列气体中的_______ 。
①CO2 ②NO ③Cl2 ④H2 ⑤HCl
其中在D装置中连接小烧杯的目的是_______ 。
Ⅱ.某小组以CoCl2·6H2O、NH4Cl、H2O2、浓氨水为原料,在活性炭催化下,合成了橙黄色晶体X。为确定其组成,进行如下实验 。
(1)经测定,样品X中钴、氨和氯的物质的量之比为1∶6∶3,钴的化合价为_______ ,制备X的化学方程式为_______ ;
(2)氨的测定:精确称取w g X,加适量水溶解,注入如图所示的三颈瓶中,然后逐滴加入足量10%NaOH溶液,通入水蒸气,将样品液中的氨全部蒸出,用V1 mL cl mol·L-1的盐酸标准溶液吸收。蒸氨结束后取下接收瓶,用c2 mol·L-1NaOH标准溶液滴定过剩的HCl,到终点时消耗V2 mL NaOH溶液。氨的测定装置(已省略加热和夹持装置)

①装置中安全管的作用原理是_______ 。②样品中氨的质量分数表达式为_______ 。

(1)实验室可以用B或C装置制取氨气,如果用B装置制取氨气其化学反应方程式为
(2)气体的性质是选择气体收集方法的主要依据。下列性质与收集方法无关的是
①密度 ②颜色 ③溶解性 ④热稳定性 ⑤与氧气反应
(3)若用A装置与D装置相连制取并收集X气体,则X可以是下列气体中的
①CO2 ②NO ③Cl2 ④H2 ⑤HCl
其中在D装置中连接小烧杯的目的是
Ⅱ.某小组以CoCl2·6H2O、NH4Cl、H2O2、浓氨水为原料,在活性炭催化下,合成了橙黄色晶体X。为确定其组成,进行如下实验 。
(1)经测定,样品X中钴、氨和氯的物质的量之比为1∶6∶3,钴的化合价为
(2)氨的测定:精确称取w g X,加适量水溶解,注入如图所示的三颈瓶中,然后逐滴加入足量10%NaOH溶液,通入水蒸气,将样品液中的氨全部蒸出,用V1 mL cl mol·L-1的盐酸标准溶液吸收。蒸氨结束后取下接收瓶,用c2 mol·L-1NaOH标准溶液滴定过剩的HCl,到终点时消耗V2 mL NaOH溶液。氨的测定装置(已省略加热和夹持装置)

①装置中安全管的作用原理是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
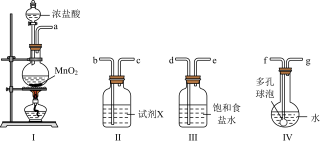
【推荐1】次氯酸消毒液高效安全,适用于一般物体表面消毒、空间和环境消毒。实验室利用如下装置制取氯气并制取次氯酸消毒液。
回答下列问题:
(1)装置合理的连接顺序为a→___________ (按气流方向填各接口的编号)。
(2)装置Ⅰ中反应的化学方程式是___________ 。
(3)装置Ⅱ中试剂X是___________ ;装置Ⅲ的作用是___________ ;装置Ⅳ中多孔球泡的作用为___________ 。
(4)反应结束后,取V中少量液体于试管中,滴入几滴石蕊观察到的现象是___________ ,请结合离子方程式说明原因___________ 。

回答下列问题:
(1)装置合理的连接顺序为a→
(2)装置Ⅰ中反应的化学方程式是
(3)装置Ⅱ中试剂X是
(4)反应结束后,取V中少量液体于试管中,滴入几滴石蕊观察到的现象是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐2】 新型材料应用前景广泛,其制备与性质研究成为热点。相关数据如下:
新型材料应用前景广泛,其制备与性质研究成为热点。相关数据如下:
(1) 的制备。
的制备。
①化学气相沉积法。
Ⅰ.一定温度下,以 气体和
气体和 为原料制备
为原料制备 ,反应的化学方程式是
,反应的化学方程式是______ 。
Ⅱ.上述反应适宜的温度范围是________ ℃(填字母)。
a.75~100 b.600~1100 c.2000~2300
②铝粉直接氮化法。
 与
与 可直接化合为
可直接化合为 固体,
固体, 能将
能将 包裹,反应难以继续进行。控制温度,在
包裹,反应难以继续进行。控制温度,在 粉中均匀掺入适量
粉中均匀掺入适量 粉,可使
粉,可使 几乎全部转化为
几乎全部转化为 固体。该过程发生的反应有:
固体。该过程发生的反应有:___________ 、___________ 和 。
。
③碳热还原法。
以 、C(石墨)和
、C(石墨)和 为原料,在高温下制备
为原料,在高温下制备 。
。
已知:i.
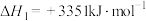
ii.
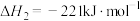
iii.
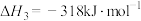
运用平衡移动原理分析反应ii对反应i的可能影响:___________ 。
(2) 的性质。
的性质。 粉末可发生水解的化学方程式是
粉末可发生水解的化学方程式是 。相同条件下,不同粒径的
。相同条件下,不同粒径的 粉末水解时溶液
粉末水解时溶液 的变化如图所示。
的变化如图所示。
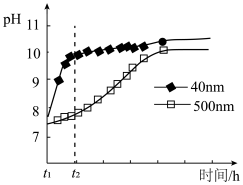
解释 时间内两条曲线差异的可能原因:
时间内两条曲线差异的可能原因:___________ 。
(3) 含量检测。向
含量检测。向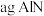 样品中加入足量浓
样品中加入足量浓 溶液,然后通入水蒸气将
溶液,然后通入水蒸气将 全部蒸出,将
全部蒸出,将 用过量的
用过量的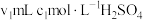 溶液吸收完全,剩余的
溶液吸收完全,剩余的 用
用 溶液恰好中和,则样品中
溶液恰好中和,则样品中 的质量分数是
的质量分数是___________ 。
 新型材料应用前景广泛,其制备与性质研究成为热点。相关数据如下:
新型材料应用前景广泛,其制备与性质研究成为热点。相关数据如下:| 物质 | 熔点/℃ | 沸点/℃ | 与 反应温度 /℃ 反应温度 /℃ | 相应化合物分解温度/℃ |
| Al | 660 | 2467 | >800 |  :>2000(>1400升华) :>2000(>1400升华) :(>181升华) :(>181升华) |
| Mg | 649 | 1090 | >300 |  :>800 :>800 |
(1)
 的制备。
的制备。①化学气相沉积法。
Ⅰ.一定温度下,以
 气体和
气体和 为原料制备
为原料制备 ,反应的化学方程式是
,反应的化学方程式是Ⅱ.上述反应适宜的温度范围是
a.75~100 b.600~1100 c.2000~2300
②铝粉直接氮化法。
 与
与 可直接化合为
可直接化合为 固体,
固体, 能将
能将 包裹,反应难以继续进行。控制温度,在
包裹,反应难以继续进行。控制温度,在 粉中均匀掺入适量
粉中均匀掺入适量 粉,可使
粉,可使 几乎全部转化为
几乎全部转化为 固体。该过程发生的反应有:
固体。该过程发生的反应有: 。
。③碳热还原法。
以
 、C(石墨)和
、C(石墨)和 为原料,在高温下制备
为原料,在高温下制备 。
。已知:i.

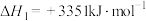
ii.

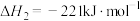
iii.

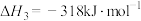
运用平衡移动原理分析反应ii对反应i的可能影响:
(2)
 的性质。
的性质。 粉末可发生水解的化学方程式是
粉末可发生水解的化学方程式是 。相同条件下,不同粒径的
。相同条件下,不同粒径的 粉末水解时溶液
粉末水解时溶液 的变化如图所示。
的变化如图所示。
解释
 时间内两条曲线差异的可能原因:
时间内两条曲线差异的可能原因:(3)
 含量检测。向
含量检测。向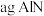 样品中加入足量浓
样品中加入足量浓 溶液,然后通入水蒸气将
溶液,然后通入水蒸气将 全部蒸出,将
全部蒸出,将 用过量的
用过量的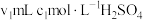 溶液吸收完全,剩余的
溶液吸收完全,剩余的 用
用 溶液恰好中和,则样品中
溶液恰好中和,则样品中 的质量分数是
的质量分数是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】某班学生在老师指导下探究氮的化合物的某些性质。
(1)同学甲在实验室利用下列装置(后面有图)制取氨气和氧气的混合气体,并完成氨的催化氧化。
A中加入浓氨水,D中加入碱石灰,E内放置催化剂(铂石棉),请回答:
①仪器B的名称:_______ 。B内只需加入一种固体试剂,该试剂的名称为_______ ,B中能产生氨气和氧气混合气体的原因(结合化学方程式回答)_______ 。
②按气流方向连接各仪器_______ (填接口字母)

(2)同学乙拟用甲同学得到的混合气体X(NO及过量的NH3),验证NO能被氨气还原并测算其转化率(忽略装置内空气的影响)。装置如下:

①装置C的作用可能是_______ 。
②若进入装置A的NO共268.8mL(已折算为标准状况,下同),氨气过量,最后收集到标准状况下190.4 mL N2,则NO的转化率为_______ 。
(3)N2O3是一种新型硝化剂。一定温度下,在恒容密闭容器中N2O3可发生下列反应:2N2O3+O2 4NO2(g);ΔH>0,下表为反应在某温度下的部分实验数据:
4NO2(g);ΔH>0,下表为反应在某温度下的部分实验数据:
计算在t=500s时,NO2的反应速率为_______ 。
(1)同学甲在实验室利用下列装置(后面有图)制取氨气和氧气的混合气体,并完成氨的催化氧化。
A中加入浓氨水,D中加入碱石灰,E内放置催化剂(铂石棉),请回答:
①仪器B的名称:
②按气流方向连接各仪器

(2)同学乙拟用甲同学得到的混合气体X(NO及过量的NH3),验证NO能被氨气还原并测算其转化率(忽略装置内空气的影响)。装置如下:

①装置C的作用可能是
②若进入装置A的NO共268.8mL(已折算为标准状况,下同),氨气过量,最后收集到标准状况下190.4 mL N2,则NO的转化率为
(3)N2O3是一种新型硝化剂。一定温度下,在恒容密闭容器中N2O3可发生下列反应:2N2O3+O2
 4NO2(g);ΔH>0,下表为反应在某温度下的部分实验数据:
4NO2(g);ΔH>0,下表为反应在某温度下的部分实验数据:| t/s | 0 | 500 | 1000 |
| c(N2O3)/mol·L-1 | 5.00 | 3.52 | 2.48 |
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐1】氮及其化合物在工农业生产和生命活动中起着重要作用。
(1)氨气是一种重要的化工原料,氨态氮肥是常用的肥料。
哈伯法合成氨技术的相关反应为:N2(g)+3H2(g) 2NH3(g) △H=-93kJ/mol,实际生产中,常用工艺条件:Fe作催化剂,控制温度773K、压强3.0×107Pa,原料气中N2和H2物质的量之比为1:2.8。
2NH3(g) △H=-93kJ/mol,实际生产中,常用工艺条件:Fe作催化剂,控制温度773K、压强3.0×107Pa,原料气中N2和H2物质的量之比为1:2.8。
①合成氨技术是氮的固定的一种,属于______ (选填“大气固氮”、“生物固氮”“人工固氮”)。
②合成氨反应常用铁触媒催化剂,下列关于催化剂的说法不正确的是_________ 。
A.可以加快反应速率 B.可以改变反应热
C.可以减少反应中的能耗 D.可以增加活化分子的数目
③关于合成氨工艺的下列理解,正确的是_________ 。
A.原料气中N2过量,是因N2相对易得,适度过量有利于提高H2的转化率
B.控制温度(773K)远高于室温,是为了保证尽可能高的平衡转化率和快的反应速率
C.当温度、压强一定时,在原料气(N2和H2的比例不变)中添加少量惰性气体,有利于提高平衡转化率
D.分离空气可得N2,通过天然气和水蒸气转化可得H2,原料气须经过净化处理,以防止催化剂中毒和安全事故发生
(2)肼(N2H4)是氮的氢化物之一,其制备方法可用次氯酸钠氧化过量的氨气。
①次氯酸钠溶液显碱性,表示原理的离子方程式是_________________________ 。
②常温下,该水解反应的平衡常数为K=1.0×10-6mol/L,则1.0mol/LNaClO溶液的pH=____ 。
③肼与N2O4氧化反应生成N2和水蒸气。
已知:N2(g)+2O2(g)=N2O4(l) △H=-19.5kJ/mol
N2H4(l)+O2(g)=N2(g)+2H2O(g) △H=-534.2kJ/mol
请写出肼和N2O4反应的热化学反应方程式_________________________________ 。
(3)在NH4HCO3溶液中,反应NH4++HCO3-+H2O NH3·H2O+H2CO3的平衡常数K=
NH3·H2O+H2CO3的平衡常数K=_____ 。(已知常温下NH3·H2O的电离平衡常数Kb=2×10-5,H2CO3的电离平衡常数Ka1=4×10-7)。
(1)氨气是一种重要的化工原料,氨态氮肥是常用的肥料。
哈伯法合成氨技术的相关反应为:N2(g)+3H2(g)
 2NH3(g) △H=-93kJ/mol,实际生产中,常用工艺条件:Fe作催化剂,控制温度773K、压强3.0×107Pa,原料气中N2和H2物质的量之比为1:2.8。
2NH3(g) △H=-93kJ/mol,实际生产中,常用工艺条件:Fe作催化剂,控制温度773K、压强3.0×107Pa,原料气中N2和H2物质的量之比为1:2.8。①合成氨技术是氮的固定的一种,属于
②合成氨反应常用铁触媒催化剂,下列关于催化剂的说法不正确的是
A.可以加快反应速率 B.可以改变反应热
C.可以减少反应中的能耗 D.可以增加活化分子的数目
③关于合成氨工艺的下列理解,正确的是
A.原料气中N2过量,是因N2相对易得,适度过量有利于提高H2的转化率
B.控制温度(773K)远高于室温,是为了保证尽可能高的平衡转化率和快的反应速率
C.当温度、压强一定时,在原料气(N2和H2的比例不变)中添加少量惰性气体,有利于提高平衡转化率
D.分离空气可得N2,通过天然气和水蒸气转化可得H2,原料气须经过净化处理,以防止催化剂中毒和安全事故发生
(2)肼(N2H4)是氮的氢化物之一,其制备方法可用次氯酸钠氧化过量的氨气。
①次氯酸钠溶液显碱性,表示原理的离子方程式是
②常温下,该水解反应的平衡常数为K=1.0×10-6mol/L,则1.0mol/LNaClO溶液的pH=
③肼与N2O4氧化反应生成N2和水蒸气。
已知:N2(g)+2O2(g)=N2O4(l) △H=-19.5kJ/mol
N2H4(l)+O2(g)=N2(g)+2H2O(g) △H=-534.2kJ/mol
请写出肼和N2O4反应的热化学反应方程式
(3)在NH4HCO3溶液中,反应NH4++HCO3-+H2O
 NH3·H2O+H2CO3的平衡常数K=
NH3·H2O+H2CO3的平衡常数K=
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】已知氮元素及其化合物的转化关系如下图所示,回答下列问题。
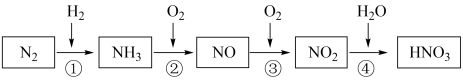
(1)①~④各步转化中,属于氮的固定的是_______ (填序号)。
(2)实验室常用加热氯化铵和氢氧化钙固体混合物的方法制取氨气。
①化学方程式是_______ 。
②干燥氨气不可选用的试剂是_______ (填字母)。
a.浓硫酸 b.碱石灰 c.NaOH固体
(3)工业制硝酸时尾气中含有NO、 ,可用以下方法吸收:
,可用以下方法吸收:
①水吸收法。结合化学方程式说明用水吸收 的缺陷
的缺陷_______ 。
②NaOH溶液吸收法。发生的反应有: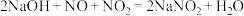 ,
,
_______ 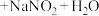 (填化学式,不需要配平方程式)。
(填化学式,不需要配平方程式)。______
③用不同浓度的NaOH溶液吸收 含量不同的尾气,关系如下图:
含量不同的尾气,关系如下图:

(α表示尾气里NO、 中
中 的含量)
的含量)
i.根据上图得知_______ (填字母)。
a.NaOH溶液浓度越大,氮氧化物的吸收率越大
b. 含量越大,氮氧化物的吸收率越大
含量越大,氮氧化物的吸收率越大
ii.当α小于50%时,加入 能提升氮氧化物的吸收率,原因是
能提升氮氧化物的吸收率,原因是_______

(1)①~④各步转化中,属于氮的固定的是
(2)实验室常用加热氯化铵和氢氧化钙固体混合物的方法制取氨气。
①化学方程式是
②干燥氨气不可选用的试剂是
a.浓硫酸 b.碱石灰 c.NaOH固体
(3)工业制硝酸时尾气中含有NO、
 ,可用以下方法吸收:
,可用以下方法吸收:①水吸收法。结合化学方程式说明用水吸收
 的缺陷
的缺陷②NaOH溶液吸收法。发生的反应有:
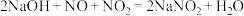 ,
,
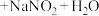 (填化学式,不需要配平方程式)。
(填化学式,不需要配平方程式)。③用不同浓度的NaOH溶液吸收
 含量不同的尾气,关系如下图:
含量不同的尾气,关系如下图:
(α表示尾气里NO、
 中
中 的含量)
的含量)i.根据上图得知
a.NaOH溶液浓度越大,氮氧化物的吸收率越大
b.
 含量越大,氮氧化物的吸收率越大
含量越大,氮氧化物的吸收率越大ii.当α小于50%时,加入
 能提升氮氧化物的吸收率,原因是
能提升氮氧化物的吸收率,原因是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐3】工业上通过氮气和氢气反应合成氨,氨经一系列反应可以得到硝酸。反应如下图所示:

请回答:
(1)合成氨反应的化学方程式是___________ 。
(2)NH3与O2制取NO的化学反应方程式___________ 。
(3)下列说法不正确 的是(选填序号字母)___________ 。
a.氮气可用作保护气
b.铵态氮肥一般不能与碱性化肥共同使用
c.硝酸可用于制化肥、农药、炸药、染料、盐类等
d.某浓硝酸中含有溶质2mol,标准状况下,该浓硝酸与足量的铜完全反应能生成1mol NO2
(4)工业制硝酸时尾气中含有NO、NO2,可用以下方法吸收:
① 水吸收法。结合化学方程式说明用水吸收NO2的缺陷___________ 。
② NaOH溶液吸收法。发生的反应有:
2NaOH + NO + NO2 =2NaNO2+ H2O
NaOH + NO2 ——___________ + NaNO2 + H2O(填化学式,不需要配平方程式)
③ 用不同浓度的NaOH溶液吸收NO2含量不同的尾气,关系如下图:(α 表示尾气里NO、NO2中NO2的含量)
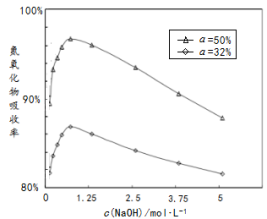
i.根据上图得知___________ (填字母)。
a. NaOH溶液浓度越大,氮氧化物的吸收率越大
b. NO2含量越大,氮氧化物的吸收率越大
ii.当α小于50%时,加入H2O2能提升氮氧化物的吸收率,原因是___________ 。

请回答:
(1)合成氨反应的化学方程式是
(2)NH3与O2制取NO的化学反应方程式
(3)下列说法
a.氮气可用作保护气
b.铵态氮肥一般不能与碱性化肥共同使用
c.硝酸可用于制化肥、农药、炸药、染料、盐类等
d.某浓硝酸中含有溶质2mol,标准状况下,该浓硝酸与足量的铜完全反应能生成1mol NO2
(4)工业制硝酸时尾气中含有NO、NO2,可用以下方法吸收:
① 水吸收法。结合化学方程式说明用水吸收NO2的缺陷
② NaOH溶液吸收法。发生的反应有:
2NaOH + NO + NO2 =2NaNO2+ H2O
NaOH + NO2 ——
③ 用不同浓度的NaOH溶液吸收NO2含量不同的尾气,关系如下图:(α 表示尾气里NO、NO2中NO2的含量)

i.根据上图得知
a. NaOH溶液浓度越大,氮氧化物的吸收率越大
b. NO2含量越大,氮氧化物的吸收率越大
ii.当α小于50%时,加入H2O2能提升氮氧化物的吸收率,原因是
您最近一年使用:0次