某同学研究过氧化钠跟水的反应,进行如下实验:向盛有少量过氧化钠固体的试管中滴加水,直到气体不再放出,加水稀释,将所得溶液平均盛放在两支试管中。一支试管中滴加酚酞试液,溶液变红,半分钟内红色褪去;另一支试管中加入少量二氧化锰,又有气体放出,待气体不再放出后,再滴加酚酞,溶液变红,持久不褪色。
(1)过氧化钠跟水反应可能的化学方程式为_____。
(2)加入二氧化锰后发生反应的化学方程式为_____ ,反应中二氧化锰的作用是_____ 。
(3)根据以上实验,过氧化钠可能的用途是_____ 。(写一种)
(1)过氧化钠跟水反应可能的化学方程式为_____。
A. |
B.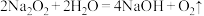 |
C. |
D.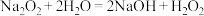 |
(3)根据以上实验,过氧化钠可能的用途是
更新时间:2024-04-10 11:28:13
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】有A、B、C、D、E、F六种物质,它们的相互转化关系如下图(反应条件略)。已知A和B是单质,B、E、F 在常温下为气体,C为淡黄色粉末。
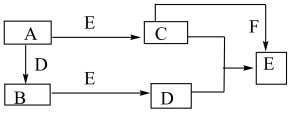
试回答:
(1)写出A、B、的化学式:A__________ ; B__________ 。
(2)写出C和D反应生成E 的化学方程式:_____________________________________ 。
(3)写出C和F反应生成E 的化学方程式:_____________________________________ 。
(4)写出C物质的电子式___________________ ,F的结构式 _____________________ 。
(5)用电子式表示D的形成过程:_______________________________ 。

试回答:
(1)写出A、B、的化学式:A
(2)写出C和D反应生成E 的化学方程式:
(3)写出C和F反应生成E 的化学方程式:
(4)写出C物质的电子式
(5)用电子式表示D的形成过程:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】煤的气化可获得清洁燃料,是实现煤的综合利用的一种重要途径,主要反应是水蒸气与灼热的木炭在高温的条件下能反应生成水煤气(两种气体),G为自然界中常见的一种气体,E与D反应生成F,各物质之间能发生下列反应,请按照要求回答问题。
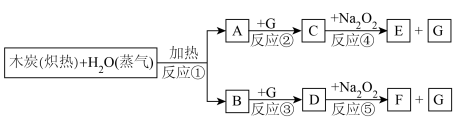
(1)写出下列物质的化学式A:_______ :B:_______ ;
(2)写出C→E的化学方程式:_______ :此反应每生成标准状况下G 11.2L转移电子数为_______ 。
(3)金属钠的两种固态氧化物 与
与 不仅颜色不同,化学性质也不同;
不仅颜色不同,化学性质也不同;
① 中阳离子与阴离子的个数之比为:
中阳离子与阴离子的个数之比为:_______ ;
②如果A和B混合气体6.0g(平均摩尔质量15g/mol)在与足量G充分反应后,通过足量Na2O2层,可使Na2O2增重_______ g;并得到O2_______ mol。

(1)写出下列物质的化学式A:
(2)写出C→E的化学方程式:
(3)金属钠的两种固态氧化物
 与
与 不仅颜色不同,化学性质也不同;
不仅颜色不同,化学性质也不同;①
 中阳离子与阴离子的个数之比为:
中阳离子与阴离子的个数之比为:②如果A和B混合气体6.0g(平均摩尔质量15g/mol)在与足量G充分反应后,通过足量Na2O2层,可使Na2O2增重
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】 A、B、C、D四种元素均属于短周期元素,且原子序数依次增大,A与B能组成原子数之比为2∶1的化合物X和1∶1的化合物Y,D与B也能组成原子数之比为2:1的化合物M和1:1的化合物Z;1molC单质跟X反应放出0.5mol气体B2,1molD单质跟X反应放出11.2L(标准)气体A2,1molZ化合物跟X反应放出0.5mol气体B2。试回答:
(1)A、B、C、D的元素符号:A______ B______ C______ D______
(2)这四种元素形成的四种简单离子的半径大小顺序为______ ;
(3)这四种元素的原子半径大小顺序为______ ;
(4)C与X反应的化学方程式______
(5)Z与X反应的离子方程式______
(1)A、B、C、D的元素符号:A
(2)这四种元素形成的四种简单离子的半径大小顺序为
(3)这四种元素的原子半径大小顺序为
(4)C与X反应的化学方程式
(5)Z与X反应的离子方程式
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】某化学课外兴趣小组探究过氧化钠与水的反应,探究过程如下:
(1)实验1:向包有过氧化钠粉末的脱脂棉上滴水,脱脂棉燃烧起来。请分析脱脂棉燃烧的原因_______ 。
(2)实验2:取一支试管,向其中加入少量过氧化钠固体,然后加入少量蒸馏水,有气泡冒出,充分振荡后再滴入酚酞试液,溶液先变红后褪色。
提出问题:溶液为什么先变红,过了一会,红色又褪去了呢?
猜想:甲同学认为是氢氧化钠溶液与空气中的二氧化碳反应的缘故,乙同学认为甲同学的猜想不正确,理由是碳酸钠溶液显碱性,也能使酚酞试液变红色。
查阅资料:
i.H2O2可以破坏酚酞的结构,使酚酞在碱性溶液中不能再显红色;
ii.NaOH溶液浓度过高,酚酞不变色或变色后迅速褪色。
设计实验方案:
①取少量褪色后的溶液于试管中,加入MnO2固体,若有气泡冒出,用_______ 检验该气体,则证明该反应过程中生成了_______ (填化学式)使溶液褪色。
②另取少量褪色后的溶液于试管中,加入蒸馏水稀释,若溶液变红,则证明溶液褪色原因可能为_______ 。
(3)为进一步探究过氧化钠与水反应的实质,运用pH传感器、温度传感器、氧气传感器等仪器进行实验探究,得到如下图象。
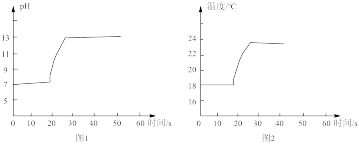
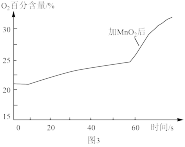
根据图象,得出结论:过氧化钠与水反应过程的方程式为_______ 、_______ 。
(1)实验1:向包有过氧化钠粉末的脱脂棉上滴水,脱脂棉燃烧起来。请分析脱脂棉燃烧的原因
(2)实验2:取一支试管,向其中加入少量过氧化钠固体,然后加入少量蒸馏水,有气泡冒出,充分振荡后再滴入酚酞试液,溶液先变红后褪色。
提出问题:溶液为什么先变红,过了一会,红色又褪去了呢?
猜想:甲同学认为是氢氧化钠溶液与空气中的二氧化碳反应的缘故,乙同学认为甲同学的猜想不正确,理由是碳酸钠溶液显碱性,也能使酚酞试液变红色。
查阅资料:
i.H2O2可以破坏酚酞的结构,使酚酞在碱性溶液中不能再显红色;
ii.NaOH溶液浓度过高,酚酞不变色或变色后迅速褪色。
设计实验方案:
①取少量褪色后的溶液于试管中,加入MnO2固体,若有气泡冒出,用
②另取少量褪色后的溶液于试管中,加入蒸馏水稀释,若溶液变红,则证明溶液褪色原因可能为
(3)为进一步探究过氧化钠与水反应的实质,运用pH传感器、温度传感器、氧气传感器等仪器进行实验探究,得到如下图象。


根据图象,得出结论:过氧化钠与水反应过程的方程式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐2】第IIB族元素(Zn、Cd、Hg)和第VIA族元素(S、Se、Te)组成的某些二元化合物常用作半导体材料,应用十分广泛。
(1)基态Se原子价电子排布式为_______ ,有_______ 种空间运动状态。
(2)碲酸(H6TeO6)是白色固体,经X射线衍射研究证明在碲酸分子内的6个羟基排列在碲原子的周围成八面体结构,碲酸中碲原子的价层电子对数为_______ 。
(3)CdTe可用作太阳能电池的吸收层,研究从太阳能电池的碲化镉吸收层(主要含CdTe、CdS)中回收碲具有重要的意义。某回收工艺的流程如图:

①碲化镉吸收层中的CdTe参与反应的化学方程式为_______ ,该反应需要控制温度为50℃的原因为_______ ;滤渣1含有的一种单质是_______ 。
②常温下,向含Cd2+、Te4+滤液中加入NaOH溶液调节pH,当pH=10时,溶液中c(Cd2+)=_______ 。(已知Ksp[Cd(OH)2]=5.3×10-15)。
(1)基态Se原子价电子排布式为
(2)碲酸(H6TeO6)是白色固体,经X射线衍射研究证明在碲酸分子内的6个羟基排列在碲原子的周围成八面体结构,碲酸中碲原子的价层电子对数为
(3)CdTe可用作太阳能电池的吸收层,研究从太阳能电池的碲化镉吸收层(主要含CdTe、CdS)中回收碲具有重要的意义。某回收工艺的流程如图:

①碲化镉吸收层中的CdTe参与反应的化学方程式为
②常温下,向含Cd2+、Te4+滤液中加入NaOH溶液调节pH,当pH=10时,溶液中c(Cd2+)=
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】过氧化钙 对环境友好,能杀菌消毒净化空气。实验室用大理石为原料制备过氧化钙,反应为
对环境友好,能杀菌消毒净化空气。实验室用大理石为原料制备过氧化钙,反应为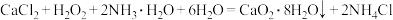 。
。
一、制
I.取适量大理石(含有铁的氧化物等杂质)溶于盐酸,搅拌,至大理石基本完全溶解。
Ⅱ.加水稀释,滴加6%过氧化氢溶液,并用 氨水调节
氨水调节 ,煮沸后趁热过滤,除去
,煮沸后趁热过滤,除去 。
。
Ⅲ.向热滤液中滴加碳酸铵溶液和少量浓氨水,加热搅拌一段时间。
Ⅳ.___________、过滤、洗涤后,将得到的固体置于烧杯中,逐滴加盐酸溶解,产生气泡,并再次煮沸。
二、制
Ⅴ.将Ⅳ所得溶液与过氧化氢、浓氨水混合,放置半小时后抽滤,洗涤, 烘干。
烘干。
回答下列问题:
(1)步骤I中使用的主要玻璃仪器有___________ 。
(2)步骤Ⅱ中除去二价铁的相关离子方程式为___________ ;煮沸后需趁热过滤,目的是___________ ;若在该步骤中使用热抽滤漏斗(见下图),比普通过滤的优点是___________ (写两条)。
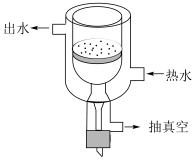
(3)步骤Ⅲ得到的固体主要是___________ (写化学式)。
(4)步骤Ⅳ经“___________ 、过滤、洗涤”,得到纯净固体后加盐酸,如果不进行再次煮沸,可能造成的影响是___________ 。
(5)关于步骤V的操作,下列方案最合理的是___________ (填序号)。
① 溶液
溶液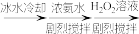
②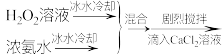
③
 对环境友好,能杀菌消毒净化空气。实验室用大理石为原料制备过氧化钙,反应为
对环境友好,能杀菌消毒净化空气。实验室用大理石为原料制备过氧化钙,反应为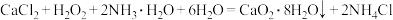 。
。一、制

I.取适量大理石(含有铁的氧化物等杂质)溶于盐酸,搅拌,至大理石基本完全溶解。
Ⅱ.加水稀释,滴加6%过氧化氢溶液,并用
 氨水调节
氨水调节 ,煮沸后趁热过滤,除去
,煮沸后趁热过滤,除去 。
。Ⅲ.向热滤液中滴加碳酸铵溶液和少量浓氨水,加热搅拌一段时间。
Ⅳ.___________、过滤、洗涤后,将得到的固体置于烧杯中,逐滴加盐酸溶解,产生气泡,并再次煮沸。
二、制

Ⅴ.将Ⅳ所得溶液与过氧化氢、浓氨水混合,放置半小时后抽滤,洗涤,
 烘干。
烘干。回答下列问题:
(1)步骤I中使用的主要玻璃仪器有
(2)步骤Ⅱ中除去二价铁的相关离子方程式为

(3)步骤Ⅲ得到的固体主要是
(4)步骤Ⅳ经“
(5)关于步骤V的操作,下列方案最合理的是
①
 溶液
溶液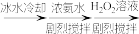
②
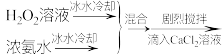
③

您最近一年使用:0次



