A、B、C、D四种元素均属于短周期元素,且原子序数依次增大,A与B能组成原子数之比为2∶1的化合物X和1∶1的化合物Y,D与B也能组成原子数之比为2:1的化合物M和1:1的化合物Z;1molC单质跟X反应放出0.5mol气体B2,1molD单质跟X反应放出11.2L(标准)气体A2,1molZ化合物跟X反应放出0.5mol气体B2。试回答:
(1)A、B、C、D的元素符号:A______ B______ C______ D______
(2)这四种元素形成的四种简单离子的半径大小顺序为______ ;
(3)这四种元素的原子半径大小顺序为______ ;
(4)C与X反应的化学方程式______
(5)Z与X反应的离子方程式______
(1)A、B、C、D的元素符号:A
(2)这四种元素形成的四种简单离子的半径大小顺序为
(3)这四种元素的原子半径大小顺序为
(4)C与X反应的化学方程式
(5)Z与X反应的离子方程式
10-11高一下·河北邢台·阶段练习 查看更多[1]
(已下线)2010—2011学年河北省南宫中学高一3月月考化学试卷
更新时间:2016-12-09 01:42:32
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】甲同学将分别Na2O2与H2O和浓盐酸反应,有如下现象:
实验I中:(1)反应的化学方程式是___ 。
实验Ⅱ中:(2)根据现象②、③,推测生成的气体中可能含有Cl2,产生Cl2的化学方程式是___ 。
(3)若向反应后的溶液中加入少量MnO2,立即产生与实验Ⅰ相同的气体,原因是___ 。
| 实验序号 | 使用药品 | 现象 |
| Ⅰ | Na2O2、H2O | ①试管壁发热 ②有无色无味气体产生 |
| Ⅱ | Na2O2、浓盐酸 | ①试管壁发热 ②有刺激性气味的气体产生 ③反应后所得溶液呈浅黄绿色 |
实验Ⅱ中:(2)根据现象②、③,推测生成的气体中可能含有Cl2,产生Cl2的化学方程式是
(3)若向反应后的溶液中加入少量MnO2,立即产生与实验Ⅰ相同的气体,原因是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】钠是很活泼的金属,在空气中燃烧的产物是Na2O2.Na2O的制取可以通过钠与硝酸钠共热反应完成:Na+NaNO3→Na2O+N2↑(未配平)。请回答下列问题:
(1)上述反应的氧化剂是_______ (写化学式)。制取Na2O时,若金属钠与NaNO3按质量比23∶17投料,充分反应后收集到的气体体积为1.12 m3(标准状况下),则制得的Na2O的质量为_______ kg。
(2)制取Na2O时由于设备密封性不好而进入了少量空气,导致制得的Na2O产品中含有Na2O2杂质。现有Na2O产品m g(假设只含有Na2O2杂质),请从下面选用合适的仪器和试剂,设计一种可选用的实验仪器组合,以完成样品中Na2O含量的测定。
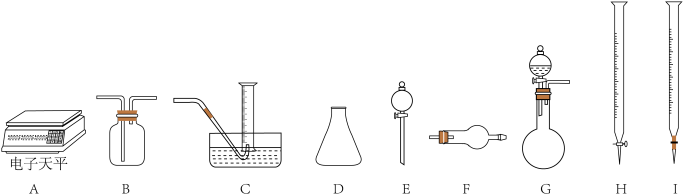
可选用的试剂:a.浓硫酸 b.水 c.盐酸标准溶液 d.NaOH标准溶液e.酚酞 f.碱石灰 g.稀盐酸
(3)某学生设计了以下实验方案来测定该试样中Na2O的质量分数,其操作流程和实验数据如下,该Na2O产品中Na2O的质量分数为_______ 。
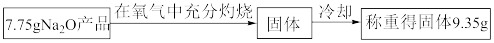
(1)上述反应的氧化剂是
(2)制取Na2O时由于设备密封性不好而进入了少量空气,导致制得的Na2O产品中含有Na2O2杂质。现有Na2O产品m g(假设只含有Na2O2杂质),请从下面选用合适的仪器和试剂,设计一种可选用的实验仪器组合,以完成样品中Na2O含量的测定。

可选用的试剂:a.浓硫酸 b.水 c.盐酸标准溶液 d.NaOH标准溶液e.酚酞 f.碱石灰 g.稀盐酸
| 实验过程中发生反应的化学方程式 | 实验所需仪器(用字母表示) | 实验所需试剂(用字母表示) | 实验需直接测定的有关物理量(用文字说明) |
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】Ⅰ、为测定金属钠样品(表面有 Na2O)中钠单质的质量分数,设计了如下实验(反应装置如图所示):
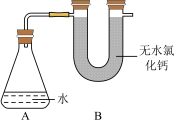
①称量 A、B 的总质量
②称取一定质量的钠样品
③将钠样品投入锥形瓶中,迅速塞紧带 U 形干燥管(内含无水 CaCl2干燥 剂)的橡皮塞 。有关数据是:称取的金属钠样品质量为 a g,A、B反应前总质量为 m g,反应后 A、B 的总质量为 n g。 请根据题意回答下列问题:
(1)A 中钠和水反应过程可看到钠浮在水面,产生这一现象原因是:_____________
(2)用 a、m、n 表示的钠单质的质量分数为_______________
(3)如果没有 B 装置对实验结果有何影响___________ 。(填“偏大”或“偏小”“不影响”)
Ⅱ、现用金属钠和空气制备纯度较高的 Na2O2,可利用的装置如下图。回答下列问题:

(4)上述装置Ⅳ中盛放的试剂是______ ,为完成实验应将装置Ⅳ接在_____ (填写字母号)。
A.I 之前 B. Ⅱ和 Ⅲ 之间 C.I 和Ⅱ 之间 D.Ⅲ之后
(5)点燃酒精灯后,观察到装置 Ⅱ 中的现象为______________ 。
Ⅲ、现用制得纯度较高的 Na2O2进行相关实验。回答下列问题:
(6)用脱脂棉包住Na2O2粉末,置于石棉网上,通过细管向脱脂棉中吹CO2,脱脂棉_______ (填“能”或“不能”)燃烧起来。
(7)盛有1.56 g Na2O2、3.36g NaHCO3的固体混合物放在密闭容器中加热,最后固体是___________ (填化学式),质量为_________ g.
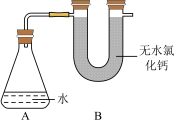
①称量 A、B 的总质量
②称取一定质量的钠样品
③将钠样品投入锥形瓶中,迅速塞紧带 U 形干燥管(内含无水 CaCl2干燥 剂)的橡皮塞 。有关数据是:称取的金属钠样品质量为 a g,A、B反应前总质量为 m g,反应后 A、B 的总质量为 n g。 请根据题意回答下列问题:
(1)A 中钠和水反应过程可看到钠浮在水面,产生这一现象原因是:
(2)用 a、m、n 表示的钠单质的质量分数为
(3)如果没有 B 装置对实验结果有何影响
Ⅱ、现用金属钠和空气制备纯度较高的 Na2O2,可利用的装置如下图。回答下列问题:

(4)上述装置Ⅳ中盛放的试剂是
A.I 之前 B. Ⅱ和 Ⅲ 之间 C.I 和Ⅱ 之间 D.Ⅲ之后
(5)点燃酒精灯后,观察到装置 Ⅱ 中的现象为
Ⅲ、现用制得纯度较高的 Na2O2进行相关实验。回答下列问题:
(6)用脱脂棉包住Na2O2粉末,置于石棉网上,通过细管向脱脂棉中吹CO2,脱脂棉
(7)盛有1.56 g Na2O2、3.36g NaHCO3的固体混合物放在密闭容器中加热,最后固体是
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐1】X、Y、Z、W、Q是元素周期表中原子序数依次增大的五种短周期主族元素,X最外层电子数是内层电子数的2倍,Y的单质与氢气在暗处能剧烈化合并发生爆炸,Z短周期元素中原子半径最大,W其氧化物是两性氧化物,Q同周期元素中,最高价氧化物对应水化物的酸性最强。
(1)元素Y在元素周期表中的位置是___________ 。
(2)Z在氧气中完全燃烧的产物的化学式为___________ 。
(3)Y、W、Q的简单离子半径由大到小的顺序是___________ (用离子符号表示)。
(4)某同学为了比较X元素和硅元素非金属性的相对强弱,用如图所示装置进行实验。___________ 、___________ ;M为___________ (填化学式),其作用是___________ 。
②能说明X元素的非金属性比硅元素强的实验现象是___________ 。
(5)元素Z与W相比,金属性较弱的是___________ (填元素名称),请写出能证明这一结论的实验事实___________ 。(列举一条)
(1)元素Y在元素周期表中的位置是
(2)Z在氧气中完全燃烧的产物的化学式为
(3)Y、W、Q的简单离子半径由大到小的顺序是
(4)某同学为了比较X元素和硅元素非金属性的相对强弱,用如图所示装置进行实验。

②能说明X元素的非金属性比硅元素强的实验现象是
(5)元素Z与W相比,金属性较弱的是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】A、B、C、D、E为原子序数依次增大的短周期元素。A、C处于同一主族,C、D、E处于同一周期,E原子的最外层电子数是A、B、C原子最外层电子数之和,D是地壳中含量最高的金属元素;A、B组成的常见气体甲能使湿润的红色石蕊试纸变蓝;E的单质与甲反应能生成B的单质,同时生成两种水溶液均呈酸性的化合物乙和丙(该反应中氧化产物只有一种),25℃时0.1 mol/L的乙溶液pH>l;D的单质既能与C元素最高价氧化物的水化物的溶液反应生成盐丁,也能与丙的水溶液反应生成盐。
请回答下列问题:
(1)甲的化学式为___________ ;B单质的电子式为____________ 。
(2)D元素的名称是______________ 。
(3)写出丁溶液中通入过量二氧化碳时的离子方程式_______________________
(4)工业上利用A、B的单质合成甲(BA3):B2 (g)+3A2 (g) 2BA3 (g) △H<0,在一定温度下,在2 L密闭容器中,2 mol单质B2和1.6mol单质A2充分反应后达到平衡,测得BA3的物质的量浓度为0.4 mol/L,计算该温度下的平衡常数K=
2BA3 (g) △H<0,在一定温度下,在2 L密闭容器中,2 mol单质B2和1.6mol单质A2充分反应后达到平衡,测得BA3的物质的量浓度为0.4 mol/L,计算该温度下的平衡常数K=______________ 。
(5)E的单质与甲反应生成的乙和丙的物质的量之比为2:4.反应中被氧化的物质与被还原的物质的物质的量之比为______________ 。
请回答下列问题:
(1)甲的化学式为
(2)D元素的名称是
(3)写出丁溶液中通入过量二氧化碳时的离子方程式
(4)工业上利用A、B的单质合成甲(BA3):B2 (g)+3A2 (g)
 2BA3 (g) △H<0,在一定温度下,在2 L密闭容器中,2 mol单质B2和1.6mol单质A2充分反应后达到平衡,测得BA3的物质的量浓度为0.4 mol/L,计算该温度下的平衡常数K=
2BA3 (g) △H<0,在一定温度下,在2 L密闭容器中,2 mol单质B2和1.6mol单质A2充分反应后达到平衡,测得BA3的物质的量浓度为0.4 mol/L,计算该温度下的平衡常数K=(5)E的单质与甲反应生成的乙和丙的物质的量之比为2:4.反应中被氧化的物质与被还原的物质的物质的量之比为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】如图为元素周期表的一部分,请参照元素①~⑧在表中的位置,回答下列问题:

(1)地壳中含量居于第二位的元素是____ 。(填序号)
(2)②的最高价氧化物的分子式为___ ;⑦的最高价氧化物对应水化物的分子式为____ 。
(3)W是第四周期与④同主族的元素。据此推测W不可能具有的性质是___ (填字母)。
A.最高正化合价为+6 B.气态氢化物比H2S稳定
C.最高价氧化物对应水化物的酸性比硫酸弱 D.单质在常温下可与氢气化合
(4)已知Cs元素位于元素周期表中第六周期第IA族,请回答下列问题:
①铯的原子序数为____ 。
②铯单质与H2O反应的化学反应方程式为____ 。
③预测铯单质的还原性比钠单质的还原性_____ (填“弱”或“强”)。
④下列推断正确的是____ (填字母)。
A.与铯处于同一主族的元素都是金属元素
B.铯单质发生反应时,铯原子易失去电子
C.碳酸铯是一种可溶性碱
D.铯离子的氧化性强于钾离子
(5)已知X为第IIA族元素(第一到第四周期),其原子序数为a,Y与X位于同一周期,且为第IIIA族元素,则Y的原子序数b与a所有可能的关系式为___ 。

(1)地壳中含量居于第二位的元素是
(2)②的最高价氧化物的分子式为
(3)W是第四周期与④同主族的元素。据此推测W不可能具有的性质是
A.最高正化合价为+6 B.气态氢化物比H2S稳定
C.最高价氧化物对应水化物的酸性比硫酸弱 D.单质在常温下可与氢气化合
(4)已知Cs元素位于元素周期表中第六周期第IA族,请回答下列问题:
①铯的原子序数为
②铯单质与H2O反应的化学反应方程式为
③预测铯单质的还原性比钠单质的还原性
④下列推断正确的是
A.与铯处于同一主族的元素都是金属元素
B.铯单质发生反应时,铯原子易失去电子
C.碳酸铯是一种可溶性碱
D.铯离子的氧化性强于钾离子
(5)已知X为第IIA族元素(第一到第四周期),其原子序数为a,Y与X位于同一周期,且为第IIIA族元素,则Y的原子序数b与a所有可能的关系式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】下表是元素周期表前20号元素的有关信息:
已知: 的半径为
的半径为 ,
, 的半径为
的半径为
回答下列问题:
(1)元素e在周期表中的位置_______ ,元素y与e同主族且多一电子层,y的原子结构示意图为_______ 。
(2)c、d、g原子半径由大到小的顺序为_______ (填元素符号)。
(3)f的单质与b的常见单质加热条件下反应,产物中含有的化学键类型为_______ 。
(4) 溶液中先加入d元素最高价氧化物对应的水化物,再通入
溶液中先加入d元素最高价氧化物对应的水化物,再通入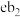 ,可观察到的现象是
,可观察到的现象是_______ ,发生反应的离子方程式为_______ 。
| 元素 | a | b | c | d | e | f | g | h |
原子半径( ) ) | 0.030 | 0.066 | 0.117 | 0.232 | 0.106 | 0.186 | 0.143 | 0.099 |
| 最高正化合价 |  |  |  |  |  |  |  | |
| 最低负化合价 |  |  |  |  |
 的半径为
的半径为 ,
, 的半径为
的半径为
回答下列问题:
(1)元素e在周期表中的位置
(2)c、d、g原子半径由大到小的顺序为
(3)f的单质与b的常见单质加热条件下反应,产物中含有的化学键类型为
(4)
 溶液中先加入d元素最高价氧化物对应的水化物,再通入
溶液中先加入d元素最高价氧化物对应的水化物,再通入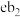 ,可观察到的现象是
,可观察到的现象是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】A、B、C、D、E、F为短周期主族元素,其原子序数依次增大。A、B 两元素最高正价和最低负价之和为零。E和A同主族;D、F是地壳中含量最高的非金属元素和金属元素。
(1)写出C元素的元素名称_______ ,其在周期表中的位置__________________ 。E离子结构示意图为__________________ ;E2D2的电子式________________________ 。
(2)由A、C以原子个数比为5︰1组成的一种化合物,其中各原子均达到稳定结构,该化合物中所含化学键类型为_________________________ 。
(3)E2D2和A2D反应的离子方程式为__________________________________________ 。
(4)由C、E组成的一种离子化合物化学式为E3C,该化合物中两种离子的半径由大到小的顺序是____________ (用元素符号表示);该化合物遇水剧烈反应,该反应的化学方程式为___________________________________ 。
(1)写出C元素的元素名称
(2)由A、C以原子个数比为5︰1组成的一种化合物,其中各原子均达到稳定结构,该化合物中所含化学键类型为
(3)E2D2和A2D反应的离子方程式为
(4)由C、E组成的一种离子化合物化学式为E3C,该化合物中两种离子的半径由大到小的顺序是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】下表是元素周期表的一部分,请回答有关问题:
(1)在①~⑨元素中,最活泼的金属元素是_______ ,最活泼的非金属元素是_______ 。(填元素符号)
(2)在①~⑨元素中,最高价氧化物对应水化物酸性最强的为_______ (写化学式)
(3)②⑤⑧的简单离子半径由小到大的顺序为_______ (写离子符号)
(4)⑦号元素的原子结构示意图为_______ 。写 出其简单离子的电子式_______ 。
(5)与⑦号元素同周期且非金属性强于⑦的元素是_______ (填元素名称),写出能说明这一事实的化学方程式_______ 。
族 周期 | I A | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 1 | ||||||||
| 2 | ① | ② | ||||||
| 3 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |
(2)在①~⑨元素中,最高价氧化物对应水化物酸性最强的为
(3)②⑤⑧的简单离子半径由小到大的顺序为
(4)⑦号元素的原子结构示意图为
(5)与⑦号元素同周期且非金属性强于⑦的元素是
您最近一年使用:0次
【推荐1】 、
、 、
、 、
、 、
、 为元素周期表中前20号元素,其原子序数依次增大。其中
为元素周期表中前20号元素,其原子序数依次增大。其中 、
、 是金属元素;
是金属元素; 和
和 同主族,它们原子的最外层电子排布式均为
同主族,它们原子的最外层电子排布式均为 ;
; 和
和 同主族,它们原子最外层的
同主族,它们原子最外层的 能级电子数是
能级电子数是 能级电子数的2倍;
能级电子数的2倍; 元素原子最外层电子数是
元素原子最外层电子数是 元素原子最外层电子数的
元素原子最外层电子数的 。已知五种元素的电负性为2.5、3.5、0.8、2.1、1.5,请回答下列问题:
。已知五种元素的电负性为2.5、3.5、0.8、2.1、1.5,请回答下列问题:
(1) 是
是______ (填元素符号,下同), 是
是______ , 是
是______ , 是
是______ , 是
是______ 。
(2)五种元素中金属性最强的是______ (填元素符号,下同),非金属性最强的是______ 。
(3)当 与
与 、
、 、
、 分别形成化合物时,
分别形成化合物时, 显
显______ (填“正”或“负”,下同)价,其他元素显______ 价。
(4)当 与
与 、
、 、
、 、
、 分别形成简单化合物(其中
分别形成简单化合物(其中 、
、 、
、 、
、 均显最高价,
均显最高价, 显最低负价)时,化合物中含有离子键的是
显最低负价)时,化合物中含有离子键的是______ (填化学式,下同),含有共价键的是______ 。
 、
、 、
、 、
、 、
、 为元素周期表中前20号元素,其原子序数依次增大。其中
为元素周期表中前20号元素,其原子序数依次增大。其中 、
、 是金属元素;
是金属元素; 和
和 同主族,它们原子的最外层电子排布式均为
同主族,它们原子的最外层电子排布式均为 ;
; 和
和 同主族,它们原子最外层的
同主族,它们原子最外层的 能级电子数是
能级电子数是 能级电子数的2倍;
能级电子数的2倍; 元素原子最外层电子数是
元素原子最外层电子数是 元素原子最外层电子数的
元素原子最外层电子数的 。已知五种元素的电负性为2.5、3.5、0.8、2.1、1.5,请回答下列问题:
。已知五种元素的电负性为2.5、3.5、0.8、2.1、1.5,请回答下列问题:(1)
 是
是 是
是 是
是 是
是 是
是(2)五种元素中金属性最强的是
(3)当
 与
与 、
、 、
、 分别形成化合物时,
分别形成化合物时, 显
显(4)当
 与
与 、
、 、
、 、
、 分别形成简单化合物(其中
分别形成简单化合物(其中 、
、 、
、 、
、 均显最高价,
均显最高价, 显最低负价)时,化合物中含有离子键的是
显最低负价)时,化合物中含有离子键的是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】A、B、C、D、E、F是高中阶段学习的常见单质或化合物,单质A在单质B中燃烧产生苍白色的火焰,产物溶于水得到常见的强酸。化合物C可由B与水反应得到,且C具有强氧化性。化合物D是淡黄色物质,可用于呼吸面具,可由一种活泼金属E在氧气中燃烧得到。D在一定条件下可转化为F,F在工业上可以制肥皂,制玻璃等。根据以上描述,请回答下列问题:
(1)物质F的俗称_______ ,C的化学式为_______ 。
(2)铁钉在B中被锈蚀为棕黄色物质,写出该反应的化学方程式,并用单线桥标出电子转移的方向和数目_______ 。
(3)写出单质E与水反应的离子方程式为_______ 。
(4)200℃时,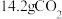 和
和 的混合物气体与足量的D反应,反应后固体增加了6.2g,则原混合物的平均相对分子质量为
的混合物气体与足量的D反应,反应后固体增加了6.2g,则原混合物的平均相对分子质量为_______ , 和
和 的物质的量之比为
的物质的量之比为_______ 。
(1)物质F的俗称
(2)铁钉在B中被锈蚀为棕黄色物质,写出该反应的化学方程式,并用单线桥标出电子转移的方向和数目
(3)写出单质E与水反应的离子方程式为
(4)200℃时,
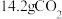 和
和 的混合物气体与足量的D反应,反应后固体增加了6.2g,则原混合物的平均相对分子质量为
的混合物气体与足量的D反应,反应后固体增加了6.2g,则原混合物的平均相对分子质量为 和
和 的物质的量之比为
的物质的量之比为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】X、Y、Z、W、R、Q是原子序数依次增大的短周期主族元素,X、R在元素周期表中的相对位置如图,X与Z能形成两种无色气体,Z是地壳中含量最多的元素,W元素的最高价氧化物的水化物既能与盐酸反应,又能与NaOH溶液反应。
回答下列问题:
(1)X在元素周期表中的位置为_________ ;Y单质的电子式为________ 。
(2)Z、W、R的简单离子半径由大到小的顺序是________ (填离子符号)。
(3)元素的非金属性R________ Q(填“>”或“<”),下列事实不能说明这一结论有_______ (填序号)。
A.H2R的酸性比HQ弱
B.R与Q在周期表中的相对位置
C.向R的氢化物的水溶液中通入Q的单质,溶液变浑浊
D.相同条件下,R和Q的单质分别与Fe反应时,R被还原的价态比Q的低
(4)将盛有YZ2气体的烧瓶浸入热水中,一段时间后,气体颜色将变________ (填“深”或“浅”);烧瓶内气体的平均相对分子质量将________ (填“增大”或“减小”)。
| X | ||
| R |
回答下列问题:
(1)X在元素周期表中的位置为
(2)Z、W、R的简单离子半径由大到小的顺序是
(3)元素的非金属性R
A.H2R的酸性比HQ弱
B.R与Q在周期表中的相对位置
C.向R的氢化物的水溶液中通入Q的单质,溶液变浑浊
D.相同条件下,R和Q的单质分别与Fe反应时,R被还原的价态比Q的低
(4)将盛有YZ2气体的烧瓶浸入热水中,一段时间后,气体颜色将变
您最近一年使用:0次



