氮氧化物、二氧化硫能引发酸雨、雾霾等。研究含氮、含硫物质的转化是工业、农业、医药、环保等领域的重要课题。回答下列问题:
(1)NO2产生硝酸型酸雨的化学方程式为___________ 。
(2)汽车尾气催化转化器可将尾气中的CO、NO均转化为无害气体,该反应的还原产物为___________ 。
(3)目前工业上烟气脱硫脱硝的工艺流程如下:
①“氧化”的目的是___________ 。
②图中产品中含硫成分为___________ (填化学式)。
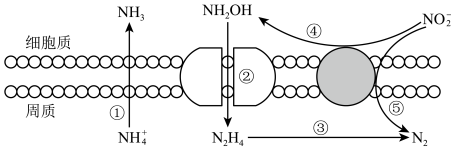
(4)海洋生物参与氮循环的过程如图所示(其它含氮物质不参与反应)。___________ 种价态。反应③和⑤中,若生成等物质的量的N2,则转移的电子数之比为___________ 。
(5)氮及其化合物在催化剂a和催化剂b的作用下转化过程如图所示。下列分析合理的是___________ 。
B.N2与 H2反应属于氮的固定过程
C.在催化剂b表面形成氮氧键时不涉及电子转移
(1)NO2产生硝酸型酸雨的化学方程式为
(2)汽车尾气催化转化器可将尾气中的CO、NO均转化为无害气体,该反应的还原产物为
(3)目前工业上烟气脱硫脱硝的工艺流程如下:
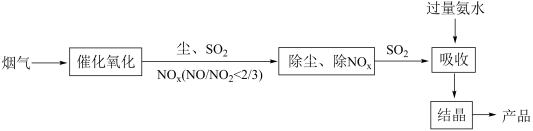
①“氧化”的目的是
②图中产品中含硫成分为
(4)海洋生物参与氮循环的过程如图所示(其它含氮物质不参与反应)。
(5)氮及其化合物在催化剂a和催化剂b的作用下转化过程如图所示。下列分析合理的是
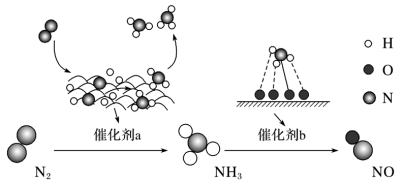
B.N2与 H2反应属于氮的固定过程
C.在催化剂b表面形成氮氧键时不涉及电子转移
更新时间:2024-04-10 12:41:55
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】已知铜在常温下能被稀硝酸溶解,其反应的化学方程式为3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O
(1)化合价升高的元素是_______ ,化合价降低的元素是_______ ,发生氧化反应的物质是_______ ,发生还原反应的物质是_______ 。
(2)用双线桥法表示下列反应中电子得失的方向和数目。
①3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O______
②2H2S + SO2=3S↓+2H2O______
③2FeCl3 +Cu=2FeCl2+CuCl2______
(1)化合价升高的元素是
(2)用双线桥法表示下列反应中电子得失的方向和数目。
①3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O
②2H2S + SO2=3S↓+2H2O
③2FeCl3 +Cu=2FeCl2+CuCl2
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】过氧化钙常温常压下为固体,微溶于水,过氧化钙不通过金属钙来制备。一种制备过氧化钙的方法是在10℃左右向一定量的氧化钙滴加适量过氧化氢溶液,生成 固体。将
固体。将 固体过滤后干燥,得到无水过氧化钙,回答下列问题:
固体过滤后干燥,得到无水过氧化钙,回答下列问题:
(1)氧化钙属于___________ (填“酸性”或“碱性”)氧化物;写出题干中描述的由氧化钙制备 的化学方程式:
的化学方程式:___________ 。
(2)用题干中描述的方法制备的过氧化钙通常不纯且氧化钙和过氧化氢难以完全反应,可能的原因是___________ ;为了检测所制备过氧化钙的纯度,一种常用的方法是将已知质量的待测样品与已知质量的 在酸性溶液中完全反应,计算出待测样品所含过氧化钙的质量,在过氧化钙与
在酸性溶液中完全反应,计算出待测样品所含过氧化钙的质量,在过氧化钙与 的反应中,过氧化钙是
的反应中,过氧化钙是___________ (填“氧化剂”或“还原剂”);
(3)取少量过氧化钙固体于试管中,加热试管,用带火星的木条深入试管口,发现___________ ,说明反应生成一种无色气体;在火力发电厂的烟道气中,二氧化碳约占碳排放总量的40%,因此提高烟道气中二氧化碳的捕集效率十分必要,若在加热条件下以过氧化钙为二氧化碳吸附剂,则吸附过程中发生反应的化学方程式是___________ 。
 固体。将
固体。将 固体过滤后干燥,得到无水过氧化钙,回答下列问题:
固体过滤后干燥,得到无水过氧化钙,回答下列问题:(1)氧化钙属于
 的化学方程式:
的化学方程式:(2)用题干中描述的方法制备的过氧化钙通常不纯且氧化钙和过氧化氢难以完全反应,可能的原因是
 在酸性溶液中完全反应,计算出待测样品所含过氧化钙的质量,在过氧化钙与
在酸性溶液中完全反应,计算出待测样品所含过氧化钙的质量,在过氧化钙与 的反应中,过氧化钙是
的反应中,过氧化钙是(3)取少量过氧化钙固体于试管中,加热试管,用带火星的木条深入试管口,发现
您最近一年使用:0次
【推荐3】回答下列问题:
(1)根据反应8NH3+3Cl2=6NH4Cl+N2。
①氧化剂是__ ,还原剂是__ ,氧化产物是__ 。
②氧化剂与还原剂的分子数之比为__ 。
③当生成28gN2时被氧化的物质为__ g。
(2)高铁酸钠(Na2FeO4)(铁为+6价)是一种新型的净水剂,可以通过下述反应制取:2Fe(OH)3+4NaOH+3NaClO=2Na2FeO4+3NaCl+5H2O。
①该反应中氧化剂是__ (用化学式表示,下同),__ 元素被氧化,还原产物为___ 。
②用双线桥在方程式中标出电子转移的情况:__ 。
(1)根据反应8NH3+3Cl2=6NH4Cl+N2。
①氧化剂是
②氧化剂与还原剂的分子数之比为
③当生成28gN2时被氧化的物质为
(2)高铁酸钠(Na2FeO4)(铁为+6价)是一种新型的净水剂,可以通过下述反应制取:2Fe(OH)3+4NaOH+3NaClO=2Na2FeO4+3NaCl+5H2O。
①该反应中氧化剂是
②用双线桥在方程式中标出电子转移的情况:
您最近一年使用:0次
【推荐1】Ⅰ、一定条件下,RO3n-和氟气(F2)可发生如下反应:RO3n-+F2+2OH-===RO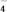 +2F-+H2O,从而可知在RO3n-中,元素R的化合价是
+2F-+H2O,从而可知在RO3n-中,元素R的化合价是________
Ⅱ、某同学写出以下三个化学方程式(未配平):
①NO+HNO3 N2O3+H2O
N2O3+H2O
②NH3+NO HNO2+H2O
HNO2+H2O
③N2O4+H2O HNO3+HNO2
HNO3+HNO2
三个反应中,一定不可能实现的是______ ;在反应①中若消耗NO 15 g,转移电子______ mol。
Ⅲ、已知Ix-和Cl2发生如下反应Ix- + Cl2 + H2O = Cl- + IO3- + H+若KIx(Ix-)与Cl2的系数之比为1∶8,则x值为_________ 。
 +2F-+H2O,从而可知在RO3n-中,元素R的化合价是
+2F-+H2O,从而可知在RO3n-中,元素R的化合价是Ⅱ、某同学写出以下三个化学方程式(未配平):
①NO+HNO3
 N2O3+H2O
N2O3+H2O②NH3+NO
 HNO2+H2O
HNO2+H2O③N2O4+H2O
 HNO3+HNO2
HNO3+HNO2三个反应中,一定不可能实现的是
Ⅲ、已知Ix-和Cl2发生如下反应Ix- + Cl2 + H2O = Cl- + IO3- + H+若KIx(Ix-)与Cl2的系数之比为1∶8,则x值为
您最近一年使用:0次
填空题
|
适中
(0.64)
【推荐2】研究NO2、SO2 、CO等大气污染气体的处理具有重要意义。
(1)NO2可用水吸收,相应的化学反应方程式为_________________ 。利用反应6NO2+ 8NH3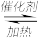 7N2+12H2O也可处理NO2。当转移1.2mol电子时,消耗的NO2在标准状况下是
7N2+12H2O也可处理NO2。当转移1.2mol电子时,消耗的NO2在标准状况下是________________ L。
(2)已知:2SO2(g)+O2(g) 2SO3(g) ΔH=−196.6 kJ·mol-1
2SO3(g) ΔH=−196.6 kJ·mol-1
2NO(g)+O2(g) 2NO2(g) ΔH=−113.0 kJ·mol-1
2NO2(g) ΔH=−113.0 kJ·mol-1
则反应NO2(g)+SO2(g) SO3(g)+NO(g)的ΔH=
SO3(g)+NO(g)的ΔH=_____________ kJ·mol-1。
一定条件下,将NO2与SO2以体积比1:2置于密闭容器中发生上述反应,下列能说明反应达到平衡状态的是__________ 。
a.体系压强保持不变 b.混合气体颜色保持不变
c.SO3和NO的体积比保持不变 d.每消耗1 mol SO3的同时生成1 molNO2
测得上述反应平衡时NO2与SO2体积比为1:6,则平衡常数K=_________ 。
(1)NO2可用水吸收,相应的化学反应方程式为
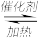 7N2+12H2O也可处理NO2。当转移1.2mol电子时,消耗的NO2在标准状况下是
7N2+12H2O也可处理NO2。当转移1.2mol电子时,消耗的NO2在标准状况下是(2)已知:2SO2(g)+O2(g)
 2SO3(g) ΔH=−196.6 kJ·mol-1
2SO3(g) ΔH=−196.6 kJ·mol-12NO(g)+O2(g)
 2NO2(g) ΔH=−113.0 kJ·mol-1
2NO2(g) ΔH=−113.0 kJ·mol-1则反应NO2(g)+SO2(g)
 SO3(g)+NO(g)的ΔH=
SO3(g)+NO(g)的ΔH=一定条件下,将NO2与SO2以体积比1:2置于密闭容器中发生上述反应,下列能说明反应达到平衡状态的是
a.体系压强保持不变 b.混合气体颜色保持不变
c.SO3和NO的体积比保持不变 d.每消耗1 mol SO3的同时生成1 molNO2
测得上述反应平衡时NO2与SO2体积比为1:6,则平衡常数K=
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】(一)为了有效实现NO和NO2的相互转化,设计如图实验:按图组装好实验装置,并检查装置气密性,实验前用排水法收集半瓶NO气体。
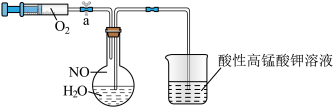
(1)打开止水夹,推动针筒活塞,使氧气进入烧瓶,观察到的现象是______ ,产生此现象的化学方程式为______ 。
(2)关上止水夹,轻轻摇动烧瓶,观察的现象为①______ ;②______ ,产生此现象的化学方程式为____ 。
(3)烧杯中盛放的是酸性高锰酸钾溶液,能吸收尾气,已知NO能与MnO 在酸性条件下反应生成NO
在酸性条件下反应生成NO 和Mn2+,写出该反应的离子方程式
和Mn2+,写出该反应的离子方程式_____ 。
(二)有关氮循环是近年来科学研究的一个热点,含氮物质有如图转换关系:
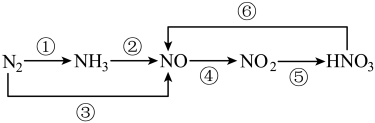
(4)转化⑤中,氧化剂与还原剂的物质的量之比为_____ 。
(5)转化②是工业生成硝酸的关键步骤,写出该转化的化学方程式______ 。

(1)打开止水夹,推动针筒活塞,使氧气进入烧瓶,观察到的现象是
(2)关上止水夹,轻轻摇动烧瓶,观察的现象为①
(3)烧杯中盛放的是酸性高锰酸钾溶液,能吸收尾气,已知NO能与MnO
 在酸性条件下反应生成NO
在酸性条件下反应生成NO 和Mn2+,写出该反应的离子方程式
和Mn2+,写出该反应的离子方程式(二)有关氮循环是近年来科学研究的一个热点,含氮物质有如图转换关系:

(4)转化⑤中,氧化剂与还原剂的物质的量之比为
(5)转化②是工业生成硝酸的关键步骤,写出该转化的化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】一定体积的NO2气体依次通过盛有以下物质的容器,饱和NaHCO3溶液→浓H2SO4→固体Na2O2,发生反应的化学方程式是:
(1)___________ ;
(2)___________ ;
(3)___________ ;
(4)___________ 。
(1)
(2)
(3)
(4)
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】回答下列问题:
(1)氮元素及其化合物的转化关系如图:

①写出X的化学式:____ 。
②图中所示,NO2转化为HNO3的反应方程式:____ 。
③关于②的反应,下列说法正确的是____ 。
a.氮元素的化合价不发生变化
b.若用NO2与H2O反应制取HNO3,另一种生成物可能是NO
c.该转化过程中,NO2既是氧化剂,又是还原剂
(2)某同学利用如图所示的装置,胶头滴管b和烧杯c中装有水,f为弹簧夹。进行氨气的喷泉实验,回答下列问题:
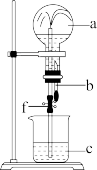
①仪器a的名称是____ 。
②写出实验室用NH4Cl和Ca(OH)2制取氨气的化学方程式:____ 。
③喷泉实验前需要在仪器A中充满干燥的氨气,可用____ (填“向上”或“向下”排空气法收集氨气;可用____ (填“浓硫酸”或“碱石灰)干燥氨气。
④引发喷泉实验的操作是____ 。
(1)氮元素及其化合物的转化关系如图:

①写出X的化学式:
②图中所示,NO2转化为HNO3的反应方程式:
③关于②的反应,下列说法正确的是
a.氮元素的化合价不发生变化
b.若用NO2与H2O反应制取HNO3,另一种生成物可能是NO
c.该转化过程中,NO2既是氧化剂,又是还原剂
(2)某同学利用如图所示的装置,胶头滴管b和烧杯c中装有水,f为弹簧夹。进行氨气的喷泉实验,回答下列问题:

①仪器a的名称是
②写出实验室用NH4Cl和Ca(OH)2制取氨气的化学方程式:
③喷泉实验前需要在仪器A中充满干燥的氨气,可用
④引发喷泉实验的操作是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】《自然》杂志曾报道我国科学家通过测量SiO2中26Al和10Be两种元素的比例确定“北京人”年龄的研究结果,这种测量方法叫“铝铍测年法”。完成下列填空:
(1)l0Be和9Be___ (填序号)。
a.是同一种原子 b.具有相同的中子数
c.具有相同的化学性质 d.互为同位素
(2)写出A1(OH)3与NaOH溶液反应的化学方程式:___ 。
(3)研究表明28A1可以衰变为26Mg,可以比较这两种元素金属性强弱的方法是__ (填序号)。
a.比较Mg(OH)2与A1(OH)3的碱性强弱
b.比较这两种元素的最高正化合价
c.将打磨过表面积相同的镁条和铝片分别和100℃热水作用,并滴入酚酞溶液
d.比较这两种金属的硬度和熔点
(4)目前还有一种测量方法叫“钾氩测年法”。
两种常见简单阴离子的核外电子排布与Ar相同,两者的半径大小关系为:___ (用化学符号表示);其中一种离子与钾同周期相邻元素的离子所形成的化合物可用作干燥剂,用电子式表示该物质的形成过程:___ 。
(1)l0Be和9Be
a.是同一种原子 b.具有相同的中子数
c.具有相同的化学性质 d.互为同位素
(2)写出A1(OH)3与NaOH溶液反应的化学方程式:
(3)研究表明28A1可以衰变为26Mg,可以比较这两种元素金属性强弱的方法是
a.比较Mg(OH)2与A1(OH)3的碱性强弱
b.比较这两种元素的最高正化合价
c.将打磨过表面积相同的镁条和铝片分别和100℃热水作用,并滴入酚酞溶液
d.比较这两种金属的硬度和熔点
(4)目前还有一种测量方法叫“钾氩测年法”。
两种常见简单阴离子的核外电子排布与Ar相同,两者的半径大小关系为:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】在高锰酸钾固体上滴加浓盐酸,马上产生黄绿色气体。反应的化学方程式为:2KMnO4 + 16HCl=2KC1 + 2MnCl2 + 5C12↑+ 8H2O
回答下列问题:
(1)此反应中的氧化剂是____ ,当在标准状况下产生0.112L氯气,转移的电子数为____ mol。
(2)氯原子的核电荷数为______ ;氧原子的原子结构示意图_______ 。
(3)在KC1固体中存在的化学键是__________ ;写出H2O电子式_________ 。
(4)工业上用氯气与消石灰作原料制造漂粉精,此反应的化学方程式是_________ 。
(5)浓盐酸的溶质是氯化氢,用一个实验证明氯化氢极易溶于水。_________ 。
回答下列问题:
(1)此反应中的氧化剂是
(2)氯原子的核电荷数为
(3)在KC1固体中存在的化学键是
(4)工业上用氯气与消石灰作原料制造漂粉精,此反应的化学方程式是
(5)浓盐酸的溶质是氯化氢,用一个实验证明氯化氢极易溶于水。
您最近一年使用:0次

 Cr2O72-
Cr2O72- Cr3+
Cr3+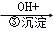 Cr(OH)3↓
Cr(OH)3↓

