关于配合物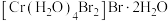 的说法错误的是
的说法错误的是
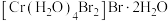 的说法错误的是
的说法错误的是| A.1 mol该配合物与足量AgNO3溶液反应生成1 mol AgBr |
| B.中心原子的配位数为6 |
| C.中心原子的化合价为+3价 |
| D.中心原子Cr采取sp3杂化 |
更新时间:2024-04-01 21:39:55
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】向盛有硫酸铜溶液的试管中滴加氨水,先生成难溶物,继续滴加氨水,难溶物溶解,得到深蓝色透明溶液。下列对此现象的说法正确的是( )
| A.反应后溶液中不存在任何沉淀,所以反应前后Cu2+的浓度不变 |
| B.沉淀溶解后,生成深蓝色的配离子[Cu(NH3)4]2+ |
| C.配位化合物中只有配位键 |
| D.在[Cu(NH3)4]2+配离子中,Cu2+给出孤电子对,NH3提供空轨道 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】如图是三种含铂元素抗癌药物的结构(按药物开发的时间排序)。顺铂进入人体细胞发生水解的产物之一Pt(NH3)2(OH)Cl会与DNA结合,破坏DNA结构,从而防止癌细胞增殖。下列说法正确的是


| A.顺铂中Cl-的配位能力强于NH3 |
| B.顺铂和碳铂完全水解的含铂产物相同 |
| C.碳铂中含有的化学键为离子键、共价键、配位键和氢键 |
| D.1 mol奥沙利铂中含配体4 mol |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】已知某紫色配合物的组成为CoCl3·5NH3·H2O,其水溶液显弱酸性,加入强碱并加热至沸腾有NH3放出,同时产生Co2O3沉淀;向一定量该配合物溶液中加过量AgNO3溶液,有AgCl沉淀生成,待沉淀完全后过滤,再加过量AgNO3溶液于滤液中,无明显变化,但加热至沸腾又有AgCl沉淀生成,且第二次沉淀量为第一次沉淀量的二分之一,则该配合物的化学式最可能为
A.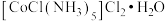 | B.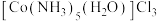 |
C.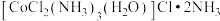 | D.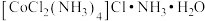 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】已知水合肼( )具有较强还原性,通常可被氧化为
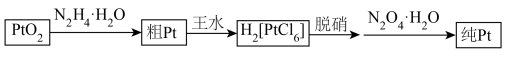
)具有较强还原性,通常可被氧化为 。现用如下流程可制得较纯的单质Pt,下列有关说法不正确的是
。现用如下流程可制得较纯的单质Pt,下列有关说法不正确的是
 )具有较强还原性,通常可被氧化为
)具有较强还原性,通常可被氧化为 。现用如下流程可制得较纯的单质Pt,下列有关说法不正确的是
。现用如下流程可制得较纯的单质Pt,下列有关说法不正确的是
| A.王水是由浓盐酸与浓硝酸组成,与粗Pt反应时浓硝酸表现出强氧化性 |
B.已知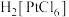 是配合物,则中心原子是Pt,配位数为6 是配合物,则中心原子是Pt,配位数为6 |
C.脱硝除去残余的 和氮氧化物,主要目的是防止其污染环境 和氮氧化物,主要目的是防止其污染环境 |
D.由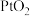 制得1mol纯Pt,理论上至少需要2mol 制得1mol纯Pt,理论上至少需要2mol 作还原剂 作还原剂 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】柠檬酸因具有酸性和较好的络合性,可用于浸出金属离子并得到柠檬酸浸出液。下图是从柠檬酸浸出液中分离出铜并制备碱式碳酸铜: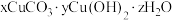 的流程
的流程

实验:(1)调pH值分离铜时,理论上铜离子完全沉淀时pH为6.67,本实验中测得pH=8时铜的沉淀率仅为7.2%,远小干理论分析结果
(2)“还原法沉铜”的步骤中,利用抗坏血酸C6H8O6能有效的将Cu(OH)2还原成金属Cu,抗坏血酸C6H8O6易被氧化为脱氢抗坏血酸C6H6O6;且受热易分解。
(3)相同条件下温度对Cu沉淀率的影响是:随着温度的升高,相同时间内Cu的沉淀率先逐渐增加,在80℃时达到最高点,后略有下降。
(4)实验称取9.55g碱式碳酸铜 产品,通入氢气充分加热反应后,得到4.8g固体残留物,同时生成2.2g二氧化碳和2.7g水。
产品,通入氢气充分加热反应后,得到4.8g固体残留物,同时生成2.2g二氧化碳和2.7g水。
则下列说法不正确的是
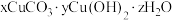 的流程
的流程
实验:(1)调pH值分离铜时,理论上铜离子完全沉淀时pH为6.67,本实验中测得pH=8时铜的沉淀率仅为7.2%,远小干理论分析结果
(2)“还原法沉铜”的步骤中,利用抗坏血酸C6H8O6能有效的将Cu(OH)2还原成金属Cu,抗坏血酸C6H8O6易被氧化为脱氢抗坏血酸C6H6O6;且受热易分解。
(3)相同条件下温度对Cu沉淀率的影响是:随着温度的升高,相同时间内Cu的沉淀率先逐渐增加,在80℃时达到最高点,后略有下降。
(4)实验称取9.55g碱式碳酸铜
 产品,通入氢气充分加热反应后,得到4.8g固体残留物,同时生成2.2g二氧化碳和2.7g水。
产品,通入氢气充分加热反应后,得到4.8g固体残留物,同时生成2.2g二氧化碳和2.7g水。则下列说法不正确的是
A.经过计算碱式碳酸铜的化学式组成为 |
| B.调pH分离铜时,因Cu2+与柠檬酸根形成配合物,则与OH-形成Cu(OH)2减少 |
C.抗坏血酸还原Cu(OH)2的化学反应方程式为: |
| D.温度超过80℃时,因抗坏血酸受热易分解,使浓度降低,还原铜的能力减弱 |
您最近一年使用:0次
【推荐2】钼在钢铁、化工、医药等领域应用广泛。以辉钼矿(主要成分为MoS2,含少量SiO2、CuO等)为原料制备Mo的工艺流程如图所示。下列说法错误的是


| A.“焙烧”时还原剂与氧化剂的物质的量之比为2:9 |
B.滤渣1为 ,滤渣3为PbS ,滤渣3为PbS |
C.“碱浸”时CuO发生反应的离子方程式: |
| D.整个过程中含钼元素物质间转化发生两个氧化还原反应 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】某物质的实验式为PtCl4·2NH3,其水溶液不导电,加入AgNO3溶液反应也不产生沉淀,用强碱处理并没有NH3放出,则下列有关说法中正确的是
| A.NH3与NO3-中氮原子的杂化方式相同 | B.配合物中心离子的电荷数和配位数均为4 |
| C.PtCl4·2NH3的立体构型为正八面体形 | D.Cl-和NH3分子均与中心离子Pt4+配位 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】设NA为阿伏加德罗常数的值,下列叙述正确的是
| A.1mol[Cu(NH3)4]2+中σ键的数目为12NA |
| B.23gCH3CH2OH中为sp3杂化的原子数为NA |
| C.0.5molSF6中S的价层电子对数为3NA |
| D.甲烷酸性燃料电池中正极有1mol气体反应时转移的电子数目2NA |
您最近一年使用:0次

 具有对称的空间结构,
具有对称的空间结构, 个
个 被
被 取代,能得到
取代,能得到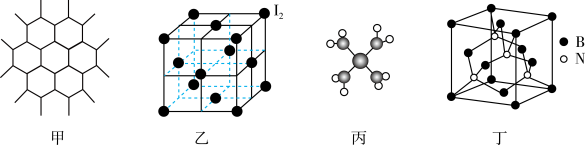
 石墨烯中,含3
石墨烯中,含3 键
键 分子周围有12个紧邻的I2分子
分子周围有12个紧邻的I2分子

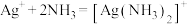
 溶液,然后再滴加2滴硫氰化钾溶液。
溶液,然后再滴加2滴硫氰化钾溶液。 中由
中由 提供孤电子对,
提供孤电子对, 提供空轨道
提供空轨道 和
和
 中含
中含 键的物质的量为
键的物质的量为


