N2CO分子呈链状结构,最稳定Lewis结构式中形式电荷为0的N原子数为x,采用sp2杂化的N原子数为y,则x、y分别为
| A.1,2 | B.4,1.2 | C.2,2 | D.2,1 |
更新时间:2024-04-26 16:11:25
|
【知识点】 利用杂化轨道理论判断分子的空间构型解读
相似题推荐
单选题
|
较难
(0.4)
解题方法
【推荐1】W、R、X、Y、Z是原子半径依次增大的前两周期主族元素,Y原子基态电子排布中有2个单电子,Z原子基态电子排布中无单电子。W、R、X、Z四种元素可以组成 型离子化合物,阴阳离子皆由两种元素组成,且均为正四面体形。下列说法正确的是
型离子化合物,阴阳离子皆由两种元素组成,且均为正四面体形。下列说法正确的是
 型离子化合物,阴阳离子皆由两种元素组成,且均为正四面体形。下列说法正确的是
型离子化合物,阴阳离子皆由两种元素组成,且均为正四面体形。下列说法正确的是A.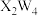 属于极性分子, 属于极性分子,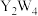 属于非极性分子 属于非极性分子 |
| B.阴阳离子的VSEPR模型不同 |
| C.X的氢化物沸点一定大于Y的氢化物沸点 |
| D.Y与H、O、Na四种元素组成物质的水溶液一定显碱性 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】某种离子液体的结构如图示,X、Y、Z、M、R为原子序数依次增大的短周期元素,Z的质子数等于X、Y的质子数之和,R为电负性最大的元素。下列说法正确的是
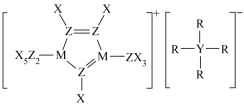
| A.Y的电负性大于Z |
| B.M、X形成的化合物分子间易形成氢键 |
| C.阴离子的空间构型为平面四边形 |
| D.分子的极性:MR3<YR3 |
您最近一年使用:0次


 结构示意图,该离子内存在极性键、配位键、离子键
结构示意图,该离子内存在极性键、配位键、离子键 和
和 原子围成的最小六元环为平面结构
原子围成的最小六元环为平面结构 原子的电子云图,一个黑点表示一个电子
原子的电子云图,一个黑点表示一个电子 晶体的晶胞示意图,
晶体的晶胞示意图, 填充在由
填充在由 构成的正四面体空隙中
构成的正四面体空隙中

