有机物在生产生活中应用广泛,某实验小组以“有机物结构的测定方法”和“配合物结构的测定方法”为研究课题设计了如下实验。
I.有机物结构的确定方法
①取6.8g该有机物A试样通过上述装置完全反应,装置甲增重3.6g,装置乙增重17.6g。
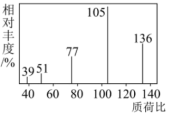
②用质谱仪测定有机物A的相对分子质量,得到如图所示的质谱图。
③用核磁共振仪处理该化合物,所得核磁共振氢谱图中4组峰的面积之比是1:2:2:3。
(1)若没有装置丙,可能带来的影响是___________ 。
(2)由上述已知条件可推出有机物A的分子式为___________ 。
(3)已知有机物A属于芳香族化合物,与乙酸的官能团种类相同,请写出其结构简式:___________ 。
Ⅱ.配合物结构的测定方法
已知:①Co的此类配合物离子较稳定,但加碱再煮沸可促进其内界解离,如: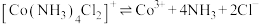 。
。
②下述实验所得样品中的Co元素为+3价,Co3+的配位数为6。
某兴趣小组用Cl-取代 离子中NH3制得配合物
离子中NH3制得配合物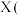 化学式为
化学式为 。该实验小组用以下方法测定所得配合物的组成。
。该实验小组用以下方法测定所得配合物的组成。
实验步骤:取mgX样品加入过量浓NaOH溶液,煮沸,将生成的NH3通入20mL0.20mol/L的稀硫酸(过量)中,再用0.1000mol/LNaOH标准溶液滴定剩余H2SO4溶液。
(4)该配合物中,配体NH3分子中的配位原子为___________ 原子(填原子符号)。
(5)若滴定过程平均消耗NaOH标准溶液20.00mL,则样品中含有NH3的物质的量为___________ mol。
(6)为了减小实验误差,上述中和滴定实验应选择___________ (填“甲基橙”或“酚酞”)做指示剂。
(7)另取mgX样品,加入过量HNO3酸化后,用AgNO3溶液滴定测得n(Cl-)=0.0036mol。请用配合物的形式表示该样品的组成:___________ 。
I.有机物结构的确定方法
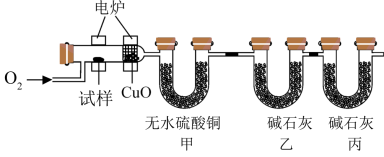
①取6.8g该有机物A试样通过上述装置完全反应,装置甲增重3.6g,装置乙增重17.6g。
②用质谱仪测定有机物A的相对分子质量,得到如图所示的质谱图。
③用核磁共振仪处理该化合物,所得核磁共振氢谱图中4组峰的面积之比是1:2:2:3。
(1)若没有装置丙,可能带来的影响是
(2)由上述已知条件可推出有机物A的分子式为
(3)已知有机物A属于芳香族化合物,与乙酸的官能团种类相同,请写出其结构简式:
Ⅱ.配合物结构的测定方法
已知:①Co的此类配合物离子较稳定,但加碱再煮沸可促进其内界解离,如:
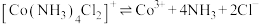 。
。②下述实验所得样品中的Co元素为+3价,Co3+的配位数为6。
某兴趣小组用Cl-取代
 离子中NH3制得配合物
离子中NH3制得配合物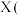 化学式为
化学式为 。该实验小组用以下方法测定所得配合物的组成。
。该实验小组用以下方法测定所得配合物的组成。实验步骤:取mgX样品加入过量浓NaOH溶液,煮沸,将生成的NH3通入20mL0.20mol/L的稀硫酸(过量)中,再用0.1000mol/LNaOH标准溶液滴定剩余H2SO4溶液。
(4)该配合物中,配体NH3分子中的配位原子为
(5)若滴定过程平均消耗NaOH标准溶液20.00mL,则样品中含有NH3的物质的量为
(6)为了减小实验误差,上述中和滴定实验应选择
(7)另取mgX样品,加入过量HNO3酸化后,用AgNO3溶液滴定测得n(Cl-)=0.0036mol。请用配合物的形式表示该样品的组成:
更新时间:2024-05-04 23:08:16
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】某化学兴趣小组设计如图所示装置,用 晶体和
晶体和 获取无水
获取无水 ,并回收过量的
,并回收过量的 。回答下列问题:
。回答下列问题:
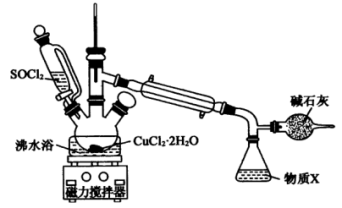
已知:① 的熔点为-105℃,沸点为76℃,遇水剧烈水解生成两种酸性气体;
的熔点为-105℃,沸点为76℃,遇水剧烈水解生成两种酸性气体;
②三颈烧瓶中发生反应的化学方程式是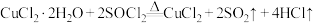 。
。
(1)图中盛有碱石灰的仪器名称为______ ,它的作用是______ 。
(2)由实验可知可以重复利用的物质为______ (填化学式)。
(3)某同学用“间接碘量法”测定无水 样品中铜元素的百分含量,过程如下:取0.6000g试样溶于水,加入过量KI固体,充分反应,生成白色CuI沉淀。滴入几滴淀粉溶液作指示剂,向其中加入
样品中铜元素的百分含量,过程如下:取0.6000g试样溶于水,加入过量KI固体,充分反应,生成白色CuI沉淀。滴入几滴淀粉溶液作指示剂,向其中加入 标准溶液,到达显色终点时,消耗
标准溶液,到达显色终点时,消耗 标准溶液40.00mL(发生反应
标准溶液40.00mL(发生反应 )。
)。
求该试样中铜元素的百分含量______ (保留小数点后一位)(写出计算过程)。
 晶体和
晶体和 获取无水
获取无水 ,并回收过量的
,并回收过量的 。回答下列问题:
。回答下列问题:
已知:①
 的熔点为-105℃,沸点为76℃,遇水剧烈水解生成两种酸性气体;
的熔点为-105℃,沸点为76℃,遇水剧烈水解生成两种酸性气体;②三颈烧瓶中发生反应的化学方程式是
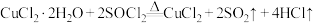 。
。(1)图中盛有碱石灰的仪器名称为
(2)由实验可知可以重复利用的物质为
(3)某同学用“间接碘量法”测定无水
 样品中铜元素的百分含量,过程如下:取0.6000g试样溶于水,加入过量KI固体,充分反应,生成白色CuI沉淀。滴入几滴淀粉溶液作指示剂,向其中加入
样品中铜元素的百分含量,过程如下:取0.6000g试样溶于水,加入过量KI固体,充分反应,生成白色CuI沉淀。滴入几滴淀粉溶液作指示剂,向其中加入 标准溶液,到达显色终点时,消耗
标准溶液,到达显色终点时,消耗 标准溶液40.00mL(发生反应
标准溶液40.00mL(发生反应 )。
)。求该试样中铜元素的百分含量
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】硫氰化钾(KSCN)是中学化学实验室的常见药品,某化学小组用图所示实验装置模拟工业制备硫氰化钾,并进行相关实验探究。

已知:①NH3不溶于CS2,CS2易挥发。
②滴加KOH溶液前,B中三颈烧瓶内发生反应CS2+3NH3 NH4SCN+NH4HS。
NH4SCN+NH4HS。
回答下列问题:
(1)装置A试管中反应的化学方程式为_______ 。
(2)装置B中盛装KOH溶液的仪器名称是_______ ,三颈烧瓶的下层CS2液体必须浸没导气管口,目的是便于充分反应和_______ 。
(3)装置B三颈烧瓶中的水除了溶解无机物外,还起到的作用是_______ 。
(4)制备KSCN晶体:待装置B三颈烧瓶内CS2和NH3充分反应后,熄灭装置A的酒精灯,关闭K1,打开K2,滴入适量KOH溶液,写出反应生成KSCN的化学方程式_______ 。反应完成后,先滤去三颈烧瓶中的固体催化剂,滤液经过_______ (填操作名称),取上层液体减压蒸发浓缩、冷却结晶、过滤、洗涤、干燥,得到硫氰化钾晶体。
(5)测定晶体中KSCN的含量:称取10.00g样品,配成1000mL溶液,取25.00mL溶液于锥形瓶中,加入适量稀硝酸,再加入几滴Fe(NO3)3溶液作指示剂,用0.1000mol∙L-1AgNO3标准溶液滴定,滴定时发生反应:SCN-+Ag+=AgSCN↓(白色),平均消耗AgNO3标准溶液24.50mL。
①刚好沉淀完时,锥形瓶中溶液的颜色变化是_______ 。
②晶体中KSCN的质量分数为_______ 。

已知:①NH3不溶于CS2,CS2易挥发。
②滴加KOH溶液前,B中三颈烧瓶内发生反应CS2+3NH3
 NH4SCN+NH4HS。
NH4SCN+NH4HS。回答下列问题:
(1)装置A试管中反应的化学方程式为
(2)装置B中盛装KOH溶液的仪器名称是
(3)装置B三颈烧瓶中的水除了溶解无机物外,还起到的作用是
(4)制备KSCN晶体:待装置B三颈烧瓶内CS2和NH3充分反应后,熄灭装置A的酒精灯,关闭K1,打开K2,滴入适量KOH溶液,写出反应生成KSCN的化学方程式
(5)测定晶体中KSCN的含量:称取10.00g样品,配成1000mL溶液,取25.00mL溶液于锥形瓶中,加入适量稀硝酸,再加入几滴Fe(NO3)3溶液作指示剂,用0.1000mol∙L-1AgNO3标准溶液滴定,滴定时发生反应:SCN-+Ag+=AgSCN↓(白色),平均消耗AgNO3标准溶液24.50mL。
①刚好沉淀完时,锥形瓶中溶液的颜色变化是
②晶体中KSCN的质量分数为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】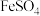 溶液放置在空气中容易变质,因此为了方便使用
溶液放置在空气中容易变质,因此为了方便使用 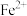 ,实验室常保存摩尔盐
,实验室常保存摩尔盐 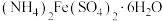 ,它比绿矾或绿矾溶液更稳定。回答下列问题。
,它比绿矾或绿矾溶液更稳定。回答下列问题。
(1)摩尔盐的制备。
①配制溶液以及后续使用的蒸馏水都必须煮沸、冷却后使用:通常向配制的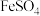 溶液中加入少量铁屑并滴加硫酸,目的是
溶液中加入少量铁屑并滴加硫酸,目的是___________ ;向 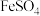 溶液中加入饱和的
溶液中加入饱和的 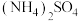 溶液,经过蒸发、冷却结晶、过滤、洗涤和干燥得到摩尔盐晶体。
溶液,经过蒸发、冷却结晶、过滤、洗涤和干燥得到摩尔盐晶体。
② 离子物质的量浓度相同的
离子物质的量浓度相同的 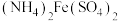 和
和 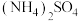 溶液相比较,物质的量浓度大小关系为:前者
溶液相比较,物质的量浓度大小关系为:前者___________ 后者(填“大于”“等于”或“小于”)。
(2)测定摩尔盐的纯度。酸性 作氧化还原滴定的氧化剂时被还原为
作氧化还原滴定的氧化剂时被还原为 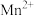 。
。
①滴定时将 溶液加入
溶液加入___________ (填“酸式”或“碱式”)滴定管,在规格为 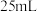 的滴定管中,若
的滴定管中,若  溶液的起始读数为
溶液的起始读数为  ,此时滴定管中
,此时滴定管中  溶液的实际体积为
溶液的实际体积为___________ (填标号)。
A.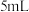 B.
B.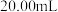 C.大于
C.大于 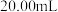 D.小于
D.小于 
②准确称量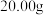 摩尔盐晶体[摩尔质量为
摩尔盐晶体[摩尔质量为 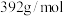 ]样品,配成溶液
]样品,配成溶液 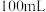 ,分别取3份
,分别取3份 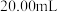 所配溶液于锥形瓶中,加稀硫酸酸化,分别用
所配溶液于锥形瓶中,加稀硫酸酸化,分别用 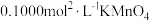 溶液滴定,到达终点所用体积分别为
溶液滴定,到达终点所用体积分别为 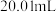 、
、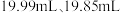 ,则滴定
,则滴定 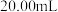 所配溶液消耗
所配溶液消耗 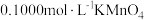 溶液的体积为
溶液的体积为___________ 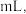 产品摩尔盐
产品摩尔盐 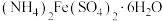 的质量分数为
的质量分数为___________ 。
③下列操作可能导致测定结果偏大的是___________ 。
A.配溶液定容时俯视刻度线
B.取摩尔盐溶液的滴定管没有润洗
C.取待测液的锥形瓶洗净后未干燥
D.酸式滴定管滴定前读数正确,滴定后仰视读数
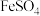 溶液放置在空气中容易变质,因此为了方便使用
溶液放置在空气中容易变质,因此为了方便使用 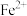 ,实验室常保存摩尔盐
,实验室常保存摩尔盐 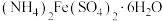 ,它比绿矾或绿矾溶液更稳定。回答下列问题。
,它比绿矾或绿矾溶液更稳定。回答下列问题。(1)摩尔盐的制备。
①配制溶液以及后续使用的蒸馏水都必须煮沸、冷却后使用:通常向配制的
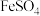 溶液中加入少量铁屑并滴加硫酸,目的是
溶液中加入少量铁屑并滴加硫酸,目的是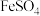 溶液中加入饱和的
溶液中加入饱和的 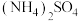 溶液,经过蒸发、冷却结晶、过滤、洗涤和干燥得到摩尔盐晶体。
溶液,经过蒸发、冷却结晶、过滤、洗涤和干燥得到摩尔盐晶体。②
 离子物质的量浓度相同的
离子物质的量浓度相同的 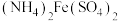 和
和 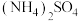 溶液相比较,物质的量浓度大小关系为:前者
溶液相比较,物质的量浓度大小关系为:前者(2)测定摩尔盐的纯度。酸性
 作氧化还原滴定的氧化剂时被还原为
作氧化还原滴定的氧化剂时被还原为 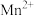 。
。①滴定时将
 溶液加入
溶液加入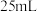 的滴定管中,若
的滴定管中,若  溶液的起始读数为
溶液的起始读数为  ,此时滴定管中
,此时滴定管中  溶液的实际体积为
溶液的实际体积为A.
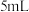 B.
B.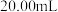 C.大于
C.大于 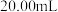 D.小于
D.小于 
②准确称量
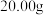 摩尔盐晶体[摩尔质量为
摩尔盐晶体[摩尔质量为 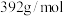 ]样品,配成溶液
]样品,配成溶液 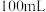 ,分别取3份
,分别取3份 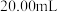 所配溶液于锥形瓶中,加稀硫酸酸化,分别用
所配溶液于锥形瓶中,加稀硫酸酸化,分别用 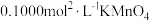 溶液滴定,到达终点所用体积分别为
溶液滴定,到达终点所用体积分别为 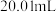 、
、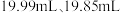 ,则滴定
,则滴定 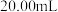 所配溶液消耗
所配溶液消耗 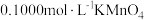 溶液的体积为
溶液的体积为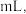 产品摩尔盐
产品摩尔盐 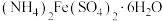 的质量分数为
的质量分数为③下列操作可能导致测定结果偏大的是
A.配溶液定容时俯视刻度线
B.取摩尔盐溶液的滴定管没有润洗
C.取待测液的锥形瓶洗净后未干燥
D.酸式滴定管滴定前读数正确,滴定后仰视读数
您最近一年使用:0次
解答题-有机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】I.回答下列问题:
(1)烃A的结构简式为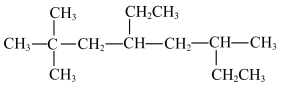 ,用系统命名法命名烃A:
,用系统命名法命名烃A:___________ 。
(2)某烃的分子式为C5H12,核磁共振氢谱图中显示4个峰,则该烃的一氯代物有___________ 种,该烃的结构简式为___________ 。
Ⅱ.有机物C常用于食品行业。已知9.0gC在足量O2中充分燃烧,将生成的混合气体依次通过足量的浓硫酸和碱石灰,分别增重5.4g和13.2g,经检验剩余气体为O2。
(3)C分子的质谱图如图所示,从图中可知其相对分子质量是___________ ,则C的分子式___________ 。___________ 。
(5)C分子的核磁共振氢谱有4个峰,峰面积之比是 ,则C的结构简式是
,则C的结构简式是___________ 。
(1)烃A的结构简式为
 ,用系统命名法命名烃A:
,用系统命名法命名烃A:(2)某烃的分子式为C5H12,核磁共振氢谱图中显示4个峰,则该烃的一氯代物有
Ⅱ.有机物C常用于食品行业。已知9.0gC在足量O2中充分燃烧,将生成的混合气体依次通过足量的浓硫酸和碱石灰,分别增重5.4g和13.2g,经检验剩余气体为O2。
(3)C分子的质谱图如图所示,从图中可知其相对分子质量是
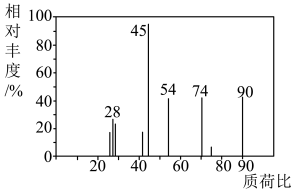
(5)C分子的核磁共振氢谱有4个峰,峰面积之比是
 ,则C的结构简式是
,则C的结构简式是
您最近一年使用:0次
解答题-有机推断题
|
适中
(0.65)
解题方法
【推荐2】已知:
请根据下图回答

(1)E中含有的官能团的名称是___________ ;③的反应类型是___________ , C跟新制的氢氧化铜反应的化学方程式为:___________ .
(2)已知B的相对分子质量为162,其燃烧产物中n(CO2):n(H2O)=2:1.则B的分子式为__________ , F的分子式为______________ .
(3)在电脑芯片生产领域,高分子光阻剂是光刻蚀0.11μm线宽芯片的关键技术.F是这种高分子光阻剂生产中的主要原料.F具有如下特点:①能跟FeCl3溶液发生显色反应;②能发生加聚反应;③芳环上的一氯代物只有两种.F在一定条件下发生加聚反应的化学方程式为:_____________ .
(4)化合物G是F的同分异构体,它属于芳香族化合物,能发生银镜反应.G可能有__________ 种结构,写出其中任意一种同分异构体的结构简式_______________ .

请根据下图回答

(1)E中含有的官能团的名称是
(2)已知B的相对分子质量为162,其燃烧产物中n(CO2):n(H2O)=2:1.则B的分子式为
(3)在电脑芯片生产领域,高分子光阻剂是光刻蚀0.11μm线宽芯片的关键技术.F是这种高分子光阻剂生产中的主要原料.F具有如下特点:①能跟FeCl3溶液发生显色反应;②能发生加聚反应;③芳环上的一氯代物只有两种.F在一定条件下发生加聚反应的化学方程式为:
(4)化合物G是F的同分异构体,它属于芳香族化合物,能发生银镜反应.G可能有
您最近一年使用:0次
解答题-有机推断题
|
适中
(0.65)
名校
【推荐1】某烃A 0.2mol在氧气中充分燃烧后,生成化合物B、C各1.2mol。
(1)烃A的分子式为___________ 。
(2)若取一定量的烃A完全燃烧后,生成B、C各3mol,则有_______ g烃A参加了反应,燃烧时消耗标准状况下的氧气________ L。
(3)若烃A不能使溴水褪色,但在一定条件下,能与氯气发生取代反应,其一氯代物只有一种,则烃A的结构简式为_______________ ;请用适当文字说明你的推断理由:__________________________________ 。
(4)若烃A能使溴水褪色,在催化剂作用下,与H2加成,其加成产物经测定,分子中含有4个甲基,烃A可能的结构简式为____________________________________ (写一个);比烃A少2个碳原子的同系物有___________ 种同分异构体,其中能和H2发生加成反应生成2-甲基丙烷的烯烃的名称是______________ 。
(1)烃A的分子式为
(2)若取一定量的烃A完全燃烧后,生成B、C各3mol,则有
(3)若烃A不能使溴水褪色,但在一定条件下,能与氯气发生取代反应,其一氯代物只有一种,则烃A的结构简式为
(4)若烃A能使溴水褪色,在催化剂作用下,与H2加成,其加成产物经测定,分子中含有4个甲基,烃A可能的结构简式为
您最近一年使用:0次
解答题-有机推断题
|
适中
(0.65)
名校
【推荐2】填空题
(1)①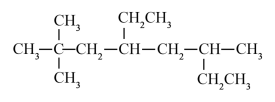 的一氯代物具有不同沸点的产物有
的一氯代物具有不同沸点的产物有_______ 种。
②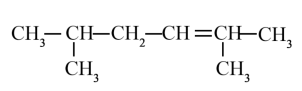 系统命名的名称为
系统命名的名称为_______ 。
③写出 丁烯在一定条件下加聚产物的结构简式
丁烯在一定条件下加聚产物的结构简式_______ 。
(2)按要求回答下列问题:
某烃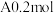 在氧气中完全燃烧后,生成化合物B、C各
在氧气中完全燃烧后,生成化合物B、C各 ,试回答:
,试回答:
①烃A的分子式为_______ ;
②若烃A不能使溴水褪色,但在一定条件下能与氯气发生取代反应,其一氯代物只有一种,则此烃A的结构简式为_______ 。
③若烃A能使溴水褪色,在催化剂作用下与 加成,其加成产物分子中含有4个甲基,烃A可能的结构简式有
加成,其加成产物分子中含有4个甲基,烃A可能的结构简式有_______ 种。
(3)请完成下列转化的化学方程式(注明反应条件)。
①甲苯与浓硝酸、浓硫酸混合制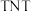
_______ ;
②1,3-丁二烯制备1,4-二溴-2-丁烯_______ 。
(1)①
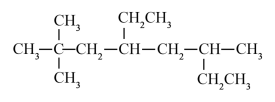 的一氯代物具有不同沸点的产物有
的一氯代物具有不同沸点的产物有②
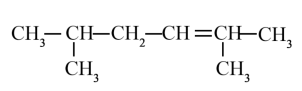 系统命名的名称为
系统命名的名称为③写出
 丁烯在一定条件下加聚产物的结构简式
丁烯在一定条件下加聚产物的结构简式(2)按要求回答下列问题:
某烃
 在氧气中完全燃烧后,生成化合物B、C各
在氧气中完全燃烧后,生成化合物B、C各 ,试回答:
,试回答:①烃A的分子式为
②若烃A不能使溴水褪色,但在一定条件下能与氯气发生取代反应,其一氯代物只有一种,则此烃A的结构简式为
③若烃A能使溴水褪色,在催化剂作用下与
 加成,其加成产物分子中含有4个甲基,烃A可能的结构简式有
加成,其加成产物分子中含有4个甲基,烃A可能的结构简式有(3)请完成下列转化的化学方程式(注明反应条件)。
①甲苯与浓硝酸、浓硫酸混合制
②1,3-丁二烯制备1,4-二溴-2-丁烯
您最近一年使用:0次
解答题-有机推断题
|
适中
(0.65)
名校
【推荐3】金刚烷是一种重要的化工原料,工业上可通过下列途径制备:
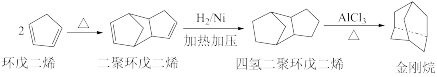
请回答下列问题:
(1)环戊二烯分子中最多有__ 个原子共平面。
(2)金刚烷的分子式为__ ,其二氯代物有_ 种。
(3)已知烯烃能发生如下反应:
 。
。
请写出下列反应产物的结构简式: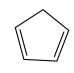

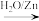
__ 。
(4)A是二聚环戊二烯的同分异构体,能使溴的四氯化碳溶液褪色,A经高锰酸钾酸性溶液加热氧化可以得到对苯二甲酸 提示:苯环上的烷基(—CH3,—CH2R,—CHR2)或烯基侧链经高锰酸钾酸性溶液氧化得羧基
提示:苯环上的烷基(—CH3,—CH2R,—CHR2)或烯基侧链经高锰酸钾酸性溶液氧化得羧基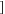 ,写出A所有可能的结构简式
,写出A所有可能的结构简式 不考虑立体异构
不考虑立体异构 :
:__ 。
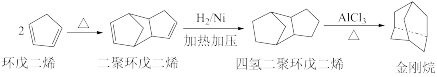
请回答下列问题:
(1)环戊二烯分子中最多有
(2)金刚烷的分子式为
(3)已知烯烃能发生如下反应:
 。
。请写出下列反应产物的结构简式:


(4)A是二聚环戊二烯的同分异构体,能使溴的四氯化碳溶液褪色,A经高锰酸钾酸性溶液加热氧化可以得到对苯二甲酸
 提示:苯环上的烷基(—CH3,—CH2R,—CHR2)或烯基侧链经高锰酸钾酸性溶液氧化得羧基
提示:苯环上的烷基(—CH3,—CH2R,—CHR2)或烯基侧链经高锰酸钾酸性溶液氧化得羧基 ,写出A所有可能的结构简式
,写出A所有可能的结构简式 不考虑立体异构
不考虑立体异构 :
:
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐1】铬、钼(Mo)、钨(W)都是ⅥB族元素,且原子序数依次增大,它们的单质和化合物在科学研究和工业生产中有广泛应用。
(1)基态钼原子的价电子排布式为___ 。
(2)钼可作有机合成的催化剂。例如,苯甲醛被还原成环己基甲醇,反应如下:
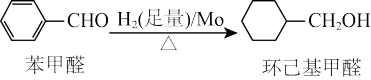
①环己基甲醇分子中采取sp3杂化方式的原子共有___ 个。
②苯甲醛分子中的所有π电子形成了一个大π键,其中的π电子数目为___ 个。
③相同温度下环己基甲醇的饱和蒸气压___ (填“大于”或“小于”)苯甲醛。
(3)配合物[Cr(OH)3(H2O)(H2NCH2CH2NH2)]中,中心离子的配位数为___ 。
(4)铬的一种氧化物的晶胞结构如图所示。
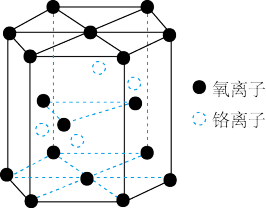
①该氧化物的化学式为___ 。
②已知晶胞底面的边长为acm,晶胞的高为bcm,NA代表阿伏加德罗常数的值,该铬的氧化物的摩尔质量为Mg/mol。该晶体的密度为___ g/cm3(用含a、b、NA和M的代数式表示。)
(1)基态钼原子的价电子排布式为
(2)钼可作有机合成的催化剂。例如,苯甲醛被还原成环己基甲醇,反应如下:
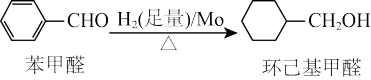
①环己基甲醇分子中采取sp3杂化方式的原子共有
②苯甲醛分子中的所有π电子形成了一个大π键,其中的π电子数目为
③相同温度下环己基甲醇的饱和蒸气压
(3)配合物[Cr(OH)3(H2O)(H2NCH2CH2NH2)]中,中心离子的配位数为
(4)铬的一种氧化物的晶胞结构如图所示。

①该氧化物的化学式为
②已知晶胞底面的边长为acm,晶胞的高为bcm,NA代表阿伏加德罗常数的值,该铬的氧化物的摩尔质量为Mg/mol。该晶体的密度为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】乙酸锰可用于制造钠离子电池的负极材料。可用如下反应制得乙酸锰:4Mn(NO3)2•6H2O+26(CH3CO)2O=4(CH3COO)3Mn+8HNO2+3O2↑+40CH3COOH
(1)Mn3+基态核外电子排布式为___ 。
(2)NO 中氮原子轨道的杂化类型是
中氮原子轨道的杂化类型是__ 。
(3)与HNO2互为等电子体的一种阴离子的化学式为___ 。
(4)配合物[Mn(CH3OH)6]2+中配位原子是___ 。
(5)CH3COOH能与H2O任意比混溶的原因,除它们都是极性分子外还有___ 。
(6)镁铝合金经过高温淬火获得一种储钠材料,其晶胞为立方结构(如图所示),图中原子位于顶点或面心。该晶体中每个铝原子周围距离最近的镁原子数目为___ ,该立方晶胞的晶胞的密度为dg·cm-3,设阿伏加德罗常数的值为NA,则该晶胞中镁铝之间的最近距离为___ pm。(列出计算式,可不化简)。
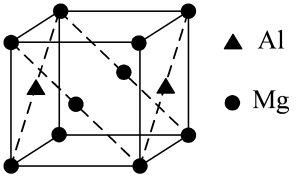
(1)Mn3+基态核外电子排布式为
(2)NO
 中氮原子轨道的杂化类型是
中氮原子轨道的杂化类型是(3)与HNO2互为等电子体的一种阴离子的化学式为
(4)配合物[Mn(CH3OH)6]2+中配位原子是
(5)CH3COOH能与H2O任意比混溶的原因,除它们都是极性分子外还有
(6)镁铝合金经过高温淬火获得一种储钠材料,其晶胞为立方结构(如图所示),图中原子位于顶点或面心。该晶体中每个铝原子周围距离最近的镁原子数目为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】某合金基体是铁碳合金,还含有一定量的Cr、Ni、Cu、C等元素。回答下列问题:
(1)基态碳原子核外电子所处的最高能层符号为_______ ,基态 的外围电子排布图为
的外围电子排布图为_______ 。
(2)六羰基铬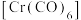 中
中 键和
键和 键的个数比为
键的个数比为_______ ,与CO互为等电子体的是_______ 。
A. B.
B.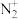 C.
C. D.
D. E.
E.
(3)完成下列含碳化合物相关分析: 杂化的碳原子有
杂化的碳原子有_______ 个。 是离子晶体,其晶格能可通过Born-Haber循环计算得到。
是离子晶体,其晶格能可通过Born-Haber循环计算得到。_______ (填“能”或“不能”)计算出Cu原子的第一电离能, 的晶格能为
的晶格能为_______  。
。
(5) 的晶胞结构如图所示,A的原子坐标参数为
的晶胞结构如图所示,A的原子坐标参数为 ,B为
,B为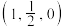 ,则C的原子坐标为
,则C的原子坐标为_______ ;已知该晶体的密度为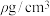 ,
, 和
和 的半径分别为
的半径分别为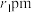 和
和 ,
, 代表阿伏加德罗常数的值,则该晶胞中离子的空间利用率为
代表阿伏加德罗常数的值,则该晶胞中离子的空间利用率为_______ (用代数式表示)。
(1)基态碳原子核外电子所处的最高能层符号为
 的外围电子排布图为
的外围电子排布图为(2)六羰基铬
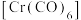 中
中 键和
键和 键的个数比为
键的个数比为A.
 B.
B.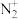 C.
C. D.
D. E.
E.
(3)完成下列含碳化合物相关分析:
A.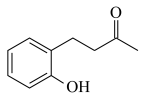 B.
B.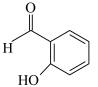
 杂化的碳原子有
杂化的碳原子有②B的沸点低于对羟基苯甲醛( )的沸点,其原因是
)的沸点,其原因是
 是离子晶体,其晶格能可通过Born-Haber循环计算得到。
是离子晶体,其晶格能可通过Born-Haber循环计算得到。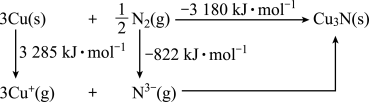
 的晶格能为
的晶格能为 。
。(5)
 的晶胞结构如图所示,A的原子坐标参数为
的晶胞结构如图所示,A的原子坐标参数为 ,B为
,B为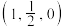 ,则C的原子坐标为
,则C的原子坐标为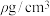 ,
, 和
和 的半径分别为
的半径分别为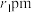 和
和 ,
, 代表阿伏加德罗常数的值,则该晶胞中离子的空间利用率为
代表阿伏加德罗常数的值,则该晶胞中离子的空间利用率为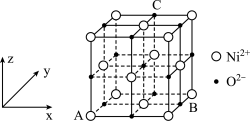
您最近一年使用:0次



