某合金基体是铁碳合金,还含有一定量的Cr、Ni、Cu、C等元素。回答下列问题:
(1)基态碳原子核外电子所处的最高能层符号为_______ ,基态 的外围电子排布图为
的外围电子排布图为_______ 。
(2)六羰基铬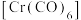 中
中 键和
键和 键的个数比为
键的个数比为_______ ,与CO互为等电子体的是_______ 。
A. B.
B.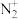 C.
C. D.
D. E.
E.
(3)完成下列含碳化合物相关分析: 杂化的碳原子有
杂化的碳原子有_______ 个。 是离子晶体,其晶格能可通过Born-Haber循环计算得到。
是离子晶体,其晶格能可通过Born-Haber循环计算得到。_______ (填“能”或“不能”)计算出Cu原子的第一电离能, 的晶格能为
的晶格能为_______  。
。
(5) 的晶胞结构如图所示,A的原子坐标参数为
的晶胞结构如图所示,A的原子坐标参数为 ,B为
,B为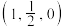 ,则C的原子坐标为
,则C的原子坐标为_______ ;已知该晶体的密度为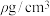 ,
, 和
和 的半径分别为
的半径分别为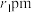 和
和 ,
, 代表阿伏加德罗常数的值,则该晶胞中离子的空间利用率为
代表阿伏加德罗常数的值,则该晶胞中离子的空间利用率为_______ (用代数式表示)。
(1)基态碳原子核外电子所处的最高能层符号为
 的外围电子排布图为
的外围电子排布图为(2)六羰基铬
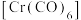 中
中 键和
键和 键的个数比为
键的个数比为A.
 B.
B.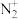 C.
C. D.
D. E.
E.
(3)完成下列含碳化合物相关分析:
A.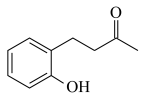 B.
B.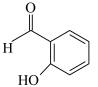
 杂化的碳原子有
杂化的碳原子有②B的沸点低于对羟基苯甲醛( )的沸点,其原因是
)的沸点,其原因是
 是离子晶体,其晶格能可通过Born-Haber循环计算得到。
是离子晶体,其晶格能可通过Born-Haber循环计算得到。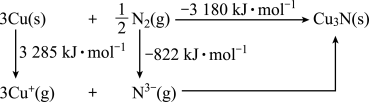
 的晶格能为
的晶格能为 。
。(5)
 的晶胞结构如图所示,A的原子坐标参数为
的晶胞结构如图所示,A的原子坐标参数为 ,B为
,B为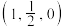 ,则C的原子坐标为
,则C的原子坐标为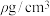 ,
, 和
和 的半径分别为
的半径分别为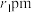 和
和 ,
, 代表阿伏加德罗常数的值,则该晶胞中离子的空间利用率为
代表阿伏加德罗常数的值,则该晶胞中离子的空间利用率为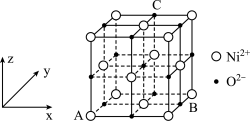
更新时间:2024-03-26 12:20:32
|
相似题推荐
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】现今世界,新药物、新材料层出不穷。
(1)香料材料苯丙烯醇(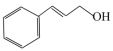 )中可能共面的碳原子数最多有
)中可能共面的碳原子数最多有______ 个。苯丙酮(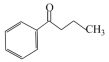 )不溶于水,苯丙烯醇(
)不溶于水,苯丙烯醇( )溶于水,二者溶解度相差较大的主要原因是
)溶于水,二者溶解度相差较大的主要原因是______ 。
(2)纳米二氧化钛 是一种光催化剂,常用于污水处理。其中一个实例如图所示。
是一种光催化剂,常用于污水处理。其中一个实例如图所示。
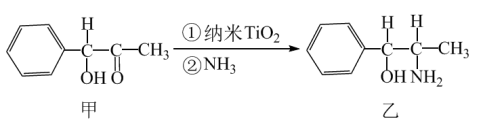
①化合物乙的分子中采取 杂化方式的原子有C和
杂化方式的原子有C和______ 。(填元素符号)
②碳原子连接4个不同的原子或原子团时,称为手性碳原子。一个化合物乙分子中含有______ 个手性碳原子。
③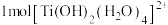 中
中 键的数目为
键的数目为______ 。
(3)砷化镓属于第三代半导体,晶胞结构与金刚石相似,如图所示。
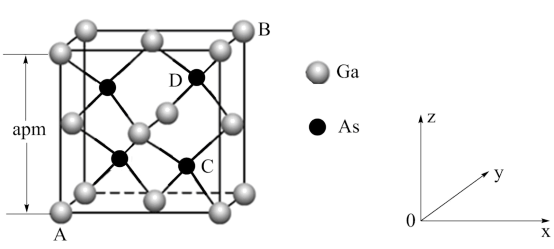
①砷化镓晶胞中镓原子的配位数为______ 。
② 原子占据的是
原子占据的是 原子围成的
原子围成的______ 空隙(填几何空间构型)。
③晶胞中原子坐标参数A为 ,B为
,B为 ,C
,C ,则D为
,则D为______ 。
④阿伏加 德罗常数的值为 ,砷化镓的密度为
,砷化镓的密度为______ 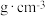 (列出计算式)
(列出计算式)
(1)香料材料苯丙烯醇(
 )中可能共面的碳原子数最多有
)中可能共面的碳原子数最多有 )不溶于水,苯丙烯醇(
)不溶于水,苯丙烯醇( )溶于水,二者溶解度相差较大的主要原因是
)溶于水,二者溶解度相差较大的主要原因是(2)纳米二氧化钛
 是一种光催化剂,常用于污水处理。其中一个实例如图所示。
是一种光催化剂,常用于污水处理。其中一个实例如图所示。
①化合物乙的分子中采取
 杂化方式的原子有C和
杂化方式的原子有C和②碳原子连接4个不同的原子或原子团时,称为手性碳原子。一个化合物乙分子中含有
③
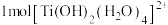 中
中 键的数目为
键的数目为(3)砷化镓属于第三代半导体,晶胞结构与金刚石相似,如图所示。

①砷化镓晶胞中镓原子的配位数为
②
 原子占据的是
原子占据的是 原子围成的
原子围成的③晶胞中原子坐标参数A为
 ,B为
,B为 ,C
,C ,则D为
,则D为④阿伏加 德罗常数的值为
 ,砷化镓的密度为
,砷化镓的密度为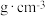 (列出计算式)
(列出计算式)
您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】元素X 位于第四周期,其基态原子的内层轨道全部排满电子,且最外层电子数为2。元素Y基态原子的3p 轨道上有4个电子。元素Z 的原子最外层电子数是其内层的3倍。
(1)在Y的氢化物(H2Y)分子中,Y原子轨道的杂化类型是__________ 。
(2)Z的氢化物(H2Z)在乙醇中的溶解度大于H2Y,其原因是________________ 。
(3)Y 与Z 可形成YZ42-
①YZ42-的空间构型为________ (用文字描述)。
②写出一种与YZ42-互为等电子体的分子的化学式:______________ 。
(4)X的氯化物与氨水反应可形成配合物[X(NH3)4]Cl2,1mol该配合物中含有σ键的数目为________________ 。
(1)在Y的氢化物(H2Y)分子中,Y原子轨道的杂化类型是
(2)Z的氢化物(H2Z)在乙醇中的溶解度大于H2Y,其原因是
(3)Y 与Z 可形成YZ42-
①YZ42-的空间构型为
②写出一种与YZ42-互为等电子体的分子的化学式:
(4)X的氯化物与氨水反应可形成配合物[X(NH3)4]Cl2,1mol该配合物中含有σ键的数目为
您最近半年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】[化学——选修3:物质结构与性质]
Ⅰ.CuCl和CuCl2都是重要的化工原料,常用作催化剂、颜料、防腐剂和消毒剂等。
已知:①CuCl可以由CuCl2用适当的还原剂如SO2、SnCl2等还原制得:
2Cu2++2Cl-+SO2+2H2O 2CuCl↓+4H++SO42-
2CuCl↓+4H++SO42-
2CuCl2+SnCl2===2CuCl↓+SnCl4
②CuCl2溶液与乙二胺(H2N—CH2—CH2—NH2)可形成配离子:
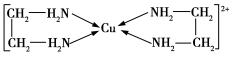
请回答下列问题:
(1)H、N、O三种元素的电负性由大到小的顺序是______________ 。
(2)SO2分子的空间构型为__________ ;与SnCl4互为等电子体的一种离子的化学式为____________ 。
(3)乙二胺分子中氮原子轨道的杂化类型为______________ 。乙二胺和三甲胺[N(CH3)3]均属于胺,但乙二胺比三甲胺的沸点高的多,原因是__________________________________ 。
(4)②中所形成的配离子中含有的化学键类型有________ (填字母)。
a.配位键 b.极性键 c.离子键 d.非极性键
Ⅱ.固体二氧化碳外形似冰,受热汽化无液体产生,俗称“干冰”,根据干冰晶胞结构回答:
(5)干冰中1个分子周围有________ 个紧邻分子。
(6)堆积方式与干冰晶胞类型相同的金属有________ (从“Cu、Mg、K、Po”中选出正确的),其空间利用率为________________ 。
Ⅲ.钇钡铜氧的晶胞结构如图。研究发现,此高温超导体中的铜元素有两种价态:+2价和+3价。
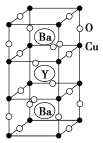
(7)根据图示晶胞结构,推算晶体中Y、Cu、Ba和O原子个数比,确定其化学式为________________ 。
(8)根据(7)所推出的化合物的组成(该化合物中各元素的化合价为Y+3,Ba+2),计算该物质中+2价和+3价的铜离子个数比为____________ 。
Ⅰ.CuCl和CuCl2都是重要的化工原料,常用作催化剂、颜料、防腐剂和消毒剂等。
已知:①CuCl可以由CuCl2用适当的还原剂如SO2、SnCl2等还原制得:
2Cu2++2Cl-+SO2+2H2O
 2CuCl↓+4H++SO42-
2CuCl↓+4H++SO42-2CuCl2+SnCl2===2CuCl↓+SnCl4
②CuCl2溶液与乙二胺(H2N—CH2—CH2—NH2)可形成配离子:

请回答下列问题:
(1)H、N、O三种元素的电负性由大到小的顺序是
(2)SO2分子的空间构型为
(3)乙二胺分子中氮原子轨道的杂化类型为
(4)②中所形成的配离子中含有的化学键类型有
a.配位键 b.极性键 c.离子键 d.非极性键
Ⅱ.固体二氧化碳外形似冰,受热汽化无液体产生,俗称“干冰”,根据干冰晶胞结构回答:
(5)干冰中1个分子周围有
(6)堆积方式与干冰晶胞类型相同的金属有
Ⅲ.钇钡铜氧的晶胞结构如图。研究发现,此高温超导体中的铜元素有两种价态:+2价和+3价。

(7)根据图示晶胞结构,推算晶体中Y、Cu、Ba和O原子个数比,确定其化学式为
(8)根据(7)所推出的化合物的组成(该化合物中各元素的化合价为Y+3,Ba+2),计算该物质中+2价和+3价的铜离子个数比为
您最近半年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】钛是一种稀有金属,具有密度小、强度高、耐腐蚀等特点,钛和钛的化合物在航天、化工、建筑、日常生活中都有着广泛的用途。已知:阿伏加德罗常数的值为 。
。
(1)基态钛原子价电子排布式为___________ ;与钛同周期的元素中,基态原子的未成对电子数与钛相同的还有___________ 种。
(2)钛的一种常见化合物是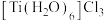 。
。 该物质中含有σ键的数目为
该物质中含有σ键的数目为___________ ,配体 的VSEPR模型名称是
的VSEPR模型名称是___________ ,其沸点高于 ,原因是
,原因是___________ 。
(3)常温下, 是易溶于
是易溶于 、易挥发的无色液体。
、易挥发的无色液体。 挥发过程中破坏的作用力类型是
挥发过程中破坏的作用力类型是___________ 。
(4) 的结构如图所示,
的结构如图所示, (IV)的配位数为
(IV)的配位数为___________ 。分子或离子中的大π键可用符号 表示,其中m代表参与形成的大π键原子数,n代表参与形成的大π键电子数(如苯分子中大π键的可表示为
表示,其中m代表参与形成的大π键原子数,n代表参与形成的大π键电子数(如苯分子中大π键的可表示为 ),则配体
),则配体 中含有的大π键应表示为
中含有的大π键应表示为___________ 。

(5)氮化钛( )晶体呈金黄色,化学稳定性好,可应用于超导材料。已知氮化钛晶体具有
)晶体呈金黄色,化学稳定性好,可应用于超导材料。已知氮化钛晶体具有 型结构,则该晶体中阳离子的配位数为
型结构,则该晶体中阳离子的配位数为___________ ;已知该晶体的晶胞参数为 ,其晶体密度的计算表达式为
,其晶体密度的计算表达式为___________  。
。
 。
。(1)基态钛原子价电子排布式为
(2)钛的一种常见化合物是
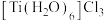 。
。 该物质中含有σ键的数目为
该物质中含有σ键的数目为 的VSEPR模型名称是
的VSEPR模型名称是 ,原因是
,原因是(3)常温下,
 是易溶于
是易溶于 、易挥发的无色液体。
、易挥发的无色液体。 挥发过程中破坏的作用力类型是
挥发过程中破坏的作用力类型是(4)
 的结构如图所示,
的结构如图所示, (IV)的配位数为
(IV)的配位数为 表示,其中m代表参与形成的大π键原子数,n代表参与形成的大π键电子数(如苯分子中大π键的可表示为
表示,其中m代表参与形成的大π键原子数,n代表参与形成的大π键电子数(如苯分子中大π键的可表示为 ),则配体
),则配体 中含有的大π键应表示为
中含有的大π键应表示为
(5)氮化钛(
 )晶体呈金黄色,化学稳定性好,可应用于超导材料。已知氮化钛晶体具有
)晶体呈金黄色,化学稳定性好,可应用于超导材料。已知氮化钛晶体具有 型结构,则该晶体中阳离子的配位数为
型结构,则该晶体中阳离子的配位数为 ,其晶体密度的计算表达式为
,其晶体密度的计算表达式为 。
。
您最近半年使用:0次
【推荐2】铁及其化合物在生活中有广泛应用。
(1)Fe3+基态核外电子排布式为_______ 。
(2)类卤素离子SCN-可用于Fe3+的检验,其对应的酸有两种,分别为硫氰酸(H-S-C≡N)和异硫氰酸(H-N=C=S),这两种酸中沸点较高的是_______ (填结构式),原因是:_______ 。
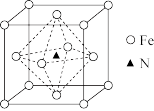
(3)氮化铁晶体的晶胞结构如图所示。该晶体中铁、氮的微粒个数之比为_____ ,与Fe3+紧邻且等距离的Fe3+数目为_____ 。
(4)某铁的化合物结构简式如图所示。
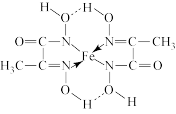
①上述化合物中所含有的非金属元素的电负性由大到小的顺序为_______ (用元素符号表示)。
②上述化合物中氮原子的杂化方式为_______ 。
(1)Fe3+基态核外电子排布式为
(2)类卤素离子SCN-可用于Fe3+的检验,其对应的酸有两种,分别为硫氰酸(H-S-C≡N)和异硫氰酸(H-N=C=S),这两种酸中沸点较高的是
(3)氮化铁晶体的晶胞结构如图所示。该晶体中铁、氮的微粒个数之比为

(4)某铁的化合物结构简式如图所示。

①上述化合物中所含有的非金属元素的电负性由大到小的顺序为
②上述化合物中氮原子的杂化方式为
您最近半年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐3】联氨(N2H4)可以用于处理高压锅炉水中的氧,防止锅炉被腐蚀,其中一种可能的反应机理如图所示。回答下列问题:

(1)N2H4的电子式为___ 。
(2)基态Cu2+核外电子排布式为___ 。
(3)Cu2O与NH3·H2O反应能形成较稳定的Cu(NH3) 的原因是
的原因是__ 。
(4)N2H4与O2的相对分子质量相近,但N2H4的熔点(2℃)沸点(114℃)分别远远高于O2的熔点(-218℃)、沸点(-183℃),原因是___ 。
(5)NaClO发生水解可生成HClO。HClO的空间构型是___ ,中心原子的杂化类型是___ 。

(1)N2H4的电子式为
(2)基态Cu2+核外电子排布式为
(3)Cu2O与NH3·H2O反应能形成较稳定的Cu(NH3)
 的原因是
的原因是(4)N2H4与O2的相对分子质量相近,但N2H4的熔点(2℃)沸点(114℃)分别远远高于O2的熔点(-218℃)、沸点(-183℃),原因是
(5)NaClO发生水解可生成HClO。HClO的空间构型是
您最近半年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】2019年为“国际化学元素周期表年”,元素周期表是认识和研究化学的重要工具。回答下列问题:
(1)对氨基苯磺酰胺的合成对抗菌药物发展意义重大。
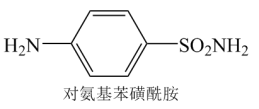
①其组成元素中,价层电子排布符合洪特规则特例的元素是__ (填元素符号,下同);其分子组成元素中,第一电离能最大的元素,其最高能级的电子云为__ 形;其分子组成元素中,属于同周期元素的电负性由小到大的排序为__ ;其分子结构中为sp3杂化的元素为__ 。
②已知对氨基苯磺酰胺易溶于盐酸,不溶于苯。分析其易溶于盐酸的主要原因:__ (至少两条)。
(2)岩盐的主要配料:精制氯化钠(NaCl)、碘酸钾(KlO3)和亚铁氰化钾{K4[Fe(CN)6]·3H2O}。
①IO 的VSEPR模型为
的VSEPR模型为__ 。
②K4[Fe(CN)6]·3H2O晶体中化学键,除了极性共价键,还有__ (填写字母)。
A.金属键 B.离子键 C.氢键 D.范德华力 E.配位键 F.非极性共价键
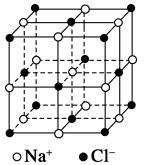
③NaCl比KI的熔沸点高,其原因是__ 。
④NaCl晶胞为典型立方晶系,若将离子视为质点,Na+位于与其最近的Cl-围成的__ 形空间的体心。已知NaCl的密度为ρg/cm3,NA表示阿伏加 德罗常数,NaCl的摩尔质量为Mg.mol-1,最邻近的同电性离子的距离为__ pm(规范列式表示)。
(1)对氨基苯磺酰胺的合成对抗菌药物发展意义重大。

①其组成元素中,价层电子排布符合洪特规则特例的元素是
②已知对氨基苯磺酰胺易溶于盐酸,不溶于苯。分析其易溶于盐酸的主要原因:
(2)岩盐的主要配料:精制氯化钠(NaCl)、碘酸钾(KlO3)和亚铁氰化钾{K4[Fe(CN)6]·3H2O}。
①IO
 的VSEPR模型为
的VSEPR模型为②K4[Fe(CN)6]·3H2O晶体中化学键,除了极性共价键,还有
A.金属键 B.离子键 C.氢键 D.范德华力 E.配位键 F.非极性共价键
③NaCl比KI的熔沸点高,其原因是
④NaCl晶胞为典型立方晶系,若将离子视为质点,Na+位于与其最近的Cl-围成的

您最近半年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】第ⅢA族的单质及一些化合物在工农业生产等领域有重要应用。回答下列问题:
(1)基态Ga原子价电子排布图为________ .
(2)经测定发现,N2O5固体由NO2+和NO3-两种离子组成,该固体中N原子杂化类型为___ ;与NO2+互为等电子体的微粒有_____ (写出一种)。
(3)铵盐大多不稳定,NH4F、NH4I中,较易分解的是_____ ,原因是______ .
(4)第二周期中,第一电离能介于B元素和N元素之间的元素有______ 种。
(5)晶体别有多种变体,但其基本结构单元都是由硼原子组成的正二十面体(见下图),每个顶点为一个硼原子,每个三角形均为等边三角形。若此结构单元为1个分子,则其分子式为____ .
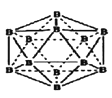
(6)冰晶石(Na3AlF6)由两种微粒构成,冰晶石的晶胞结构如图甲所示,●位于大立方体的顶点和面心,ο位于大立方体的12条棱的中点和8个小立方体的体心,那么大立方体的体心处所代表的微粒是_________ (填微粒符号)。

(7)A1单质的晶体中原子的堆积方式如图乙所示,其晶胞特征如图丙所示,原子之间相互位置关系的平面图如图丁所示:
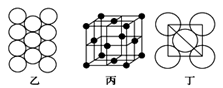
若已知Al的原子半径为dnm,NA代表阿伏伽德罗常数,Al的相对原子质量为M,则一个晶胞中Al原子的数目_____ 个;Al晶体的密度为_____ g/cm3(用字母表示)。
(1)基态Ga原子价电子排布图为
(2)经测定发现,N2O5固体由NO2+和NO3-两种离子组成,该固体中N原子杂化类型为
(3)铵盐大多不稳定,NH4F、NH4I中,较易分解的是
(4)第二周期中,第一电离能介于B元素和N元素之间的元素有
(5)晶体别有多种变体,但其基本结构单元都是由硼原子组成的正二十面体(见下图),每个顶点为一个硼原子,每个三角形均为等边三角形。若此结构单元为1个分子,则其分子式为

(6)冰晶石(Na3AlF6)由两种微粒构成,冰晶石的晶胞结构如图甲所示,●位于大立方体的顶点和面心,ο位于大立方体的12条棱的中点和8个小立方体的体心,那么大立方体的体心处所代表的微粒是

(7)A1单质的晶体中原子的堆积方式如图乙所示,其晶胞特征如图丙所示,原子之间相互位置关系的平面图如图丁所示:

若已知Al的原子半径为dnm,NA代表阿伏伽德罗常数,Al的相对原子质量为M,则一个晶胞中Al原子的数目
您最近半年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】
金属钛被誉为21世纪金属,其单质和化合物具有广泛的应用价值。以TiCl4为原料,经过一系列反应可以制得TiN和纳米TiO2(如下图所示)。
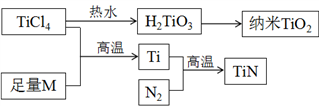
图中的M是短周期金属元素,M的部分电离能如下表:
请回答下列问题:
(1)M是___ (填元素符号),该金属晶体的堆积模型为六方最密堆积,配位数为____ 。
(2)Ti(BH4)2是一种过渡元素硼氢化物储氢材料。基态Ti2+的电子排布式为_______ , BH 的立体构型是
的立体构型是________ 。
(3)纳米TiO2是一种应用广泛的高效催化剂。
①电镀厂排放的废水中常含有剧毒的CN-,可在TiO2的催化下,先用NaClO将CN-氧化成CNO-,再在酸性条件下CNO-继续被NaClO氧化成N2和CO2。H、C、N、O四种元素的电负性由小到大的顺序为________________ ;与CN-互为等电子体微粒的化学式为________ (任写两种)。
②纳米TiO2可催化、光解附着于物体表面的甲醛、乙醛等有机物,能起到净化室内空气的功效。结合化学用语解释甲醛易溶于水的原因_________________ ;乙醛分子中碳原子的杂化轨道类型为___________ 。
(4)氮化钛广泛用于耐高温、耐磨损及航空航天等领域。
①科学家通过X射线探明KCl、MgO、CaO、TiN的晶体与NaCl的晶体结构相似。且知三种离子晶体的晶格能数据如下:
KCl、CaO、TiN三种离子晶体熔点的高低的顺序为________________ 。
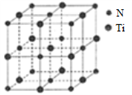
②某氮化钛晶体是典型的NaCl型晶体,晶胞结构如图所示,该晶胞中N、Ti之间的最近距离为a pm,则该氮化钛的密度为__________ g·cm-3(阿伏伽德罗常数的值用NA表示)。
金属钛被誉为21世纪金属,其单质和化合物具有广泛的应用价值。以TiCl4为原料,经过一系列反应可以制得TiN和纳米TiO2(如下图所示)。

图中的M是短周期金属元素,M的部分电离能如下表:
| I1 | I2 | I3 | I4 | I5 | |
| 电离能/(kJ·mol-1) | 738 | 1451 | 7733 | 10540 | 13630 |
(1)M是
(2)Ti(BH4)2是一种过渡元素硼氢化物储氢材料。基态Ti2+的电子排布式为
 的立体构型是
的立体构型是(3)纳米TiO2是一种应用广泛的高效催化剂。
①电镀厂排放的废水中常含有剧毒的CN-,可在TiO2的催化下,先用NaClO将CN-氧化成CNO-,再在酸性条件下CNO-继续被NaClO氧化成N2和CO2。H、C、N、O四种元素的电负性由小到大的顺序为
②纳米TiO2可催化、光解附着于物体表面的甲醛、乙醛等有机物,能起到净化室内空气的功效。结合化学用语解释甲醛易溶于水的原因
(4)氮化钛广泛用于耐高温、耐磨损及航空航天等领域。
①科学家通过X射线探明KCl、MgO、CaO、TiN的晶体与NaCl的晶体结构相似。且知三种离子晶体的晶格能数据如下:
| 离子晶体 | NaCl | KCl | CaO |
| 晶格能/(kJ·mol-1) | 786 | 715 | 3401 |
②某氮化钛晶体是典型的NaCl型晶体,晶胞结构如图所示,该晶胞中N、Ti之间的最近距离为a pm,则该氮化钛的密度为

您最近半年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】【物质结构与性质】纯铜在工业上主要用来制造导线、电器元件等,铜能形成多种-1和+2价态的化合物且其化合物常带有颜色。
(1)写出基态Cu+的核外电子排布式____________ ;
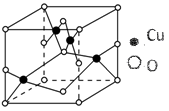
(2)如图结构是铜的某氧化物的晶体结构的最小重复单元,则该氧化物的化学式为____________ ;
(3)向硫酸铜溶液中滴加氨水会生成蓝色沉淀,在滴加氨水至沉淀刚好全部溶解时可得到蓝色溶液,继续向其中加入极性较小的乙醇可以生成深蓝色的[Cu(NH3)4]SO4•H2O沉淀。
①该沉淀中S原子的杂化类型为____________ ;
②写出一种与NH3分子互为等电子体的阳离子的化学式____________ 。
(4)NH3的沸点高于PH3,原因是____________
(5)CuO的熔点比CuCl的熔点____________ (填“高”或“低”),其原因是____________ 。
(1)写出基态Cu+的核外电子排布式
(2)如图结构是铜的某氧化物的晶体结构的最小重复单元,则该氧化物的化学式为

(3)向硫酸铜溶液中滴加氨水会生成蓝色沉淀,在滴加氨水至沉淀刚好全部溶解时可得到蓝色溶液,继续向其中加入极性较小的乙醇可以生成深蓝色的[Cu(NH3)4]SO4•H2O沉淀。
①该沉淀中S原子的杂化类型为
②写出一种与NH3分子互为等电子体的阳离子的化学式
(4)NH3的沸点高于PH3,原因是
(5)CuO的熔点比CuCl的熔点
您最近半年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】氢、氮、氧、硫、镁、铁、铜、锌等元素及其化合物在人们的日常生活中有着广泛的用途。回答下列问题:
(1)某同学根据已学知识,推断 Mg 基态原子的核外电子排布为,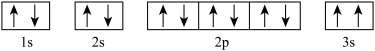 该同学所画的电子排布图违背了
该同学所画的电子排布图违背了____
(2)Cu 位于____ 族____ 区,Cu+价电子排布式为____ 。
(3)MgCO3的分解温度____ BaCO3(填“>” 或、“<”)
(4)Ge、As、Se 元素的第一电离能由大到小的顺序为____
(5)已知 H3BO3是一元酸,1molH3BO3在水中完全电离得到的阴离子中含有σ键的数目为____
(6)下列有关说法不正确的是____ 。
A.热稳定性:NH3 >PH3,原因是NH3分子间存在氢键,而PH3分子间存在范德华力
B.SO2与 CO2的化学性质有些类似,但空间结构与杂化方式不同
C.熔、沸点: SiF4< SiCl4< SiBr4 <SiI4,原因是分子中共价键键能逐渐增大
D.熔点: CaO > KCl > KBr,原因是晶格能逐渐减小
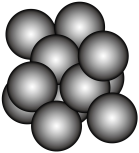
(7)晶体 Cu 的堆积方式如图所示,其中Cu原子在二维平面里放置时的配位数为_________ ,设Cu原子半径为a,晶体的空间利用率为______ 。(用含π,a、的式子表示,不必化简)
(1)某同学根据已学知识,推断 Mg 基态原子的核外电子排布为,
 该同学所画的电子排布图违背了
该同学所画的电子排布图违背了(2)Cu 位于
(3)MgCO3的分解温度
(4)Ge、As、Se 元素的第一电离能由大到小的顺序为
(5)已知 H3BO3是一元酸,1molH3BO3在水中完全电离得到的阴离子中含有σ键的数目为
(6)下列有关说法不正确的是
A.热稳定性:NH3 >PH3,原因是NH3分子间存在氢键,而PH3分子间存在范德华力
B.SO2与 CO2的化学性质有些类似,但空间结构与杂化方式不同
C.熔、沸点: SiF4< SiCl4< SiBr4 <SiI4,原因是分子中共价键键能逐渐增大
D.熔点: CaO > KCl > KBr,原因是晶格能逐渐减小
(7)晶体 Cu 的堆积方式如图所示,其中Cu原子在二维平面里放置时的配位数为

您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】已知A、B、C、D、E、F为元素周期表中原子序数依次增大的前20号元素,A与B,C、D与E分别位于同一周期。A原子L层上有2对成对电子,B、C、D的核外电子排布相同的简单离子可形成一种C3DB6型离子晶体X,CE、FA为电子数相同的离子晶体。
(1)写出A元素的基态原子外围电子排布式:_______________________________ 。F的离子电子排布式:__________ 。
(2)写出X涉及化工生产中的一个化学方程式:______________________ 。
(3)试解释工业冶炼D不以DE3而是以D2A3为原料的原因:_____________ 。
(4)CE、FA的晶格能分别为786 kJ·mol-1、3 401 kJ·mol-1,试分析导致两者晶格能差异的主要原因是___________________________ 。
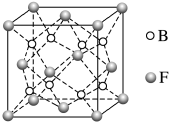
(5)F与B可形成离子化合物,其晶胞结构如图所示。F与B形成的离子化合物的化学式为________________ ;该离子化合物晶体的密度为ag·cm-3,则晶胞的体积是____________________ (只要求列出算式)。
(1)写出A元素的基态原子外围电子排布式:
(2)写出X涉及化工生产中的一个化学方程式:
(3)试解释工业冶炼D不以DE3而是以D2A3为原料的原因:
(4)CE、FA的晶格能分别为786 kJ·mol-1、3 401 kJ·mol-1,试分析导致两者晶格能差异的主要原因是
(5)F与B可形成离子化合物,其晶胞结构如图所示。F与B形成的离子化合物的化学式为

您最近半年使用:0次



