铁及其化合物在生活中有广泛应用。
(1)Fe3+基态核外电子排布式为_______ 。
(2)类卤素离子SCN-可用于Fe3+的检验,其对应的酸有两种,分别为硫氰酸(H-S-C≡N)和异硫氰酸(H-N=C=S),这两种酸中沸点较高的是_______ (填结构式),原因是:_______ 。
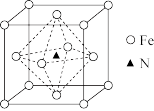
(3)氮化铁晶体的晶胞结构如图所示。该晶体中铁、氮的微粒个数之比为_____ ,与Fe3+紧邻且等距离的Fe3+数目为_____ 。
(4)某铁的化合物结构简式如图所示。
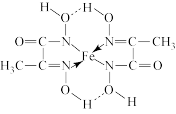
①上述化合物中所含有的非金属元素的电负性由大到小的顺序为_______ (用元素符号表示)。
②上述化合物中氮原子的杂化方式为_______ 。
(1)Fe3+基态核外电子排布式为
(2)类卤素离子SCN-可用于Fe3+的检验,其对应的酸有两种,分别为硫氰酸(H-S-C≡N)和异硫氰酸(H-N=C=S),这两种酸中沸点较高的是
(3)氮化铁晶体的晶胞结构如图所示。该晶体中铁、氮的微粒个数之比为

(4)某铁的化合物结构简式如图所示。

①上述化合物中所含有的非金属元素的电负性由大到小的顺序为
②上述化合物中氮原子的杂化方式为
更新时间:2022-04-21 19:08:34
|
相似题推荐
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】O、S、Cl、Fe、Cu五种元素的单质及其化合物在工农业生产和生活中有着广泛的应用。请回答下列问题:
(1)基态Fe原子价电子的轨道表示式为_______ 。
(2)O、S、Cl的电负性由大到小的顺序是_______ (填元素符号)。
(3)O、S的最简单氢化物中键角较大的是_______ (填化学式),原因是_______ 。
(4) 的空间结构为
的空间结构为_______ 。
(5)O、Cu组成的一种化合物的晶胞结构示意图如下。
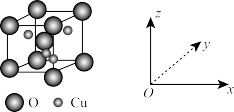
则该化合物的化学式为_______ 。
(1)基态Fe原子价电子的轨道表示式为
(2)O、S、Cl的电负性由大到小的顺序是
(3)O、S的最简单氢化物中键角较大的是
(4)
 的空间结构为
的空间结构为(5)O、Cu组成的一种化合物的晶胞结构示意图如下。

则该化合物的化学式为
您最近半年使用:0次
【推荐2】锗(Ge)是典型的半导体元素,在电子、材料等领域应用广泛。回答下列问题:
(1)Ge与C是同族元素,C原子之间可以形成双键、叁键,但Ge原子之间难以形成双键或叁键。从原子结构、熔点/℃角度分析,原因是______________ 。
(2)比较下列锗卤化物的熔点和沸点,分析其变化规律及原因____________ 。
(3)光催化还原CO2制备CH4反应中,带状纳米Zn2GeO4是该反应的良好催化剂。Zn、Ge、O电负性由大至小的顺序是______________ 。
(4)Ge单晶具有金刚石型结构,其中Ge原子的杂化方式为__________ ,微粒之间存在的作用力是________ 。
(5)晶胞有两个基本要素:
①原子坐标参数,表示晶胞内部各原子的相对位置。如图为Ge单晶的晶胞,其中原子坐标参数A为(0,0,0);B为( ,0,
,0, );C(
);C( ,0,
,0, ),则D原子的坐标参数为
),则D原子的坐标参数为_________ 。
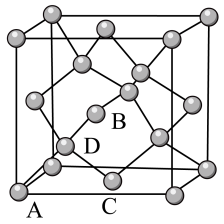
②晶胞参数:描述晶胞的大小和形状。已知Ge单晶的晶胞参数a=565.76pm,其密度为_______ g/cm3(列出计算式即可)。
(1)Ge与C是同族元素,C原子之间可以形成双键、叁键,但Ge原子之间难以形成双键或叁键。从原子结构、熔点/℃角度分析,原因是
(2)比较下列锗卤化物的熔点和沸点,分析其变化规律及原因
| GeCl4 | GeBr4 | Gel4 | |
| 熔点/℃ | -49.5 | 26 | 146 |
| 沸点/℃ | 83.1 | 186 | 约400 |
(4)Ge单晶具有金刚石型结构,其中Ge原子的杂化方式为
(5)晶胞有两个基本要素:
①原子坐标参数,表示晶胞内部各原子的相对位置。如图为Ge单晶的晶胞,其中原子坐标参数A为(0,0,0);B为(
 ,0,
,0, );C(
);C( ,0,
,0, ),则D原子的坐标参数为
),则D原子的坐标参数为
②晶胞参数:描述晶胞的大小和形状。已知Ge单晶的晶胞参数a=565.76pm,其密度为
您最近半年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】1932年美国化学家鲍林首先提出了电负性的概念。电负性(用X表示)也是元素的一种重要性质,下表给出的是原子序数小于20的16种元素的电负性数值:
请仔细分析,回答下列有关问题:
(1)预测周期表中电负性最大的元素应为_______ ;估计钙元素的电负性的取值范围:_______ <X<_______ 。
(2)经验规律告诉我们:当形成化学键的两原子相应元素的电负性差值大于1.7时,所形成的一般为离子键;当小于1.7时,一般为共价键。试推断AlBr3中形成的化学键的类型为_______ 。
(3)请你预测Br与I元素的X数值的大小关系:X(Br)_______ X(I)。
(4)某有机化合物分子中含有S—N键,你认为该共用电子对偏向于_______ 原子(填元素符号)。
(5)根据表中的所给数据分析: 同主族内的不同元素的X值变化的规律是_______ ;
(6)化合物NaH能与水反应产生氢气,所以可用做生氢剂,写出该反应的化学方程式:_______ 。
(7)下列表述中,不能证明氯的非金属性比硫强的是_______ 。
A.气态氢化物的稳定性:HCl>H2S
B.两元素的电负性:S<Cl
C.最高价含氧酸的酸性:HClO4>H2SO4
D.常温时,硫单质为固态,氯单质为气态
E.两者间可发生反应:Cl2+H2S=2HCl+S↓
| 元素 | H | Li | Be | B | C | N | O | F |
| 电负性 | 2.1 | 1.0 | 1.5 | 2.0 | 2.5 | 3.0 | 3.5 | 4.0 |
| 元素 | Na | Mg | Al | Si | P | S | Cl | K |
| 电负性 | 0.9 | 1.2 | 1.5 | 1.7 | 2.1 | 2.3 | 3.0 | 0.8 |
(1)预测周期表中电负性最大的元素应为
(2)经验规律告诉我们:当形成化学键的两原子相应元素的电负性差值大于1.7时,所形成的一般为离子键;当小于1.7时,一般为共价键。试推断AlBr3中形成的化学键的类型为
(3)请你预测Br与I元素的X数值的大小关系:X(Br)
(4)某有机化合物分子中含有S—N键,你认为该共用电子对偏向于
(5)根据表中的所给数据分析: 同主族内的不同元素的X值变化的规律是
(6)化合物NaH能与水反应产生氢气,所以可用做生氢剂,写出该反应的化学方程式:
(7)下列表述中,不能证明氯的非金属性比硫强的是
A.气态氢化物的稳定性:HCl>H2S
B.两元素的电负性:S<Cl
C.最高价含氧酸的酸性:HClO4>H2SO4
D.常温时,硫单质为固态,氯单质为气态
E.两者间可发生反应:Cl2+H2S=2HCl+S↓
您最近半年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】钛的化合物如TiO2、Ti(BH4)2等均有着广泛用途。
(1)基态Ti3+的未成对电子数为______________ ; 的空间构型为
的空间构型为______________ 。
(2)TiO2是常用的具有较高催化活性和稳定性的光催化剂。在TiO2催化作用下,可将CN−氧化成CNO−,进而得到N2。写出与CNO−互为等电子体的分子的化学式______________ (任填一种)。
(3)纳米TiO2催化的一个实例如图所示,化合物甲的分子中采取sp2方式杂化的碳原子数为____________ 个,化合物乙中采取sp3方式杂化的原子对应的元素的电负性由大到小的顺序为______________ 。

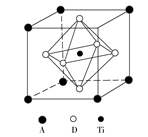
(4)主族元素A和钛同周期,具有相同的最外层电子数,元素D原子的p能级所含电子总数与s能级所含电子总数相等,且其形成的氢化物分子之间存在氢键。元素A、元素D和钛三者形成的晶体的晶胞如图所示,写出该晶体的化学式______________ (用元素符号表示)。
(1)基态Ti3+的未成对电子数为
 的空间构型为
的空间构型为(2)TiO2是常用的具有较高催化活性和稳定性的光催化剂。在TiO2催化作用下,可将CN−氧化成CNO−,进而得到N2。写出与CNO−互为等电子体的分子的化学式
(3)纳米TiO2催化的一个实例如图所示,化合物甲的分子中采取sp2方式杂化的碳原子数为

(4)主族元素A和钛同周期,具有相同的最外层电子数,元素D原子的p能级所含电子总数与s能级所含电子总数相等,且其形成的氢化物分子之间存在氢键。元素A、元素D和钛三者形成的晶体的晶胞如图所示,写出该晶体的化学式

您最近半年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】回答下列问题:
(1)金属铝质轻且有良好的防腐蚀性,在国防工业中有非常重要的作用。铝原子核外有_____ 种不同空间运动状态的电子,其最高能级的电子云形状为_____ 。
(2)过渡金属元素铬(Cr)是不锈钢的重要成分,在工农业生产和国防建设中有着广泛应用。回答下列问题:
①对于基态Cr原子,下列叙述正确的是_____ (填标号)。
A.轨道处于半充满时体系总能量低,核外电子排布应为[Ar]3d54s1
B.4s电子能量较高,总是在比3s电子离核更远的地方运动
C.电负性比钾高,原子对键合电子的吸引力比钾大
②[Cr(NH3)3(H2O)2Cl]2+中配体分子NH3、H2O以及分子PH3的空间结构和相应的键角如图所示。
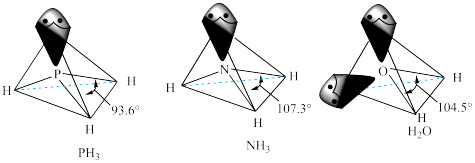
PH3中P的杂化类型是_____ ,H2O的键角小于NH3的,分析原因:_____ 。
(3)多原子分子中各原子若在同一平面,且有相互平行的p轨道,则p电子可在多个原子间运动,形成“离域π键”,如SO2分子中存在“离域π键”,可表示成π ,则
,则 (咪唑)中的“离域π键”可表示为
(咪唑)中的“离域π键”可表示为________ 。
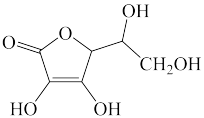
(4)抗坏血酸的分子结构如图所示,分子中碳原子的轨道杂化类型为_____ ;推测抗坏血酸在水中的溶解性:_____ (填“难溶”或“易溶”)于水;坏血酸分子_____ (填“是”或“不是”)手性分子。
(1)金属铝质轻且有良好的防腐蚀性,在国防工业中有非常重要的作用。铝原子核外有
(2)过渡金属元素铬(Cr)是不锈钢的重要成分,在工农业生产和国防建设中有着广泛应用。回答下列问题:
①对于基态Cr原子,下列叙述正确的是
A.轨道处于半充满时体系总能量低,核外电子排布应为[Ar]3d54s1
B.4s电子能量较高,总是在比3s电子离核更远的地方运动
C.电负性比钾高,原子对键合电子的吸引力比钾大
②[Cr(NH3)3(H2O)2Cl]2+中配体分子NH3、H2O以及分子PH3的空间结构和相应的键角如图所示。

PH3中P的杂化类型是
(3)多原子分子中各原子若在同一平面,且有相互平行的p轨道,则p电子可在多个原子间运动,形成“离域π键”,如SO2分子中存在“离域π键”,可表示成π
 ,则
,则 (咪唑)中的“离域π键”可表示为
(咪唑)中的“离域π键”可表示为(4)抗坏血酸的分子结构如图所示,分子中碳原子的轨道杂化类型为

您最近半年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐3】[2016·新课标I]锗(Ge)是典型的半导体元素,在电子、材料等领域应用广泛。回答下列问题:
(1)基态Ge原子的核外电子排布式为[Ar]_______________ ,有__________ 个未成对电子。
(2)Ge与C是同族元素,C原子之间可以形成双键、叁键,但Ge原子之间难以形成双键或叁键。从原子结构角度分析,原因是______________________________ 。
(3)比较下列锗卤化物的熔点和沸点,分析其变化规律及原因______________________________ 。
(4)光催化还原CO2制备CH4反应中,带状纳米Zn2GeO4是该反应的良好催化剂。Zn、Ge、O电负性由大至小的顺序是______________________________ 。
(5)Ge单晶具有金刚石型结构,其中Ge原子的杂化方式为_______________ ,微粒之间存在的作用力是_______________ 。
(6)晶胞有两个基本要素:
①原子坐标参数,表示晶胞内部各原子的相对位置。如图为Ge单晶的晶胞,其中原子坐标参数A为(0,0,0);B为( ,0,
,0, );C为(
);C为( ,
, ,0)。则D原子的坐标参数为
,0)。则D原子的坐标参数为_______________ 。_____ g·cm−3(列出计算式即可)。
(1)基态Ge原子的核外电子排布式为[Ar]
(2)Ge与C是同族元素,C原子之间可以形成双键、叁键,但Ge原子之间难以形成双键或叁键。从原子结构角度分析,原因是
(3)比较下列锗卤化物的熔点和沸点,分析其变化规律及原因
| GeCl4 | GeBr4 | GeI4 | |
| 熔点/℃ | −49.5 | 26 | 146 |
| 沸点/℃ | 83.1 | 186 | 约400 |
(5)Ge单晶具有金刚石型结构,其中Ge原子的杂化方式为
(6)晶胞有两个基本要素:
①原子坐标参数,表示晶胞内部各原子的相对位置。如图为Ge单晶的晶胞,其中原子坐标参数A为(0,0,0);B为(
 ,0,
,0, );C为(
);C为( ,
, ,0)。则D原子的坐标参数为
,0)。则D原子的坐标参数为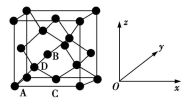
您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】元素X 位于第四周期,其基态原子的内层轨道全部排满电子,且最外层电子数为2。元素Y基态原子的3p 轨道上有4个电子。元素Z 的原子最外层电子数是其内层的3倍。
(1)在Y的氢化物(H2Y)分子中,Y原子轨道的杂化类型是__________ 。
(2)Z的氢化物(H2Z)在乙醇中的溶解度大于H2Y,其原因是________________ 。
(3)Y 与Z 可形成YZ42-
①YZ42-的空间构型为________ (用文字描述)。
②写出一种与YZ42-互为等电子体的分子的化学式:______________ 。
(4)X的氯化物与氨水反应可形成配合物[X(NH3)4]Cl2,1mol该配合物中含有σ键的数目为________________ 。
(1)在Y的氢化物(H2Y)分子中,Y原子轨道的杂化类型是
(2)Z的氢化物(H2Z)在乙醇中的溶解度大于H2Y,其原因是
(3)Y 与Z 可形成YZ42-
①YZ42-的空间构型为
②写出一种与YZ42-互为等电子体的分子的化学式:
(4)X的氯化物与氨水反应可形成配合物[X(NH3)4]Cl2,1mol该配合物中含有σ键的数目为
您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】已知A、B、C、D、E、F、G都是元素周期表中短周期主族元素,它们的原子序数依次增大。A原子的电子只有一种自旋取向,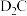 中阴、阳离子具有相同的电子层结构,B、C均可分别与A形成10电子分子,B、C处于同一周期,两者可以形成许多种共价化合物,C、F处于同一主族,B原子最外p能级上的电子处于半充满状态,C的最外层电子数是内层电子数的3倍,E是的第三周期元素的简单离子中半径最小。元素H原子M能层为全充满状态,且核外只有一个未成对电子的某金属元素,回答下列问题:
中阴、阳离子具有相同的电子层结构,B、C均可分别与A形成10电子分子,B、C处于同一周期,两者可以形成许多种共价化合物,C、F处于同一主族,B原子最外p能级上的电子处于半充满状态,C的最外层电子数是内层电子数的3倍,E是的第三周期元素的简单离子中半径最小。元素H原子M能层为全充满状态,且核外只有一个未成对电子的某金属元素,回答下列问题:
(1)E元素基态原子的简化电子排布式为________ 。E元素原子的第一电离能________ 镁(填“>”“<”或“=”)
(2)F、G元素对应的最高价含氧酸中酸性较强的化学式为________ 。离子半径: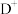
________ (填“<”“>”或“=”)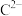 。
。
(3)元素C的简单气态氢化物的沸点________ (填“高于”或“低于”)元素F的简单气态氢化物的沸点,其主要原因是________________________ 。
(4)金属元素H的基态原子核外电子有________ 种空间运动状态。
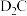 中阴、阳离子具有相同的电子层结构,B、C均可分别与A形成10电子分子,B、C处于同一周期,两者可以形成许多种共价化合物,C、F处于同一主族,B原子最外p能级上的电子处于半充满状态,C的最外层电子数是内层电子数的3倍,E是的第三周期元素的简单离子中半径最小。元素H原子M能层为全充满状态,且核外只有一个未成对电子的某金属元素,回答下列问题:
中阴、阳离子具有相同的电子层结构,B、C均可分别与A形成10电子分子,B、C处于同一周期,两者可以形成许多种共价化合物,C、F处于同一主族,B原子最外p能级上的电子处于半充满状态,C的最外层电子数是内层电子数的3倍,E是的第三周期元素的简单离子中半径最小。元素H原子M能层为全充满状态,且核外只有一个未成对电子的某金属元素,回答下列问题:(1)E元素基态原子的简化电子排布式为
(2)F、G元素对应的最高价含氧酸中酸性较强的化学式为
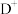
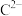 。
。(3)元素C的简单气态氢化物的沸点
(4)金属元素H的基态原子核外电子有
您最近半年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐3】铜是人类最早使用的金属之一,金属铜及其化合物在工业生产及生活中用途非常广泛。回答下列问题:
(1)基态+2价铜离子M能层电子排布式是___________ ;第4周期中基态原子未成对电子数与铜原子相同的元素有________ 种。
(2)Cu+能与SCN-形成CuSCN沉淀。请写出一种与SCN-互为等电子体的微粒_________ 。SCN-对应的酸有硫氰酸(H-S-C N)和异硫氰酸(H-N=C=S),这两种酸熔点更高的是
N)和异硫氰酸(H-N=C=S),这两种酸熔点更高的是_______ (填名称),原因是_____________________ 。
(3)Cu2+能与NH3形成平面正方形的[Cu(NH3)4]2+。NH3分子的空间构型为__________ ;[Cu(NH3)4]2+中Cu采取dspx杂化,x的值是__________ 。
(4)已知Cu2O 熔点为1235 ℃,K2O 熔点为770℃,前者熔点较高,其原因是___________ 。
(5)Cu3N 的晶胞(立方)结构如下图所示:
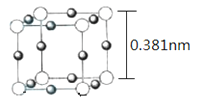
①距离最近的两个Cu+间的距离为________ nm。(保留两位小数)
②Cu3N 晶体的密度为____________ g·cm-3。(NA表示阿伏伽德罗常数的值,列出计算式,不必计算出结果)
(1)基态+2价铜离子M能层电子排布式是
(2)Cu+能与SCN-形成CuSCN沉淀。请写出一种与SCN-互为等电子体的微粒
 N)和异硫氰酸(H-N=C=S),这两种酸熔点更高的是
N)和异硫氰酸(H-N=C=S),这两种酸熔点更高的是(3)Cu2+能与NH3形成平面正方形的[Cu(NH3)4]2+。NH3分子的空间构型为
(4)已知Cu2O 熔点为1235 ℃,K2O 熔点为770℃,前者熔点较高,其原因是
(5)Cu3N 的晶胞(立方)结构如下图所示:

①距离最近的两个Cu+间的距离为
②Cu3N 晶体的密度为
您最近半年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】(1)钛镁合金是制造高性能飞机的重要材料。金属钛、镁均采用六方最密堆积,下列说法正确的是_____ (填序号)。
A.钛镁合金用于制造高性能飞机主要是由于它们的价格昂贵,制造出的飞机能卖好价钱
B.钛、镁金属晶体中,其配位数均为12
C.金属钛的熔点(1668℃)很高,与金属键无关
(2)钙钛型复合氧化物可用于制造航母中的热敏传感器,其晶胞结构如图所示,其中A为晶胞的顶点,A可以是Ca、Sr、Ba或Pb,当B是V、Cr、Mn或Fe时,这种化合物具有很好的电学性能。下列说法正确的是______ (填序号)。
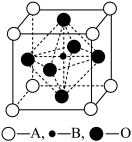
A.金属Ca、Sr、Ba采用体心立方密堆积
B.用A、B、O表示的钙钛型复合氧化物晶体的化学式可表示为ABO3
C.在制造Fe薄片时,金属键完全断裂
D.V、Cr、Mn、Fe晶体中均存在金属阳离子和阴离子
(3)辽宁号航母飞行甲板等都是由铁及其合金制造的。铁有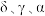 三种同素异形体,其晶胞结构如图所示。
三种同素异形体,其晶胞结构如图所示。
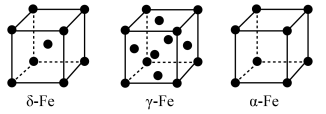
① 晶胞中含有的铁原子数为
晶胞中含有的铁原子数为___________ 。
②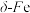 、
、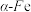 两种晶体中铁原子的配位数之比为
两种晶体中铁原子的配位数之比为___________ 。
③若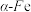 晶胞的边长为a cm,
晶胞的边长为a cm,  晶胞的边长为b cm,则两种晶体的密度之比为
晶胞的边长为b cm,则两种晶体的密度之比为___________ 。
A.钛镁合金用于制造高性能飞机主要是由于它们的价格昂贵,制造出的飞机能卖好价钱
B.钛、镁金属晶体中,其配位数均为12
C.金属钛的熔点(1668℃)很高,与金属键无关
(2)钙钛型复合氧化物可用于制造航母中的热敏传感器,其晶胞结构如图所示,其中A为晶胞的顶点,A可以是Ca、Sr、Ba或Pb,当B是V、Cr、Mn或Fe时,这种化合物具有很好的电学性能。下列说法正确的是

A.金属Ca、Sr、Ba采用体心立方密堆积
B.用A、B、O表示的钙钛型复合氧化物晶体的化学式可表示为ABO3
C.在制造Fe薄片时,金属键完全断裂
D.V、Cr、Mn、Fe晶体中均存在金属阳离子和阴离子
(3)辽宁号航母飞行甲板等都是由铁及其合金制造的。铁有
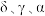 三种同素异形体,其晶胞结构如图所示。
三种同素异形体,其晶胞结构如图所示。
①
 晶胞中含有的铁原子数为
晶胞中含有的铁原子数为②
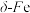 、
、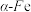 两种晶体中铁原子的配位数之比为
两种晶体中铁原子的配位数之比为③若
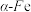 晶胞的边长为a cm,
晶胞的边长为a cm,  晶胞的边长为b cm,则两种晶体的密度之比为
晶胞的边长为b cm,则两种晶体的密度之比为
您最近半年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐2】晶体具有周期性的微观结构,表现出许多独特的性质,用于制造各种材料。
(1)干冰常用作制冷剂、人工降雨材料等,晶胞结构如图。

①1个 分子周围等距且最近的
分子周围等距且最近的 分子有
分子有___________ 个。
②铜金合金的晶胞结构与干冰相似,若顶点为 、面心为
、面心为 ,则铜金合金晶体中
,则铜金合金晶体中 与
与 原子数之比为是
原子数之比为是___________ 。
③如图是冰的结构。下列事实能解释干冰的密度比冰大的是___________ (填字母序号)。
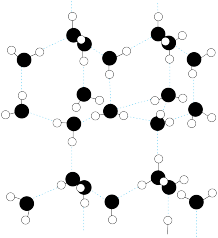
a.二氧化碳分子的质量大于水分子
b.于冰晶胞中二氧化碳分子堆积得更密集
c.水分子极性强,分子间作用力大
d.冰中氢键存在方向性,晶体有较大空隙,空间利用率低
(2)单晶硅等作为制造太阳能电池的材料已得到广泛应用,结构如图。

①单晶硅中最小的环上有___________ 个 原子。
原子。
② 单晶硅中含有
单晶硅中含有___________ 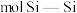 键,
键,
(3) 是一种碳的单质,结构如下,1个
是一种碳的单质,结构如下,1个 晶胞中含有
晶胞中含有___________ 个分子

(4) 晶体与
晶体与 晶体结构相似,结构如图
晶体结构相似,结构如图

① 的熔点远高于
的熔点远高于 ,结合下表说明理由:
,结合下表说明理由:___________
②设阿伏加德罗常数的值为 ,距离最近的两个
,距离最近的两个 间距为
间距为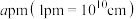 ,
, 的摩尔质量为
的摩尔质量为 ,则晶体的密度为
,则晶体的密度为___________ 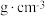 (列出计算式)
(列出计算式)
(1)干冰常用作制冷剂、人工降雨材料等,晶胞结构如图。

①1个
 分子周围等距且最近的
分子周围等距且最近的 分子有
分子有②铜金合金的晶胞结构与干冰相似,若顶点为
 、面心为
、面心为 ,则铜金合金晶体中
,则铜金合金晶体中 与
与 原子数之比为是
原子数之比为是③如图是冰的结构。下列事实能解释干冰的密度比冰大的是

a.二氧化碳分子的质量大于水分子
b.于冰晶胞中二氧化碳分子堆积得更密集
c.水分子极性强,分子间作用力大
d.冰中氢键存在方向性,晶体有较大空隙,空间利用率低
(2)单晶硅等作为制造太阳能电池的材料已得到广泛应用,结构如图。

①单晶硅中最小的环上有
 原子。
原子。②
 单晶硅中含有
单晶硅中含有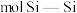 键,
键,(3)
 是一种碳的单质,结构如下,1个
是一种碳的单质,结构如下,1个 晶胞中含有
晶胞中含有
(4)
 晶体与
晶体与 晶体结构相似,结构如图
晶体结构相似,结构如图
①
 的熔点远高于
的熔点远高于 ,结合下表说明理由:
,结合下表说明理由:| 晶体 | 离子间距/pm | 熔点/℃ |
 |  | 801 |
 | 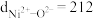 | 1960 |
 ,距离最近的两个
,距离最近的两个 间距为
间距为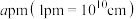 ,
, 的摩尔质量为
的摩尔质量为 ,则晶体的密度为
,则晶体的密度为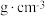 (列出计算式)
(列出计算式)
您最近半年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】硒是典型的半导体材料。
(1)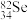 是硒的一种放射性同位素,其中子数与价电子数之差为
是硒的一种放射性同位素,其中子数与价电子数之差为___________ , 、
、 、
、 其沸点从大到小的顺序是
其沸点从大到小的顺序是___________ 。
(2) 是一种无色液体,其分子空间构型是
是一种无色液体,其分子空间构型是___________ (填标号)。
a.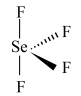 b.
b.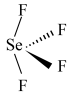 c.
c. d.
d. e.
e.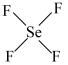
 与
与 结构相似,其键角较大的是
结构相似,其键角较大的是___________ 。
(3)锂硒电池正极的充放电原理为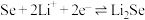
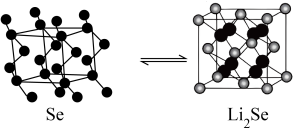
硒晶胞中含有___________ 个 原子,若
原子,若 晶胞参数边长为
晶胞参数边长为 ,在
,在 晶胞中2个
晶胞中2个 、
、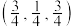 间距离是
间距离是___________  ,
, 填充在
填充在 的
的___________ 型空隙中,充电过程正极材料体积___________ (填“膨胀”、“不变”或“收缩”)
(4) 与
与 可形成直线型阴离子(结构如下),其中
可形成直线型阴离子(结构如下),其中
___________ 。

(1)
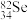 是硒的一种放射性同位素,其中子数与价电子数之差为
是硒的一种放射性同位素,其中子数与价电子数之差为 、
、 、
、 其沸点从大到小的顺序是
其沸点从大到小的顺序是(2)
 是一种无色液体,其分子空间构型是
是一种无色液体,其分子空间构型是a.
 b.
b. c.
c. d.
d. e.
e.
 与
与 结构相似,其键角较大的是
结构相似,其键角较大的是(3)锂硒电池正极的充放电原理为
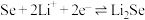

硒晶胞中含有
 原子,若
原子,若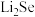 晶胞参数边长为
晶胞参数边长为 ,在
,在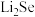 晶胞中2个
晶胞中2个 、
、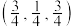 间距离是
间距离是 ,
, 填充在
填充在 的
的(4)
 与
与 可形成直线型阴离子(结构如下),其中
可形成直线型阴离子(结构如下),其中

您最近半年使用:0次



