回答下列问题:
(1)金属铝质轻且有良好的防腐蚀性,在国防工业中有非常重要的作用。铝原子核外有_____ 种不同空间运动状态的电子,其最高能级的电子云形状为_____ 。
(2)过渡金属元素铬(Cr)是不锈钢的重要成分,在工农业生产和国防建设中有着广泛应用。回答下列问题:
①对于基态Cr原子,下列叙述正确的是_____ (填标号)。
A.轨道处于半充满时体系总能量低,核外电子排布应为[Ar]3d54s1
B.4s电子能量较高,总是在比3s电子离核更远的地方运动
C.电负性比钾高,原子对键合电子的吸引力比钾大
②[Cr(NH3)3(H2O)2Cl]2+中配体分子NH3、H2O以及分子PH3的空间结构和相应的键角如图所示。
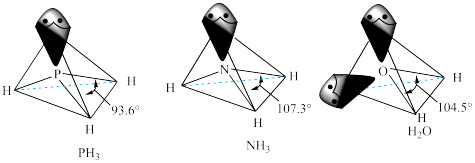
PH3中P的杂化类型是_____ ,H2O的键角小于NH3的,分析原因:_____ 。
(3)多原子分子中各原子若在同一平面,且有相互平行的p轨道,则p电子可在多个原子间运动,形成“离域π键”,如SO2分子中存在“离域π键”,可表示成π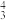 ,则
,则 (咪唑)中的“离域π键”可表示为
(咪唑)中的“离域π键”可表示为________ 。
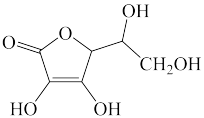
(4)抗坏血酸的分子结构如图所示,分子中碳原子的轨道杂化类型为_____ ;推测抗坏血酸在水中的溶解性:_____ (填“难溶”或“易溶”)于水;坏血酸分子_____ (填“是”或“不是”)手性分子。
(1)金属铝质轻且有良好的防腐蚀性,在国防工业中有非常重要的作用。铝原子核外有
(2)过渡金属元素铬(Cr)是不锈钢的重要成分,在工农业生产和国防建设中有着广泛应用。回答下列问题:
①对于基态Cr原子,下列叙述正确的是
A.轨道处于半充满时体系总能量低,核外电子排布应为[Ar]3d54s1
B.4s电子能量较高,总是在比3s电子离核更远的地方运动
C.电负性比钾高,原子对键合电子的吸引力比钾大
②[Cr(NH3)3(H2O)2Cl]2+中配体分子NH3、H2O以及分子PH3的空间结构和相应的键角如图所示。

PH3中P的杂化类型是
(3)多原子分子中各原子若在同一平面,且有相互平行的p轨道,则p电子可在多个原子间运动,形成“离域π键”,如SO2分子中存在“离域π键”,可表示成π
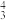 ,则
,则 (咪唑)中的“离域π键”可表示为
(咪唑)中的“离域π键”可表示为(4)抗坏血酸的分子结构如图所示,分子中碳原子的轨道杂化类型为

更新时间:2023-01-06 15:04:03
|
相似题推荐
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】FeCl3溶液中的Fe3+可用KSCN溶液检验,还可与苯酚发生显色反应,用于酚羟基的检验。
(1) Fe3+的基态简化电子排布式为__________ ,Cl的价电子排布图为_____________ 。
(2) 1个苯酚分子中含有的p-pσ键的数目为_____ ,有____ 个含单电子的p轨道肩并肩平行。
(3) C、N、O三种元素第一电离能从大到小为(填元素名称)_____ ,与SCN-互为等电子体且只含两种元素的分子是_______ (写两种,填化学式)。
(4)基态氮原子价电子排布图不是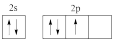 , 是因为该排布方式违背了
, 是因为该排布方式违背了________ 。
(5)设计简单的实验证明非金属性:C<N (需回答实验操作、现象及结论)____________ 。
(1) Fe3+的基态简化电子排布式为
(2) 1个苯酚分子中含有的p-pσ键的数目为
(3) C、N、O三种元素第一电离能从大到小为(填元素名称)
(4)基态氮原子价电子排布图不是
 , 是因为该排布方式违背了
, 是因为该排布方式违背了(5)设计简单的实验证明非金属性:C<N (需回答实验操作、现象及结论)
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】A、B、C、D、E、F均为36号以前的元素,原子序数依次增大。A元素在p区,其基态原子最外层有1个未成对电子;B、C、D为相邻元素,B的最高价氧化物的水化物可以和B的氢化物发生反应;请回答下列问题:
(1)A基态原子的电子排布式为_______ ,其原子核外占据最高能层电子的电子云轮廓图是_______ 形状。
(2)C基态原子的轨道表示式为_______ 。
(3)B、C、D的第一电离能由小到大的顺序是_______ (填元素符号,下同),电负性由小到大的顺序是_______ 。
(4)E的基态原子价层电子在不同形状的原子轨道中运动的电子数相等,并且D、E形成的简单离子电子层结构相同,E在周期表中的位置_______ ,D、E形成的简单离子半径较小的是_______ (填离子符号)。
(5)F元素的基态原子的M能层全充满;N层没有成对电子,只有1个未成对电子。F的元素符号为_______ ,其基态原子的价层电子排布式为_______ ,在元素周期表中位于_______ 区(填“s”、“p”、“d”或“ds”)。
(1)A基态原子的电子排布式为
(2)C基态原子的轨道表示式为
(3)B、C、D的第一电离能由小到大的顺序是
(4)E的基态原子价层电子在不同形状的原子轨道中运动的电子数相等,并且D、E形成的简单离子电子层结构相同,E在周期表中的位置
(5)F元素的基态原子的M能层全充满;N层没有成对电子,只有1个未成对电子。F的元素符号为
您最近一年使用:0次
【推荐3】有A、B、C、D、E、F、G七种元素,它们的原子序数依次增大。其中A、B、C、D、E 、F为短周期主族元素, G为第四周期元素。请回答问题。
(1)F是___________ ,D是___________ (填元素符号)。
(2)B基态原子中能量最高的电子,原子轨道呈___________ 形。
(3)比较键长:A-C___________ A-B (填“>”、“=”或“<”)
(4)G3+ 离子电子排布式为___________ 。
(5)某同学根据上述信息,推断D基态原子的核外电子排布图为,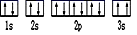 该同学所画的电子排布图违背了
该同学所画的电子排布图违背了___________ 。
(6)金属铜和B的最高价氧化物的水化物的稀溶液可以反应,反应的离子方程式为:___________ 。
| A是宇宙中最丰富的元素,其电子数和电子层数相等 |
| B原子的核外p电子数比s电子数少1 |
| C基态原子L层无空轨道,且成对电子与不成对电子占据的轨道数相等 |
| D原子的第一至第四电离能分别是:I1=730 kJ/mol、I2 = 1455 kJ/mol、I3 = 8633 kJ/mol、I4= 11580 kJ/mol |
| E常温常压下,单质是淡黄色固体,常在火山口附近沉积 |
| F电负性比E大,其单质的水溶液具有漂白性 |
| G在周期表的第八列,是地壳中含量第二位的金属 |
(2)B基态原子中能量最高的电子,原子轨道呈
(3)比较键长:A-C
(4)G3+ 离子电子排布式为
(5)某同学根据上述信息,推断D基态原子的核外电子排布图为,
 该同学所画的电子排布图违背了
该同学所画的电子排布图违背了(6)金属铜和B的最高价氧化物的水化物的稀溶液可以反应,反应的离子方程式为:
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐1】回答下列各小题
(1)现代化学中,常利用_________ 上的特征谱线来鉴定元素。基态氮原子价电子排布图不是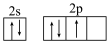 ,是因为该排布方式违背了
,是因为该排布方式违背了__________________ 。
(2)元素硒的基态原子的电子排布式简写为_________ ,第四周期中,与硒原子未成对电子数相同的金属元素有_________ 种。
(3)金属A的原子只有3个电子层,其第一至第四电离能如下:
则A原子的价层电子排布式为__________________ 。
(4)元素铜的第二电离能_________ (填“大于”“小于”或“等于”)锌的第二电离能。
(5) 、
、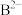 、
、 、D、E、
、D、E、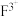 分别表示含10个电子的六种粒子(离子或分子)。其中:
分别表示含10个电子的六种粒子(离子或分子)。其中:
a. 、
、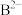 、
、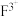 核外电子层结构相同 b.C是由两种元素组成的
核外电子层结构相同 b.C是由两种元素组成的
c.D是两种元素组成的四原子分子 d.E在常温下是无色液体
e.往含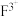 的溶液中滴加含
的溶液中滴加含 的溶液至过量,先有白色沉淀生成,后沉淀消失
的溶液至过量,先有白色沉淀生成,后沉淀消失
①D的空间构型为__________________ ;
②上述粒子中所含元素原子的第一电离能由大到小的顺序为_________ (用元素符号表示);
③用电子式表示 的形成过程
的形成过程____________________________________ ;
④与C组成元素相同且含18个电子的分子M中,孤电子对与 键的数目之比为
键的数目之比为_________ 。
(1)现代化学中,常利用
 ,是因为该排布方式违背了
,是因为该排布方式违背了(2)元素硒的基态原子的电子排布式简写为
(3)金属A的原子只有3个电子层,其第一至第四电离能如下:
电离能( ) ) |  |  |  |  |
| A | 932 | 1821 | 15390 | 21771 |
(4)元素铜的第二电离能
(5)
 、
、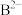 、
、 、D、E、
、D、E、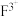 分别表示含10个电子的六种粒子(离子或分子)。其中:
分别表示含10个电子的六种粒子(离子或分子)。其中:a.
 、
、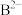 、
、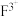 核外电子层结构相同 b.C是由两种元素组成的
核外电子层结构相同 b.C是由两种元素组成的c.D是两种元素组成的四原子分子 d.E在常温下是无色液体
e.往含
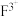 的溶液中滴加含
的溶液中滴加含 的溶液至过量,先有白色沉淀生成,后沉淀消失
的溶液至过量,先有白色沉淀生成,后沉淀消失①D的空间构型为
②上述粒子中所含元素原子的第一电离能由大到小的顺序为
③用电子式表示
 的形成过程
的形成过程④与C组成元素相同且含18个电子的分子M中,孤电子对与
 键的数目之比为
键的数目之比为
您最近一年使用:0次
【推荐2】回答下列问题
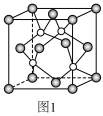
(1)铜的氢化物晶体的一种结构如图1所示,写出此氢化物在氯气中燃烧的化学方程式____________ ;____________ ;_________ ; 的原因是
的原因是____________ ;
(5)活性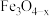 是
是 转化为
转化为 的催化剂,其可能反应机理如图所示.根据元素电负性的变化规律,如图所示的反应步骤I可描述为
的催化剂,其可能反应机理如图所示.根据元素电负性的变化规律,如图所示的反应步骤I可描述为____________ 。
(1)铜的氢化物晶体的一种结构如图1所示,写出此氢化物在氯气中燃烧的化学方程式
 的原因是
的原因是(5)活性
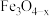 是
是 转化为
转化为 的催化剂,其可能反应机理如图所示.根据元素电负性的变化规律,如图所示的反应步骤I可描述为
的催化剂,其可能反应机理如图所示.根据元素电负性的变化规律,如图所示的反应步骤I可描述为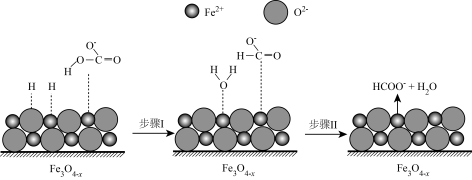
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】我国硒含量居世界首位,含硒化合物与材料被广泛应用于合成化学、催化化学医学研究、环境保护、农业化学品等方面。
(1)硒原子核外电子排布式为_______
(2)人体代谢甲硒醇(CH3SeH)后可增加抗癌活性,甲硒醇分子中碳原子和硒原子的杂化类型分别是_______ 、_______ 。下表中有机物沸点不同的原因是_______ 。
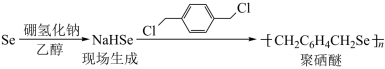
(3)NaHSe可用于合成聚硒醚,NaHSe晶体类型为_______ ,得到NaHSe过程中生成的化学键类型为_______ 。聚硒醚能清除水中的铅污染,其原因是_______ 。
(4)硒酸是一种强酸,根据价层电子对互斥理论的推测,其阴离子空间构型是_______
(5)Na2Se的晶体结构如下图所示,其晶胞参数为anm,阿伏加德罗常数值为NA.则Na2Se的晶胞密度为_______ g·cm-3(列出计算式)。

(1)硒原子核外电子排布式为
(2)人体代谢甲硒醇(CH3SeH)后可增加抗癌活性,甲硒醇分子中碳原子和硒原子的杂化类型分别是
| 有机物 | 甲醇 | 甲硫醇 | 甲硒醇 |
| 沸点/℃ | 64.7 | 5.95 | 25.05 |

(4)硒酸是一种强酸,根据价层电子对互斥理论的推测,其阴离子空间构型是
(5)Na2Se的晶体结构如下图所示,其晶胞参数为anm,阿伏加德罗常数值为NA.则Na2Se的晶胞密度为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】电能是一种无污染、可再生的二级能源。储电材料种类繁多。如图是两种储电材料,请阅读试题,观察图片,回答问题。
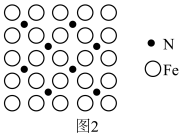
Ⅰ.新型碳氮材料的储电能力应用前景广阔。其基本构成单元如图所示。
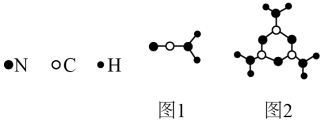
(1)图1中化学键σ键与π键之比为________ ;图2中碳原子的杂化方式为________ 。
(2)在基态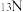 原子中,核外存在
原子中,核外存在_____ 对自旋相反的电子,核外电子占据的最高能级的电子云轮廓图为____ 形。
(3)碳的最高价含氧酸根的空间构型是__________ ;硝酸的酸性强于亚硝酸的原因是__________ 。
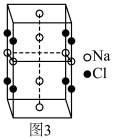
Ⅱ.传统锂电池的主要成分是 ,其晶胞结构如图所示;因结构中存在笼状空隙,可以与
,其晶胞结构如图所示;因结构中存在笼状空隙,可以与 和
和 发生位置替换,形成储电性能更加优良的化合物
发生位置替换,形成储电性能更加优良的化合物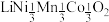 。
。
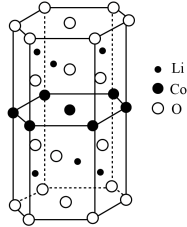
(4)基态 原子的价电子排布式为
原子的价电子排布式为_____________ ;化合物 中O元素在晶胞中的位置,除了位于正六棱柱的顶点外,其他具体位置是
中O元素在晶胞中的位置,除了位于正六棱柱的顶点外,其他具体位置是__________ 。
(5)已知化合物中各原子半径依次为: ,晶胞的棱长为m,底边边长为n,该晶体的空间利用率的计算表达式为
,晶胞的棱长为m,底边边长为n,该晶体的空间利用率的计算表达式为__________ (用含有a、b、c、d、e、m、n的式子表示)。
Ⅰ.新型碳氮材料的储电能力应用前景广阔。其基本构成单元如图所示。

(1)图1中化学键σ键与π键之比为
(2)在基态
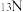 原子中,核外存在
原子中,核外存在(3)碳的最高价含氧酸根的空间构型是
Ⅱ.传统锂电池的主要成分是
 ,其晶胞结构如图所示;因结构中存在笼状空隙,可以与
,其晶胞结构如图所示;因结构中存在笼状空隙,可以与 和
和 发生位置替换,形成储电性能更加优良的化合物
发生位置替换,形成储电性能更加优良的化合物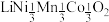 。
。
(4)基态
 原子的价电子排布式为
原子的价电子排布式为 中O元素在晶胞中的位置,除了位于正六棱柱的顶点外,其他具体位置是
中O元素在晶胞中的位置,除了位于正六棱柱的顶点外,其他具体位置是(5)已知化合物中各原子半径依次为:
 ,晶胞的棱长为m,底边边长为n,该晶体的空间利用率的计算表达式为
,晶胞的棱长为m,底边边长为n,该晶体的空间利用率的计算表达式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】A、B、C、D、E均为短周期元素,非金属元素A的最外层电子数与其周期数相等,B的成对电子与未成对电子所占据的原子轨道数相等。单质B在单质C中充分燃烧生成BC2。 D+与C2-具有相同的电子数。A在E中燃烧,产物溶于水会得到一种强酸。
(1)B在元素周期表中的位置是________ ,写出一种工业制备单质E的化学方程式:_____ 。
(2)B、C、D组成的一种盐中,B的质量分数为17. 91%,D的质量分数为34. 3 3%。该盐的化学式为________ ,其阴离子中B原子的杂化方式为__________ 。
(3)由这些元素组成的某些物质的组成和结构信息如下表:
a的电子式为_________ ;b的化学式为________ ;c的空间构型为___________ 。
(1)B在元素周期表中的位置是
(2)B、C、D组成的一种盐中,B的质量分数为17. 91%,D的质量分数为34. 3 3%。该盐的化学式为
(3)由这些元素组成的某些物质的组成和结构信息如下表:
| 物质 | 组成和结构 |
| a | A、D两元素组成的离子化合物 |
| b | 由C、D两元素组成的含有非极性键的离子化合物 |
| c | 化学组成为BCE2 |
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】 是环境友好材料,能光催化降解有机物。回答下列问题:
是环境友好材料,能光催化降解有机物。回答下列问题:
(1)基态Ti原子核外电子占据的最高能级符号为___________ ,价电子中未成对电子有___________ 个。
(2)二氧化钛与 (光气)、
(光气)、 (二氯亚砜)等氯化试剂反应可用于制取四氯化钛。
(二氯亚砜)等氯化试剂反应可用于制取四氯化钛。
① (光气)的立体构型为
(光气)的立体构型为___________ , 中
中 键和
键和 键的数目比为
键的数目比为___________ 。
② (二氯亚砜)是
(二氯亚砜)是___________ 分子。(填“极性”或“非极性”)
(3)香豆素(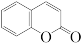 )是一种天然香料,能被
)是一种天然香料,能被 光降解。
光降解。
①分子中C原子的杂化类型是___________ 。
②已知单双键交替的共轭结构可以形成大π键,大π键可用符号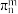 表示,其中n代表参与形成大π键的原子数,m代表参与形成大π键的电子数(如苯分子中的大π键可表示为
表示,其中n代表参与形成大π键的原子数,m代表参与形成大π键的电子数(如苯分子中的大π键可表示为 ),则香豆素中的大π键应表示为
),则香豆素中的大π键应表示为___________ 。
 是环境友好材料,能光催化降解有机物。回答下列问题:
是环境友好材料,能光催化降解有机物。回答下列问题:(1)基态Ti原子核外电子占据的最高能级符号为
(2)二氧化钛与
 (光气)、
(光气)、 (二氯亚砜)等氯化试剂反应可用于制取四氯化钛。
(二氯亚砜)等氯化试剂反应可用于制取四氯化钛。①
 (光气)的立体构型为
(光气)的立体构型为 中
中 键和
键和 键的数目比为
键的数目比为②
 (二氯亚砜)是
(二氯亚砜)是(3)香豆素(
 )是一种天然香料,能被
)是一种天然香料,能被 光降解。
光降解。①分子中C原子的杂化类型是
②已知单双键交替的共轭结构可以形成大π键,大π键可用符号
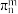 表示,其中n代表参与形成大π键的原子数,m代表参与形成大π键的电子数(如苯分子中的大π键可表示为
表示,其中n代表参与形成大π键的原子数,m代表参与形成大π键的电子数(如苯分子中的大π键可表示为 ),则香豆素中的大π键应表示为
),则香豆素中的大π键应表示为
您最近一年使用:0次



