有A、B、C、D、E、F、G七种元素,它们的原子序数依次增大。其中A、B、C、D、E 、F为短周期主族元素, G为第四周期元素。请回答问题。
(1)F是___________ ,D是___________ (填元素符号)。
(2)B基态原子中能量最高的电子,原子轨道呈___________ 形。
(3)比较键长:A-C___________ A-B (填“>”、“=”或“<”)
(4)G3+ 离子电子排布式为___________ 。
(5)某同学根据上述信息,推断D基态原子的核外电子排布图为,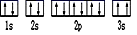 该同学所画的电子排布图违背了
该同学所画的电子排布图违背了___________ 。
(6)金属铜和B的最高价氧化物的水化物的稀溶液可以反应,反应的离子方程式为:___________ 。
| A是宇宙中最丰富的元素,其电子数和电子层数相等 |
| B原子的核外p电子数比s电子数少1 |
| C基态原子L层无空轨道,且成对电子与不成对电子占据的轨道数相等 |
| D原子的第一至第四电离能分别是:I1=730 kJ/mol、I2 = 1455 kJ/mol、I3 = 8633 kJ/mol、I4= 11580 kJ/mol |
| E常温常压下,单质是淡黄色固体,常在火山口附近沉积 |
| F电负性比E大,其单质的水溶液具有漂白性 |
| G在周期表的第八列,是地壳中含量第二位的金属 |
(2)B基态原子中能量最高的电子,原子轨道呈
(3)比较键长:A-C
(4)G3+ 离子电子排布式为
(5)某同学根据上述信息,推断D基态原子的核外电子排布图为,
 该同学所画的电子排布图违背了
该同学所画的电子排布图违背了(6)金属铜和B的最高价氧化物的水化物的稀溶液可以反应,反应的离子方程式为:
更新时间:2022-09-26 19:58:47
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】如图所示是部分短周期元素原子半径与原子序数的关系,回答下列问题:
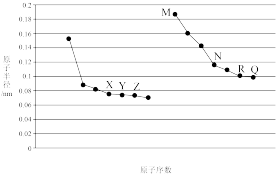
(1)X在周期表中的位置是_______ 。
(2)X、Q的最高价氧化物对应的水化物中,酸性较强的物质是_______ 。(填化学式)。
(3)用电子式表示化合物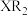 的形成过程
的形成过程_______ 。
(4)请写出实验室制备Y的气态氢化物的化学方程式_______ 。
(5)铜与Y的最高价氧化物对应的水化合物浓溶液发生反应的离子方程式为_______ 。
(6)在溶液中,元素Z、M、R形成的某化合物与R的最高价氧化物对应的水化合物稀溶液之间反应既能产生无色刺激性气味气体,又能产生淡黄色沉淀,请写出发生反应的离子方程式_______ 。
(7)为验证卤族部分元素单质氯化性的递变规律,设计如图装置进行实验,请回答:
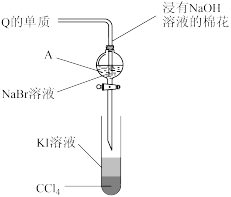
为验证 与
与 的氧化性强弱:通入一定量Q的单质,充分反应后,将A中液体滴入试管内,取下试管,充分振荡、静置,可观察到
的氧化性强弱:通入一定量Q的单质,充分反应后,将A中液体滴入试管内,取下试管,充分振荡、静置,可观察到_______ ;该实验必须控制加入的Q单质的量,否则得不出 的氧化性比
的氧化性比 强。理由是
强。理由是_______ 。

(1)X在周期表中的位置是
(2)X、Q的最高价氧化物对应的水化物中,酸性较强的物质是
(3)用电子式表示化合物
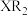 的形成过程
的形成过程(4)请写出实验室制备Y的气态氢化物的化学方程式
(5)铜与Y的最高价氧化物对应的水化合物浓溶液发生反应的离子方程式为
(6)在溶液中,元素Z、M、R形成的某化合物与R的最高价氧化物对应的水化合物稀溶液之间反应既能产生无色刺激性气味气体,又能产生淡黄色沉淀,请写出发生反应的离子方程式
(7)为验证卤族部分元素单质氯化性的递变规律,设计如图装置进行实验,请回答:

为验证
 与
与 的氧化性强弱:通入一定量Q的单质,充分反应后,将A中液体滴入试管内,取下试管,充分振荡、静置,可观察到
的氧化性强弱:通入一定量Q的单质,充分反应后,将A中液体滴入试管内,取下试管,充分振荡、静置,可观察到 的氧化性比
的氧化性比 强。理由是
强。理由是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】如图是中学化学中常见四种物质在一定条件下的转化关系(其他产物已略去)。根据所学知识,回答下列问题:
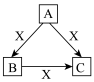
(1)若B、X都是气体单质,C遇空气变为红棕色气体,A遇湿润的红色石蕊试纸变蓝,A在纯氧气中点燃可生成单质B,则A是____ 。写出反应A→C的化学方程式_______
(2)若A是地壳中含量第二位的金属单质,X是一种常见最高价易挥发的含氧酸,常温下,发生如图转化关系,则X是____ (填化学名称),B是____ ,写出反应A→C的离子方程式:______ ;C→B的离子方程式:_______ 。

(1)若B、X都是气体单质,C遇空气变为红棕色气体,A遇湿润的红色石蕊试纸变蓝,A在纯氧气中点燃可生成单质B,则A是
(2)若A是地壳中含量第二位的金属单质,X是一种常见最高价易挥发的含氧酸,常温下,发生如图转化关系,则X是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐3】我国电池的年市场消费量约为80亿只,其中70%是锌锰干电池,利用废旧锌锰干电池的炭包(含碳粉、Fe、Cu、Ag和MnO2等物质)制备纯MnO2的工艺如下图所示:
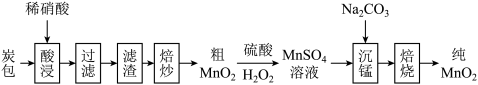
回答下列问题:
(1)在“酸浸”时为了加快浸出速率,可采取的措施有___________ 。(写出一点即可)。“酸浸”过程中稀硝酸是过量的,Fe和稀硝酸反应生成NO的离子方程式为___________ ,用于检验该反应生成的金属阳离子的试剂是___________ 。
(2)“焙炒”的目的是___________ 。
(3)在粗MnO2溶解时,氧化剂与还原剂的物质的量之比为___________ ,溶解过程中所用的H2O2高于理论用量,原因是___________ 。
(4)沉锰后焙烧时,发生反应的化学方程式为___________ 。

回答下列问题:
(1)在“酸浸”时为了加快浸出速率,可采取的措施有
(2)“焙炒”的目的是
(3)在粗MnO2溶解时,氧化剂与还原剂的物质的量之比为
(4)沉锰后焙烧时,发生反应的化学方程式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】已知X、Y、Z、M、G、Q是六种短周期主族元素,原子序数依次增大,X、Z、Q的单质在常温下呈气态;Y的原子最外层电子数是其电子层数的2倍;X与M同主族;Z、G分别是地壳中含量最高的非金属元素和金属元素。请回答下列问题:
(1)M在元素周期表中的位置为____________ 。
(2)X 与Y能形成多种化合物,其中既含极性键又含非极性键,且相对分子质量最小的物质是(写分子式)_______ ,在实验室中,制取该物质的反应原理是(写化学方程:式)________ 。
(3)MX与水反应可放出气体,该反应的化学方程式为____________ 。.
(4)常温下不能与G的单质发生反应的是(填序号)_________ 。
a.CuSO4溶液 b. Fe2O3 c.浓硫酸 d. NaOH溶液 e. Na2CO3固体
(5)工业上若以石墨为电极电解制G的单质,阳极产生混合气体的成分是(写化学式)______ 。
(1)M在元素周期表中的位置为
(2)X 与Y能形成多种化合物,其中既含极性键又含非极性键,且相对分子质量最小的物质是(写分子式)
(3)MX与水反应可放出气体,该反应的化学方程式为
(4)常温下不能与G的单质发生反应的是(填序号)
a.CuSO4溶液 b. Fe2O3 c.浓硫酸 d. NaOH溶液 e. Na2CO3固体
(5)工业上若以石墨为电极电解制G的单质,阳极产生混合气体的成分是(写化学式)
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】A、B、C、D、E都为短周期元素,A是相对原子质量最小的元素;B的+1价阳离子和C的-1价阴离子都与氖原子具有相同的电子层结构;D在C的下一周期,可与B形成BD型离子化合物;E和C为同一周期元素,其最高价氧化物对应的水化物为一种强酸。请根据以上信息回答下列问题:
(1)C元素在元素周期表中的位置是________________
(2)画出B元素的离子结构示意图______________
(3)与E的氢化物分子所含电子总数相等的分子是_____ (举一例,填化学式,下同)、离子是_________
(4)D的单质与B的最高价氧化物对应的水化物的溶液发生反应的离子方程式为_________
(5)写出A元素与B元素形成化合物的化学式________
(6)下列可以判断C和D非金属性强弱的是_______
a.单质的熔点C比D低 b.单质与氢气反应C比D剧烈
c.气态氢化物稳定性C比D稳定 d.单质的密度C比D小
(1)C元素在元素周期表中的位置是
(2)画出B元素的离子结构示意图
(3)与E的氢化物分子所含电子总数相等的分子是
(4)D的单质与B的最高价氧化物对应的水化物的溶液发生反应的离子方程式为
(5)写出A元素与B元素形成化合物的化学式
(6)下列可以判断C和D非金属性强弱的是
a.单质的熔点C比D低 b.单质与氢气反应C比D剧烈
c.气态氢化物稳定性C比D稳定 d.单质的密度C比D小
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】下表为元素周期表的一部分,其中的编号代表对应的元素。
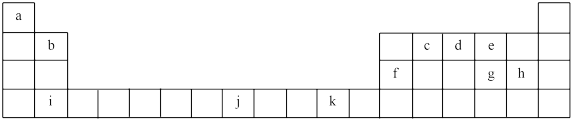
请回答下列问题:
(1)表中属于d区的元素是_______ (填元素名称),其形成的常见阳离子中化学性质较稳定的是_______ (填离子符号)。
(2)e基态原子中能量最高的电子,其电子云轮廓图的取向有_______ 个。
(3)下列状态的f的微粒中,电离最外层的一个电子所需能量最小的是_______(填序号)。
(4)某种离子化合物由a、d两元素形成,猜测其电子式为_______ 。
(5)与k同周期的所有元素的基态原子中未成对电子数最多的是_______ (填元素符号),写出该元素的基态原子的价电子排布式:_______ 。
(6)常温下,液态化合物geh2与水剧烈反应,产生能使品红溶液褪色的ge2气体,向反应后的溶液中加入AgNO3溶液,有不溶于稀硝酸的白色沉淀析出。根据实验现象,写出geh2与水反应的化学方程式_______ 。
(7)碱性条件下,ca4燃料电池的负极反应式为:_______ 。
(8)Xe是第五周期的稀有气体元素,与F形成的XeF2室温下易升华。XeF2中心原子的价层电子对数为_______ ,下列对XeF2中心原子杂化方式推断合理的是_______ (填标号)。
A.sp B.sp2 C.sp3 D.sp3d

请回答下列问题:
(1)表中属于d区的元素是
(2)e基态原子中能量最高的电子,其电子云轮廓图的取向有
(3)下列状态的f的微粒中,电离最外层的一个电子所需能量最小的是_______(填序号)。
| A.[Ne] | B.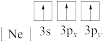 | C.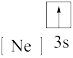 | D. |
(5)与k同周期的所有元素的基态原子中未成对电子数最多的是
(6)常温下,液态化合物geh2与水剧烈反应,产生能使品红溶液褪色的ge2气体,向反应后的溶液中加入AgNO3溶液,有不溶于稀硝酸的白色沉淀析出。根据实验现象,写出geh2与水反应的化学方程式
(7)碱性条件下,ca4燃料电池的负极反应式为:
(8)Xe是第五周期的稀有气体元素,与F形成的XeF2室温下易升华。XeF2中心原子的价层电子对数为
A.sp B.sp2 C.sp3 D.sp3d
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐1】A、B、C、D、E、F均为36号以前的元素。请完成下列空白:
(1)A元素的原子最外层电子排布式为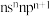 ,位于元素周期表第
,位于元素周期表第___________ 周期第___________ 族。
(2)B元素基态原子的最外层有2个未成对电子,次外层有2个电子,其元素符号为___________ 。
(3)C元素基态的正三价离子的3d轨道为半充满,其元素符号为___________ ,其基态原子的电子排布式为___________ 。
(4)D元素基态原子的M层全充满;N层没有成对电子,只有一个未成对电子。D元素位于元素周期表___________ 区(填“s”、“p”、“d”、“”或“ds”)。其基态原子的价层电子的轨道表示为___________ 。
(5)E、F元素的基态原子都只有一个未成对电子;它们相互作用可形成中学化学常见的离表示式为子化合物,并且阴、阳离子的电子层结构相同,最高能级的电子对数等于其最高能层的电子层数;则此离子化合物的化学式为___________ 。
(1)A元素的原子最外层电子排布式为
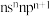 ,位于元素周期表第
,位于元素周期表第(2)B元素基态原子的最外层有2个未成对电子,次外层有2个电子,其元素符号为
(3)C元素基态的正三价离子的3d轨道为半充满,其元素符号为
(4)D元素基态原子的M层全充满;N层没有成对电子,只有一个未成对电子。D元素位于元素周期表
(5)E、F元素的基态原子都只有一个未成对电子;它们相互作用可形成中学化学常见的离表示式为子化合物,并且阴、阳离子的电子层结构相同,最高能级的电子对数等于其最高能层的电子层数;则此离子化合物的化学式为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】太阳能的开发利用在新能源研究中占据重要地位.单晶硅太阳能电池片在加工时,一般掺杂微置的锎、硼、镓、硒等.
回答下列问题:
(1)二价铜离子的电子排布式为___________ .已知高温下Cu2O比CuO更稳定,试从铜原子核外电子结构变化角度解释
(2)(2)铜与类卤素(SCN)2反应生成Cu(SCN)2,1mol(SCN)2中含有π键的数目为_________ .类卤素(SCN)2对应的酸有两种,理论上硫氰酸(H﹣S﹣C≡N)的沸点低于异硫氰酸(H﹣N=C=S)的沸点,其原因是_________________ .
(3)硼元素具有缺电子性,其化合物可与具有孤电子对的分子或离子形成配合物,如BF3能与NH3反应生成BF3·NH3;在BF3·NH3中B原子的杂化方式为_________ ,B与N之间形成配位键,氮原子提供_____________ .
(4)六方氮化硼晶体结构与石墨晶体相似,层间相互作用为________ ;六方氮化硼在高温高压下,可以转化为立方氮化硼,其结构和硬度都与金刚石相似,晶胞边长为361.5pm,立方氮化硼的密度是__________ g/cm3;(只要求列算式).
(5)如图是立方氮化硼晶胞沿z轴的投影图,请在图中圆球上涂“●”和画“×”分别标明B与N的相对位置:________
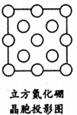
回答下列问题:
(1)二价铜离子的电子排布式为
(2)(2)铜与类卤素(SCN)2反应生成Cu(SCN)2,1mol(SCN)2中含有π键的数目为
(3)硼元素具有缺电子性,其化合物可与具有孤电子对的分子或离子形成配合物,如BF3能与NH3反应生成BF3·NH3;在BF3·NH3中B原子的杂化方式为
(4)六方氮化硼晶体结构与石墨晶体相似,层间相互作用为
(5)如图是立方氮化硼晶胞沿z轴的投影图,请在图中圆球上涂“●”和画“×”分别标明B与N的相对位置:

您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐3】现有七种元素,其中A、B、C、D、E为短周期主族元素,F、G为第四周期元素,它们的原子序数依次增大。请根据下列相关信息,回答问题。
(1)已知BA5为离子化合物,写出其电子式:____________ 。
(2)B基态原子中能量最高的电子,其电子云在空间有________ 个方向,原子轨道呈________ 形。
(3)某同学根据上述信息,推断C基态原子的核外电子排布图为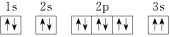 。该同学所画的电子排布图违背了
。该同学所画的电子排布图违背了________ 。
(4)G位于__________ 族__________ 区,价电子排布式为__________ 。
| 元素 | 相关信息 |
| A | 元素的核外电子数和电子层数相等,也是宇宙中最丰富的元素 |
| B | 元素原子的核外p电子数比s电子数少1 |
| C | 原子的第一至第四电离能分别是 I1=738 kJ/mol;I2=1 451 kJ/mol; I3=7 733 kJ/mol;I4=10 540 kJ/mol |
| D | 原子核外所有p轨道全满或半满 |
| E | 元素的主族序数与周期数的差为4 |
| F | 是前四周期中电负性最小的元素 |
| G | 在周期表的第七列 |
(2)B基态原子中能量最高的电子,其电子云在空间有
(3)某同学根据上述信息,推断C基态原子的核外电子排布图为
 。该同学所画的电子排布图违背了
。该同学所画的电子排布图违背了(4)G位于
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】根据元素的特征完成下列问题。
I.元素A、B、J、D、E、F、G是元素周期表前四周期的常见元素,且原子序数依次增大,其相关信息如表所示,请回答下列问题。
(1)在下列物质中属于离子化合物的是有___________ ,仅含共价键的有___________ 。
①AF ②DF ③ ④
④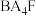
(2)E的单质与D的最高价氧化物对应水化物溶液反应的离子方程式为___________ 。
(3)B原子能与碳原子形成化学式为 的链状分子,其中所有原子都满足8电子稳定结构。
的链状分子,其中所有原子都满足8电子稳定结构。 的电子式为
的电子式为___________ 。
(4)在X中,G元素基态离子的价层电子的轨道排布式为___________ 。
Ⅱ.几种短周期元素的原子结构和性质如下所示:
(5)元素②的离子结构示意图为___________ 。
(6)元素⑦的简单氢化物与少量⑤的单质反应时,观察到有大量白烟产生,同时得到氮气。该反应中,氧化剂与还原剂的物质的量之比为___________ 。
(7)元素①和③的单质相互反应得到产物Y。用电子式表示Y 形成过程为___________ 。
I.元素A、B、J、D、E、F、G是元素周期表前四周期的常见元素,且原子序数依次增大,其相关信息如表所示,请回答下列问题。
| A | 原子核外电子只有一种运动状态 |
| B | 简单离子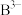 与D的离子具有相同电子排布 与D的离子具有相同电子排布 |
| J | 基态原子中s电子总数与p电子总数相等 |
| D | 元素的焰色试验呈黄色 |
| E | 基态原子价层电子排布式为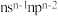 |
| F | 在基态原子的最外层上,p轨道有2个电子的自旋状态与其他电子相反 |
| G | 生活中使用最多的一种金属,其某种盐X溶液常用于刻蚀铜制印刷电路 |
①AF ②DF ③
 ④
④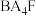
(2)E的单质与D的最高价氧化物对应水化物溶液反应的离子方程式为
(3)B原子能与碳原子形成化学式为
 的链状分子,其中所有原子都满足8电子稳定结构。
的链状分子,其中所有原子都满足8电子稳定结构。 的电子式为
的电子式为(4)在X中,G元素基态离子的价层电子的轨道排布式为
Ⅱ.几种短周期元素的原子结构和性质如下所示:
| 序号 | ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ |
| 最外层电子数 | 6 | 1 | 1 | ||||
| 原子半径/nm | 0.074 | 0.16 | 0.152 | 0.11 | 0.099 | 0.186 | 0.075 |
| 主要化合价 | +2 | -3,+5 | -1,+7 | -3,+5 |
(6)元素⑦的简单氢化物与少量⑤的单质反应时,观察到有大量白烟产生,同时得到氮气。该反应中,氧化剂与还原剂的物质的量之比为
(7)元素①和③的单质相互反应得到产物Y。用电子式表示Y 形成过程为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】下图是元素周期表(局部示意图),其中a、b、c、d、e、f为元素代号。

(1)写出a的基态原子核外电子排布式 _______ ;画出b的基态原子的轨道表示式 _______ ;
(2)b和e两元素的原子以_______ (填化学键类型)形成化合物;
(3)b、c、d三种元素中,原子半径最大的是_______ (用其原子结构示意图 表示)离子半径最大的是_______ (用离子的电子式 表示);
(4)举一实验事实来比较说明c与d的金属性强弱关系_______ ;
(5)下列有关元素周期表的叙述中,错误的是_______(填序号)

(1)写出a的基态原子
(2)b和e两元素的原子以
(3)b、c、d三种元素中,原子半径最大的是
(4)举一实验事实来比较说明c与d的金属性强弱关系
(5)下列有关元素周期表的叙述中,错误的是_______(填序号)
| A.位于金属非金属分界线附近的元素既表现金属的某些性质,又表现非金属的某些性质 |
| B.人们在金属非金属分界线附近寻找催化剂 |
| C.元素b的最高价氧化物对应的水化物的酸性是最强的 |
D.在 的七种元素中,f的金属性最强 的七种元素中,f的金属性最强 |
您最近一年使用:0次
【推荐3】根据原子结构、元素周期表和元素周期律的知识回答下列问题:
(1)X元素基态原子次外层电子数是最外层电子数的 ,其价电子轨道表示式是
,其价电子轨道表示式是____ 。
(2)Y是1~36号元素原子核外电子排布中未成对电子数最多的元素,Y元素的名称是____ ,在元素周期表中的位置是___ 。
(3)Z元素基态原子的轨道表示式是图中的____ (填写序号),____ 。
a.能量最低原理 b.泡利不相容原理 c.洪特规则
(4)第三周期元素的气态电中性基态原子失去最外层一个电子转化为气态基态正离子所需的最低能量叫作第一电离能(I1)。如图所示:____ 。
②根据图中提供的信息,可推断出I氧____ I氟(填“>”“<”或“=”,下同)。
③根据第一电离能的含义和元素周期律,可推断出I镁____ I钙。
(1)X元素基态原子次外层电子数是最外层电子数的
 ,其价电子轨道表示式是
,其价电子轨道表示式是(2)Y是1~36号元素原子核外电子排布中未成对电子数最多的元素,Y元素的名称是
(3)Z元素基态原子的轨道表示式是图中的
①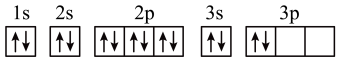
②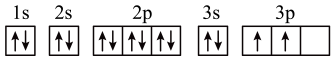
a.能量最低原理 b.泡利不相容原理 c.洪特规则
(4)第三周期元素的气态电中性基态原子失去最外层一个电子转化为气态基态正离子所需的最低能量叫作第一电离能(I1)。如图所示:
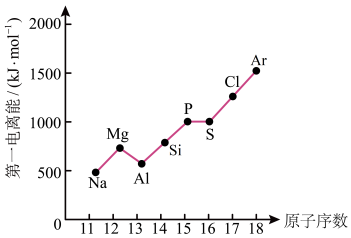
②根据图中提供的信息,可推断出I氧
③根据第一电离能的含义和元素周期律,可推断出I镁
您最近一年使用:0次



