回答下列问题
(1)铜的氢化物晶体的一种结构如图1所示,写出此氢化物在氯气中燃烧的化学方程式____________ ;____________ ;_________ ; 的原因是
的原因是____________ ;
(5)活性 是
是 转化为
转化为 的催化剂,其可能反应机理如图所示.根据元素电负性的变化规律,如图所示的反应步骤I可描述为
的催化剂,其可能反应机理如图所示.根据元素电负性的变化规律,如图所示的反应步骤I可描述为____________ 。
(1)铜的氢化物晶体的一种结构如图1所示,写出此氢化物在氯气中燃烧的化学方程式
 的原因是
的原因是(5)活性
 是
是 转化为
转化为 的催化剂,其可能反应机理如图所示.根据元素电负性的变化规律,如图所示的反应步骤I可描述为
的催化剂,其可能反应机理如图所示.根据元素电负性的变化规律,如图所示的反应步骤I可描述为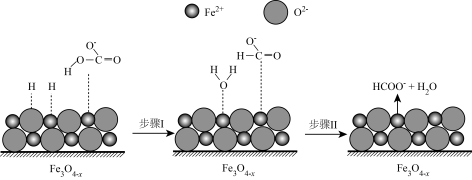
更新时间:2024-04-15 09:13:31
|
相似题推荐
解答题-结构与性质
|
适中
(0.65)
【推荐1】东晋《华阳国志南中志》卷四中已有关于白铜的记载,云南镍白铜(铜镍合金)闻名中外,曾主要用于造币,亦可用于制作仿银饰品。回答下列问题:
(1)镍元素基态原子的电子排布式为_____ ,3d能级上的未成对的电子数为_____ 。
(2)硫酸镍溶于氨水形成[Ni(NH3)6]SO4蓝色溶液。
①[Ni(NH3)6]SO4中阴离子的立体构型是_____ 。
②氨的沸点_____ (“高于”或“低于”)膦(PH3),原因是_____ ;氨是_____ 分子(填“极性”或“非极性”),中心原子的轨道杂化类型为_____ 。
(3)单质铜及镍都是由_____ 键形成的晶体,元素铜与镍的第二电离能分别为:I(Cu)=1959kJ/mol,I(Ni)=1753kJ/mol,I(Cu)>I(Ni)的原因是_____ 。
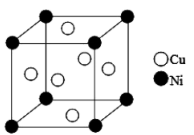
(4)某镍白铜合金的立方晶胞结构如图所示。晶胞中铜原子与镍原子的数量比为_____ 。
(1)镍元素基态原子的电子排布式为
(2)硫酸镍溶于氨水形成[Ni(NH3)6]SO4蓝色溶液。
①[Ni(NH3)6]SO4中阴离子的立体构型是
②氨的沸点
(3)单质铜及镍都是由
(4)某镍白铜合金的立方晶胞结构如图所示。晶胞中铜原子与镍原子的数量比为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】下表为元素周期表的一部分,其中的编号代表对应的元素。
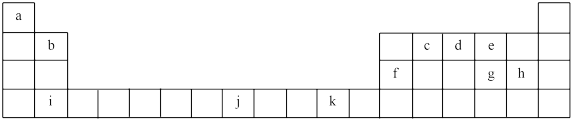
请回答下列问题:
(1)表中属于d区的元素是_______ (填元素名称),其形成的常见阳离子中化学性质较稳定的是_______ (填离子符号)。
(2)e基态原子中能量最高的电子,其电子云轮廓图的取向有_______ 个。
(3)下列状态的f的微粒中,电离最外层的一个电子所需能量最小的是_______(填序号)。
(4)某种离子化合物由a、d两元素形成,猜测其电子式为_______ 。
(5)与k同周期的所有元素的基态原子中未成对电子数最多的是_______ (填元素符号),写出该元素的基态原子的价电子排布式:_______ 。
(6)常温下,液态化合物geh2与水剧烈反应,产生能使品红溶液褪色的ge2气体,向反应后的溶液中加入AgNO3溶液,有不溶于稀硝酸的白色沉淀析出。根据实验现象,写出geh2与水反应的化学方程式_______ 。
(7)碱性条件下,ca4燃料电池的负极反应式为:_______ 。
(8)Xe是第五周期的稀有气体元素,与F形成的XeF2室温下易升华。XeF2中心原子的价层电子对数为_______ ,下列对XeF2中心原子杂化方式推断合理的是_______ (填标号)。
A.sp B.sp2 C.sp3 D.sp3d

请回答下列问题:
(1)表中属于d区的元素是
(2)e基态原子中能量最高的电子,其电子云轮廓图的取向有
(3)下列状态的f的微粒中,电离最外层的一个电子所需能量最小的是_______(填序号)。
| A.[Ne] | B.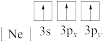 | C.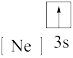 | D. |
(5)与k同周期的所有元素的基态原子中未成对电子数最多的是
(6)常温下,液态化合物geh2与水剧烈反应,产生能使品红溶液褪色的ge2气体,向反应后的溶液中加入AgNO3溶液,有不溶于稀硝酸的白色沉淀析出。根据实验现象,写出geh2与水反应的化学方程式
(7)碱性条件下,ca4燃料电池的负极反应式为:
(8)Xe是第五周期的稀有气体元素,与F形成的XeF2室温下易升华。XeF2中心原子的价层电子对数为
A.sp B.sp2 C.sp3 D.sp3d
您最近一年使用:0次
【推荐3】若元素原子的最外电子层只有一个电子,该电子的电子层数n=4。请回答下列问题:
(1)符合上述条件的元素共有_______ 种。
(2)在符合上述条件的元素中,原子序数最小的在周期表的_______ 区(用符号填空),原子序数最大的在周期表的第_______ 周期、_______ 族。
(3)过渡元素的金属离子与水分子形成的配合物是否有颜色,与其d轨道电子排布有关。一般而言,为d0或d10排布时,无颜色,为d1~d9排布时,有颜色,如[Co(H2O)6]2+显粉红色。据此判断,[Mn(H2O)6]2+_______ 颜色(填“无”或“有”)。
(4)符合上述条件的元素中,原子序数最大、且与水分子形成的配合物有颜色的简单离子的符号为_______ 。
(1)符合上述条件的元素共有
(2)在符合上述条件的元素中,原子序数最小的在周期表的
(3)过渡元素的金属离子与水分子形成的配合物是否有颜色,与其d轨道电子排布有关。一般而言,为d0或d10排布时,无颜色,为d1~d9排布时,有颜色,如[Co(H2O)6]2+显粉红色。据此判断,[Mn(H2O)6]2+
(4)符合上述条件的元素中,原子序数最大、且与水分子形成的配合物有颜色的简单离子的符号为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】已知①---⑩号元素在周期表中的位置如图。试回答下列问题:
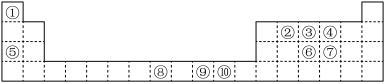
(1)上述元素中属于d区的有:________ 。
(2)②、③、④三种元素的第一电离能由大到小的顺序为_________ (用元素符号表示)。
(3)⑧号元素在元素周期表中的位置是_______________ ,其原子核外未成对电子数为_______________ ,⑩号原子处于基态时核外电子排布式为___________ ,已知元素⑩和⑦的电负性分别为1.9和2.5,则⑩与⑦形成的化合物属于__________ (填“离子”或“共价”)化合物。
(4)③号元素原子与①号元素原子形成的原子个数比为 的分子X在①与④形成的化合物Y中的溶解度很大,其主要原因是
的分子X在①与④形成的化合物Y中的溶解度很大,其主要原因是____________ 。
(5)④号和⑦号元素组成的原子个数比为3:1的-2价阴离子的空间构型、中心原子的杂化类型分别是:____________ ,____________ 。

(1)上述元素中属于d区的有:
(2)②、③、④三种元素的第一电离能由大到小的顺序为
(3)⑧号元素在元素周期表中的位置是
(4)③号元素原子与①号元素原子形成的原子个数比为
 的分子X在①与④形成的化合物Y中的溶解度很大,其主要原因是
的分子X在①与④形成的化合物Y中的溶解度很大,其主要原因是(5)④号和⑦号元素组成的原子个数比为3:1的-2价阴离子的空间构型、中心原子的杂化类型分别是:
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】研究发现,铝元素能损害人的脑细胞。适当地补充碘元素可预防甲状腺肿大,但摄入过多也会导致甲状腺肿大,因此补充人体所需的元素时也要适可而止。试回答下列问题:
(1)Fe也是人体需要补充的元素之一,试写出Fe2+的核外电子排布式:__ 。
(2)与Al同一周期的Na、Mg元素也是人体所需元素,Na、Mg、Al基态原子第一电离能的大小关系是__ 。
(3)氯化铝的熔点是194℃,氧化铝的熔点是2054℃,但是工业上不能用电解熔融氯化铝的方法获取铝单质,这是因为__ 。
(4)F与I是同一主族的元素,BeF2与H2O都是由三个原子构成的共价化合物分子,二者分子中的中心原子Be和O的杂化方式分别为__ 、__ ,BeF2分子的立体构型是___ ,H2O分子的立体构型是__ 。
(5)I2晶体的晶胞结构如图所示,该晶胞中含有__ 个I2分子,设该晶胞的晶胞参数为acm,则I2的密度是__ g·cm-3。

(1)Fe也是人体需要补充的元素之一,试写出Fe2+的核外电子排布式:
(2)与Al同一周期的Na、Mg元素也是人体所需元素,Na、Mg、Al基态原子第一电离能的大小关系是
(3)氯化铝的熔点是194℃,氧化铝的熔点是2054℃,但是工业上不能用电解熔融氯化铝的方法获取铝单质,这是因为
(4)F与I是同一主族的元素,BeF2与H2O都是由三个原子构成的共价化合物分子,二者分子中的中心原子Be和O的杂化方式分别为
(5)I2晶体的晶胞结构如图所示,该晶胞中含有

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】铁被誉为“第一金属”,铁及其化合物在生活中有广泛应用。回答下列问题:
(1)基态Fe3+的电子排布式为___ 。
(2)实验室用KSCN溶液、苯酚(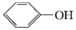 )检验Fe3+。N、O、S的第一电离能由大到小的顺序为
)检验Fe3+。N、O、S的第一电离能由大到小的顺序为__ (用元素符号表示),苯酚中碳原子的杂化轨道类型为__ 。
(3)FeCl3的熔点为306℃,沸点为315℃,FeCl3的晶体类型是__ 。FeSO4常作补铁剂,SO 的立体构型是
的立体构型是__ 。
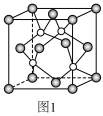
(4)氮化铁晶体的晶体结构示意图如图1所示。该晶体中铁、氮的微粒个数之比为__ 。
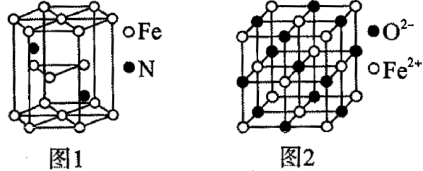
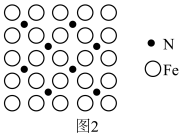
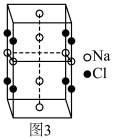
(5)氧化亚铁晶体的晶胞如图2所示。已知:氧化亚铁晶体的密度为ρg·cm-3,NA代表阿伏加德罗常数的值。在该晶胞中,与Fe2+紧邻且等距离的Fe2+数目为__ ;Fe2+与O2-的最短间距为__ pm。
(1)基态Fe3+的电子排布式为
(2)实验室用KSCN溶液、苯酚(
 )检验Fe3+。N、O、S的第一电离能由大到小的顺序为
)检验Fe3+。N、O、S的第一电离能由大到小的顺序为(3)FeCl3的熔点为306℃,沸点为315℃,FeCl3的晶体类型是
 的立体构型是
的立体构型是(4)氮化铁晶体的晶体结构示意图如图1所示。该晶体中铁、氮的微粒个数之比为

(5)氧化亚铁晶体的晶胞如图2所示。已知:氧化亚铁晶体的密度为ρg·cm-3,NA代表阿伏加德罗常数的值。在该晶胞中,与Fe2+紧邻且等距离的Fe2+数目为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】元素X位于第四周期,其基态原子的内层轨道全部排满电子,且最外层电子数为1。在气体分析中,常用XCl的盐酸溶液吸收并定量测定CO的含量,原理为:2XCl+2CO+ 2H2O==X2Cl2·2CO·2H2O
(1)X原子基态核外电子排布式为_________ ;
(2)C、H、O三种元素的电负性由大到小的顺序为________ ;
(3)H2O中氧原子的轨道杂化类型为__________ ;
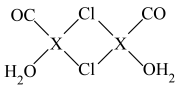
(4)X2Cl2·2CO·2H2O是一种配合物,结构如图所示,每个X原子能与其他原子形成3个配位键,在图中用“→"标出相应的配位键__ 。CO与N2分子的结构相似,则1molX2Cl2·2CO·2H2O含有δ键的数目为__ 。
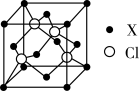
(5)化合物XCl晶体的晶胞如图所示,距离每个X离子最近的Cl的个数为________ 。
(1)X原子基态核外电子排布式为
(2)C、H、O三种元素的电负性由大到小的顺序为
(3)H2O中氧原子的轨道杂化类型为
(4)X2Cl2·2CO·2H2O是一种配合物,结构如图所示,每个X原子能与其他原子形成3个配位键,在图中用“→"标出相应的配位键

(5)化合物XCl晶体的晶胞如图所示,距离每个X离子最近的Cl的个数为

您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】四种常见元素的性质或结构信息如表所示,请问答下列问题。
(1)R的基态原子价层电子排布式为_______ ,这四种元素的电负性由大到小的顺序为_______ (写元素符号)。
(2)A、B、D均可形成多种氢化物,其中分子构型为三角锥的氢化物分子式为_______ ,分子构型为正四面体的氢化物分子式为_______ ,中心原子存在 、
、 两种杂化类型的物质的结构式为
两种杂化类型的物质的结构式为_______ 。与A的常见单质互为等电子体的上述元素的氧化物分子式为_______ 。
| 元素 | A | B | R | D |
| 相关信息 | 基态原子核外电子占据3个能级且最高能级上有3个电子 | B的单质是最常见半导体材料 | 位于第四周期ⅠB族 | 是非金属元素,其形成的某种单质是电的良导体,有的分子形状似足球 |
(2)A、B、D均可形成多种氢化物,其中分子构型为三角锥的氢化物分子式为
 、
、 两种杂化类型的物质的结构式为
两种杂化类型的物质的结构式为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐3】硬铝(主要成分为Al、Cu、Mg、M、Si)主要用于生产各种构件和铆钉,在造船和建筑等行业也有广泛的应用。回答下列问题。
(1)处于基态的Al原子和Mg原子,下列参数中Al原子较大的是______ (填标号)。
A.未成对电子数 B.第一电离能 C.原子半径
(2)硅元素很难形成含多重键的化合物,最近我国科学家在合成的二硅炔镁盐中探测到有“Si=Si”键的存在。硅元素难以形成“Si=Si”键的原因是______ 。
(3)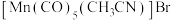 是一种重要的配合物,
是一种重要的配合物,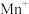 的配位数为
的配位数为______ , 提供孤电子对的原子为
提供孤电子对的原子为______ ,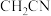 分子中碳原子的杂化类型为
分子中碳原子的杂化类型为______ , 中三种元素的电负性由大到小的顺序为
中三种元素的电负性由大到小的顺序为______ 。
(4)氧化镁晶胞属于立方形晶胞,其晶胞参数为anm。晶胞中每个 周围紧邻且距离相等的
周围紧邻且距离相等的 共有
共有______ 个,其最近距离为______ nm。设阿伏加德罗常数的值为 ,则氧化镁晶体的密度为
,则氧化镁晶体的密度为______  (列出计算表达式)。
(列出计算表达式)。

(1)处于基态的Al原子和Mg原子,下列参数中Al原子较大的是
A.未成对电子数 B.第一电离能 C.原子半径
(2)硅元素很难形成含多重键的化合物,最近我国科学家在合成的二硅炔镁盐中探测到有“Si=Si”键的存在。硅元素难以形成“Si=Si”键的原因是
(3)
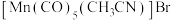 是一种重要的配合物,
是一种重要的配合物,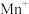 的配位数为
的配位数为 提供孤电子对的原子为
提供孤电子对的原子为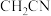 分子中碳原子的杂化类型为
分子中碳原子的杂化类型为 中三种元素的电负性由大到小的顺序为
中三种元素的电负性由大到小的顺序为(4)氧化镁晶胞属于立方形晶胞,其晶胞参数为anm。晶胞中每个
 周围紧邻且距离相等的
周围紧邻且距离相等的 共有
共有 ,则氧化镁晶体的密度为
,则氧化镁晶体的密度为 (列出计算表达式)。
(列出计算表达式)。
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐1】BaTiO3和MgTiO3都是重要的介电材料,BaTiO3可利用熔融态的反应:TiO2+BaCO3=BaTiO3+CO2↑制备。试回答下列问题:
(1)基态Ti原子中有___________ 个未成对电子,若其价层的某一个电子受激发后得到激发态的Ti原子,该激发态的Ti原子中最多有 ___________ 个未成对电子。
(2)制备BaTiO3的反应的各物质中,电负性最小的元素是___________ (填元素符号)。
(3)BaCO3中阴离子的中心原子的价层电子对数为___________ ,写出一个与该阴离子互为等电子体的分子的化学式___________ 。
(4)TiO2的熔沸点远高于CO2的原因是___________ ,MgTiO3的熔点高于BaTiO3的原因是___________ 。
(5)在BaTiO3的立方晶胞结构中,Ba2+位于晶胞顶点位置,则Ti4+最可能位于___________ ,O2-最可能位于___________ 。将晶胞中部分Ba2+替换为Mg2+或Ca2+可改良材料性能,设晶胞中分别有x、y个Ba2+被替换为Mg2+、Ca2+,则改良后的晶胞化学式为___________ 。
(1)基态Ti原子中有
(2)制备BaTiO3的反应的各物质中,电负性最小的元素是
(3)BaCO3中阴离子的中心原子的价层电子对数为
(4)TiO2的熔沸点远高于CO2的原因是
(5)在BaTiO3的立方晶胞结构中,Ba2+位于晶胞顶点位置,则Ti4+最可能位于
您最近一年使用:0次
【推荐2】教材插图具有简洁而又内涵丰富的特点。请回答以下问题:
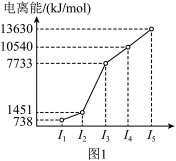
(1)第三周期的某主族元素,其第一至第五电离能数据如图1所示,则该元素对应的原子有____ 种不同运动状态的电子。
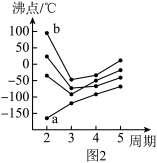
(2)图2中,每条折线表示周期表ⅣA~ⅦA中的某一族元素氢化物的沸点变化。每个小黑点代表一种氢化物,其中a点代表的是____ (填化学式),图中b的沸点大于a,原因是____ 。
(3)CO2在高温高压下所形成的晶体其晶胞如图3所示。则该晶体的类型属于_____ 晶体。

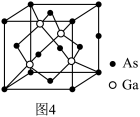
(4)GaAs晶体结构如图4所示,晶体中每个Ga原子与____ 个As原子相连,与同一个Ga原子相连的As原子构成的空间构型为____ 。
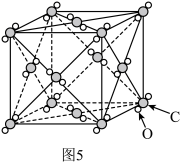
(5)干冰是分子晶体,晶体结构如图5所示,一个干冰晶胞中有____ 个CO2分子。
(1)第三周期的某主族元素,其第一至第五电离能数据如图1所示,则该元素对应的原子有

(2)图2中,每条折线表示周期表ⅣA~ⅦA中的某一族元素氢化物的沸点变化。每个小黑点代表一种氢化物,其中a点代表的是

(3)CO2在高温高压下所形成的晶体其晶胞如图3所示。则该晶体的类型属于

(4)GaAs晶体结构如图4所示,晶体中每个Ga原子与

(5)干冰是分子晶体,晶体结构如图5所示,一个干冰晶胞中有

您最近一年使用:0次
【推荐3】VA族元素及其化合物在生产、生活中用途广泛。
(1)①P、S、 电负性由大到小的顺序是
电负性由大到小的顺序是_______ 。
② 俗称雄黄,其中基态
俗称雄黄,其中基态 原子的核外电子排布式为
原子的核外电子排布式为
_______ ,有_______ 个未成对电子。
③ 常用于制造火柴,P和S的第一电离能较大的是
常用于制造火柴,P和S的第一电离能较大的是_______ 。
(2)白磷在氯气中燃烧可以得到 和
和 ,其中气态
,其中气态 分子的立体构型为
分子的立体构型为_______ 。
(3) 、
、 、
、 中沸点最高的是
中沸点最高的是_______ ,其主要原因是_______ 。
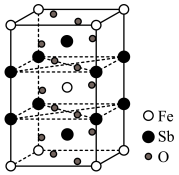
(4)锑酸亚铁晶胞如图所示,则:锑酸亚铁的化学式为_______ 。
(1)①P、S、
 电负性由大到小的顺序是
电负性由大到小的顺序是②
 俗称雄黄,其中基态
俗称雄黄,其中基态 原子的核外电子排布式为
原子的核外电子排布式为
③
 常用于制造火柴,P和S的第一电离能较大的是
常用于制造火柴,P和S的第一电离能较大的是(2)白磷在氯气中燃烧可以得到
 和
和 ,其中气态
,其中气态 分子的立体构型为
分子的立体构型为(3)
 、
、 、
、 中沸点最高的是
中沸点最高的是(4)锑酸亚铁晶胞如图所示,则:锑酸亚铁的化学式为

您最近一年使用:0次



