A、B、C、D、E均为短周期元素,非金属元素A的最外层电子数与其周期数相等,B的成对电子与未成对电子所占据的原子轨道数相等。单质B在单质C中充分燃烧生成BC2。 D+与C2-具有相同的电子数。A在E中燃烧,产物溶于水会得到一种强酸。
(1)B在元素周期表中的位置是________ ,写出一种工业制备单质E的化学方程式:_____ 。
(2)B、C、D组成的一种盐中,B的质量分数为17. 91%,D的质量分数为34. 3 3%。该盐的化学式为________ ,其阴离子中B原子的杂化方式为__________ 。
(3)由这些元素组成的某些物质的组成和结构信息如下表:
a的电子式为_________ ;b的化学式为________ ;c的空间构型为___________ 。
(1)B在元素周期表中的位置是
(2)B、C、D组成的一种盐中,B的质量分数为17. 91%,D的质量分数为34. 3 3%。该盐的化学式为
(3)由这些元素组成的某些物质的组成和结构信息如下表:
| 物质 | 组成和结构 |
| a | A、D两元素组成的离子化合物 |
| b | 由C、D两元素组成的含有非极性键的离子化合物 |
| c | 化学组成为BCE2 |
更新时间:2017-08-16 19:23:08
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】下表列出了①~⑨九种元素在周期表中的位置:
请按要求回答下列问题。
(1)元素④的名称是______
(2)元素⑦的原子结构示意图是____________ 。
(3)按气态氢化物的稳定性由弱到强的顺序排列,⑥④⑦的氢化物稳定性:________ (写氢化物的化学式)。
(4)④的最简单氢化物比⑦的最简单氢化物沸点高,原因是_______________________ .
(5)元素⑤的单质在氧气中燃烧所得产物中化学键的类型为_____________________
(6)用电子式表示①与⑨反应得到的化合物的形成过程_______________ 。
(7)两种均由①④⑤⑦四种元素组成的化合物,在水溶液中发生反应的离子反应方程式为________
(8)第三周期元素Na Mg Al S Cl 的简单离子半径由大到小的顺序是______ (用离子符号表示)
(9)已知1g①的单质燃烧生成液态产物时放出142.9kJ的热量,写出表示该单质燃烧热的热化学方程式:____________
| ⅠA | 0 | |||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | ② | ③ | ④ | ⑧ | ||||
| 3 | ⑤ | ⑥ | ⑦ | ⑨ |
请按要求回答下列问题。
(1)元素④的名称是
(2)元素⑦的原子结构示意图是
(3)按气态氢化物的稳定性由弱到强的顺序排列,⑥④⑦的氢化物稳定性:
(4)④的最简单氢化物比⑦的最简单氢化物沸点高,原因是
(5)元素⑤的单质在氧气中燃烧所得产物中化学键的类型为
(6)用电子式表示①与⑨反应得到的化合物的形成过程
(7)两种均由①④⑤⑦四种元素组成的化合物,在水溶液中发生反应的离子反应方程式为
(8)第三周期元素Na Mg Al S Cl 的简单离子半径由大到小的顺序是
(9)已知1g①的单质燃烧生成液态产物时放出142.9kJ的热量,写出表示该单质燃烧热的热化学方程式:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】(1)A、B、C、D、E均是短周期元素,其原子序数依次增大,A和B同周期,A原子最外层电子数是内层电子数的二倍,B元素族序数是周期数的三倍,B的阴离子与C的阳离子电子层结构相同,C的单质与B的单质在不同条件下反应,可生成C2B或C2B2,D单质是一种淡黄色固体。请回答:
①C2B2的电子式是___________ ,D、E可形成化合物DE2中,存在下列哪些静电作用力______ 。
a.极性键 b.非极性键 c.范德华力 d.氢键 e.离子键
②B、C、E的离子半径由大到小的顺序为_______________ (用化学式回答),举一个事实证明E和D非金属性的强弱___________________ (用离子反应方程式表示)。
(2)氨和二氧化碳反应可生成尿素CO(NH2)2。尿素在一定条件下会失去氨而缩合,如两分子尿素失去一分子氨形成二聚物:
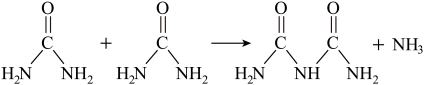
当尿素三聚时,得到两种产物,其中一种为环状结构,请画出其结构式___________ 。
(3)已知某元素的原子序数是33,试推测该元素:
①原子的原子结构示意图______________ 。
②在元素周期表中的位置______________ 。
①C2B2的电子式是
a.极性键 b.非极性键 c.范德华力 d.氢键 e.离子键
②B、C、E的离子半径由大到小的顺序为
(2)氨和二氧化碳反应可生成尿素CO(NH2)2。尿素在一定条件下会失去氨而缩合,如两分子尿素失去一分子氨形成二聚物:

当尿素三聚时,得到两种产物,其中一种为环状结构,请画出其结构式
(3)已知某元素的原子序数是33,试推测该元素:
①原子的原子结构示意图
②在元素周期表中的位置
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】已知X、Y、Z、M、G、Q是六种短周期主族元素,分别在三个周期且原子序数依次增大。X、Z、Q的单质在常温下呈气态;Y的原子最外层电子数是其电子层数的2倍;X与M同主族;Z、G分别是地壳中含量最高的非金属元素和金属元素。
请回答下列问题:
(1)Z在元素周期表中的位置为
(2)Z和Q的最低价氢化物沸点更高的是(写化学式)
(3)上述元素的最高价氧化物对应的水化物酸性最强的是(写化学式)
(4)M2Z2的电子式为
(5)常温下,能与G的单质发生反应的是(填字母序号)
A.CuSO4溶液 B.浓硫酸 C.NaOH溶液 D.Na2CO3固体
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】A、B、C、D、E、F六种元素,它们的核电荷数均小于18,且原子序数逐渐增大。已知:A、C、F三种原子的最外层共有11个电子,且这三种元素的最高价氧化物的水化物之间两两皆能反应,均生成盐和水。D元素原子的最外层电子数比次外层电子数少4个,E元素原子的次外层电子数比最外层电子数多3个。请回答下列问题:
(1)写出D的名称___________ ,E的最高价氧化物的水化物的分子式___________ 。
(2)画出B元素的原子结构示意图___________ 。
(3)若构成F元素的一种核素的中子数为18,写出该核素的表示符号___________ 。
(4)A与C、C与F元素最高价氧化物的水化物反应的离子方程式依次为:___________ 、___________ 。
(1)写出D的名称
(2)画出B元素的原子结构示意图
(3)若构成F元素的一种核素的中子数为18,写出该核素的表示符号
(4)A与C、C与F元素最高价氧化物的水化物反应的离子方程式依次为:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】A、B、C、D、E为短周期主族元素,且原子序数依次增大,质子数之和为39,B、C同周期,A、D同主族,A为短周期原子半径最小的元素,C原子最外层电子数为次外层的3倍,A、C常温下能形成两种液态化合物A2C和A2C2,E元素的周期数与主族序数相等。请用化学用语回答下列问题:
(1)C元素在周期表中的位置为________ ;由 A、C、D 三种元素组成的化合物中含有的化学键为___________ 。
(2)写出A2C的电子式_____ ,A2C2的结构式________ 。
(3)废印刷电路板上含有铜,以往的回收方法是将其灼烧使铜转化为氧化铜,再用硫酸溶解。现改用A2C2和稀硫酸浸泡废印刷电路板既达到上述目的,又保护了环境,试写出反应的离子方程式:_____________ 。
(4)元素D的单质在一定条件下,能与A 单质化合生成一种化合物DA,其电子式为________ ,DA能与水反应放出氢气,若将 0.1 molDA和 0.1 mol E 单质混合加入足量的水,充分反应后生成的气体在标准状况下的体积是______ L。
(1)C元素在周期表中的位置为
(2)写出A2C的电子式
(3)废印刷电路板上含有铜,以往的回收方法是将其灼烧使铜转化为氧化铜,再用硫酸溶解。现改用A2C2和稀硫酸浸泡废印刷电路板既达到上述目的,又保护了环境,试写出反应的离子方程式:
(4)元素D的单质在一定条件下,能与A 单质化合生成一种化合物DA,其电子式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】A、B、C、D四种元素,原子序数依次增大,A原子的最外层上有4个电子;B的阴离子和C的阳离子具有相同的电子层结构,两元素的单质反应,生成一种淡黄色的固体E,D的L层电子数等于K、M两个电子层上的电子数之和。
完成下列填空:
(1)C离子的结构示意图为___ ,D在周期表中位置是___ 。
(2)写出E的电子式:__ 。
(3)A、D两元素形成的化合物属___ (填“离子”或“共价”)化合物,1mol该化合物含___ mole-。
(4)写出D的最高价氧化物的水化物和A单质反应的化学方程式:___ 。
(5)元素硒(Se)被誉为“生命的奇效元素”,与D元素同主族,则下列关于硒的叙述错误的是___ (填序号)。
a.Se元素的最高化合价为+6
b.硒的最高价氧化物对应水化物的化学式H2SeO3
c.硒的非金属性比氧元素弱
d.气态氢化物的热稳定性:H2Se>H2D
完成下列填空:
(1)C离子的结构示意图为
(2)写出E的电子式:
(3)A、D两元素形成的化合物属
(4)写出D的最高价氧化物的水化物和A单质反应的化学方程式:
(5)元素硒(Se)被誉为“生命的奇效元素”,与D元素同主族,则下列关于硒的叙述错误的是
a.Se元素的最高化合价为+6
b.硒的最高价氧化物对应水化物的化学式H2SeO3
c.硒的非金属性比氧元素弱
d.气态氢化物的热稳定性:H2Se>H2D
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐1】钇钡铜氧(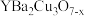 )是一种高温超导材料(其中Y显+3价,Cu显+2、+3价)。回答下列问题:
)是一种高温超导材料(其中Y显+3价,Cu显+2、+3价)。回答下列问题:
(1)钇(Y)是一种重要的稀土金属,与Sc(钪)同族相邻。则钇原子核外有_______ 个价电子,钇位于元素周期表的_______ 区。
(2)在 中,
中, 的空间构型为
的空间构型为_______ ,C原子的杂化形式为_______ ; 、
、 受热分解分别生成BaO、CaO,BaO、CaO熔点较高的是
受热分解分别生成BaO、CaO,BaO、CaO熔点较高的是_______ (填化学式)。
(3)基态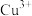 的核外电子排布式为
的核外电子排布式为_______ 。
(4)若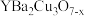 (0≤x≤0.5)材料在T℃下有超导性,当x=0.2时,
(0≤x≤0.5)材料在T℃下有超导性,当x=0.2时,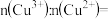
_______ 。
(5)铜有CuO和 两种氧化物,后者比前者的热稳定性强,原因是
两种氧化物,后者比前者的热稳定性强,原因是_______ 。
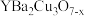 )是一种高温超导材料(其中Y显+3价,Cu显+2、+3价)。回答下列问题:
)是一种高温超导材料(其中Y显+3价,Cu显+2、+3价)。回答下列问题:(1)钇(Y)是一种重要的稀土金属,与Sc(钪)同族相邻。则钇原子核外有
(2)在
 中,
中, 的空间构型为
的空间构型为 、
、 受热分解分别生成BaO、CaO,BaO、CaO熔点较高的是
受热分解分别生成BaO、CaO,BaO、CaO熔点较高的是(3)基态
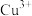 的核外电子排布式为
的核外电子排布式为(4)若
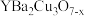 (0≤x≤0.5)材料在T℃下有超导性,当x=0.2时,
(0≤x≤0.5)材料在T℃下有超导性,当x=0.2时,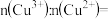
(5)铜有CuO和
 两种氧化物,后者比前者的热稳定性强,原因是
两种氧化物,后者比前者的热稳定性强,原因是
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】将过量的氨水加到硫酸铜溶液中,溶液最终变成深蓝色,继续加入乙醇,析出深蓝色的晶体[Cu(NH3)4]SO4·H2O。
(1)Cu2+价电子排布式为___________ ;[Cu(NH3)4]SO4·H2O中,1mol[Cu(NH3)4]2+含有σ键的数目为___________ 。
(2)SO42-中S原子轨道杂化类型为___________ ,H3O+几何构型为___________ 。
(3)NH3极易溶于H2O中,可能的原因为___________ 。
(4)N、O、S第一电离能由大到小的顺序为___________ 。
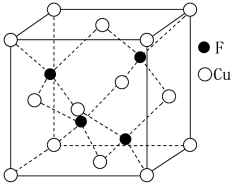
(5)Cu与F形成的化合物的晶胞结构如图所示,若晶体密度为ag·cm-3,则Cu与F最近距离为___________ pm(用NA表示阿伏伽德罗常数的值,列出计算表达式,不用化简)。
(1)Cu2+价电子排布式为
(2)SO42-中S原子轨道杂化类型为
(3)NH3极易溶于H2O中,可能的原因为
(4)N、O、S第一电离能由大到小的顺序为

(5)Cu与F形成的化合物的晶胞结构如图所示,若晶体密度为ag·cm-3,则Cu与F最近距离为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】我国科学家研发的全球首套“液态阳光”项目使双碳目标更近一步。该项目通过太阳能发电电解水制氢,再将 加氢合成
加氢合成 。
。
(1)太阳能电池板的主要材料为单晶硅。
①单晶硅属于_______ 晶体。
②单晶硅的熔点低于金刚石的,原因是_______ 。
(2)在催化剂作用下, 与
与 反应得到
反应得到 。
。
① 分子的空间结构为
分子的空间结构为_______ 。
② 和
和 分子中
分子中 键数目之比为
键数目之比为_______ 。
③ 比
比 在水中的溶解度大,这是因为
在水中的溶解度大,这是因为_______ 。
(3) 催化剂可实现
催化剂可实现 高选择性加氢合成
高选择性加氢合成 ,其晶胞结构如图所示。
,其晶胞结构如图所示。_______ (填“ ”或“
”或“ ”),理由是
”),理由是_______ 。
② 晶胞的棱长分别为
晶胞的棱长分别为 、
、 、
、 ,其晶体密度为
,其晶体密度为_______  (列算式)。已知:
(列算式)。已知: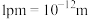 ,
, 为阿伏加德罗常数的值
为阿伏加德罗常数的值
 加氢合成
加氢合成 。
。(1)太阳能电池板的主要材料为单晶硅。
①单晶硅属于
②单晶硅的熔点低于金刚石的,原因是
(2)在催化剂作用下,
 与
与 反应得到
反应得到 。
。①
 分子的空间结构为
分子的空间结构为②
 和
和 分子中
分子中 键数目之比为
键数目之比为③
 比
比 在水中的溶解度大,这是因为
在水中的溶解度大,这是因为(3)
 催化剂可实现
催化剂可实现 高选择性加氢合成
高选择性加氢合成 ,其晶胞结构如图所示。
,其晶胞结构如图所示。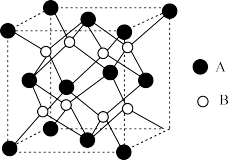
 ”或“
”或“ ”),理由是
”),理由是②
 晶胞的棱长分别为
晶胞的棱长分别为 、
、 、
、 ,其晶体密度为
,其晶体密度为 (列算式)。已知:
(列算式)。已知: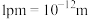 ,
, 为阿伏加德罗常数的值
为阿伏加德罗常数的值
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐1】卤素(F、Cl、Bi、I )可形成许多结构和性质特殊的化合物。回答下列问题。
(1)F 原子的核外电子有___________ 种空间运动状态,F 的第一电离能___________ 、填“<”或“>”)Ne 的第一电离能。
(2)− 40℃时 ,F2与冰反应生成 HOF和 HF 。常温常压下,HOF 为无色气体,固态 HOF 的晶体类型为___________ ,HOF水解的产物为___________ (填化学式)。
(3)Cl2O 的中心原子为O,O原子的轨道杂化方式为___________ ;ClO2的中心原子为 Cl,其分子 空间构型与Cl2O 相同,但ClO2中存在大π键( ),则ClO2中 O−C1−O 键角
),则ClO2中 O−C1−O 键角______ (填 “>”“<”或“=”)Cl2O中 Cl−O−Cl键角。
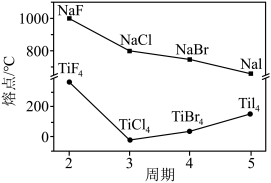
(4)卤化钠(NaX) 和四卤化钛(TiX4)的熔点如图所示,TiX4的熔点呈如图变化趋势的原因为_______ 。________ ,若阿伏加德罗常数的值为NA, 则化合物X 的密度为___________ g/cm³(用含NA、a、c的代数式表示)。
(1)F 原子的核外电子有
(2)− 40℃时 ,F2与冰反应生成 HOF和 HF 。常温常压下,HOF 为无色气体,固态 HOF 的晶体类型为
(3)Cl2O 的中心原子为O,O原子的轨道杂化方式为
 ),则ClO2中 O−C1−O 键角
),则ClO2中 O−C1−O 键角(4)卤化钠(NaX) 和四卤化钛(TiX4)的熔点如图所示,TiX4的熔点呈如图变化趋势的原因为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】有A、B、C、D四种元素,其中A元素和B元素的原子都有1个未成对电子,A+比B-少一个电子层,B原子得一个电子后3p轨道全满;C原子的p轨道中有3个未成对电子,其气态氢化物在水中的溶解度是同族元素所形成的氢化物中最大的;D的最高化合价和最低化合价的代数和为4,其最高价氧化物中含D的质量分数为40%,且其核内质子数等于中子数。R是由A、D两元素形成的离子化合物,其中A与D离子数之比为2∶1。请回答下列问题:
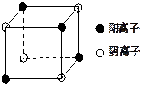
⑴A单质、B单质、化合物R的熔点大小顺序为下列的________________ (填序号):
①A单质>B单质>R; ②R>A单质>B单质;
③B单质>R >A单质; ④A单质>R>B单质。
⑵在CB3分子中C元素原子的原子轨道发生的是________ 杂化,其固体的晶体类型为______________ ;
⑶写出D原子的核外价电子排布式___________ ,C的氢化物比D的氢化物在水中溶解度大得多的可能原因_________________________________________________ ;
⑷右图是D和Fe形成的晶体FeD2最小单元“晶胞”,FeD2晶体
中阴、阳离子数之比为_____________ ,FeD2物质中具有的化
学键类型为________________ 。
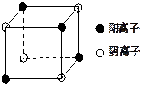
⑴A单质、B单质、化合物R的熔点大小顺序为下列的
①A单质>B单质>R; ②R>A单质>B单质;
③B单质>R >A单质; ④A单质>R>B单质。
⑵在CB3分子中C元素原子的原子轨道发生的是
⑶写出D原子的核外价电子排布式
⑷右图是D和Fe形成的晶体FeD2最小单元“晶胞”,FeD2晶体
中阴、阳离子数之比为
学键类型为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】卤素及其化合物在生产生活中应用广泛。请回答:
(1)基态 原子的价层电子轨道表示式为
原子的价层电子轨道表示式为_______ 。
(2)卤族元素可与其他元素形成多种化合物。
①下列说法不正确的是_______ 。
A.能量最低的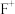 的
的 轨道有一个成单电子
轨道有一个成单电子
B.得到一个电子释放的能量,
C.化学键的极性: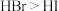
D. 分子的空间构型:直线形
分子的空间构型:直线形
② 中
中 原子的杂化方式是
原子的杂化方式是_______ ,预测该分子可与 、
、 中的
中的_______ 发生化学反应,预测依据是_______ 。
③ 分子之间形成的氢键强于
分子之间形成的氢键强于 分子之间形成的氢键,但在压力相同时
分子之间形成的氢键,但在压力相同时 的沸点仍高于
的沸点仍高于 ,解释原因:
,解释原因:_______ 。
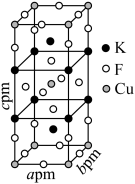
(3)金属元素M与F形成的氟化物晶胞结构如图。已知该物质中M的配位数为8,则氟化物的化学式是_______ ,F的配位数为_______ 。

(1)基态
 原子的价层电子轨道表示式为
原子的价层电子轨道表示式为(2)卤族元素可与其他元素形成多种化合物。
①下列说法不正确的是
A.能量最低的
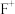 的
的 轨道有一个成单电子
轨道有一个成单电子B.得到一个电子释放的能量,

C.化学键的极性:
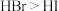
D.
 分子的空间构型:直线形
分子的空间构型:直线形②
 中
中 原子的杂化方式是
原子的杂化方式是 、
、 中的
中的③
 分子之间形成的氢键强于
分子之间形成的氢键强于 分子之间形成的氢键,但在压力相同时
分子之间形成的氢键,但在压力相同时 的沸点仍高于
的沸点仍高于 ,解释原因:
,解释原因:(3)金属元素M与F形成的氟化物晶胞结构如图。已知该物质中M的配位数为8,则氟化物的化学式是

您最近一年使用:0次



