是环境友好材料,能光催化降解有机物。回答下列问题:
是环境友好材料,能光催化降解有机物。回答下列问题:(1)基态Ti原子核外电子占据的最高能级符号为
(2)二氧化钛与
 (光气)、
(光气)、 (二氯亚砜)等氯化试剂反应可用于制取四氯化钛。
(二氯亚砜)等氯化试剂反应可用于制取四氯化钛。①
 (光气)的立体构型为
(光气)的立体构型为 中
中 键和
键和 键的数目比为
键的数目比为②
 (二氯亚砜)是
(二氯亚砜)是(3)香豆素(
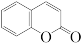 )是一种天然香料,能被
)是一种天然香料,能被 光降解。
光降解。①分子中C原子的杂化类型是
②已知单双键交替的共轭结构可以形成大π键,大π键可用符号
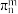 表示,其中n代表参与形成大π键的原子数,m代表参与形成大π键的电子数(如苯分子中的大π键可表示为
表示,其中n代表参与形成大π键的原子数,m代表参与形成大π键的电子数(如苯分子中的大π键可表示为 ),则香豆素中的大π键应表示为
),则香豆素中的大π键应表示为相似题推荐
| 元素 | A | B | C | D |
| 性质 结构 信息 | A的气态氢化物能使湿润的红色石蕊试纸变蓝色,且能与A最高价氧化物对应的水化物发生化合反应 | 原子的M层有1对成对的p电子 | 原子核外有5种能量不同的电子,最外层电子数为7 | 有两种常见氧化物,其中有一种是冶金工业常用的还原剂 |
(2)上述某种元素形成的最简单气态氢化物为非极性分子,该分子的电子式为
(3)D与同主族相邻元素的最高价氧化物的熔点比较:
(4)B和C两元素非金属性较强的是
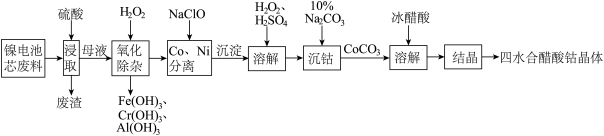
(1)Co元素位于元素周期表的
 的价电子排布式
的价电子排布式(2)下列说法正确的是
| A.浸取时硫酸的浓度越大越好 |
| B.过氧化氢在氧化除杂和溶解中的作用是不同的 |
| C.结晶时可采用蒸发结晶 |
D.沉钴时可用 代替 代替 |
 转化为
转化为 而
而 不发生变化,从而实现钴镍分离,写出该过程中发生反应的离子方程式
不发生变化,从而实现钴镍分离,写出该过程中发生反应的离子方程式(4)可用CO气体与碱性醋酸钴溶液在一定条件下反应,制备催化剂四羰基钴钠
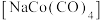 ,一定条件反应原理
,一定条件反应原理 。在不同条件下制备四羰基钴钠,然后探究其催化环氧乙烷(EQ)羰基化合成MHP的性能,结果如图所示。
。在不同条件下制备四羰基钴钠,然后探究其催化环氧乙烷(EQ)羰基化合成MHP的性能,结果如图所示。
①根据合成四羰基钴钠的反应原理,分析温度(低于100℃),压强对该反应的反应速率及醋酸钴转化率的影响
②由图可知,四羰基钴钠催化环氧乙烷(EQ)羰基化合成MHP时,当温度高于90℃时,MHP的收率迅速降低的主要原因可能为
【推荐3】钛酸锌锂(Li2ZnTi3O8)是锂离子电池电极材料的一种,具有循环性能良好、安全性能优异、结构性能稳定的优点,可以通过TiO2、Li2CO3、(CH3COO)2Zn·2H2O等原料,采用高温固相法合成。回答下列问题:
(1)基态Ti原子的价电子排布式为
(2)CH3COO−中含有的σ键和π键的个数比为 的等电子体
的等电子体
(3)Ti与Zn原子都采用六方最密堆积形成金属晶体,两者半径大小相近:Ti(144.8pm)、Zn(133.3pm),但金属Ti的熔点(1660℃)比Zn(419.53℃)高得多,原因是
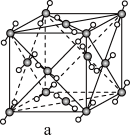
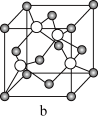
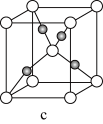
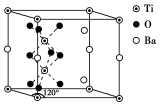
(4)某六方晶系的一种钛钡矿石的晶胞如图所示,距离晶胞内的钛原子最近的氧原子有
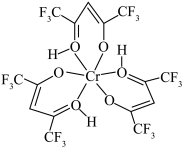
(2)Cr3+的未成对电子数有
(3)六氟代乙酰丙酮铬(Ⅲ)螯合物中含有的化学键有
a.极性共价键 b.非极性共价键 c.离子键
(4)六氟代乙酰丙酮(
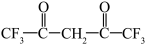 )中
)中 键有
键有(5)分子H2O、NH3、CH4中键角由大到小的顺序是
(1)在基态14C原子中,核外存在
(2)碳在形成化合物时,其键型以共价键为主,原因是
(3)CS2分子中,共价键的类型有
(4)碳有多种同素异形体,其中石墨烯与金刚石的晶体结构如图所示:

①在石墨烯晶体中,每个C原子连接
②在金刚石晶体中,C原子所连接的最小环也为六元环,每个C原子连接
(1)写出以下元素的名称: B
(2)用电子式表示C2D的形成过程:
(3)由B、C两元素所形成的原子个数比为1:1的化合物属于
(4)实验室常用A、B两元素所形成的原子个数为1:1的化合物来制备一种常见气体,写出实验室中用固体药品制备该气体的的化学方程式
(5)写出B的原子结构示意图
(6)写出均由A、B、C、D四种元素组成的两种物质之间发生反应的离子方程式
(7)由A、B两元素形成的单质在以铂作电极稀硫酸作电解液形成的燃料电池中,正极的电极方程式为
(1)K元素处于周期表的
(2)将TiO2与BaCO3加热熔融可制得BaTiO3,TiO2中Ti的离子结构示意图为
(3)含有多个配位原子的配体与同一中心离子(或原子)通过螯合配位成环而形成的配合物为螯合物。EDTA(
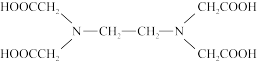 )与Ba2+形成的螯合物结构如图所示,该螯合物中采取sp3杂化的原子有
)与Ba2+形成的螯合物结构如图所示,该螯合物中采取sp3杂化的原子有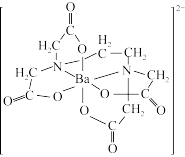
(4)KH2PO4的晶胞结构如图所示。
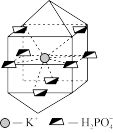
①KH2PO4中阴离子的配位数为
②若该晶胞的体积为V nm3,则该KH2PO4晶体的密度为
(1)Q+核外电子排布式为
(2)化合物X2W2中W的杂化方式为
 的立体构型是
的立体构型是(3)Y、R的最高价氧化物的沸点较高的是
(4)将Q单质的粉末加入到ZX3的浓溶液中,并通入W2,充分反应后溶液呈深蓝色,该反应的离子方程式为
 广泛应用于太阳能电池领域。以
广泛应用于太阳能电池领域。以 、NaOH和抗坏血酸为原料,可制备
、NaOH和抗坏血酸为原料,可制备 。
。(1)S、O两种元素可以形成多种阴离子,如
 、
、 等,这两种离子的空间结构分别为:
等,这两种离子的空间结构分别为:(2)
 可用于制备
可用于制备 晶体,实验如下:
晶体,实验如下:步骤1:向盛有硫酸铜水溶液的试管中边振荡边滴加氨水,观察到蓝色沉淀。
步骤2:继续滴加氨水至产生蓝色沉淀全部溶解,得到深蓝色的透明溶液。
步骤3:再向其中加入乙醇,析出深蓝色晶体。
①步骤1中生成的沉淀是
②
 中含有的
中含有的 键数为
键数为③步骤3中加入乙醇的作用是
(3)抗坏血酸的分子结构如图1所示,分子中碳原子的轨道杂化类型为
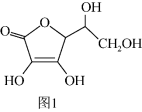
(4)一个
 晶胞(见图2)中,Cu原子的数目为
晶胞(见图2)中,Cu原子的数目为
(2)中国古代四大发明之一黑火药,它的爆炸反应为S+2KNO3+3C=A+N2↑+3CO2↑ (条件未标出,其中A的化学式未知)
①上述反应物中有三种元素处于同一周期,其第一电离能从大到小的顺序为
②A的晶体类型为
 的空间构型是
的空间构型是③KNO3、N2、S三种晶体的熔、沸点从高到低的顺序为
(3)NiAs的晶胞结构如图所示:
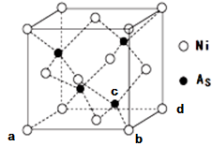
①镍离子的配位数为
②若a点的坐标为(0,0,0),b点的坐标为(1,0,0),d点的坐标为(1,1,0)则c点的坐标为
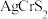 (
(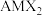 家族成员之一,A为一价金属,M为三价金属,X为氧族元素)在室温下具有超离子行为。回答下列问题
家族成员之一,A为一价金属,M为三价金属,X为氧族元素)在室温下具有超离子行为。回答下列问题(1)基态铬原子的价电子排布式为
(2)同周期元素Si、P、S的第一电离能由大到小的顺序为
(3)硫元素能形成多种微粒如
 、
、 、
、 、
、 、
、 等。
等。 的中心原子的杂化类型是
的中心原子的杂化类型是(4)
 中Cr元素化合价为+6价,常温下呈蓝色,则其结构式可能为
中Cr元素化合价为+6价,常温下呈蓝色,则其结构式可能为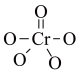 | 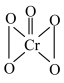 | 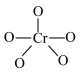 |
| A | B | C |

(6)已知晶体的密度为
 ,
, 为阿伏加德罗常数的值,则相邻
为阿伏加德罗常数的值,则相邻 与
与 之间的最短距离为=
之间的最短距离为=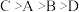 ;D和氢原子可形成4核10电子分子,该分子可使湿润的红色石器试纸变蓝:A、C同周期,B和C同主族;A与B可形成两种离子化合物
;D和氢原子可形成4核10电子分子,该分子可使湿润的红色石器试纸变蓝:A、C同周期,B和C同主族;A与B可形成两种离子化合物 、
、 ,氢原子与B可形成两种共价化合物
,氢原子与B可形成两种共价化合物 、
、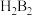 。试回答下列问题:
。试回答下列问题:(1)C元素的元素符号为
(2)写出D元素形成的
 分子的结构式
分子的结构式 键与
键与 键的数目比为
键的数目比为(3)B、D元素的第一电离能大小关系为:B
(4)
 对应的水化物的碱性比
对应的水化物的碱性比
 的电子式
的电子式(5)化合物
 、
、 它们结构与组成相似,热稳定性更强的是
它们结构与组成相似,热稳定性更强的是 的沸点比
的沸点比 高得多的原因是
高得多的原因是(6)下列选项能作为C元素和氧元素非金属性强弱比较的依据的是
a.C的氧化物对应的水化物的酸性弱于盐酸
b.C元素的电负性小于氯的电负性
c.化学反应:
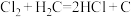
(7)B和C可以形成化合物
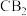 ,
,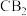 分子中空间结构为
分子中空间结构为(8)元素B和铜原子形成的化合物
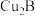 晶体结构可能是
晶体结构可能是