已知四种短周期元素的原子序数的大小顺序为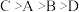 ;D和氢原子可形成4核10电子分子,该分子可使湿润的红色石器试纸变蓝:A、C同周期,B和C同主族;A与B可形成两种离子化合物
;D和氢原子可形成4核10电子分子,该分子可使湿润的红色石器试纸变蓝:A、C同周期,B和C同主族;A与B可形成两种离子化合物 、
、 ,氢原子与B可形成两种共价化合物
,氢原子与B可形成两种共价化合物 、
、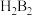 。试回答下列问题:
。试回答下列问题:
(1)C元素的元素符号为_____ ;写出A的电子排布式______ 。
(2)写出D元素形成的 分子的结构式
分子的结构式____ ,其中 键与
键与 键的数目比为
键的数目比为______ 。
(3)B、D元素的第一电离能大小关系为:B_______ D(填“<”或“>”)。
(4) 对应的水化物的碱性比
对应的水化物的碱性比
______ (填“强”或“弱”);写出 的电子式
的电子式________ 。
(5)化合物 、
、 它们结构与组成相似,热稳定性更强的是
它们结构与组成相似,热稳定性更强的是__________ (填化学式), 的沸点比
的沸点比 高得多的原因是
高得多的原因是_______________ 。
(6)下列选项能作为C元素和氧元素非金属性强弱比较的依据的是_________ 。
a.C的氧化物对应的水化物的酸性弱于盐酸
b.C元素的电负性小于氯的电负性
c.化学反应: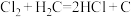
(7)B和C可以形成化合物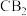 ,
,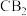 分子中空间结构为
分子中空间结构为___ (填“V型”成“直线型”)。中心原子C采用____ 杂化。
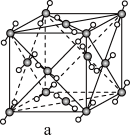
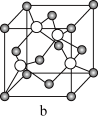
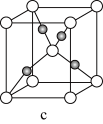
(8)元素B和铜原子形成的化合物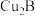 晶体结构可能是
晶体结构可能是______ (填字母)。
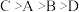 ;D和氢原子可形成4核10电子分子,该分子可使湿润的红色石器试纸变蓝:A、C同周期,B和C同主族;A与B可形成两种离子化合物
;D和氢原子可形成4核10电子分子,该分子可使湿润的红色石器试纸变蓝:A、C同周期,B和C同主族;A与B可形成两种离子化合物 、
、 ,氢原子与B可形成两种共价化合物
,氢原子与B可形成两种共价化合物 、
、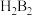 。试回答下列问题:
。试回答下列问题:(1)C元素的元素符号为
(2)写出D元素形成的
 分子的结构式
分子的结构式 键与
键与 键的数目比为
键的数目比为(3)B、D元素的第一电离能大小关系为:B
(4)
 对应的水化物的碱性比
对应的水化物的碱性比
 的电子式
的电子式(5)化合物
 、
、 它们结构与组成相似,热稳定性更强的是
它们结构与组成相似,热稳定性更强的是 的沸点比
的沸点比 高得多的原因是
高得多的原因是(6)下列选项能作为C元素和氧元素非金属性强弱比较的依据的是
a.C的氧化物对应的水化物的酸性弱于盐酸
b.C元素的电负性小于氯的电负性
c.化学反应:
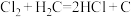
(7)B和C可以形成化合物
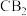 ,
,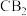 分子中空间结构为
分子中空间结构为(8)元素B和铜原子形成的化合物
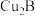 晶体结构可能是
晶体结构可能是


更新时间:2020-11-24 22:11:13
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
【推荐1】A、B、C、D、E为原子序数依次增大的短周期元素,已知A、B、E 三种原子最外层共有10个电子,且这3种元素的最高价氧化物的水化物两两皆能发生反应生成盐和水,C元素的最外层电子数比次外层电子数少4,D元素原子次外层电子数比最外层电子数多3。
(1)写出对应的元素符号:C________ ,D_______
(2)用电子式表示A与E两元素形成化合物的过程:___________________________ ;
(1)写出对应的元素符号:C
(2)用电子式表示A与E两元素形成化合物的过程:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】有A、B、C、D、E五种短周期元素,已知相邻的A、B、C、D四种元素原子核外共有56个电子,在周期表中的位置如图所示。E的单质可与酸反应,1molE单质与足量酸作用,在标准状况下能产生33.6LH2;E的阳离子与A的阴离子核外电子层结构完全相同,回答下列问题:
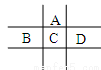
(1)五种元素的名称:A_______ ,B________ ,C________ ,D________ ,E________ 。
(2)B单质在D单质中燃烧,反应现象是_________ ,生成物的化学式为______________ 。
(3)D与E形成的化合物的化学键类型是______________ 。
(4)向D与E形成的化合物的水溶液中滴入烧碱溶液直至过量时,观察到的现象是___________ ,有关反应的离子方程式为______________ 。
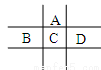
(1)五种元素的名称:A
(2)B单质在D单质中燃烧,反应现象是
(3)D与E形成的化合物的化学键类型是
(4)向D与E形成的化合物的水溶液中滴入烧碱溶液直至过量时,观察到的现象是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】短周期主族元素A、B、C、D在周期表中的相对位置如图所示。已知B的简单氢化物和它的最高价氧化物对应的水化物相遇产生白烟,并生成离子化合物。
请回答下列问题:
(1)A在元素周期表中的位置是___________ 。
(2)D的简单阴离子的结构示意图为___________ ;B的简单氢化物的电子式为___________ 。
(3)写出一个置换反应证明D的非金属性比C的强:___________ (写离子方程式)。
(4)在A、B、C、D的最高价氧化物对应的水化物中,酸性最强的是___________ (填化学式);在A和氢形成的化合物中,一定条件下能与水发生加成反应的是___________ (填一种结构简式)。
(5)实验室中常用热的烧碱溶液清洗试管里残留的C单质,在该反应中C单质既是氧化剂又是还原剂,且生成两种盐,其中一种盐中C的化合价为+4,写出该反应的化学方程式:___________ 。
 |  | ||
 |  | ||
(1)A在元素周期表中的位置是
(2)D的简单阴离子的结构示意图为
(3)写出一个置换反应证明D的非金属性比C的强:
(4)在A、B、C、D的最高价氧化物对应的水化物中,酸性最强的是
(5)实验室中常用热的烧碱溶液清洗试管里残留的C单质,在该反应中C单质既是氧化剂又是还原剂,且生成两种盐,其中一种盐中C的化合价为+4,写出该反应的化学方程式:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】X、Y、Z、R为前四周期元素,且原子序数依次增大。XY2是红棕色气体;X与氢元素可形成XH3;Z基态原子的M层与K层电子数相等;R2+离子的3d轨道中有9个电子。请回答下列问题:
(1)Y基态原子的电子轨道表示式是________ ;XH3的空间构型是_______________ ;
(2)Z所在周期中第一电离能最大的主族元素是________ ;
(3)X、Y可组成分子式为X2Y的物质,请写出其结构式:________________ ,其中心原子杂化方式是___________ ,写出一种与其等电子体的分子______________________
(4)往RCl2溶液中通入XH3气体,最终形成[R(NH3)4]Cl2,在实验过程中可观察到的现象是_______________ ,1mol[R(NH3)4]Cl2含有的σ键的数目为__________
(1)Y基态原子的电子轨道表示式是
(2)Z所在周期中第一电离能最大的主族元素是
(3)X、Y可组成分子式为X2Y的物质,请写出其结构式:
(4)往RCl2溶液中通入XH3气体,最终形成[R(NH3)4]Cl2,在实验过程中可观察到的现象是
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐2】新型SiC增强铝基复合材料,可展开柔性砷化镓太阳能电池系统,助力“天问一号”开展火星探测。回答下列问题:
(1)基态Si原子中,电子占据的最高能级符号为_______ ,Ga的基态原子的价电子排布式是_______ 。
(2)第三周期元素中,第一电离能介于铝和磷之间的元素除硅外,还有_______ (填元素符号)
(3)碳化硅和硅晶体都具有金刚石型结构,碳化硅熔点高于硅的原因是_______ 。
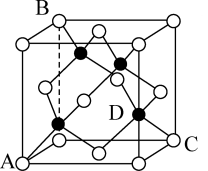
(4)GaAs的晶胞如图所示。_______ 。
②下列说法正确的是_______ (填字母)
A.砷化镓晶胞结构与NaCl相同 B.GaP与GaAs互为等电子体
C.电负性:As<Ga D.砷化镓晶体中含有配位键
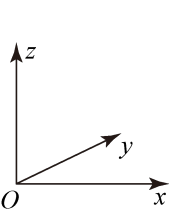
(5)原子坐标参数表示晶胞内部各原子的相对位置。图中各原子坐标参数A为(0,0,0);B为(0,1,1);C为(1,1,0);则D原子的坐标参数为_______ 。
(1)基态Si原子中,电子占据的最高能级符号为
(2)第三周期元素中,第一电离能介于铝和磷之间的元素除硅外,还有
(3)碳化硅和硅晶体都具有金刚石型结构,碳化硅熔点高于硅的原因是
(4)GaAs的晶胞如图所示。
②下列说法正确的是
A.砷化镓晶胞结构与NaCl相同 B.GaP与GaAs互为等电子体
C.电负性:As<Ga D.砷化镓晶体中含有配位键
(5)原子坐标参数表示晶胞内部各原子的相对位置。图中各原子坐标参数A为(0,0,0);B为(0,1,1);C为(1,1,0);则D原子的坐标参数为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】下表为长式周期表的一部分,其中的序号代表对应的元素。
(1)写出上表中元素⑨的三价离子的结构示意图_______ 。
(2)元素⑩的晶体中原子堆积方式是_______ ,晶体中原子的空间利用率是_______
(3)元素②的第二电离能_______ Na(填写“>”“=”或“<”)的第二电离能;元素⑨的氧化物MXO晶体晶胞结构为NaCl型,由于晶体缺陷,x值为0.88,若晶体中的M分别为M2﹢、M3﹢,此晶体中M2﹢与M3﹢的最简整数比为_______
(4)在测定元素①与⑥形成化合物的相对分子质量时,实验测得的值一般高于理论值的主要原因是_______ 。
(5)用惰性电极电解足量的由元素⑦与元素⑧形成的化合物的水溶液,写出电解反应的离子方程式为_______ 。
| ① | |||||||||||||||||
| ② | ③ | ④ | ⑤ | ⑥ | |||||||||||||
| ⑦ | ⑧ | ||||||||||||||||
| ⑨ | ⑩ |
(2)元素⑩的晶体中原子堆积方式是
(3)元素②的第二电离能
(4)在测定元素①与⑥形成化合物的相对分子质量时,实验测得的值一般高于理论值的主要原因是
(5)用惰性电极电解足量的由元素⑦与元素⑧形成的化合物的水溶液,写出电解反应的离子方程式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】已知A、B、C、D、E为元素周期表中前四周期元素,且原子序数依次增大,A是短周期中原子半径最大的元素,B元素3p能级半充满;C是所在周期电负性最大的元素;D是第四周期未成对电子最多的元素;E元素位于元素周期表的第11列。试回答下列有关的问题:
(1)E元素位于元素周期表的_______ 区。
(2)画出A、B、C中第一电离能最大的元素的原子结构式意图,_______ ;这三种元素最高价氧化物的水化物形成的溶液,物质的量浓度相同时,pH由大到小的顺序_______ (写化学式)。
(3)D可形成化合物 。
。
① 中配体的
中配体的 模型名称是
模型名称是_______ 。该化合物中阴离子的中心原子的轨道杂化类型为_______ 。
② 中
中 的键角
的键角____ 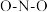 的键角(填“>”、<”、“=”),原因是
的键角(填“>”、<”、“=”),原因是____ 。
(1)E元素位于元素周期表的
(2)画出A、B、C中第一电离能最大的元素的原子结构式意图,
(3)D可形成化合物
 。
。①
 中配体的
中配体的 模型名称是
模型名称是②
 中
中 的键角
的键角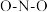 的键角(填“>”、<”、“=”),原因是
的键角(填“>”、<”、“=”),原因是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
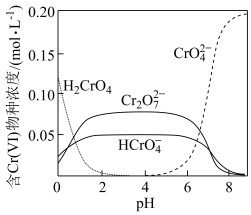
【推荐2】处理废水中Cr(Ⅵ)的常用方法包括绿矾还原法、铁粉还原法和离子交换法等。含Cr(Ⅵ)物种浓度随pH的变化如下图所示。
①“还原”时, 被还原成Cr3+的离子方程式为
被还原成Cr3+的离子方程式为___________ 。
②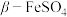 的晶胞沿c轴(c轴垂直于a、b轴)方向投影的平面图如下图所示,其中硫原子的杂化方式为
的晶胞沿c轴(c轴垂直于a、b轴)方向投影的平面图如下图所示,其中硫原子的杂化方式为___________ ;已知该晶胞中S原子的数目为4,试预测Fe2+是否占据该晶胞的所有顶点、面心和体心,并说明理由___________ 。___________ 。
(3)离子交换法。阴离子交换树脂(ROH,R为高分子阳离子骨架)去除酸性废水中Cr(Ⅵ)的原理为 。
。
①树脂失效后,用NaOH溶液将树脂再生,发生反应的化学方程式为___________ 。
②某树脂的Cr(Ⅵ)摩尔交换总容量为1.45mol·L-1,即每升湿树脂最多吸收1.45molCr(Ⅵ)。现将Cr(Ⅵ)含量为50mg·L-1的废水以1.0L∙h-1的流量通过填充有30mL湿树脂的淡化室。试通过计算说明,通废水20h时,该离子交换树脂是否达到吸收饱和___________ 。[Cr(Ⅵ)均以铬元素计,写出计算过程]
①“还原”时,
 被还原成Cr3+的离子方程式为
被还原成Cr3+的离子方程式为②
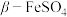 的晶胞沿c轴(c轴垂直于a、b轴)方向投影的平面图如下图所示,其中硫原子的杂化方式为
的晶胞沿c轴(c轴垂直于a、b轴)方向投影的平面图如下图所示,其中硫原子的杂化方式为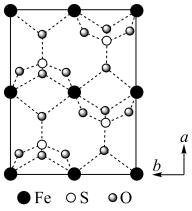
(3)离子交换法。阴离子交换树脂(ROH,R为高分子阳离子骨架)去除酸性废水中Cr(Ⅵ)的原理为
 。
。①树脂失效后,用NaOH溶液将树脂再生,发生反应的化学方程式为
②某树脂的Cr(Ⅵ)摩尔交换总容量为1.45mol·L-1,即每升湿树脂最多吸收1.45molCr(Ⅵ)。现将Cr(Ⅵ)含量为50mg·L-1的废水以1.0L∙h-1的流量通过填充有30mL湿树脂的淡化室。试通过计算说明,通废水20h时,该离子交换树脂是否达到吸收饱和
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】N、F、Cu、Se及其化合物在化工、医药、材料等方面应用十分广泛。回答下列有关问题:
(1)N原子中最高能级的电子的电子云轮廓图为_______ ;基态Cu+的核外电子排布为_____
(2)化合物(CH3)3N可用于制备医药、农药。分子中N原子杂化方式为_______ 杂化,该物质能溶于水的原因是_______
(3)Cu与Ag为同族元素,熔点:Cu_______ Ag(填“>”或“<”),原因是 _______ 。
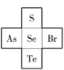
(4)S、Se、Te在元素周期表中与其他元素的位置关系如图所示,则Te、As、Se、Br四种元素的第一电离能由大到小的顺序为_______ ,SeO 的空间构型为
的空间构型为_______ 。
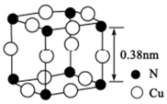
(5)氮、铜形成的一种化合物的晶胞结构如图所示。与每个Cu原子紧邻的Cu原子有_______ 个,令阿伏加德罗常数的值为NA,该晶体的密度为_____ g/cm3(列式计算)
(1)N原子中最高能级的电子的电子云轮廓图为
(2)化合物(CH3)3N可用于制备医药、农药。分子中N原子杂化方式为
(3)Cu与Ag为同族元素,熔点:Cu
(4)S、Se、Te在元素周期表中与其他元素的位置关系如图所示,则Te、As、Se、Br四种元素的第一电离能由大到小的顺序为
 的空间构型为
的空间构型为
(5)氮、铜形成的一种化合物的晶胞结构如图所示。与每个Cu原子紧邻的Cu原子有

您最近一年使用:0次
【推荐1】回答下列问题: 晶体在
晶体在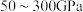 的高压下和
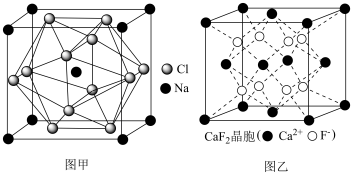
的高压下和 反应生成如图甲所示的晶胞结构,则该晶体的化学式为
反应生成如图甲所示的晶胞结构,则该晶体的化学式为___________ 已知阿伏伽德罗常数为NA,晶胞边长为anm,则该晶体的摩尔体积 Vm为___________ m3 /mol。
(2) 的晶胞如上图乙所示,
的晶胞如上图乙所示, 的配位数为
的配位数为 ___________ 晶体密度为 ,相邻的两个
,相邻的两个 的最近核间距为anm,则
的最近核间距为anm,则 的摩尔质量为
的摩尔质量为___________ 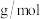 (用表示
(用表示 ,
, 为阿伏加德罗常数的值,)。
为阿伏加德罗常数的值,)。
(3)晶体中 、
、 、
、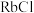 、
、 的熔点由高到低的顺序为
的熔点由高到低的顺序为___________ ,原因为___________ 。
(4)N、O、Ba简单氢化物的沸点由高到低的顺序为___________ (填化学式)。
(5)硼烷-吡啶( )是一种中等强度的还原性试剂,在质子性溶剂中,它的稳定性和溶解性均优于硼氢化钠(NaBH4),则硼氢化钠电子式为
)是一种中等强度的还原性试剂,在质子性溶剂中,它的稳定性和溶解性均优于硼氢化钠(NaBH4),则硼氢化钠电子式为___________ 。硼烷-吡啶组成元素的电负性从大到小的顺序是___________ 。
 晶体在
晶体在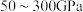 的高压下和
的高压下和 反应生成如图甲所示的晶胞结构,则该晶体的化学式为
反应生成如图甲所示的晶胞结构,则该晶体的化学式为(2)
 的晶胞如上图乙所示,
的晶胞如上图乙所示, 的配位数为
的配位数为  ,相邻的两个
,相邻的两个 的最近核间距为anm,则
的最近核间距为anm,则 的摩尔质量为
的摩尔质量为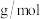 (用表示
(用表示 ,
, 为阿伏加德罗常数的值,)。
为阿伏加德罗常数的值,)。(3)晶体中
 、
、 、
、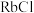 、
、 的熔点由高到低的顺序为
的熔点由高到低的顺序为(4)N、O、Ba简单氢化物的沸点由高到低的顺序为
(5)硼烷-吡啶(
 )是一种中等强度的还原性试剂,在质子性溶剂中,它的稳定性和溶解性均优于硼氢化钠(NaBH4),则硼氢化钠电子式为
)是一种中等强度的还原性试剂,在质子性溶剂中,它的稳定性和溶解性均优于硼氢化钠(NaBH4),则硼氢化钠电子式为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】如图所示,直线交点处的圆圈为NaCl晶体中Na+离子或Cl-离子所处的位置。这两种离子在空间三个互相垂直的方向上都是等距离排列的。

(1)晶体中,在每个Na+离子的周围与它最接近的且距离相等的Na+离子共有____ 个。
(2)已知食盐晶体的密度为2.2g/cm3,阿伏加德罗常数为6.02×1023mol-1。食盐晶体中两个距离最近的钠离子中心间的距离为________________ cm。计算过程如下:
_________________________________________________________________________________________________________________________________________________________ 。

(1)晶体中,在每个Na+离子的周围与它最接近的且距离相等的Na+离子共有
(2)已知食盐晶体的密度为2.2g/cm3,阿伏加德罗常数为6.02×1023mol-1。食盐晶体中两个距离最近的钠离子中心间的距离为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐3】Ⅰ.回答下列问题:
(1)写出溴原子的核外电子排布式_________ ,写出Fe的原子结构示意图_________
(2)元素金(Au)处于周期表中的第六周期,与Cu同族,一种铜金合金晶体的晶胞中Cu原子处于面心,Au原子处于顶角位置,则该合金中Cu原子与Au原子数目之比为_________ ;该晶体中,原子之间的相互作用是_________ 。
(3)某钙钛型复合氧化物如图所示,以A原子为晶胞的顶角,A位可以是Ca、Sr、Ba或Pb,当B位是V、Cr、Mn、Fe等时,这种化合物具有CMR效应。

①用A、B、O表示这类特殊晶体的化学式_________ 。
②下列有关说法正确的是_________ 。
A.镧、锰、氧分别位于周期表f、d、p区
B.氧元素的第一电离能比氮元素的第一电离能大
C.锰的电负性为1.59,铬的电负性为1.66,说明锰的金属性比铬强
D.铬的价电子排布与钾相同
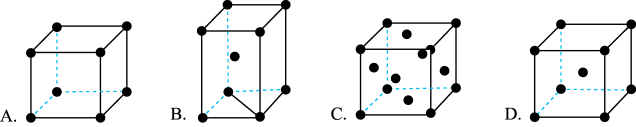
Ⅱ.如图所示为金属原子的四种基本堆积(分别为:简单立方堆积、六方最密堆积、面心立方最密堆积、体心立方堆积)模型,请回答以下问题:
(4)某金属R的晶胞为D型,已知R原子半径为rcm,相对原子质量为M,阿伏加德罗常数为NA,则R金属的密度_________ g/cm3。(用含r、M、NA字母的式子表示)
(1)写出溴原子的核外电子排布式
(2)元素金(Au)处于周期表中的第六周期,与Cu同族,一种铜金合金晶体的晶胞中Cu原子处于面心,Au原子处于顶角位置,则该合金中Cu原子与Au原子数目之比为
(3)某钙钛型复合氧化物如图所示,以A原子为晶胞的顶角,A位可以是Ca、Sr、Ba或Pb,当B位是V、Cr、Mn、Fe等时,这种化合物具有CMR效应。

①用A、B、O表示这类特殊晶体的化学式
②下列有关说法正确的是
A.镧、锰、氧分别位于周期表f、d、p区
B.氧元素的第一电离能比氮元素的第一电离能大
C.锰的电负性为1.59,铬的电负性为1.66,说明锰的金属性比铬强
D.铬的价电子排布与钾相同
Ⅱ.如图所示为金属原子的四种基本堆积(分别为:简单立方堆积、六方最密堆积、面心立方最密堆积、体心立方堆积)模型,请回答以下问题:

(4)某金属R的晶胞为D型,已知R原子半径为rcm,相对原子质量为M,阿伏加德罗常数为NA,则R金属的密度
您最近一年使用:0次



