铜是人类最早使用的金属之一,金属铜及其化合物在工业生产及生活中用途非常广泛。回答下列问题:
(1)基态+2价铜离子M能层电子排布式是___________ ;第4周期中基态原子未成对电子数与铜原子相同的元素有________ 种。
(2)Cu+能与SCN-形成CuSCN沉淀。请写出一种与SCN-互为等电子体的微粒_________ 。SCN-对应的酸有硫氰酸(H-S-C N)和异硫氰酸(H-N=C=S),这两种酸熔点更高的是
N)和异硫氰酸(H-N=C=S),这两种酸熔点更高的是_______ (填名称),原因是_____________________ 。
(3)Cu2+能与NH3形成平面正方形的[Cu(NH3)4]2+。NH3分子的空间构型为__________ ;[Cu(NH3)4]2+中Cu采取dspx杂化,x的值是__________ 。
(4)已知Cu2O 熔点为1235 ℃,K2O 熔点为770℃,前者熔点较高,其原因是___________ 。
(5)Cu3N 的晶胞(立方)结构如下图所示:
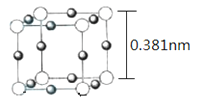
①距离最近的两个Cu+间的距离为________ nm。(保留两位小数)
②Cu3N 晶体的密度为____________ g·cm-3。(NA表示阿伏伽德罗常数的值,列出计算式,不必计算出结果)
(1)基态+2价铜离子M能层电子排布式是
(2)Cu+能与SCN-形成CuSCN沉淀。请写出一种与SCN-互为等电子体的微粒
 N)和异硫氰酸(H-N=C=S),这两种酸熔点更高的是
N)和异硫氰酸(H-N=C=S),这两种酸熔点更高的是(3)Cu2+能与NH3形成平面正方形的[Cu(NH3)4]2+。NH3分子的空间构型为
(4)已知Cu2O 熔点为1235 ℃,K2O 熔点为770℃,前者熔点较高,其原因是
(5)Cu3N 的晶胞(立方)结构如下图所示:

①距离最近的两个Cu+间的距离为
②Cu3N 晶体的密度为
更新时间:2018-05-13 09:38:18
|
相似题推荐
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】(1)LiAlH4是有机合成中常用的还原剂,LiAlH4中的阴离子空间构型是___________________ ,中心原子的杂化形式为________ 。LiAlH4中,存在________ (填标号)。
A.离子键 B.σ键 C.π键 D.氢键
(2)①根据价层电子对互斥理论,H2S、SO2、SO3的气态分子中,中心原子价层电子对数不同于其他分子的是________ 。
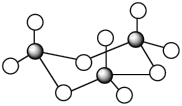
②气态三氧化硫以单分子形式存在,其分子的立体构型为________ 形,其中共价键的类型有________ 种;固体三氧化硫中存在如图所示的三聚分子,该分子中S原子的杂化轨道类型为________ 。
(3)《中华本草》等中医典籍中,记载了炉甘石(ZnCO3)入药,可用于治疗皮肤炎症或表面创伤。ZnCO3中,阴离子空间构型为__________ ,C原子的杂化形式为________ 。
(4)X射线衍射测定等发现,I3AsF6中存在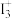 离子。
离子。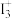 离子的几何构型为
离子的几何构型为________ ,中心原子的杂化形式为________ 。
(5)CO2和CH3OH分子中C原子的杂化形式分别为________ 和________ 。
(6)AsCl3分子的立体构型为____________ ,其中As的杂化轨道类型为________ 。
A.离子键 B.σ键 C.π键 D.氢键
(2)①根据价层电子对互斥理论,H2S、SO2、SO3的气态分子中,中心原子价层电子对数不同于其他分子的是
②气态三氧化硫以单分子形式存在,其分子的立体构型为

(3)《中华本草》等中医典籍中,记载了炉甘石(ZnCO3)入药,可用于治疗皮肤炎症或表面创伤。ZnCO3中,阴离子空间构型为
(4)X射线衍射测定等发现,I3AsF6中存在
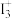 离子。
离子。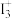 离子的几何构型为
离子的几何构型为(5)CO2和CH3OH分子中C原子的杂化形式分别为
(6)AsCl3分子的立体构型为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】[化学——选修3:物质结构与性质]磷存在于人体所有细胞中,是维持骨骼和牙齿的必要物质,几乎参与所有生理上的化学反应。回答下列问题:
(1)基态P原子的核外电子排布式为________ ,有________ 个未成对电子。
(2)磷的一种同素异形体——白磷(P4)的立体构型为________ ,其键角为__________ ,推测其在CS2中的溶解度________ (填“大于”或“小于”)在水中的溶解度。
(3)两种三角锥形气态氢化物膦(PH3)和氨(NH3)的键角分别为93.6º和107º,试分析PH3的键角小于NH3的原因______________________________ 。
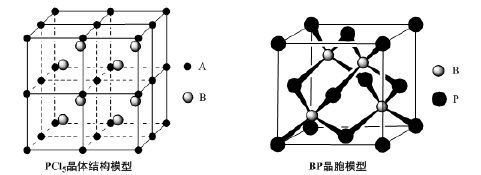
(4)常温下PCl5是一种白色晶体,其立方晶系晶体结构模型如上左图所示,由A、B两种微粒构成。将其加热至148℃熔化,形成一种能导电的熔体。已知A、B两种微粒分别与CCl4、SF6互为等电子体,则A为______ ,其中心原子杂化轨道类型为__________ ,B为________ 。
(5)磷化硼(BP)是一种超硬耐磨涂层材料,上右图为其立方晶胞,其中的每个原子均满足8电子稳定结构,试判断其熔点__________ (填“高于”或“低于”)金刚石熔点。
已知其B—P键长均为x cm,则其密度为________ g﹒cm—3(列出计算式即可)。
(1)基态P原子的核外电子排布式为
(2)磷的一种同素异形体——白磷(P4)的立体构型为
(3)两种三角锥形气态氢化物膦(PH3)和氨(NH3)的键角分别为93.6º和107º,试分析PH3的键角小于NH3的原因

(4)常温下PCl5是一种白色晶体,其立方晶系晶体结构模型如上左图所示,由A、B两种微粒构成。将其加热至148℃熔化,形成一种能导电的熔体。已知A、B两种微粒分别与CCl4、SF6互为等电子体,则A为
(5)磷化硼(BP)是一种超硬耐磨涂层材料,上右图为其立方晶胞,其中的每个原子均满足8电子稳定结构,试判断其熔点
已知其B—P键长均为x cm,则其密度为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】实验室常利用“棕色环”现象检验NO3—离子。其方法为:取含有NO3—的溶液于试管中,加入FeSO4溶液振荡,然后沿着试管内壁加入浓H2SO4,在溶液的界面上出现“棕色环”。回答下列问题:
(1)基态Fe2+核外未成对电子个数为_____ 。
(2)形成“棕色环”主要发生如下反应:
3[Fe( H2O)6]2++ NO3-+4H+=3[Fe(H2O)6]3++ NO ↑+2H2O
[Fe( H2O)6]2++ NO=[Fe(NO) (H2O)5]2+(棕色)+ H2O
[Fe(NO)(H2O)5]2+中,配体是______ 、______ ,配位数为______ 。
(3)与NO互为等电子体的微粒是_____ (任写一例)。
(4)SO42-的空间构型是_____ ,其中S原子的杂化方式是________ 。
(5)铁原子在不同温度下排列构成不同晶体结构,在912℃以下排列构成的晶体叫做α-铁;在912℃至1394℃之间排列构成的晶体叫做γ-铁;在1394℃以上排列构成的晶体,叫做δ-铁。晶胞剖面结构如图所示:

①α-铁的原子堆积方式为_____ 。δ-铁配位数为____ 。
②已知γ-铁晶体密度为d g/cm3,则Fe原子的半径为____ nm(用含d、NA的式子表示)。
(1)基态Fe2+核外未成对电子个数为
(2)形成“棕色环”主要发生如下反应:
3[Fe( H2O)6]2++ NO3-+4H+=3[Fe(H2O)6]3++ NO ↑+2H2O
[Fe( H2O)6]2++ NO=[Fe(NO) (H2O)5]2+(棕色)+ H2O
[Fe(NO)(H2O)5]2+中,配体是
(3)与NO互为等电子体的微粒是
(4)SO42-的空间构型是
(5)铁原子在不同温度下排列构成不同晶体结构,在912℃以下排列构成的晶体叫做α-铁;在912℃至1394℃之间排列构成的晶体叫做γ-铁;在1394℃以上排列构成的晶体,叫做δ-铁。晶胞剖面结构如图所示:

①α-铁的原子堆积方式为
②已知γ-铁晶体密度为d g/cm3,则Fe原子的半径为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】不锈钢以其优异的抗腐蚀性能越来越受到人们的青睐,它主要是由铁、铬、镍、铜、碳等元素所组成的合金。请完成以下有关物质结构的问题:
(1)写出Fe2+的最高能层的电子排布式:________________ 。
(2)[Cr(H2O)4Cl2] Cl·2H2O中Cr的配位数为________________ ;
已知CrO5中Cr为+6价,则CrO5的结构式为________ 。
(3)金属镍粉在CO气流中轻微加热,生成无色挥发性液体Ni(CO)n,推测Ni(CO)n的晶体类型为_______ ;已知该物质的中心原子价电子数与配体提供电子总数之和为18,则n=__________ ;与Ni(CO)n中配体互为等电子体的阴离子化学式为________________ 。
(4)金刚砂(SiC)结构与金刚石结构相似,若将金刚石晶体中一半的C原子换成Si原子且同种原子不成键,则得到金刚砂(SiC)结构。SiC是_________ 晶体,键角是_________ ;在SiC中,如果以一个硅原子为中心,则与硅原子次近的第二层有________ 个硅原子。
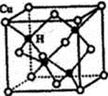
(5)铜是第四周期最重要的过渡元素之一,其单质及化合物具有广泛用途。CuH的晶体结构如下图所示,若CuH的密度为d g·cm-3,阿伏伽德罗常数的值为NA,则该晶胞的边长为______ cm(用含d和Na的式子表示)。
(1)写出Fe2+的最高能层的电子排布式:
(2)[Cr(H2O)4Cl2] Cl·2H2O中Cr的配位数为
已知CrO5中Cr为+6价,则CrO5的结构式为
(3)金属镍粉在CO气流中轻微加热,生成无色挥发性液体Ni(CO)n,推测Ni(CO)n的晶体类型为
(4)金刚砂(SiC)结构与金刚石结构相似,若将金刚石晶体中一半的C原子换成Si原子且同种原子不成键,则得到金刚砂(SiC)结构。SiC是
(5)铜是第四周期最重要的过渡元素之一,其单质及化合物具有广泛用途。CuH的晶体结构如下图所示,若CuH的密度为d g·cm-3,阿伏伽德罗常数的值为NA,则该晶胞的边长为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】钯(46Pd)催化剂在有机合成中有着重要的地位。请回答以下问题:
(1)钯与镍是同族元素,它们位于周期表的____ (选填s、p、d、ds、f)区。
(2)四(三苯基膦)钯(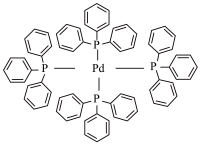 )是一种常见的钯催化剂,也是一种配合物,其配位数为
)是一种常见的钯催化剂,也是一种配合物,其配位数为_____ ,其中“三苯基膦”中磷原子与键合的三个碳原子构成的立体结构为__ 。
(3)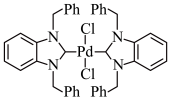 是苯并咪唑类卡宾化合物之一(-Ph代表苯基),常用作有机合成的催化剂,其晶体类型为
是苯并咪唑类卡宾化合物之一(-Ph代表苯基),常用作有机合成的催化剂,其晶体类型为____ 。配体中碳原子的杂化类型有____ ,其中氯原子的价电子轨道表达式为___ 。
(1)钯与镍是同族元素,它们位于周期表的
(2)四(三苯基膦)钯(
 )是一种常见的钯催化剂,也是一种配合物,其配位数为
)是一种常见的钯催化剂,也是一种配合物,其配位数为(3)
 是苯并咪唑类卡宾化合物之一(-Ph代表苯基),常用作有机合成的催化剂,其晶体类型为
是苯并咪唑类卡宾化合物之一(-Ph代表苯基),常用作有机合成的催化剂,其晶体类型为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】选做【化学——物质结构与性质】
氢能的存储是氢能应用的主要瓶颈,配位氢化物、富氢载体化合物是目前所采用的主要储氢材料。
(1)Ti(BH4)2是一种过渡元素硼氢化物储氢材料。
①在基态Ti2+中,电子占据的最高能层符号为________ ,该能层具有的原子轨道数为______ 。
②BH4-的空间构型是________ (用文字描述)。
(2)液氨是富氢物质,是氢能的理想载体,利用 ,实现储氢和输氢。下列说法正确的是
,实现储氢和输氢。下列说法正确的是________ 。
a.[Cu(NH3)4]2+中,N原子是配位原子
b.NH3分子中氮原子的轨道杂化方式为sp2杂化
c.键角NH4+<NH3
d.相同压强时,NH3的沸点比PH3的沸点高
(3)富氢材料NH3和F2在Cu催化剂存在下反应直接得到NF3

上述化学方程式中的5种物质所属的晶体类型有________ (填序号)
a.离子晶体 b.分子晶体
c.原子晶体 d.金属晶体
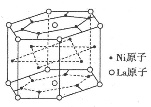
(4)某种合金材料有较大的储氢容量,其晶体结构的最小单元如图所示。则这种合金的化学式为________________ 。
氢能的存储是氢能应用的主要瓶颈,配位氢化物、富氢载体化合物是目前所采用的主要储氢材料。
(1)Ti(BH4)2是一种过渡元素硼氢化物储氢材料。
①在基态Ti2+中,电子占据的最高能层符号为
②BH4-的空间构型是
(2)液氨是富氢物质,是氢能的理想载体,利用
 ,实现储氢和输氢。下列说法正确的是
,实现储氢和输氢。下列说法正确的是a.[Cu(NH3)4]2+中,N原子是配位原子
b.NH3分子中氮原子的轨道杂化方式为sp2杂化
c.键角NH4+<NH3
d.相同压强时,NH3的沸点比PH3的沸点高
(3)富氢材料NH3和F2在Cu催化剂存在下反应直接得到NF3

上述化学方程式中的5种物质所属的晶体类型有
a.离子晶体 b.分子晶体
c.原子晶体 d.金属晶体
(4)某种合金材料有较大的储氢容量,其晶体结构的最小单元如图所示。则这种合金的化学式为

您最近一年使用:0次
【推荐1】国家航天局计划2020年实施火星探测任务。据了解火星上存在大量的含氮化合物,科学家推测火星生命可能主要以氮、碳、硅、铜为基体构成。
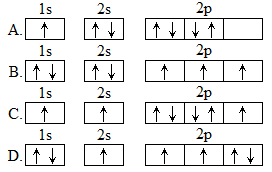
(1)下列氮原子的电子排布图表示的状态中,能量最高的是___________ (填字母标号)。
(2)某种铀氮化物的晶体结构是NaCl型。NaCl的Bom-Haber循环如下图所示。已知:元素的一个气态基态原子获得电子成为气态阴离子时所放出的能量称为电子亲和能。下列有关说法正确的是___________ (填字母标号)。
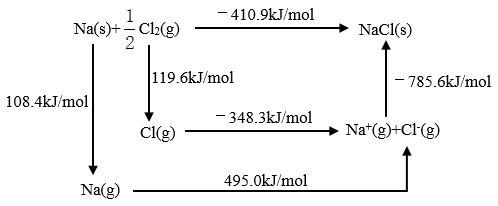
a.Cl-Cl键的键能为119.6kJ/mol
b.Na的第一电离能为603.4kJ/mol
c.NaCl的晶格能为785.6kJ/mol
d.Cl的第一电子亲和能为348.3kJ/mol
(3)乙二胺(H2N—CH2—CH2—NH2)是一种重要的配体,可简写为En。
①乙二胺分子中氮原子的杂化轨道类型为___________ 。
②乙二胺和三甲胺[N(CH3)3]均属于胺,且相对分子质量相近,但乙二胺比三甲胺的沸点高得多,原因是___________ 。
③乙二胺能与Mg2+、Cu2+等金属离子形成稳定环状离子,其中与乙二胺形成的化合物稳定性相对较高的是___________ (填“Mg2+”或“Cu2+”)。
(4)K3[Fe(CN)6](铁氰化钾)溶液可以检验铁陨石中铁元素价态。
①铁氰化钾中不存在的作用力有___________ (填字母)。
a.离子键 b.极性键 c.非极性键
d.π键 e.配位键 f.氢键
②1mol[Fe(CN)6]3-中含有的σ键数目为___________ (用NA表示阿伏加德罗常数的值)。
(5)CuF的晶胞结构如下图所示。在CuF晶体中距离Cu+最近的F-有___________ 个。已知CuF的密度为7.5g∙cm-3,则CuF的晶胞参数a=___________ nm(列出计算式)。

(1)下列氮原子的电子排布图表示的状态中,能量最高的是

(2)某种铀氮化物的晶体结构是NaCl型。NaCl的Bom-Haber循环如下图所示。已知:元素的一个气态基态原子获得电子成为气态阴离子时所放出的能量称为电子亲和能。下列有关说法正确的是

a.Cl-Cl键的键能为119.6kJ/mol
b.Na的第一电离能为603.4kJ/mol
c.NaCl的晶格能为785.6kJ/mol
d.Cl的第一电子亲和能为348.3kJ/mol
(3)乙二胺(H2N—CH2—CH2—NH2)是一种重要的配体,可简写为En。
①乙二胺分子中氮原子的杂化轨道类型为
②乙二胺和三甲胺[N(CH3)3]均属于胺,且相对分子质量相近,但乙二胺比三甲胺的沸点高得多,原因是
③乙二胺能与Mg2+、Cu2+等金属离子形成稳定环状离子,其中与乙二胺形成的化合物稳定性相对较高的是
(4)K3[Fe(CN)6](铁氰化钾)溶液可以检验铁陨石中铁元素价态。
①铁氰化钾中不存在的作用力有
a.离子键 b.极性键 c.非极性键
d.π键 e.配位键 f.氢键
②1mol[Fe(CN)6]3-中含有的σ键数目为
(5)CuF的晶胞结构如下图所示。在CuF晶体中距离Cu+最近的F-有

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】由IIA元素与VA元素所形成的化合物种类繁多,它们是探测器、激光器、微波器的重要材料。回答下列问题:
(1)基态Ga原子核外电子排布式为[Ar]______ 。
(2)氧原子价电子层上的电子可以进行重排以便提供一个空轨道与氮原子形成配位键,该氧原子重排后的价电子排布图为________ ,电子重排后的氧原子能量有所升高,原因是不符合_____ (填“泡利原理”或“洪特规则”)。
(3)自然界中不存在单质硼,硼的氢化物也很少,主要存在的是硼的含氧化合物,根据下表数据分析其原因是______ 。
(4)比较大小:键角PH3________ (填“>”或“<”,下同)NH3;熔、沸点:PH3_______ NH3。
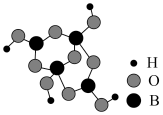
(5)如图为四硼酸根离子球棍模型,该离子符号为_______ ,其中硼原子轨道的杂化类型有______ 。
(6)叠氮酸铵(NH4N3)是一种具有爆炸性的无色晶体。叠氮酸根( )的空间结构为
)的空间结构为______ ;叠氮酸铵的晶胞如图所示,其晶胞参数为a nm和0.5a nm,阿伏加德罗常数的值为NA,NH4N3的密度为____ g·cm-3。

(1)基态Ga原子核外电子排布式为[Ar]
(2)氧原子价电子层上的电子可以进行重排以便提供一个空轨道与氮原子形成配位键,该氧原子重排后的价电子排布图为
(3)自然界中不存在单质硼,硼的氢化物也很少,主要存在的是硼的含氧化合物,根据下表数据分析其原因是
| 化学键 | B-H | B-O | B-B |
| 键能(kJ∙mol-1) | 389 | 561 | 293 |
(5)如图为四硼酸根离子球棍模型,该离子符号为

(6)叠氮酸铵(NH4N3)是一种具有爆炸性的无色晶体。叠氮酸根(
 )的空间结构为
)的空间结构为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】联氨(N2H4)可以用于处理高压锅炉水中的氧,防止锅炉被腐蚀,其中一种可能的反应机理如图所示,回答下列问题:
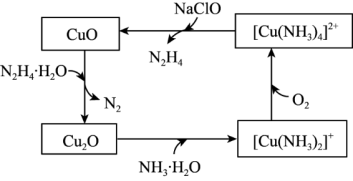
(1)[Cu(NH3)4]2+是一种常见的配离子,其中心离子为_______ ,配位原子为_______ ,配位数_______ 。
(2)写出碱性条件下,[Cu(NH3)4]2+与NaClO反应的离子方程式_______ 。
(3)N2H4中心原子的杂化类型是_______ 。N2H4与O2的相对分子质量相近,但N2H4的熔点(2℃)沸点(114℃)分别远远高于O2的熔点(-218℃)、沸点(-183℃),原因是_______ 。
(4)NaClO发生水解可生成HClO。HClO的空间构型是_______ 。
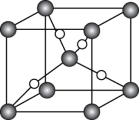
(5)已知Cu2O晶胞的结构如图所示:
①在该晶胞中,Cu+的配位数_______ 。
②已知该晶体密度为ρg/cm3,NA表示阿伏加德罗常数的数值,则晶胞参数a(立方体边长)为_______ pm(用含ρ和NA的代数式表示)。

(1)[Cu(NH3)4]2+是一种常见的配离子,其中心离子为
(2)写出碱性条件下,[Cu(NH3)4]2+与NaClO反应的离子方程式
(3)N2H4中心原子的杂化类型是
(4)NaClO发生水解可生成HClO。HClO的空间构型是
(5)已知Cu2O晶胞的结构如图所示:
①在该晶胞中,Cu+的配位数
②已知该晶体密度为ρg/cm3,NA表示阿伏加德罗常数的数值,则晶胞参数a(立方体边长)为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐1】某些过渡元素的相关化合物在化工、医药、材料等领域有着极为广泛的应用。回答下列问题:
(1)现有铜锌元素的3种微粒:①锌:[Ar]3d104s1;②铜:[Ar]3d104s1;③铜:[Ar]3d10,失去一个电子需要的最低能量由大到小的顺序是___________(填字母)。
(2)国际权威学术期刊《自然》最近报道,我国科学家选择碲化锆(ZrTes)和砷化镉(Cd3As2)为材料验证了三维量子霍尔效应。
①Zr是Ti的同族相邻元素,位于周期表的___________ 区。
②Cd2+与NH3可形成配离子[Cd(NH3)4]2+。
i.该离子中不含的化学键类型有___________ (填字母)。
A.离子键 B.配位键 C.σ键 D.共价键 E.π键 F.氢键
ii.已知该离子中2个NH3被2个Cl-替代只得到一种结构,则该离子的立体构型为___________ 。
(3)二烃基锌(R-Zn-R)分子中烃基R与锌以σ键结合,C2H5-Zn-C2H5分子中原子的杂化方式有___________ ,如表是2种二烃基锌的沸点数据,则烃基R1是___________ ,推断的依据是___________ 。
(4)硫酸氧钛(Ti)是一种优良的催化剂,其阳离子为如图所示链状聚合形式的离子,聚合度为n。则该阳离子的化学式为___________ 。
(1)现有铜锌元素的3种微粒:①锌:[Ar]3d104s1;②铜:[Ar]3d104s1;③铜:[Ar]3d10,失去一个电子需要的最低能量由大到小的顺序是___________(填字母)。
| A.①②③ | B.③①② | C.③②① | D.①③② |
①Zr是Ti的同族相邻元素,位于周期表的
②Cd2+与NH3可形成配离子[Cd(NH3)4]2+。
i.该离子中不含的化学键类型有
A.离子键 B.配位键 C.σ键 D.共价键 E.π键 F.氢键
ii.已知该离子中2个NH3被2个Cl-替代只得到一种结构,则该离子的立体构型为
(3)二烃基锌(R-Zn-R)分子中烃基R与锌以σ键结合,C2H5-Zn-C2H5分子中原子的杂化方式有
| 物质 | R1-Zn-R1 | C2H5-Zn-C2H5 |
| 沸点(℃) | 46 | 118 |

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】(1)普鲁士蓝的化学式为Fe4[Fe(CN)6]3,该物质中存在的化学键有离子键、_______ 和_______ ;含有的Fe3+的核外电子排布式为_______________ 。
(2)KCN 可被H2O2氧化为KOCN
①KOCN 可作为制药原料,其晶体类型是__________ ;碳原子采取sp杂化,1mol该物质中含有的π键数目为___________ 。含有的三种非金属元素的电负性由大到小的顺序是________ 。②H2O2常温下是液体,沸点较高(150℃),其主要原因是____________ 。
(3)成语“信口雌黄”中的雌黄分子式为As2S3,分子结构如下左图,As 原子的杂化方式为____ ,雌黄和SnCl2 在盐酸中反应转化为雌黄(As4S4) 和SnCl4,SnCl4分子的空间构型为_______ 。
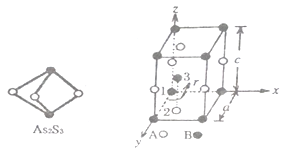
(4)某晶体的晶胞结构如上右图所示,该晶体的化学式为______________ ,该晶胞参数分别为apm,cpm,γ=120°如图示;1号原子坐标为(0,0,0),2 号原子坐标为(1/3,2/3,0),则3号原子坐标为____________ ,计算上述晶体中A和B 两原子间的最小核间距为________ pm。
(2)KCN 可被H2O2氧化为KOCN
①KOCN 可作为制药原料,其晶体类型是
(3)成语“信口雌黄”中的雌黄分子式为As2S3,分子结构如下左图,As 原子的杂化方式为

(4)某晶体的晶胞结构如上右图所示,该晶体的化学式为
您最近一年使用:0次
【推荐3】翡翠的主要成分为NaAlSi2O6,还含有其他多种金属阳离子,其中Cr3+的含量决定其绿色的深浅,是决定翡翠品质的重要因素之一
(1)基态Cr3+最外电子层的电子排布图(轨道表示式)为_______ 。
(2)NaAlSi2O6所含元素中,第一电离能最小的是_______ ,原因是_______
(3)配合物K[Cr(C2O4)2(H2O)]中的配体是_______ ,H2O的沸点比CO2的高了许多,主要原因是_______ 。
(4)已知某FeSO4·xH2O的结构如图所示。

粒子内部的键角SO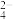
_______ H2O(填“>”“<”或“=”),从杂化类型及斥力大小角度说明判断的理由:_______ 。
(5)Ca、O、Cr可以形成一种具有特殊导电性的复合氧化物,晶胞结构如图所示,其中Ca2+、O2-采用面心立方最密堆积方式。
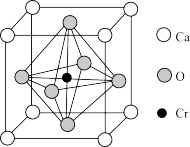
①该晶体的化学式为_______ 。
②已知钙离子、氧离子半径分别为100pm、140pm,晶胞中Cr4+位于O2-所形成的正八面体的体心,该正八面体的边长为_______ pm。
(1)基态Cr3+最外电子层的电子排布图(轨道表示式)为
(2)NaAlSi2O6所含元素中,第一电离能最小的是
(3)配合物K[Cr(C2O4)2(H2O)]中的配体是
(4)已知某FeSO4·xH2O的结构如图所示。

粒子内部的键角SO
(5)Ca、O、Cr可以形成一种具有特殊导电性的复合氧化物,晶胞结构如图所示,其中Ca2+、O2-采用面心立方最密堆积方式。

①该晶体的化学式为
②已知钙离子、氧离子半径分别为100pm、140pm,晶胞中Cr4+位于O2-所形成的正八面体的体心,该正八面体的边长为
您最近一年使用:0次



