[化学——选修3:物质结构与性质]磷存在于人体所有细胞中,是维持骨骼和牙齿的必要物质,几乎参与所有生理上的化学反应。回答下列问题:
(1)基态P原子的核外电子排布式为________ ,有________ 个未成对电子。
(2)磷的一种同素异形体——白磷(P4)的立体构型为________ ,其键角为__________ ,推测其在CS2中的溶解度________ (填“大于”或“小于”)在水中的溶解度。
(3)两种三角锥形气态氢化物膦(PH3)和氨(NH3)的键角分别为93.6º和107º,试分析PH3的键角小于NH3的原因______________________________ 。
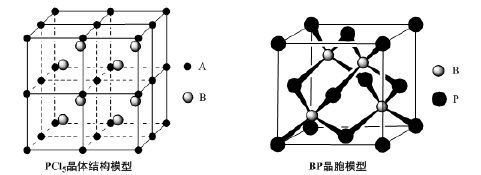
(4)常温下PCl5是一种白色晶体,其立方晶系晶体结构模型如上左图所示,由A、B两种微粒构成。将其加热至148℃熔化,形成一种能导电的熔体。已知A、B两种微粒分别与CCl4、SF6互为等电子体,则A为______ ,其中心原子杂化轨道类型为__________ ,B为________ 。
(5)磷化硼(BP)是一种超硬耐磨涂层材料,上右图为其立方晶胞,其中的每个原子均满足8电子稳定结构,试判断其熔点__________ (填“高于”或“低于”)金刚石熔点。
已知其B—P键长均为x cm,则其密度为________ g﹒cm—3(列出计算式即可)。
(1)基态P原子的核外电子排布式为
(2)磷的一种同素异形体——白磷(P4)的立体构型为
(3)两种三角锥形气态氢化物膦(PH3)和氨(NH3)的键角分别为93.6º和107º,试分析PH3的键角小于NH3的原因

(4)常温下PCl5是一种白色晶体,其立方晶系晶体结构模型如上左图所示,由A、B两种微粒构成。将其加热至148℃熔化,形成一种能导电的熔体。已知A、B两种微粒分别与CCl4、SF6互为等电子体,则A为
(5)磷化硼(BP)是一种超硬耐磨涂层材料,上右图为其立方晶胞,其中的每个原子均满足8电子稳定结构,试判断其熔点
已知其B—P键长均为x cm,则其密度为
更新时间:2017-02-23 10:28:35
|
相似题推荐
解答题-结构与性质
|
适中
(0.65)
【推荐1】原子序数小于36 的X、Y、Z、W 四种元素,其中X 形成的单质是最轻的物质,Y 原子基态时最外层电子数是其内层电子数的2 倍,Z 原子基态时2p 原子轨道上有3 个未成对的电子,W 的原子序数为29回答下列问题:
(1)Y2X2中Y 原子的杂化类型为______ ,1mol Y2X2含有 键的数目为
键的数目为 ______ 。
(2)Y 的一种氧化物与Z 的一种氧化物互为等电子体,Z 的这种氧化物分子式是______ 。
(3)标准状况2.24L Z 的简单氢化物溶于Z 的最高价氧化物的水化物稀溶液,放热Q kJ,该反应的热化学方程式为______ 。
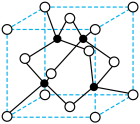
(4)元素W 的一种氯化物晶体的晶胞结构如图所示,该氯化物的化学式是______ ,氯化物晶体溶于足量Z 的最高价氧化物的水化物的浓溶液反应的离子方程式为 ______ 。
(1)Y2X2中Y 原子的杂化类型为
 键的数目为
键的数目为 (2)Y 的一种氧化物与Z 的一种氧化物互为等电子体,Z 的这种氧化物分子式是
(3)标准状况2.24L Z 的简单氢化物溶于Z 的最高价氧化物的水化物稀溶液,放热Q kJ,该反应的热化学方程式为
(4)元素W 的一种氯化物晶体的晶胞结构如图所示,该氯化物的化学式是

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】近日,我国研究人员利用硫氰酸甲基铵{[CH3NH3]+[SCN]-}气相辅助生长技术,成功制得稳定的钙钛矿型甲脒铅碘(FAPbI3)。请回答下列问题:
(1)基态S原子的价电子排布图为_______ 。
(2)硫氰酸根离子(SCN-)的结构式为_______ 。
(3)甲脒(FA)的结构简式为
①其组成元素的电负性由小到大的排序为_______ ,其中碳原子的杂化方式为_______ 。
②甲脒比丙烷的熔点更高的原因是_______ 。
(4)水中铅测定方法是用双硫腙与铅反应生成红色双硫腙铅络合物(图1)

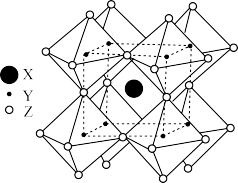
图1 图2
①该络合物可溶于四氯化碳,其晶体类型为_______ 。
②该络合物分子内不存在的微粒间作用力有_______ 。(选填序号)
a.σ键b.π键c.非极性键d.配位键e.离子键
(5)FAPbI3的晶体结构单元如图2所示,图中Y表示Pb,位于八面体中心,则甲脒的碘配位数为___ 。
(1)基态S原子的价电子排布图为
(2)硫氰酸根离子(SCN-)的结构式为
(3)甲脒(FA)的结构简式为

①其组成元素的电负性由小到大的排序为
②甲脒比丙烷的熔点更高的原因是
(4)水中铅测定方法是用双硫腙与铅反应生成红色双硫腙铅络合物(图1)


图1 图2
①该络合物可溶于四氯化碳,其晶体类型为
②该络合物分子内不存在的微粒间作用力有
a.σ键b.π键c.非极性键d.配位键e.离子键
(5)FAPbI3的晶体结构单元如图2所示,图中Y表示Pb,位于八面体中心,则甲脒的碘配位数为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐3】完成下列问题。
(1)硼元素原子核外电子排布式_______ 。溴离子的最外层轨道式是_______ 。氮原子的核外电子中,未成对电子数与成对电子数之比为_______ 。
(2)下列能说明氯的非金属性强于溴的事实是_______ (选填编号)。
a.HClO酸性强于HBrO
b.HBr的分解温度低于HCl
c.向溴化亚铁溶液中滴入少量氯水,溶液颜色变黄
d.BrCl+H2O→HBrO+HCl是非氧化还原反应
(3)写出氢氧化铝在酸性溶液中的电离方程式_______ 。
(4)已知SiF4的沸点为-65℃,则SiCl4的沸点_______ (填“高”或“低”)于-65℃,其原因是:_______ 。
(5)一银制摆件因日久在表面生成硫化银而变黑,使银器复原的一种方法是利用原电池原理:在一铝锅中盛水,将该银器浸入,并与锅底接触,放置一段时间,黑色褪去。构成原电池负极的材料是_______ 。操作后可闻盐水微有臭味,估计具有臭味的物质是_______ 。
(1)硼元素原子核外电子排布式
(2)下列能说明氯的非金属性强于溴的事实是
a.HClO酸性强于HBrO
b.HBr的分解温度低于HCl
c.向溴化亚铁溶液中滴入少量氯水,溶液颜色变黄
d.BrCl+H2O→HBrO+HCl是非氧化还原反应
(3)写出氢氧化铝在酸性溶液中的电离方程式
(4)已知SiF4的沸点为-65℃,则SiCl4的沸点
(5)一银制摆件因日久在表面生成硫化银而变黑,使银器复原的一种方法是利用原电池原理:在一铝锅中盛水,将该银器浸入,并与锅底接触,放置一段时间,黑色褪去。构成原电池负极的材料是
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】合成氨是人类科学技术上的一项重大突破,是化学和技术对社会发展与进步的巨大贡献之一。在制取合成氨原料气的过程中,常混有一些杂质,如CO会使催化剂中毒。除去CO的化学反应方程式(HAc表示醋酸): Cu(NH3)2Ac+CO+NH3==Cu(NH3)3 (CO) Ac。
请回答下列问题:
(1)C、N、O的第一电离能由大到小的顺序为________ 。
(2)配合物Cu(NH3)3 (CO) Ac中心原子的配位数为________ ,基态铜原子核外电子排布式为_________________ 。
(3)写出与CO互为等电子体的粒子________ (任写一个) 。
(4)在一定条件下NH3与CO2能合成化肥尿素[CO(NH2)2],尿素中,C原子轨道的杂化类型为________ ;1 mol尿素分子中,σ键的个数为____________ 。(设NA为阿伏伽德罗常数的值)
(5)铜金合金形成的晶胞如图所示,其中Cu、Au原子个数比为________ 。铜单质晶胞与铜金合金的晶胞相似,晶胞边长为3.61×10-8cm,则铜的密度为________ g/cm-3(结果保留3位有效数字)。

请回答下列问题:
(1)C、N、O的第一电离能由大到小的顺序为
(2)配合物Cu(NH3)3 (CO) Ac中心原子的配位数为
(3)写出与CO互为等电子体的粒子
(4)在一定条件下NH3与CO2能合成化肥尿素[CO(NH2)2],尿素中,C原子轨道的杂化类型为
(5)铜金合金形成的晶胞如图所示,其中Cu、Au原子个数比为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐2】化合物A(H3BNH3)是一种潜在的储氢材料,可由六元环状物质(HB=NH)3,其结构简式如下: ,通过反应3CH4+2(HB=NH)3+6H2O→3CO2+6H3BNH3制得。A在一定条件下通过多步去氢可最终转化为氮化硼(BN)。请回答:
,通过反应3CH4+2(HB=NH)3+6H2O→3CO2+6H3BNH3制得。A在一定条件下通过多步去氢可最终转化为氮化硼(BN)。请回答:
(1)与(HB=NH)3互为等电子体的分子为___________ (填分子式)。
(2)氮化硼(BN)有多种晶型,其中立方氮化硼与金刚石的构型类似,则其晶胞中共有___________ 个硼原子,___________ 个氮原子。
(3)人工可以合成硼的一系列氢化物,其物理性质与烷烃相似,故称之为硼烷。工业上采用LiAlH4和BF3,在乙醚介质中反应制得乙硼烷(B2H6) ,同时生成另外两种产物,该反应的化学方程式为___________ 。
(4)相关化学键的键能如下表所示,简要分析和解释下列事实。
自然界中不存在硼单质,硼氢化物也很少,主要是含氧化物,其原因为___________ 。
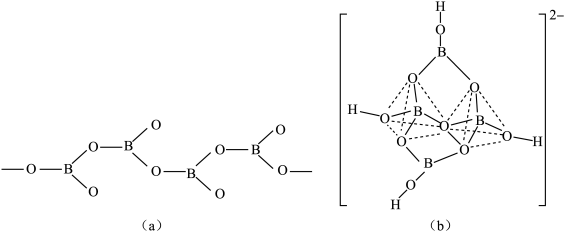
(5)在硼酸盐中,阴离子有链状、环状、骨架状等多种结构形式,图(a)为一种无限长单链状结构的多硼酸根,其化学式为___________ ;图(b)为硼砂晶体中的阴离子,其中硼原子采取的杂化类型___________ 。
 ,通过反应3CH4+2(HB=NH)3+6H2O→3CO2+6H3BNH3制得。A在一定条件下通过多步去氢可最终转化为氮化硼(BN)。请回答:
,通过反应3CH4+2(HB=NH)3+6H2O→3CO2+6H3BNH3制得。A在一定条件下通过多步去氢可最终转化为氮化硼(BN)。请回答:(1)与(HB=NH)3互为等电子体的分子为
(2)氮化硼(BN)有多种晶型,其中立方氮化硼与金刚石的构型类似,则其晶胞中共有
(3)人工可以合成硼的一系列氢化物,其物理性质与烷烃相似,故称之为硼烷。工业上采用LiAlH4和BF3,在乙醚介质中反应制得乙硼烷(B2H6) ,同时生成另外两种产物,该反应的化学方程式为
(4)相关化学键的键能如下表所示,简要分析和解释下列事实。
| 化学键 | B-H | B-O | B-B |
| 键能(KJ·mol-1) | 389 | 561 | 293 |
自然界中不存在硼单质,硼氢化物也很少,主要是含氧化物,其原因为
(5)在硼酸盐中,阴离子有链状、环状、骨架状等多种结构形式,图(a)为一种无限长单链状结构的多硼酸根,其化学式为

您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】原子序数小于36的X、Y、Z、W四种元素,其中X是周期表中原子半径最小的元素,Y原子基态时最外层电子数是其内层电子总数的2倍,Z原子基态时2p原子轨道上有3个未成对的电子,W的原子序数为28。回答下列问题:
(1)化合物ZX3与化合物YX4的VSPER构型相同,均为正四面体,其分子中化学键的键角较大的是____ (用分子式表示,下同),原因是______________________________ 。
(2)与Z同主族且上下相邻的三种非金属元素与X可形成结构相似的三种物质,试推测三者的稳定性由大到小的顺序________________ ,理由是___________________ ;三者的沸点由高到低的顺序是________ ,解释原因_____________________________ 。
(3)1mol Y2X2 含有σ键的数目为________ 。
(4)元素Y的一种氧化物与元素Z的一种氧化物互为等电子体,元素Z的这种氧化物的分子式是___________ 。
(5)W元素在周期表的位置是_________。
(1)化合物ZX3与化合物YX4的VSPER构型相同,均为正四面体,其分子中化学键的键角较大的是
(2)与Z同主族且上下相邻的三种非金属元素与X可形成结构相似的三种物质,试推测三者的稳定性由大到小的顺序
(3)1mol Y2X2 含有σ键的数目为
(4)元素Y的一种氧化物与元素Z的一种氧化物互为等电子体,元素Z的这种氧化物的分子式是
(5)W元素在周期表的位置是_________。
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
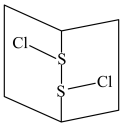
【推荐1】 具有易液化、含氢密度高、应用广泛等优点,
具有易液化、含氢密度高、应用广泛等优点, 的合成及应用一直是科学研究的重要课题。
的合成及应用一直是科学研究的重要课题。
(1)以 、
、 合成
合成 ,Fe是常用的催化剂。
,Fe是常用的催化剂。 遇酸能转化成铵盐。
遇酸能转化成铵盐。
① 中N原子的杂化类型为
中N原子的杂化类型为_______ ;VSEPR模型为_______ 。
②实际生产中采用铁的氧化物 、FeO,使用前用
、FeO,使用前用 和
和 的混合气体将它们还原为具有活性的金属铁。铁的两种晶胞(所示图形为正方体)结构示意如下:
的混合气体将它们还原为具有活性的金属铁。铁的两种晶胞(所示图形为正方体)结构示意如下:

图1晶胞的棱长为a pm(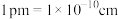 ),
), 代表阿伏加德罗常数,则其密度
代表阿伏加德罗常数,则其密度
_______  。
。
(2)原子中运动的电子有两种相反的自旋状态,若一种自旋状态用“ ”表示,与之相反的用“
”表示,与之相反的用“ ”表示,称为电子的自旋磁量子数。对于基态的氮原子,其价电子自旋磁量子数的代数和为
”表示,称为电子的自旋磁量子数。对于基态的氮原子,其价电子自旋磁量子数的代数和为_______ 。
(3)铁触媒是普遍使用的以铁为主体的多成分催化剂,通常还含有 、
、 、CaO、MgO、
、CaO、MgO、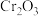 等氧化物中的几种。
等氧化物中的几种。
①第四周期ds区元素中,与基态Cr原子最外层电子数目相同的元素的元素符号为_______ 。
②上述氧化物所涉及的元素中,处于元素周期表中p区的元素有_______ (填元素符号)
(4)我国科研人员研制出了M-LiH(M为Fe、Mn等金属)等催化剂,使得合成氨工业的温度,压强分别降到了350℃、1 MPa,这是近年来合成氨反应研究中的重要突破。
①基态Mn原子未成对的电子数为_______ 。
②第三电离能
_______  (填“>”或“<”),原因是
(填“>”或“<”),原因是_______ 。
(5)常温下 是橙黄色液体,其分子结构如图所示。少量泄漏会产生窒息性气味,遇水易水解,并产生酸性悬浊液。
是橙黄色液体,其分子结构如图所示。少量泄漏会产生窒息性气味,遇水易水解,并产生酸性悬浊液。 分子是
分子是_______ 分子(填“极性”或“非极性”),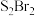 与
与 分子结构相似,熔沸点
分子结构相似,熔沸点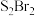
_______  (填“>”或“<”)。
(填“>”或“<”)。
 具有易液化、含氢密度高、应用广泛等优点,
具有易液化、含氢密度高、应用广泛等优点, 的合成及应用一直是科学研究的重要课题。
的合成及应用一直是科学研究的重要课题。(1)以
 、
、 合成
合成 ,Fe是常用的催化剂。
,Fe是常用的催化剂。 遇酸能转化成铵盐。
遇酸能转化成铵盐。①
 中N原子的杂化类型为
中N原子的杂化类型为②实际生产中采用铁的氧化物
 、FeO,使用前用
、FeO,使用前用 和
和 的混合气体将它们还原为具有活性的金属铁。铁的两种晶胞(所示图形为正方体)结构示意如下:
的混合气体将它们还原为具有活性的金属铁。铁的两种晶胞(所示图形为正方体)结构示意如下:
图1晶胞的棱长为a pm(
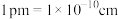 ),
), 代表阿伏加德罗常数,则其密度
代表阿伏加德罗常数,则其密度
 。
。(2)原子中运动的电子有两种相反的自旋状态,若一种自旋状态用“
 ”表示,与之相反的用“
”表示,与之相反的用“ ”表示,称为电子的自旋磁量子数。对于基态的氮原子,其价电子自旋磁量子数的代数和为
”表示,称为电子的自旋磁量子数。对于基态的氮原子,其价电子自旋磁量子数的代数和为(3)铁触媒是普遍使用的以铁为主体的多成分催化剂,通常还含有
 、
、 、CaO、MgO、
、CaO、MgO、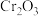 等氧化物中的几种。
等氧化物中的几种。①第四周期ds区元素中,与基态Cr原子最外层电子数目相同的元素的元素符号为
②上述氧化物所涉及的元素中,处于元素周期表中p区的元素有
(4)我国科研人员研制出了M-LiH(M为Fe、Mn等金属)等催化剂,使得合成氨工业的温度,压强分别降到了350℃、1 MPa,这是近年来合成氨反应研究中的重要突破。
①基态Mn原子未成对的电子数为
②第三电离能

 (填“>”或“<”),原因是
(填“>”或“<”),原因是(5)常温下
 是橙黄色液体,其分子结构如图所示。少量泄漏会产生窒息性气味,遇水易水解,并产生酸性悬浊液。
是橙黄色液体,其分子结构如图所示。少量泄漏会产生窒息性气味,遇水易水解,并产生酸性悬浊液。 分子是
分子是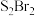 与
与 分子结构相似,熔沸点
分子结构相似,熔沸点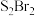
 (填“>”或“<”)。
(填“>”或“<”)。
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】研究发现,在CO2低压合成甲醇反应(CO2+3H2=CH3OH+H2O)中,Co氧化物负载的Mn氧化物纳米粒子催化剂具有高活性,显示出良好的应用前景。回答下列问题∶
(1)Co基态原子核外价层电子排布式为___________ ,其原子核外未成对电子数是___________ 个。元素Co与Mn相比,第一电离能较大的是___________ 。
(2)在CO2低压合成甲醇反应所涉及的三种无机物中,沸点从高到低的顺序为___________ ,原因是___________ 。
(3)CO2和CH3OH分子中C原子的杂化形式分别为___________ 和___________ 。
(4)硝酸锰是制备上述反应催化剂的原料,Mn(NO3)2中的化学键除了σ键外,还存在___________ 键。
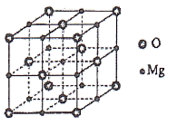
(5)MgO具有NaCl型结构(如下图),其中阴离子采用面心立方最密堆积方式,则一个晶胞中Mg2+的个数是___________ 个。若MgO晶胞参数为a nm, 则晶体密度为___________ g·cm-3(列出计算式)
(1)Co基态原子核外价层电子排布式为
(2)在CO2低压合成甲醇反应所涉及的三种无机物中,沸点从高到低的顺序为
(3)CO2和CH3OH分子中C原子的杂化形式分别为
(4)硝酸锰是制备上述反应催化剂的原料,Mn(NO3)2中的化学键除了σ键外,还存在
(5)MgO具有NaCl型结构(如下图),其中阴离子采用面心立方最密堆积方式,则一个晶胞中Mg2+的个数是

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】完成下列问题。
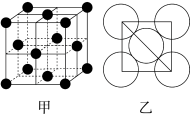
(1)金属铝的晶胞结构如图甲所示,原子之间相互位置关系的平面图如图乙所示。若已知Al的原子半径为rcm,NA代表阿伏加德罗常数的值,该晶体的密度为_______  (用含NA、r的最简式表示)。
(用含NA、r的最简式表示)。
(2)2022年北京冬季奥运会场馆建设使用了大量不锈钢材质,不锈钢属于铁碳合金,常含铬、镍等元素。
①碳的一种单质石墨是单层二维蜂窝状晶格结构的新材料(如图1),其中碳原子采取_______ 杂化,在层中每个碳原子周围等距且紧邻的碳原子个数为_______ 。

②铁合金用途广泛,某种铁镁合金储氢效率很高,其晶胞如图2所示。晶体中每个镁原子周围等距且紧邻的镁原子有_______ 个,该铁镁合金中原子个数比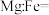
_______ ;原子坐标参数可以表示晶胞内部各原子的相对位置,其中原子坐标参数A为(0,0,0),C为( ,
, ,0),B点坐标参数为
,0),B点坐标参数为_______ 。

(1)金属铝的晶胞结构如图甲所示,原子之间相互位置关系的平面图如图乙所示。若已知Al的原子半径为rcm,NA代表阿伏加德罗常数的值,该晶体的密度为
 (用含NA、r的最简式表示)。
(用含NA、r的最简式表示)。
(2)2022年北京冬季奥运会场馆建设使用了大量不锈钢材质,不锈钢属于铁碳合金,常含铬、镍等元素。
①碳的一种单质石墨是单层二维蜂窝状晶格结构的新材料(如图1),其中碳原子采取

②铁合金用途广泛,某种铁镁合金储氢效率很高,其晶胞如图2所示。晶体中每个镁原子周围等距且紧邻的镁原子有
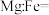
 ,
, ,0),B点坐标参数为
,0),B点坐标参数为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐1】元素X、Y、Z为前四周期元素,X的基态原子核外电子有21种运动状态,元素Y的原子最外层电子数是其内层的3倍,Z与X、Y不在同一周期,且Z原子核外p电子比s电子多5个。
(1)X基态原子的核外电子排布式为_______ ,Y的原子结构示意图_______ 。
(2)X是石油化工中重要的催化剂之一,如催化异丙苯( )裂化生成苯和丙烯。
)裂化生成苯和丙烯。
① 1 mol苯分子中含有σ 键的数目为_______ mol。
② 异丙苯分子中碳原子轨道的杂化类型为_______ 。
(3)Y的氢化物沸点高于同族氢化物沸点的原因_______ 。
(4)XZ3易溶于水,熔点为960 ℃,熔融状态下能够导电,据此可判断XY3晶体属于_______ (填晶体类型)。
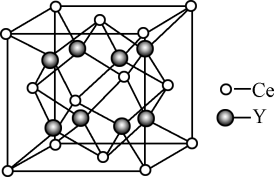
(5)元素Ce与X同族,其与Y形成的化合物晶体的晶胞结构如下图,该化合物的化学式为_______ 。
(1)X基态原子的核外电子排布式为
(2)X是石油化工中重要的催化剂之一,如催化异丙苯(
 )裂化生成苯和丙烯。
)裂化生成苯和丙烯。① 1 mol苯分子中含有σ 键的数目为
② 异丙苯分子中碳原子轨道的杂化类型为
(3)Y的氢化物沸点高于同族氢化物沸点的原因
(4)XZ3易溶于水,熔点为960 ℃,熔融状态下能够导电,据此可判断XY3晶体属于
(5)元素Ce与X同族,其与Y形成的化合物晶体的晶胞结构如下图,该化合物的化学式为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】翡翠的主要成分为NaAlSi2O6,还含有其他多种金属阳离子,其中Cr3+的含量决定其绿色的深浅,是决定翡翠品质的重要因素之一。
(1)基态Cr3+最外电子层的电子排布图(轨道表示式)为___________ 。
(2)下列状态的铝中,电离最外层一个电子所需能量最大的是___________ ,最小的是___________ (填标号)。
A. B.
B.  C.
C.  D.
D. 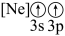
(3)配合物K[Cr(C2O4)(H2O)]中的配体是___________ ,H2O的沸点比CO2的高了许多,主要原因是___________ 。
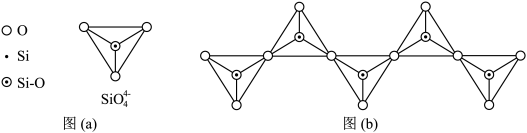
(4)在翡翠等硅酸盐中, 四面体(如下图(a))通过共用顶角氧离子可形成岛状、链状、层状、骨架网状四大类结构型式。图(b)为一种无限长单链结构的多硅酸根,其中Si原子的杂化形式为
四面体(如下图(a))通过共用顶角氧离子可形成岛状、链状、层状、骨架网状四大类结构型式。图(b)为一种无限长单链结构的多硅酸根,其中Si原子的杂化形式为___________ ,其化学式为___________ 。低温石英中也存在有顶角相连的硅氧四面体形成螺旋上升的长链,没有封闭的环状结构,这一结构决定了它具有___________ 。
(5)在金属材料中添加AlCr2颗粒,可以增强材料的耐腐蚀性、硬度和机械性能。AlCr2具有体心四方结构,如图所示,处于顶角位置的是___________ 原子。设Cr和Al原子半径分别为rCr和rAl,则金属原子空间占有率为___________ % (列出计算表达式)。

(1)基态Cr3+最外电子层的电子排布图(轨道表示式)为
(2)下列状态的铝中,电离最外层一个电子所需能量最大的是
A.
 B.
B.  C.
C.  D.
D. 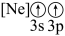
(3)配合物K[Cr(C2O4)(H2O)]中的配体是
(4)在翡翠等硅酸盐中,
 四面体(如下图(a))通过共用顶角氧离子可形成岛状、链状、层状、骨架网状四大类结构型式。图(b)为一种无限长单链结构的多硅酸根,其中Si原子的杂化形式为
四面体(如下图(a))通过共用顶角氧离子可形成岛状、链状、层状、骨架网状四大类结构型式。图(b)为一种无限长单链结构的多硅酸根,其中Si原子的杂化形式为
(5)在金属材料中添加AlCr2颗粒,可以增强材料的耐腐蚀性、硬度和机械性能。AlCr2具有体心四方结构,如图所示,处于顶角位置的是

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】单晶边缘纳米催化剂技术为工业上有效利用二氧化碳提供了一条经济可行的途径,其中单晶氧化镁负载镍催化剂表现出优异的抗积碳和抗烧结性能。回答问题:
(1)基态镍原子d轨道中成对电子与单电子的数目比为___________ ,下列现象与原子核外电子跃迁有关的是___________ (填序号)
a.焰火 b.LED灯光 c.金属导电
(2)第二周期元素的第一电离能(I1)随原子序数(Z)的变化如图1所示。I1随Z的递增而呈增大趋势的原因是___________ ,导致I1在a点出现齿峰的原因是___________ 。
(3)丁二酮肟常用于检验Ni2+,在稀氨水介质中,丁二酮肟与Ni2+反应生成鲜红色沉淀的结构如图2所示,该结构中N原子的杂化轨道类型为___________ ,N原子与其它原子之间存在的作用力有___________ (填序号)
a.氢键 b.π键 c.σ键 d.配位键
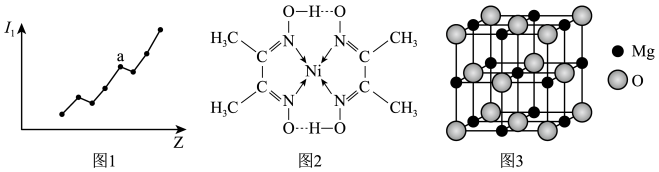
(4)MgO具有NaCl型结构(如图3),其中阴离子采用面心立方最密堆积方式,X射线衍射实验测得MgO的晶胞边长为a nm,则MgO晶体的密度为___________ g/cm3 (设NA为阿伏加德罗常数的值)。
(1)基态镍原子d轨道中成对电子与单电子的数目比为
a.焰火 b.LED灯光 c.金属导电
(2)第二周期元素的第一电离能(I1)随原子序数(Z)的变化如图1所示。I1随Z的递增而呈增大趋势的原因是
(3)丁二酮肟常用于检验Ni2+,在稀氨水介质中,丁二酮肟与Ni2+反应生成鲜红色沉淀的结构如图2所示,该结构中N原子的杂化轨道类型为
a.氢键 b.π键 c.σ键 d.配位键

(4)MgO具有NaCl型结构(如图3),其中阴离子采用面心立方最密堆积方式,X射线衍射实验测得MgO的晶胞边长为a nm,则MgO晶体的密度为
您最近一年使用:0次



