硒是典型的半导体材料。
(1)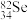 是硒的一种放射性同位素,其中子数与价电子数之差为
是硒的一种放射性同位素,其中子数与价电子数之差为___________ , 、
、 、
、 其沸点从大到小的顺序是
其沸点从大到小的顺序是___________ 。
(2) 是一种无色液体,其分子空间构型是
是一种无色液体,其分子空间构型是___________ (填标号)。
a.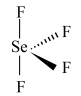 b.
b.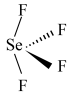 c.
c. d.
d. e.
e.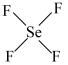
 与
与 结构相似,其键角较大的是
结构相似,其键角较大的是___________ 。
(3)锂硒电池正极的充放电原理为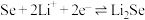
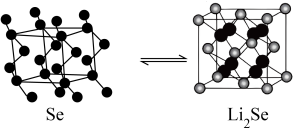
硒晶胞中含有___________ 个 原子,若
原子,若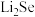 晶胞参数边长为
晶胞参数边长为 ,在
,在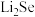 晶胞中2个
晶胞中2个 、
、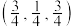 间距离是
间距离是___________  ,
, 填充在
填充在 的
的___________ 型空隙中,充电过程正极材料体积___________ (填“膨胀”、“不变”或“收缩”)
(4) 与
与 可形成直线型阴离子(结构如下),其中
可形成直线型阴离子(结构如下),其中
___________ 。

(1)
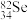 是硒的一种放射性同位素,其中子数与价电子数之差为
是硒的一种放射性同位素,其中子数与价电子数之差为 、
、 、
、 其沸点从大到小的顺序是
其沸点从大到小的顺序是(2)
 是一种无色液体,其分子空间构型是
是一种无色液体,其分子空间构型是a.
 b.
b. c.
c. d.
d. e.
e.
 与
与 结构相似,其键角较大的是
结构相似,其键角较大的是(3)锂硒电池正极的充放电原理为
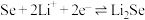

硒晶胞中含有
 原子,若
原子,若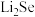 晶胞参数边长为
晶胞参数边长为 ,在
,在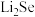 晶胞中2个
晶胞中2个 、
、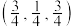 间距离是
间距离是 ,
, 填充在
填充在 的
的(4)
 与
与 可形成直线型阴离子(结构如下),其中
可形成直线型阴离子(结构如下),其中

更新时间:2024-01-17 19:23:21
|
相似题推荐
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】X是合成碳酸二苯酯的一种有效的氧化还原催化助剂,可由EDTA与Fe3+反应得到。

(1)EDTA中碳原子杂化轨道类型为______ ;EDTA中四种元素的电负性由小到大的顺序为________ 。
(2)Fe3+基态外围电子排布式为______ 。
(3)EDTA与正二十一烷的相对分子质量非常接近,但EDTA的沸点(540.6 ℃)比正二十一烷的沸点(100 ℃)高的原因是______ 。
(4)1 mol 碳酸分子中含有σ键的数目为______ 。
(5)X中的配位原子是______ 。

(1)EDTA中碳原子杂化轨道类型为
(2)Fe3+基态外围电子排布式为
(3)EDTA与正二十一烷的相对分子质量非常接近,但EDTA的沸点(540.6 ℃)比正二十一烷的沸点(100 ℃)高的原因是
(4)1 mol 碳酸分子中含有σ键的数目为
(5)X中的配位原子是
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】铬及其化合物用途广泛。回答下列问题:
(1)基态Cr原子有___ 个未成对电子。
(2)重铬酸铵[(NH4)2Cr2O7]为桔黄色单斜结晶,常用作有机合成催化剂,Cr2O 的结构如图。1mol该物质中含σ键的数目为
的结构如图。1mol该物质中含σ键的数目为__ NA。
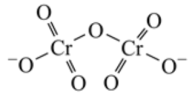
(3)铬能形成多种配合物。
①配合物a、b、c的化学式如下:
a.[Cr(H2O)4Cl2]Cl·2H2O b.[Cr(H2O)5Cl]Cl2·H2O c.[Cr(H2O)6]Cl3
相同物质的量的a、b、c分别与足量AgNO3溶液反应,生成AgCl的物质的量之比为___ 。
②Reineckesalt的结构如图所示:其中配位原子为___ (填元素符号);阳离子的空间结构为__ ,NCS-中碳原子杂化方式为__ 。
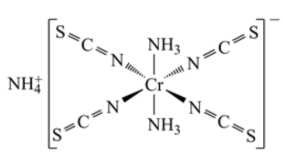
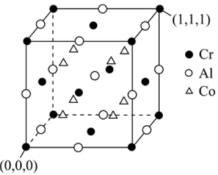
(4)一种半金属磁体的结构如图所示。距离每个Cr最近的Al有___ 个,距离Cr(0,0,0)的Co的原子坐标为___ 。
(1)基态Cr原子有
(2)重铬酸铵[(NH4)2Cr2O7]为桔黄色单斜结晶,常用作有机合成催化剂,Cr2O
 的结构如图。1mol该物质中含σ键的数目为
的结构如图。1mol该物质中含σ键的数目为
(3)铬能形成多种配合物。
①配合物a、b、c的化学式如下:
a.[Cr(H2O)4Cl2]Cl·2H2O b.[Cr(H2O)5Cl]Cl2·H2O c.[Cr(H2O)6]Cl3
相同物质的量的a、b、c分别与足量AgNO3溶液反应,生成AgCl的物质的量之比为
②Reineckesalt的结构如图所示:其中配位原子为

(4)一种半金属磁体的结构如图所示。距离每个Cr最近的Al有

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】B、N、Co均为新型材料的重要组成元素。请回答下列问题:
(1)基态Co原子核外电子占据________ 种不同的能级,其中有________ 个未成对电子。
(2)Co能形成[Co(CNO)6]3-。
①1mol该离子中含有σ键的数目为________ 。
②C、N、O三种基态原子的第一电离能由大到小的顺序为________ (用元素符号表示)。
③在相同的压强下,CO晶体的熔点高于N2晶体的原因为_______________________ 。
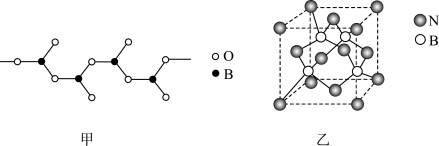
(3)BN晶体有多种结构,其中立方氮化硼具有金刚石型结构(如图乙)。
①晶体的最小环中含有________ 个B原子。
②若晶胞参数为anm,晶胞密度为ρg·cm-3,则阿伏加 德罗常数的值可表示为________ 。
(1)基态Co原子核外电子占据
(2)Co能形成[Co(CNO)6]3-。
①1mol该离子中含有σ键的数目为
②C、N、O三种基态原子的第一电离能由大到小的顺序为
③在相同的压强下,CO晶体的熔点高于N2晶体的原因为

(3)BN晶体有多种结构,其中立方氮化硼具有金刚石型结构(如图乙)。
①晶体的最小环中含有
②若晶胞参数为anm,晶胞密度为ρg·cm-3,则阿伏加 德罗常数的值可表示为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐1】深入认识物质的结构有助于进一步开发物质的用途。
(1) 的空间构型为
的空间构型为_______ 中心原子S的杂化方式为_______ 。
(2)从结构的角度解释: MgCO3 热分解温度低于CaCO3热分解温度的原因是_______ 。
(3)某些金属或金属化合物焰色反应能产生特殊的焰色。下列对其原理的分析中,正确的是_______(填序号)。
(4)氟代硼铍酸钾(含K、B、Be、O、F元素)晶体是唯一可直接倍频产生深紫外激光的非线性光学晶体。氟硼酸钾是制备氟代硼铍酸钾的原料之一,高温下分解为KF和BF3,氟硼酸钾晶体中所含的化学键有_______ (填序号)。
a.离子键 b. 非极性键 c.极性键 d.配位键 e.金属键
(5)BeO晶体也是制备氟代硼铍酸钾的原料,下图为其晶胞结构示意图。

①沿着晶胞体对角线方向的投影,下列图中能正确描述投影结果的是_______ (填序号)

②设O与Be的最近距离为a cm, NA表示阿伏加德罗常数的值,则BeO晶体的密度为_______ g∙cm-3。
(1)
 的空间构型为
的空间构型为(2)从结构的角度解释: MgCO3 热分解温度低于CaCO3热分解温度的原因是
(3)某些金属或金属化合物焰色反应能产生特殊的焰色。下列对其原理的分析中,正确的是_______(填序号)。
| A.电子从基态跃起到较高的激发态 | B.电子从较高的激发态跃迁到基态 |
| C.焰色反应的光谱属吸收光谱 | D.焰色反应的光谱属于发射光谱 |
a.离子键 b. 非极性键 c.极性键 d.配位键 e.金属键
(5)BeO晶体也是制备氟代硼铍酸钾的原料,下图为其晶胞结构示意图。

①沿着晶胞体对角线方向的投影,下列图中能正确描述投影结果的是

②设O与Be的最近距离为a cm, NA表示阿伏加德罗常数的值,则BeO晶体的密度为
您最近一年使用:0次
【推荐2】铜、银、金在元素周期表中属于同一族元素,应用很广。
(1)我国秦俑彩绘和汉代器物上用的颜料被称为“中国蓝”,其成分为BaCuSi4O10。写出该物质中基态铜离子的价电子排布式______
(2)铜可形成多种配合物,如[Cu(NH3)4]SO4、K2[Cu(CN)3]等。配离子Cu(CN) 中σ键和π键的个数比为
中σ键和π键的个数比为___ ,中心离子Cu+的杂化类型是sp2,该配离子的空间构型为___ ;CN-中配位原子是_____ (填名称),原因是___ 。
(3)金性质稳定,常用作饰品,但金可以被王水溶解,其方程式为Au+HNO3+4HCl=H[AuCl4]+NO↑+2H2O,该反应中形成的化学键有___________ 。
a.金属键 b.离子键 c.配位键 d.极性键 e.非极性键 f.氢键
(4)由Cs、Au、Cl三种元素组成的化合物其晶胞如下图。小球为Cl,面上大球为Cs,其余球为Au。


该化合物中金原子有2种不同的化学环境,形成2种不同的配合阴离子,它们分别是[AuCl4]-和___________ ,该化合物的化学式为___________ 。
(5)某种铜银合金晶体具有储氢功能,它是面心立方最密堆积结构,Cu原子位于面心,Ag原子位于顶点,H原子可进入由Cu原子和Ag原子构成的四面体空隙中。若晶胞参数为anm,阿伏加德罗常数为NA,写出储氢后晶体密度的计算式___________ g·cm-3(不需要计算出结果)。
(1)我国秦俑彩绘和汉代器物上用的颜料被称为“中国蓝”,其成分为BaCuSi4O10。写出该物质中基态铜离子的价电子排布式
(2)铜可形成多种配合物,如[Cu(NH3)4]SO4、K2[Cu(CN)3]等。配离子Cu(CN)
 中σ键和π键的个数比为
中σ键和π键的个数比为(3)金性质稳定,常用作饰品,但金可以被王水溶解,其方程式为Au+HNO3+4HCl=H[AuCl4]+NO↑+2H2O,该反应中形成的化学键有
a.金属键 b.离子键 c.配位键 d.极性键 e.非极性键 f.氢键
(4)由Cs、Au、Cl三种元素组成的化合物其晶胞如下图。小球为Cl,面上大球为Cs,其余球为Au。


该化合物中金原子有2种不同的化学环境,形成2种不同的配合阴离子,它们分别是[AuCl4]-和
(5)某种铜银合金晶体具有储氢功能,它是面心立方最密堆积结构,Cu原子位于面心,Ag原子位于顶点,H原子可进入由Cu原子和Ag原子构成的四面体空隙中。若晶胞参数为anm,阿伏加德罗常数为NA,写出储氢后晶体密度的计算式
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】分铜液净化渣主要含铜、碲(Te)、锑(Sb)、砷(As)等元素的化合物,一种回收工艺流程如图所示:

已知:①“碱浸”时,铜、锑转化为难溶氢氧化物或氧化物,碱浸液含有Na2TeO3、Na3AsO4。
②“酸浸”时,锑元素反应生成难溶的Sb2O(SO4)4浸渣。
回答下列问题:
(1)碲(Te)元素位于元素周期表第_____ 周期_____ 族;SbCl3的VSEPR模型名称为_____ 。
(2)“碱浸”时,加快碱浸的措施有_____ (写两种)。
(3)向碱浸液加入盐酸调节pH=4,得到的滤液中As元素最主要的存在形式为_____ (常温下,H3AsO4的各级电离常数为Ka1=6.3×10-3、Ka2=1.0×10-7、Ka3=3.2×10-12)。
(4)“氯盐酸浸”时,SO2的作用_____ 。
(5)SbCl3“水解”生成SbOCl的化学方程式为_____ ;实验室配制SbCl3溶液的方法是_____ 。

已知:①“碱浸”时,铜、锑转化为难溶氢氧化物或氧化物,碱浸液含有Na2TeO3、Na3AsO4。
②“酸浸”时,锑元素反应生成难溶的Sb2O(SO4)4浸渣。
回答下列问题:
(1)碲(Te)元素位于元素周期表第
(2)“碱浸”时,加快碱浸的措施有
(3)向碱浸液加入盐酸调节pH=4,得到的滤液中As元素最主要的存在形式为
| A.H3AsO4 | B. | C. | D. |
(5)SbCl3“水解”生成SbOCl的化学方程式为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐1】I.CP是一种起爆药,化学式为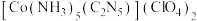 ,CP可由5-氰基四唑(结构简式如下图所示)和
,CP可由5-氰基四唑(结构简式如下图所示)和 反应制备。
反应制备。

(1)Co原子基态电子排布式为___________ ,C、N、O元素的第一电离能由大到小的顺序为___________ 。
(2)5-氰基四唑分子中C原子的杂化类型为___________ ;1 mol 5-氰基四唑分子中含有σ键的数目为___________ 。
(3)在 配合物中
配合物中
①Co3+的配体为___________ (填分子式)。
② 空间构型
空间构型___________ 。
Ⅱ.偏钛酸钡在小型变压器,话筒和扩音器中均有应用,其晶胞结构如图所示,
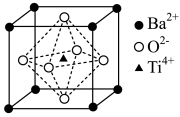
(4)偏钛酸钡的化学式为___________ 。
(5)与Ba2+最近且等距离的O2-为___________ 个。
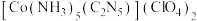 ,CP可由5-氰基四唑(结构简式如下图所示)和
,CP可由5-氰基四唑(结构简式如下图所示)和 反应制备。
反应制备。
(1)Co原子基态电子排布式为
(2)5-氰基四唑分子中C原子的杂化类型为
(3)在
 配合物中
配合物中①Co3+的配体为
②
 空间构型
空间构型Ⅱ.偏钛酸钡在小型变压器,话筒和扩音器中均有应用,其晶胞结构如图所示,

(4)偏钛酸钡的化学式为
(5)与Ba2+最近且等距离的O2-为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】回答下列问题:
(1)氮和铁能形成一种磁性材料,其晶胞如图所示,该晶胞中Fe原子的个数为___________ ,该该磁性材料的化学式为___________ 。___________ 个氯离子,阴离子与阳离子的个数比是___________ 。___________ 。 )的沸点为65℃,甲醛HCHO(
)的沸点为65℃,甲醛HCHO( )沸点为-19℃。两者的相对分子质量接近,但甲醇的沸点比甲醛高,主要原因是
)沸点为-19℃。两者的相对分子质量接近,但甲醇的沸点比甲醛高,主要原因是___________ 。
(5)NH3、CH4、HF、H2O分子中,价键的极性由强到弱的顺序是___________ 。
(6)F、Cl、Br、I、At等简称卤素,(CN)2称为“拟卤素”,在性质上与卤素相似,(CN)2里各原子均满足8电子稳定结构。写出(CN)2的电子式___________ 。
(1)氮和铁能形成一种磁性材料,其晶胞如图所示,该晶胞中Fe原子的个数为



 )的沸点为65℃,甲醛HCHO(
)的沸点为65℃,甲醛HCHO( )沸点为-19℃。两者的相对分子质量接近,但甲醇的沸点比甲醛高,主要原因是
)沸点为-19℃。两者的相对分子质量接近,但甲醇的沸点比甲醛高,主要原因是(5)NH3、CH4、HF、H2O分子中,价键的极性由强到弱的顺序是
(6)F、Cl、Br、I、At等简称卤素,(CN)2称为“拟卤素”,在性质上与卤素相似,(CN)2里各原子均满足8电子稳定结构。写出(CN)2的电子式
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐3】元素锑(Sb)位于周期表第五周期ⅤA族,科研工作者精准合成了SbxOy、SbI3•3S8等二维无机分子晶体,为潜在的分子电子设备研究创设了机会;合成了Na[Sb(PDTA)]•H2O等配合物,在冶金工业中应用广泛。
(1)基态S原子的价电子轨道表示式(排布图)为_____ 。
(2)SbI3中心原子的杂化方式为______ ;第一电离能:I1(Sb)<I1(I),原因是_____ 。
(3)SbI3•3S8双分子晶体中存在的微粒间作用力有_____ 。
A.离子键 B.π键 C.非极性共价键 D.氢键 E.范德华力
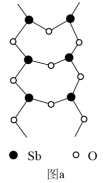
(4)SbxOy的一种双链基本结构单元如图a,则其化学式为_____ 。
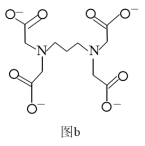
(5)PDTA的结构如图b,Na[Sb(PDTA)]•H2O中心原子的配位数为6,则配位原子是_____ 。
(1)基态S原子的价电子轨道表示式(排布图)为
(2)SbI3中心原子的杂化方式为
(3)SbI3•3S8双分子晶体中存在的微粒间作用力有
A.离子键 B.π键 C.非极性共价键 D.氢键 E.范德华力
(4)SbxOy的一种双链基本结构单元如图a,则其化学式为

(5)PDTA的结构如图b,Na[Sb(PDTA)]•H2O中心原子的配位数为6,则配位原子是

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】中科院大连化学物理研究所科学家用Ni-BaH3/Al2O3、Ni-LiH等作催化剂,实现了在常压、100~300℃的条件下合成氨,这一成果发表在《Nature Energy》杂志上。
(1)基态 的核外电子排布式为
的核外电子排布式为___________ ,若该离子核外电子空间运动状态有15种,则该离子处于___________ (填“基”或“激发”)态。
(2)氨在粮食生产、国防中有着无可替代的地位,也是重要的化工原料,可用于合成氨基酸、硝酸、TNT等。甘氨酸(NH2CH2COOH)是组成最简单的氨基酸,熔点为182℃,沸点为233℃。
①硝酸溶液中 的空间构型为
的空间构型为___________ 。
②甘氨酸的晶体类型是___________ ,其熔、沸点远高于相对分子质量几乎相等的丙酸(熔点为-21℃,沸点为141℃)的主要原因:一是甘氨酸能形成内盐;二是___________ 。
(3)比较NH3分子(前者)和在 中NH3(后者)分子中∠H-N-H的键角大小,前者
中NH3(后者)分子中∠H-N-H的键角大小,前者______ 后者。(填“>”、“<”或“=”)
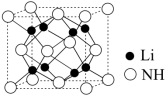
(4)亚氨基锂(Li2NH,摩尔质量为M g/mol),是一种储氢容量高、安全性能好的固体储氢材料,其晶胞结构如图所示,若晶胞参数为d pm,密度为ρ g/cm3,则阿伏加德罗常数
_______  (列出表达式)。
(列出表达式)。
(1)基态
 的核外电子排布式为
的核外电子排布式为(2)氨在粮食生产、国防中有着无可替代的地位,也是重要的化工原料,可用于合成氨基酸、硝酸、TNT等。甘氨酸(NH2CH2COOH)是组成最简单的氨基酸,熔点为182℃,沸点为233℃。
①硝酸溶液中
 的空间构型为
的空间构型为②甘氨酸的晶体类型是
(3)比较NH3分子(前者)和在
 中NH3(后者)分子中∠H-N-H的键角大小,前者
中NH3(后者)分子中∠H-N-H的键角大小,前者(4)亚氨基锂(Li2NH,摩尔质量为M g/mol),是一种储氢容量高、安全性能好的固体储氢材料,其晶胞结构如图所示,若晶胞参数为d pm,密度为ρ g/cm3,则阿伏加德罗常数

 (列出表达式)。
(列出表达式)。
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】前四周期元素A、B、C、D、E的原子序数依次增大,A元素原子的核外电子只有一种运动状态;基态B原子s能级的电子总数比p能级的多1;基态C原子和基态E原子中成对电子数均是未成对电子数的3倍;D形成简单离子的半径在同周期元素形成的简单离子中最小。回答下列问题:
(1)E的元素名称为_______ ,它位于元素周期表的_______ 区。
(2)元素A、B、C中,电负性最大的是_______ (填元素符号,下同),元素B、C、D第一电离能由大到小的顺序为_______ 。
(3)与同族其他元素X形成的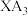 相比,
相比, 易液化的原因是
易液化的原因是_______ 。
(4) 中B原子轨道的杂化类型为
中B原子轨道的杂化类型为_______ , 离子的空间结构为
离子的空间结构为_______ 。
(5)化合物DB是人工合成的半导体材料,它的晶胞结构与金刚石(晶胞结构如图所示)相似。若DB的晶胞参数为a pm,则晶体的密度为_______  (用
(用 表示阿伏加德罗常数)。
表示阿伏加德罗常数)。

(1)E的元素名称为
(2)元素A、B、C中,电负性最大的是
(3)与同族其他元素X形成的
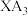 相比,
相比, 易液化的原因是
易液化的原因是(4)
 中B原子轨道的杂化类型为
中B原子轨道的杂化类型为 离子的空间结构为
离子的空间结构为(5)化合物DB是人工合成的半导体材料,它的晶胞结构与金刚石(晶胞结构如图所示)相似。若DB的晶胞参数为a pm,则晶体的密度为
 (用
(用 表示阿伏加德罗常数)。
表示阿伏加德罗常数)。
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】甲烷在镍催化作用下可与水反应制合成气(CO和H2),再制成甲醇代替燃油。
(1)CH4和H2O所含的三种元素电负性从小到大的顺序为________ 。
(2)CH4和CO2分子中碳原子的杂化类型分别是_____ 和_______ 。
(3)基态Ni原子的电子排布式为______ ,该元素位于元素周期表的第_____ 族。
(4)金属镍粉在CO气流中轻微加热,生成无色挥发性液态Ni(CO)4,该分子呈正四面体构型。则1mol Ni(CO)4 中含有____ mol σ键,Ni(CO)4的晶体类型为_____ ,Ni(CO)4易溶于下列___ (填选项字母) 中。
a.水 b.四氧化碳 C.苯 d.硫酸镍溶液
(5)如图是一种镍镧合金储氢后的晶胞结构示意图。该合金中原子个数比La:Ni=_____ ,储氢后,含1molLa的合金可吸附H2的数目为______ 。

(1)CH4和H2O所含的三种元素电负性从小到大的顺序为
(2)CH4和CO2分子中碳原子的杂化类型分别是
(3)基态Ni原子的电子排布式为
(4)金属镍粉在CO气流中轻微加热,生成无色挥发性液态Ni(CO)4,该分子呈正四面体构型。则1mol Ni(CO)4 中含有
a.水 b.四氧化碳 C.苯 d.硫酸镍溶液
(5)如图是一种镍镧合金储氢后的晶胞结构示意图。该合金中原子个数比La:Ni=

您最近一年使用:0次



