元素锑(Sb)位于周期表第五周期ⅤA族,科研工作者精准合成了SbxOy、SbI3•3S8等二维无机分子晶体,为潜在的分子电子设备研究创设了机会;合成了Na[Sb(PDTA)]•H2O等配合物,在冶金工业中应用广泛。
(1)基态S原子的价电子轨道表示式(排布图)为_____ 。
(2)SbI3中心原子的杂化方式为______ ;第一电离能:I1(Sb)<I1(I),原因是_____ 。
(3)SbI3•3S8双分子晶体中存在的微粒间作用力有_____ 。
A.离子键 B.π键 C.非极性共价键 D.氢键 E.范德华力
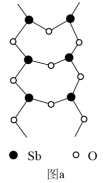
(4)SbxOy的一种双链基本结构单元如图a,则其化学式为_____ 。
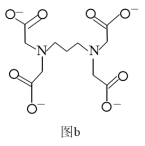
(5)PDTA的结构如图b,Na[Sb(PDTA)]•H2O中心原子的配位数为6,则配位原子是_____ 。
(1)基态S原子的价电子轨道表示式(排布图)为
(2)SbI3中心原子的杂化方式为
(3)SbI3•3S8双分子晶体中存在的微粒间作用力有
A.离子键 B.π键 C.非极性共价键 D.氢键 E.范德华力
(4)SbxOy的一种双链基本结构单元如图a,则其化学式为

(5)PDTA的结构如图b,Na[Sb(PDTA)]•H2O中心原子的配位数为6,则配位原子是

更新时间:2022-01-15 15:58:46
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】下表是元素周期表的一部分,表中所列的字母分别代表某一化学元素。 和
和 形成的
形成的 分子的结构式是
分子的结构式是___________ ,分子中含有___________ (填“极性”或“非极性”)键。
(2)元素 的最简单气态氢化物的电子式是
的最简单气态氢化物的电子式是___________ 。元素 和
和 中,最简单气态氢化物的沸点较高的是
中,最简单气态氢化物的沸点较高的是___________ (用化学式表示),原因是___________ 。
(3)元素 和
和 形成的最简单化合物分子的空间结构是
形成的最简单化合物分子的空间结构是___________ (用文字表述)。元素 、
、 、
、 中,简单离子半径从大到小的顺序是
中,简单离子半径从大到小的顺序是___________ (用离子符号表示)。
(4)元素 的外围电子轨道表示式是
的外围电子轨道表示式是___________ 。元素 、
、 、
、 中,第一电离能从大到小的顺序是
中,第一电离能从大到小的顺序是___________ (用元素符号表示)。
(5)元素 的最简单气态氢化物和最高价氧化物对应的水化物可以发生反应,该反应的化学方程式是
的最简单气态氢化物和最高价氧化物对应的水化物可以发生反应,该反应的化学方程式是___________ 。元素 和
和 的最高价氧化物对应的水化物可以发生反应,该反应的离子方程式是
的最高价氧化物对应的水化物可以发生反应,该反应的离子方程式是___________ 。

 和
和 形成的
形成的 分子的结构式是
分子的结构式是(2)元素
 的最简单气态氢化物的电子式是
的最简单气态氢化物的电子式是 和
和 中,最简单气态氢化物的沸点较高的是
中,最简单气态氢化物的沸点较高的是(3)元素
 和
和 形成的最简单化合物分子的空间结构是
形成的最简单化合物分子的空间结构是 、
、 、
、 中,简单离子半径从大到小的顺序是
中,简单离子半径从大到小的顺序是(4)元素
 的外围电子轨道表示式是
的外围电子轨道表示式是 、
、 、
、 中,第一电离能从大到小的顺序是
中,第一电离能从大到小的顺序是(5)元素
 的最简单气态氢化物和最高价氧化物对应的水化物可以发生反应,该反应的化学方程式是
的最简单气态氢化物和最高价氧化物对应的水化物可以发生反应,该反应的化学方程式是 和
和 的最高价氧化物对应的水化物可以发生反应,该反应的离子方程式是
的最高价氧化物对应的水化物可以发生反应,该反应的离子方程式是
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐2】氨硼烷 含氢量高、热稳定性好,是具有潜力的储氢材料。回答下列问题:
含氢量高、热稳定性好,是具有潜力的储氢材料。回答下列问题:
(1)氮在元素周期表中的位置是_______ ,基态N原子中电子占据最高能级的电子云轮廓图为_______ 状,基态N原子的电子排布图为_______ 。
(2)B的第一电离能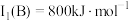 ,判断
,判断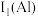
_______  (填“>”或“<”),结合电子排布式说明判断理由
(填“>”或“<”),结合电子排布式说明判断理由_______ 。
(3) 分子中,与N原子相连的H呈正电性
分子中,与N原子相连的H呈正电性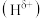 ,与B原子相连的H呈负电性
,与B原子相连的H呈负电性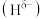 。在H、B、N三种元素中:
。在H、B、N三种元素中:
①电负性由大到小的顺序是_______ 。
②原子半径由大到小的顺序是_______ 。
③根据对角线规则,在B、N所在周期中,有一种元素与 元素性质具有相似性,写出其对应的氢氧化物与烧碱溶液反应的化学方程式
元素性质具有相似性,写出其对应的氢氧化物与烧碱溶液反应的化学方程式_______ 。
(4)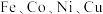 是目前氨硼烷水解产氢催化剂研究的热点。不同催化剂催化氨硼烷水解产氢的性能如图所示。这四种催化剂中:
是目前氨硼烷水解产氢催化剂研究的热点。不同催化剂催化氨硼烷水解产氢的性能如图所示。这四种催化剂中:
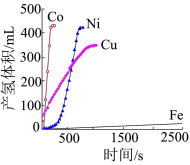
①催化效果最好的金属基态原子中未成对的电子数为_______ 。
②催化效果最差的金属其二价阳离子外围电子排布式为_______ 。
③催化效果第三的金属位于元素周期表的_______ 区。
 含氢量高、热稳定性好,是具有潜力的储氢材料。回答下列问题:
含氢量高、热稳定性好,是具有潜力的储氢材料。回答下列问题:(1)氮在元素周期表中的位置是
(2)B的第一电离能
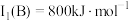 ,判断
,判断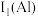
 (填“>”或“<”),结合电子排布式说明判断理由
(填“>”或“<”),结合电子排布式说明判断理由(3)
 分子中,与N原子相连的H呈正电性
分子中,与N原子相连的H呈正电性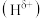 ,与B原子相连的H呈负电性
,与B原子相连的H呈负电性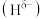 。在H、B、N三种元素中:
。在H、B、N三种元素中:①电负性由大到小的顺序是
②原子半径由大到小的顺序是
③根据对角线规则,在B、N所在周期中,有一种元素与
 元素性质具有相似性,写出其对应的氢氧化物与烧碱溶液反应的化学方程式
元素性质具有相似性,写出其对应的氢氧化物与烧碱溶液反应的化学方程式(4)
 是目前氨硼烷水解产氢催化剂研究的热点。不同催化剂催化氨硼烷水解产氢的性能如图所示。这四种催化剂中:
是目前氨硼烷水解产氢催化剂研究的热点。不同催化剂催化氨硼烷水解产氢的性能如图所示。这四种催化剂中:
①催化效果最好的金属基态原子中未成对的电子数为
②催化效果最差的金属其二价阳离子外围电子排布式为
③催化效果第三的金属位于元素周期表的
您最近一年使用:0次
【推荐3】现有属于前四周期的A、B、C、D、E、F、G七种元素,原子序数依次增大。A元素的价电子构型为nsnnpn+1;C元素为最活泼的非金属元素;D元素核外有三个电子层,最外层电子数是核外电子总数的 ;E元素正三价离子的3d轨道为半充满状态;F元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子;G元素与A元素位于同一主族,其某种氧化物有剧毒。
;E元素正三价离子的3d轨道为半充满状态;F元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子;G元素与A元素位于同一主族,其某种氧化物有剧毒。
(1)G的元素名称为__________________
(2)A、B、C三种元素电负性由大到小的顺序为_____________________ (用元素符号表示),第一电离能D _______ Al(填“>”“<”或“=”),其原因是___________________________ 。
(3)C元素的电子排布图为__________________ ;E3+的离子符号为__________________
(4)F元素位于元素周期表的______ 区,其基态原子的电子排布式为___________________
(5)G元素可能的性质_______________
A.其单质可作为半导体材料 B.其电负性大于磷
C.最高价氧化物对应的水化物是强酸 D.其第一电离能小于硒
 ;E元素正三价离子的3d轨道为半充满状态;F元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子;G元素与A元素位于同一主族,其某种氧化物有剧毒。
;E元素正三价离子的3d轨道为半充满状态;F元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子;G元素与A元素位于同一主族,其某种氧化物有剧毒。(1)G的元素名称为
(2)A、B、C三种元素电负性由大到小的顺序为
(3)C元素的电子排布图为
(4)F元素位于元素周期表的
(5)G元素可能的性质
A.其单质可作为半导体材料 B.其电负性大于磷
C.最高价氧化物对应的水化物是强酸 D.其第一电离能小于硒
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】如图是元素周期表中的前四周期,①~⑨为相应的元素,请从中选择合适的元素回答问题:

(1)根据元素原子的外围电子排布特征,元素周期表可划分为五个区域,⑨元素位于周期表的________ 区。
(2)④、⑥两元素形成的化合物的立体构型为________ ,其中心原子的杂化轨道类型为________ 。
(3)元素⑧的离子与NH3形成的配离子的结构式为_______________________ 。
(4)在①与④形成的相对分子质量最小的化合物A中,写出与化合物A互为等电子体的一种阳离子______ (填离子符号)。写出A的水溶液中存在的氢键:
__________________________________________________ (任写两种)。
(5)关于元素①与元素⑤形成的1︰1的化合物,下列说法正确的是______ (填字母序号)。
A.该化合物中的所有原子都满足最外层8电子稳定结构
B.该化合物分子中σ键和π键数目比为1︰1
C.该化合物是由极性键和非极性键形成的极性分子
D.该化合物分子的空间构型为直线形
(6)元素⑦与CO可形成X(CO)5型化合物,该化合物常温下呈液态,熔点为-20.5 ℃,沸点为103 ℃,易溶于非极性溶剂,据此可判断该化合物晶体属于________ 晶体(填晶体类型),化合物中⑦的化合价为:_______ 。根据等电子体理论,该化合物的配体的结构式为:_______ ,CaC2中,阴离子的电子式为: ____________________ 。

(1)根据元素原子的外围电子排布特征,元素周期表可划分为五个区域,⑨元素位于周期表的
(2)④、⑥两元素形成的化合物的立体构型为
(3)元素⑧的离子与NH3形成的配离子的结构式为
(4)在①与④形成的相对分子质量最小的化合物A中,写出与化合物A互为等电子体的一种阳离子
(5)关于元素①与元素⑤形成的1︰1的化合物,下列说法正确的是
A.该化合物中的所有原子都满足最外层8电子稳定结构
B.该化合物分子中σ键和π键数目比为1︰1
C.该化合物是由极性键和非极性键形成的极性分子
D.该化合物分子的空间构型为直线形
(6)元素⑦与CO可形成X(CO)5型化合物,该化合物常温下呈液态,熔点为-20.5 ℃,沸点为103 ℃,易溶于非极性溶剂,据此可判断该化合物晶体属于
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】C、N、P、S、Fe、Cu是与人类生产、生活息息相关的化学元素,利用所学知识回答下列问题:
(1)基态Cu原子核外电子排布式为___ ,则高温下的稳定性CuO___ Cu2O(填“>”或“<”);
(2)经研究Cu的某种化合物能催化氧化CO(NH2)2,其中C、N的杂化方式分别为___ ,___ ;
(3)Si、P、S元素的第一电离能由大到小的顺序是___ ;
(4)OF2的空间构型是___ ,分子极性:H2O___ OF2(填“>”或“<”),理由是___ ;
(5)[Fe(CN)6]3-中配位键和π键的个数之比为___ ;
(6)邻羟基苯甲醛的沸点低于对羟基苯甲醛的沸点,原因是___ 。
(1)基态Cu原子核外电子排布式为
(2)经研究Cu的某种化合物能催化氧化CO(NH2)2,其中C、N的杂化方式分别为
(3)Si、P、S元素的第一电离能由大到小的顺序是
(4)OF2的空间构型是
(5)[Fe(CN)6]3-中配位键和π键的个数之比为
(6)邻羟基苯甲醛的沸点低于对羟基苯甲醛的沸点,原因是
您最近一年使用:0次
【推荐3】氮的化合物在工业生产中有重要用途,请回答下列问题:
(1)[Ni(N2H4)2](N3)2是一种富氮含能材料。写出一种与N 互为等电子体的分子:
互为等电子体的分子:_______ (填化学式);实验数据表明键角:NH3>PH3>AsH3,分析原因是_______ 。
(2)氮与碳还能形成一种离子液体的正离子 ,为使该正离子以单个形式存在以获得良好的溶解性能,与N原子相连的-C2H5,不能被H原子替换,原因是
,为使该正离子以单个形式存在以获得良好的溶解性能,与N原子相连的-C2H5,不能被H原子替换,原因是_______ 。
(3)配合物顺铂[Pt(NH3)2Cl2]是临床使用的第一代铂类抗癌药物。顺铂的抗癌机理:在铜转运蛋白的作用下,顺铂进入人体细胞发生水解,生成的Pt(NH3)2(OH)Cl破坏DNA的结构,阻止癌细胞增殖。如:
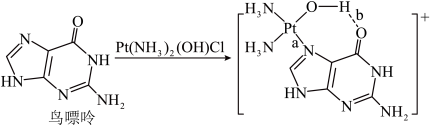
①基态Cu原子价层电子的轨道表示式为_______ ,鸟嘌呤中氮原子的杂化方式为______ 。构成鸟嘌呤的元素电负性由大到小的顺序_______ 。
②在Pt(NH3)2Cl2中,配体与铂(Ⅱ)的结合能力:Cl-_______ NH3(填“>”或“<”)。
③顺铂和反铂互为同分异构体,两者的结构和性质如表。
请从分子结构角度解释顺铂在水中的溶解度大于反铂的原因是________ 。
④顺铂的发现与铂电极的使用有关。铂晶胞为正方体,边长为a nm,结构如图。铂晶体的摩尔体积Vm=_______ m3/mol(阿伏加德罗常数为NA)。(已知:单位物质的量的物质所具有的体积叫做摩尔体积)

(1)[Ni(N2H4)2](N3)2是一种富氮含能材料。写出一种与N
 互为等电子体的分子:
互为等电子体的分子:(2)氮与碳还能形成一种离子液体的正离子
 ,为使该正离子以单个形式存在以获得良好的溶解性能,与N原子相连的-C2H5,不能被H原子替换,原因是
,为使该正离子以单个形式存在以获得良好的溶解性能,与N原子相连的-C2H5,不能被H原子替换,原因是(3)配合物顺铂[Pt(NH3)2Cl2]是临床使用的第一代铂类抗癌药物。顺铂的抗癌机理:在铜转运蛋白的作用下,顺铂进入人体细胞发生水解,生成的Pt(NH3)2(OH)Cl破坏DNA的结构,阻止癌细胞增殖。如:

①基态Cu原子价层电子的轨道表示式为
②在Pt(NH3)2Cl2中,配体与铂(Ⅱ)的结合能力:Cl-
③顺铂和反铂互为同分异构体,两者的结构和性质如表。
| 顺铂 | 反铂 | |
| 结构 |  | 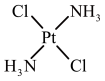 |
| 25℃时溶解度/g | 0.2577 | 0.0366 |
④顺铂的发现与铂电极的使用有关。铂晶胞为正方体,边长为a nm,结构如图。铂晶体的摩尔体积Vm=

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐1】氮族、氧族元素的化合物在生活、生产中有广泛应用。回答下列问题:
(1)SO2与O3互为等电子体,预测O3的立体构型是___ 。
(2)N2H4是火箭发射的燃料,也是一种化工原料。N2H4+H2SO4 N2H6SO4,1molN2H
N2H6SO4,1molN2H 中含
中含___ 个配位键和___ 个σ键。
(3)氮化钛(Ti3N4)为金黄色晶体,由于其具有令人满意的仿金效果,因此越来越广泛地被利用成为黄金的代替品。
①基态Ti3+中有___ 个未成对电子,与钛同族且相邻的元素Zr(锆)的基态原子价电子排布式为___ 。
②TiCl4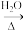 H2TiO3
H2TiO3 TiO2(纳米)。纳米二氧化钛是高效催化剂。例如:
TiO2(纳米)。纳米二氧化钛是高效催化剂。例如:


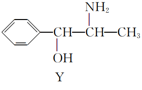
X到Y的转变过程中,碳原子的杂化类型变化是___ 。
(1)SO2与O3互为等电子体,预测O3的立体构型是
(2)N2H4是火箭发射的燃料,也是一种化工原料。N2H4+H2SO4
 N2H6SO4,1molN2H
N2H6SO4,1molN2H 中含
中含(3)氮化钛(Ti3N4)为金黄色晶体,由于其具有令人满意的仿金效果,因此越来越广泛地被利用成为黄金的代替品。
①基态Ti3+中有
②TiCl4
 H2TiO3
H2TiO3 TiO2(纳米)。纳米二氧化钛是高效催化剂。例如:
TiO2(纳米)。纳米二氧化钛是高效催化剂。例如:


X到Y的转变过程中,碳原子的杂化类型变化是
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】金属钛被誉为“未来金属”,钛及其化合物被广泛应用于飞机、火箭、卫星、舰艇、医疗等领域。“嫦娥五号”首次实现了我国地外天体采样返回,它的成功发射标志着我国航天技术向前迈出了一大步,其制作材料中包含了 元素。2022年2月我国科学家在《科学》杂志发表反型钙钛矿太阳能电池研究方面的最新科研成果论文,为钙钛矿电池研究开辟了新方向。
元素。2022年2月我国科学家在《科学》杂志发表反型钙钛矿太阳能电池研究方面的最新科研成果论文,为钙钛矿电池研究开辟了新方向。
(1)钛位于周期表的___________ 区,基态钛原子价电子排布式为___________ 。
(2) 是一种储氢材料,可由
是一种储氢材料,可由 和
和 反应制得。请写出一个与
反应制得。请写出一个与 互为等电子体的微粒
互为等电子体的微粒___________ (化学式)。
(3)钛的某配合物可用于催化环烯烃聚合,其结构如图所示:
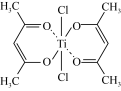
①该配合物中碳原子的杂化类型___________ 。
②该配合物中存在的化学键有___________ (填字母)。
a.共价键 b.金属键 c.配位键 d.氢键
(4)钛与卤素形成的化合物 、
、 、
、 、
、 熔点依次为377℃、
熔点依次为377℃、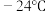 、38.3℃、153℃,其中
、38.3℃、153℃,其中 、
、 、
、 熔点依次升高的原因是
熔点依次升高的原因是___________ 。
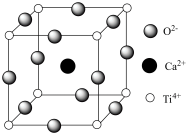
(5) 的晶胞如图所示,
的晶胞如图所示, 的配位数是
的配位数是___________ ,若 位于晶胞顶点,则
位于晶胞顶点,则 位于晶胞
位于晶胞___________ 位置,若晶胞参数为a nm,则晶体密度为___________  (列出计算式,阿伏加德罗常数用NA表示)。
(列出计算式,阿伏加德罗常数用NA表示)。
 元素。2022年2月我国科学家在《科学》杂志发表反型钙钛矿太阳能电池研究方面的最新科研成果论文,为钙钛矿电池研究开辟了新方向。
元素。2022年2月我国科学家在《科学》杂志发表反型钙钛矿太阳能电池研究方面的最新科研成果论文,为钙钛矿电池研究开辟了新方向。(1)钛位于周期表的
(2)
 是一种储氢材料,可由
是一种储氢材料,可由 和
和 反应制得。请写出一个与
反应制得。请写出一个与 互为等电子体的微粒
互为等电子体的微粒(3)钛的某配合物可用于催化环烯烃聚合,其结构如图所示:

①该配合物中碳原子的杂化类型
②该配合物中存在的化学键有
a.共价键 b.金属键 c.配位键 d.氢键
(4)钛与卤素形成的化合物
 、
、 、
、 、
、 熔点依次为377℃、
熔点依次为377℃、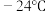 、38.3℃、153℃,其中
、38.3℃、153℃,其中 、
、 、
、 熔点依次升高的原因是
熔点依次升高的原因是(5)
 的晶胞如图所示,
的晶胞如图所示, 的配位数是
的配位数是 位于晶胞顶点,则
位于晶胞顶点,则 位于晶胞
位于晶胞 (列出计算式,阿伏加德罗常数用NA表示)。
(列出计算式,阿伏加德罗常数用NA表示)。
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】人们对含硼(元素符号为“B”)物质结构的研究,极大地推动了结构化学的发展。回答下列问题:
(1)基态B原子价层电子的电子排布式为___________ ,核外电子占据最高能层的符号是___________ ,占据该能层未成对电子的电子云轮廓图形状为___________ 。
(2)1923年化学家Lewis提出了酸碱电子理论。酸碱电子理论认为:凡是可以接受电子对的物质称为酸,凡是可以给出电子对的物质称为碱。已知BF3与F-反应可生成BF ,则该反应中BF3属于
,则该反应中BF3属于___________ (填“酸”或“碱”),原因是___________ 。
(3)NaBH4是有机合成中常用的还原剂,NaBH4中的阴离子空间构型是___________ ,中心原子的杂化形式为___________ ,NaBH4中存在___________ (填标号)
a.离子键 b.金属键 c.σ键 d.π键 e.氢键
(4)请比较第一电离能:IB___________ IBe(填“>”或“<”),原因是___________ 。
(5)六方氮化硼的结构与石墨类似,B—N共价单键的键长理论值为158pm,而六方氮化硼层内B、N原子间距的实测值为145pm,造成这一差值的原因是___________ 。
(1)基态B原子价层电子的电子排布式为
(2)1923年化学家Lewis提出了酸碱电子理论。酸碱电子理论认为:凡是可以接受电子对的物质称为酸,凡是可以给出电子对的物质称为碱。已知BF3与F-反应可生成BF
 ,则该反应中BF3属于
,则该反应中BF3属于(3)NaBH4是有机合成中常用的还原剂,NaBH4中的阴离子空间构型是
a.离子键 b.金属键 c.σ键 d.π键 e.氢键
(4)请比较第一电离能:IB
(5)六方氮化硼的结构与石墨类似,B—N共价单键的键长理论值为158pm,而六方氮化硼层内B、N原子间距的实测值为145pm,造成这一差值的原因是
您最近一年使用:0次
【推荐1】晶体按其几何形态的对称程度可分为七类,其中四方晶系是非常重要的一类。
(1)铁和氨在640℃时可发生置换反应,一种产物的晶胞结构如图所示,该反应的化学方程式为_______ 。 晶体具有优异的非线性光学性能。分别用○、●表示
晶体具有优异的非线性光学性能。分别用○、●表示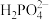 和
和 ,
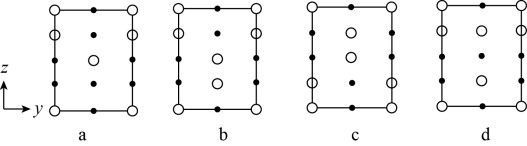
, 晶体的四方晶胞如图(a)所示,图(b)、图(c)分别显示的是
晶体的四方晶胞如图(a)所示,图(b)、图(c)分别显示的是 、
、 在晶胞xz面、yz面上的位置:
在晶胞xz面、yz面上的位置:_______ (填标号)。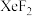 晶体也属四方晶系,晶胞参数如图所示,晶胞棱边夹角均为90°,该晶胞中有
晶体也属四方晶系,晶胞参数如图所示,晶胞棱边夹角均为90°,该晶胞中有_______ 个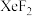 分子。以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称为原子的分数坐标,如A点原子的分数坐标为
分子。以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称为原子的分数坐标,如A点原子的分数坐标为 。已知
。已知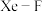 键键长为rpm,则B点原子的分数坐标为
键键长为rpm,则B点原子的分数坐标为_______ 。 在小正方体的棱上,两端均与Fe相连,立方体中心空隙可容纳
在小正方体的棱上,两端均与Fe相连,立方体中心空隙可容纳 ,如图所示(
,如图所示( 在图中省略)。
在图中省略)。 与
与 之间最近距离为
之间最近距离为_______ pm,设阿伏加德罗常数的值为NA,则该晶体的密度为_______ g/cm3。
(1)铁和氨在640℃时可发生置换反应,一种产物的晶胞结构如图所示,该反应的化学方程式为
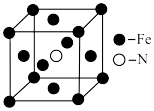
 晶体具有优异的非线性光学性能。分别用○、●表示
晶体具有优异的非线性光学性能。分别用○、●表示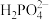 和
和 ,
, 晶体的四方晶胞如图(a)所示,图(b)、图(c)分别显示的是
晶体的四方晶胞如图(a)所示,图(b)、图(c)分别显示的是 、
、 在晶胞xz面、yz面上的位置:
在晶胞xz面、yz面上的位置: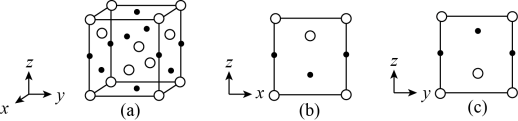
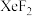 晶体也属四方晶系,晶胞参数如图所示,晶胞棱边夹角均为90°,该晶胞中有
晶体也属四方晶系,晶胞参数如图所示,晶胞棱边夹角均为90°,该晶胞中有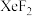 分子。以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称为原子的分数坐标,如A点原子的分数坐标为
分子。以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称为原子的分数坐标,如A点原子的分数坐标为 。已知
。已知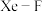 键键长为rpm,则B点原子的分数坐标为
键键长为rpm,则B点原子的分数坐标为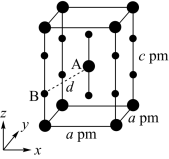
 在小正方体的棱上,两端均与Fe相连,立方体中心空隙可容纳
在小正方体的棱上,两端均与Fe相连,立方体中心空隙可容纳 ,如图所示(
,如图所示( 在图中省略)。
在图中省略)。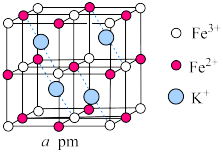
 与
与 之间最近距离为
之间最近距离为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】A、B、C、D、E 为主族元素,A、B、C 同周期且原子半径逐渐减小,A、B 原子的最外层电子数之和等于 C、D 原子的最外层电子数之和。A 元素基态原子的最外层电子排布为 nsnnpn,B 的氢化物可 与其最高价氧化物的水化物反应生成盐。D元素位于元素周期表中长周期,是维持青少年骨骼正常生长发育的重要元素之一,其原子最外层电子数等于最内层电子数。E是元素周期表中原子半径最小的元素。试 回答下列问题:
(1)C 元素基态原子的核外电子排布式是________ 。
(2)A、B 两元素各有多种氢化物,其电子总数为 10 的氢化物中沸点最高的是________ (填化学式)。
(3)B 和 E 可形成离子化合物 BE5,它的所有原子的最外层都符合相应的稀有气体原子电子层结构,该物质适当加热就分解成两种气体,试完成:
①该离子化合物的电子式为________ 。
②该离子化合物溶于水后溶液呈________ 性(填“酸”“碱”或“中”),其原因是________ (用化学方程式表示) 。
(4)下列晶体结构示意图中(黑点表示阳离子,白点表示阴离子),能表示 C 与 D 形成的离子化合物结构的是________ (填字母标号 a 或 b)。

(1)C 元素基态原子的核外电子排布式是
(2)A、B 两元素各有多种氢化物,其电子总数为 10 的氢化物中沸点最高的是
(3)B 和 E 可形成离子化合物 BE5,它的所有原子的最外层都符合相应的稀有气体原子电子层结构,该物质适当加热就分解成两种气体,试完成:
①该离子化合物的电子式为
②该离子化合物溶于水后溶液呈
(4)下列晶体结构示意图中(黑点表示阳离子,白点表示阴离子),能表示 C 与 D 形成的离子化合物结构的是

您最近一年使用:0次
【推荐3】前四周期元素A、B、C、D、E的原子序数依次增大。A的负一价阴离子与 电子层结构相同,B的电负性比D的大,B和D位于不同主族。C元素原子的最外层电子数比次外层电子数少5;基态D原子的价层电子排布式为
电子层结构相同,B的电负性比D的大,B和D位于不同主族。C元素原子的最外层电子数比次外层电子数少5;基态D原子的价层电子排布式为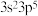 ,基态E原子的未成对电子数为6.回答下列问题:
,基态E原子的未成对电子数为6.回答下列问题:
(1)基态E原子的电子排布式为
___________ 。
(2) 和
和 的晶体类型都是
的晶体类型都是___________ ,熔点、沸点:
___________ (填“高于”“低于”或“等于”) 的,原因是
的,原因是___________ 。
(3)D有 、
、 、
、 、
、 价,其对应含氧酸的酸性由弱到强的顺序为
价,其对应含氧酸的酸性由弱到强的顺序为___________ (填化学式)。
(4)B、E组成一种晶体M,晶胞如图所示。小黑球代表B,小白球代表E,M的化学式为___________ 。

 电子层结构相同,B的电负性比D的大,B和D位于不同主族。C元素原子的最外层电子数比次外层电子数少5;基态D原子的价层电子排布式为
电子层结构相同,B的电负性比D的大,B和D位于不同主族。C元素原子的最外层电子数比次外层电子数少5;基态D原子的价层电子排布式为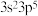 ,基态E原子的未成对电子数为6.回答下列问题:
,基态E原子的未成对电子数为6.回答下列问题:(1)基态E原子的电子排布式为

(2)
 和
和 的晶体类型都是
的晶体类型都是
 的,原因是
的,原因是(3)D有
 、
、 、
、 、
、 价,其对应含氧酸的酸性由弱到强的顺序为
价,其对应含氧酸的酸性由弱到强的顺序为(4)B、E组成一种晶体M,晶胞如图所示。小黑球代表B,小白球代表E,M的化学式为

您最近一年使用:0次



