中科院大连化学物理研究所科学家用Ni-BaH3/Al2O3、Ni-LiH等作催化剂,实现了在常压、100~300℃的条件下合成氨,这一成果发表在《Nature Energy》杂志上。
(1)基态 的核外电子排布式为
的核外电子排布式为___________ ,若该离子核外电子空间运动状态有15种,则该离子处于___________ (填“基”或“激发”)态。
(2)氨在粮食生产、国防中有着无可替代的地位,也是重要的化工原料,可用于合成氨基酸、硝酸、TNT等。甘氨酸(NH2CH2COOH)是组成最简单的氨基酸,熔点为182℃,沸点为233℃。
①硝酸溶液中 的空间构型为
的空间构型为___________ 。
②甘氨酸的晶体类型是___________ ,其熔、沸点远高于相对分子质量几乎相等的丙酸(熔点为-21℃,沸点为141℃)的主要原因:一是甘氨酸能形成内盐;二是___________ 。
(3)比较NH3分子(前者)和在 中NH3(后者)分子中∠H-N-H的键角大小,前者
中NH3(后者)分子中∠H-N-H的键角大小,前者______ 后者。(填“>”、“<”或“=”)
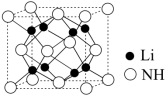
(4)亚氨基锂(Li2NH,摩尔质量为M g/mol),是一种储氢容量高、安全性能好的固体储氢材料,其晶胞结构如图所示,若晶胞参数为d pm,密度为ρ g/cm3,则阿伏加德罗常数
_______  (列出表达式)。
(列出表达式)。
(1)基态
 的核外电子排布式为
的核外电子排布式为(2)氨在粮食生产、国防中有着无可替代的地位,也是重要的化工原料,可用于合成氨基酸、硝酸、TNT等。甘氨酸(NH2CH2COOH)是组成最简单的氨基酸,熔点为182℃,沸点为233℃。
①硝酸溶液中
 的空间构型为
的空间构型为②甘氨酸的晶体类型是
(3)比较NH3分子(前者)和在
 中NH3(后者)分子中∠H-N-H的键角大小,前者
中NH3(后者)分子中∠H-N-H的键角大小,前者(4)亚氨基锂(Li2NH,摩尔质量为M g/mol),是一种储氢容量高、安全性能好的固体储氢材料,其晶胞结构如图所示,若晶胞参数为d pm,密度为ρ g/cm3,则阿伏加德罗常数

 (列出表达式)。
(列出表达式)。
更新时间:2024-01-07 00:11:03
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】钨锰铁矿[主要成分为(Fe,Mn)WO4,还含有石英及少量P、As的化合物],由钨锰铁矿的精矿粉制备金属钨的工艺流程如图所示:

(1)已知W为第六周期元素,与Cr同族,但核外电子排布完全符合构造原理,写出W的基态价电子排布式___ 。用钨做白炽灯灯丝是利用其___ (填具体性质)。
(2)“滤渣II”中除含有Mg3(PO4)2、Mg3(AsO4)2外,还含有__ (写化学式)。
(3)“萃取”时发生的反应为3(R3NH)2SO4(油层)+H2W12O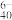 (水层)=(R3NH)6H2W12O40(油层)+3SO
(水层)=(R3NH)6H2W12O40(油层)+3SO (水层),该步骤主要目的是除去
(水层),该步骤主要目的是除去___ 。最适合作“反萃取剂”的是___ 。
(4)焦炭和氢气都可以将三氧化钨还原成钨单质,但工业上常用氢气作还原剂,此反应是___ (填“吸热”或“放热”)反应,不用焦炭的原因是__ 。
(5)某小组利用可逆反应,W(s)+I2(g) WI2(g) △H<0,设计如图装置提纯粗钨(杂质熔点高,且不能与碘发生反应)。粗钨装入石英管一端,抽成真空后引入适量碘并封管,置于加热炉中。最终纯钨在
WI2(g) △H<0,设计如图装置提纯粗钨(杂质熔点高,且不能与碘发生反应)。粗钨装入石英管一端,抽成真空后引入适量碘并封管,置于加热炉中。最终纯钨在___ 区(填“Ⅰ”或“Ⅱ”)。


(1)已知W为第六周期元素,与Cr同族,但核外电子排布完全符合构造原理,写出W的基态价电子排布式
(2)“滤渣II”中除含有Mg3(PO4)2、Mg3(AsO4)2外,还含有
(3)“萃取”时发生的反应为3(R3NH)2SO4(油层)+H2W12O
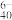 (水层)=(R3NH)6H2W12O40(油层)+3SO
(水层)=(R3NH)6H2W12O40(油层)+3SO (水层),该步骤主要目的是除去
(水层),该步骤主要目的是除去(4)焦炭和氢气都可以将三氧化钨还原成钨单质,但工业上常用氢气作还原剂,此反应是
(5)某小组利用可逆反应,W(s)+I2(g)
 WI2(g) △H<0,设计如图装置提纯粗钨(杂质熔点高,且不能与碘发生反应)。粗钨装入石英管一端,抽成真空后引入适量碘并封管,置于加热炉中。最终纯钨在
WI2(g) △H<0,设计如图装置提纯粗钨(杂质熔点高,且不能与碘发生反应)。粗钨装入石英管一端,抽成真空后引入适量碘并封管,置于加热炉中。最终纯钨在
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐2】金属镍 及其化合物在合金材料以及催化剂等方面应用广泛。镍原子及其离子易形成配合物,如
及其化合物在合金材料以及催化剂等方面应用广泛。镍原子及其离子易形成配合物,如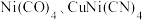 等。回答下列问题:
等。回答下列问题:
(1)基态镍原子中核外电子所在最高能层有_______ 个原子轨道。下列基态氨原子的轨道表示式中,仅违背洪特规则的是_______ (填字母)。
A.
B.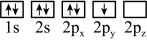
C.
D.
(2) 可通过反应
可通过反应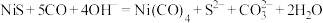 合成。
合成。
① 的中心原子为
的中心原子为 杂化,
杂化, 的空间构型是
的空间构型是_______ ,推测
_______ 是分子(填“极性”或“非极性”)。
②氧族元素的氢化物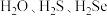 ,沸点由高到低的顺序为
,沸点由高到低的顺序为_______ (填化学式,下同),还原性由强到弱的顺序为_______ ,键角由大到小的顺序为_______ 。
(3)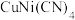 是一种二维负热膨胀材料,其结构如图所示,该结构中所含
是一种二维负热膨胀材料,其结构如图所示,该结构中所含 键与
键与 键数目之比为
键数目之比为_______ 。

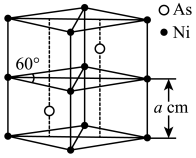
(4)红镍矿是一种重要的含镍矿物,其主要成分的晶胞如图所示(底面为菱形),则每个 原子周围与之紧邻的
原子周围与之紧邻的 原子数为
原子数为_______ 。该晶体的密度为 ,设阿伏加德罗常数的值为
,设阿伏加德罗常数的值为 ,则晶胞中
,则晶胞中 和
和 的最近距离为
的最近距离为_______  。
。
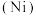 及其化合物在合金材料以及催化剂等方面应用广泛。镍原子及其离子易形成配合物,如
及其化合物在合金材料以及催化剂等方面应用广泛。镍原子及其离子易形成配合物,如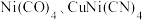 等。回答下列问题:
等。回答下列问题:(1)基态镍原子中核外电子所在最高能层有
A.

B.

C.

D.

(2)
 可通过反应
可通过反应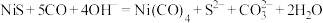 合成。
合成。①
 的中心原子为
的中心原子为 杂化,
杂化, 的空间构型是
的空间构型是
②氧族元素的氢化物
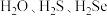 ,沸点由高到低的顺序为
,沸点由高到低的顺序为(3)
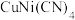 是一种二维负热膨胀材料,其结构如图所示,该结构中所含
是一种二维负热膨胀材料,其结构如图所示,该结构中所含 键与
键与 键数目之比为
键数目之比为
(4)红镍矿是一种重要的含镍矿物,其主要成分的晶胞如图所示(底面为菱形),则每个
 原子周围与之紧邻的
原子周围与之紧邻的 原子数为
原子数为 ,设阿伏加德罗常数的值为
,设阿伏加德罗常数的值为 ,则晶胞中
,则晶胞中 和
和 的最近距离为
的最近距离为 。
。
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】下表是元素周期表的一部分。表中所列的字母分别代表一种化学元素。
试回答下列问题:
(1)请写出元素N的基态原子电子排布式______ 。
(2)ME2L2常温下为深红色液体,能与CCl4、CS2等互溶,据此可判断ME2L2是______ (填“极性”或“非极性”)分子。
(3)在①苯、②CH3OH、③HCHO、④CS2、⑤CCl4五种有机溶剂中,碳原子采取sp2杂化的分子有______ (填序号),CS2分子的空间构型是______ 。
(4)元素N可以形成分子式为Co(NH3)5BrSO4,配位数均为6的两种配合物,若往其中一种配合物的溶液中加入BaCl2溶液时,无明显现象,若加入AgNO3溶液时,产生淡黄色沉淀,则该配合物的化学式为______ 。SO42-的空间构型是______ 其中S原子的杂化类型是______
| A | |||||||||||||||||
| B | C | D | E | F | |||||||||||||
| G | H | I | J | K | L | ||||||||||||
| M | N | ||||||||||||||||
试回答下列问题:
(1)请写出元素N的基态原子电子排布式
(2)ME2L2常温下为深红色液体,能与CCl4、CS2等互溶,据此可判断ME2L2是
(3)在①苯、②CH3OH、③HCHO、④CS2、⑤CCl4五种有机溶剂中,碳原子采取sp2杂化的分子有
(4)元素N可以形成分子式为Co(NH3)5BrSO4,配位数均为6的两种配合物,若往其中一种配合物的溶液中加入BaCl2溶液时,无明显现象,若加入AgNO3溶液时,产生淡黄色沉淀,则该配合物的化学式为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐1】氮化镓(GaN)材料是第三代半导体的代表,通常以GaCl3为镓源,NH3为氮源制备,具有出色的抗击穿能力,能耐受更高的电子密度。
(1)基态Ga价电子排布图为___________ 。
(2)Ga、N和O的第一电离能由小到大的顺序为___________ ,NO 的空间构型为
的空间构型为___________ ,与其互为等电子体的微粒有___________ (任写一种)
(3)GaCl3熔点为77.9℃,气体在270℃左右以二聚物存在,GaF3熔点1000℃,GaCl3二聚体的结构式为___________ ,其熔点低于GaF3的原因为___________ 。
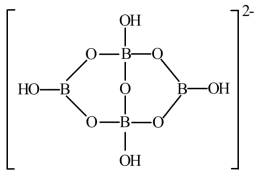
(4)与镓同主族的B具有缺电子性,硼砂(四硼酸钠Na2B4O7·10H2O)中B4O 是由两个H3BO3和两个[B(OH)4]-缩合而成的双六元环,应写成[B4O5(OH)4]2-的形式,结构如图所示,则该离子存在的作用力有
是由两个H3BO3和两个[B(OH)4]-缩合而成的双六元环,应写成[B4O5(OH)4]2-的形式,结构如图所示,则该离子存在的作用力有___________ ,B原子的杂化方式为___________ 。
A.离子键 B.共价键 C.金属键 D.范德华力 E.氢键 F.配位键
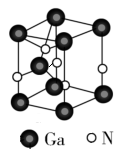
(5)氮化镓的晶胞如图所示,Ga原子与N原子半径分别为a pm和b pm,阿伏加德罗常数的值为NA,晶胞密度为c g/cm3,则该晶胞的空间利用率为___________ (已知空间利用率为晶胞内原子体积占晶胞体积的百分比)。
(1)基态Ga价电子排布图为
(2)Ga、N和O的第一电离能由小到大的顺序为
 的空间构型为
的空间构型为(3)GaCl3熔点为77.9℃,气体在270℃左右以二聚物存在,GaF3熔点1000℃,GaCl3二聚体的结构式为
(4)与镓同主族的B具有缺电子性,硼砂(四硼酸钠Na2B4O7·10H2O)中B4O
 是由两个H3BO3和两个[B(OH)4]-缩合而成的双六元环,应写成[B4O5(OH)4]2-的形式,结构如图所示,则该离子存在的作用力有
是由两个H3BO3和两个[B(OH)4]-缩合而成的双六元环,应写成[B4O5(OH)4]2-的形式,结构如图所示,则该离子存在的作用力有
A.离子键 B.共价键 C.金属键 D.范德华力 E.氢键 F.配位键
(5)氮化镓的晶胞如图所示,Ga原子与N原子半径分别为a pm和b pm,阿伏加德罗常数的值为NA,晶胞密度为c g/cm3,则该晶胞的空间利用率为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐2】2022年春晚中舞蹈诗剧《只此青绿》生动还原了北宋名画《千里江山图》,《千里江山图》之所以色彩艳丽,璀璨夺目,与所使用矿物颜料有关,请回答下列问题:
(1)石青,又名蓝矿石,化学式为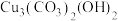 。基态
。基态 原子的价电子排布式为
原子的价电子排布式为_______ ;原子中电子有两种相反的自旋状态,分别用 和
和 表示,称为电子的自旋磁量子数,则
表示,称为电子的自旋磁量子数,则 中电子自旋磁量子数的代数和为
中电子自旋磁量子数的代数和为_______ 。
(2)亚铁氰化钾,呈黄色结晶性粉末,化学式为 。
。 中配体
中配体 的配位原子是
的配位原子是_______ (填元素符号); 中
中 原子的杂化方式
原子的杂化方式_______ ;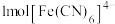 中含
中含 键为
键为_______  。
。
(3) 呈黑色或灰黑色,已知:晶胞中
呈黑色或灰黑色,已知:晶胞中 的位置如图1所示,
的位置如图1所示, 位于
位于 所构成的四面体中心,晶胞的侧视图如图2所示。
所构成的四面体中心,晶胞的侧视图如图2所示。

 填充了晶胞中四面体空隙的百分率是
填充了晶胞中四面体空隙的百分率是_______ , 配位数为
配位数为_______ ;已知图1中 原子的坐标参数为
原子的坐标参数为 ,则与
,则与 原子距离最近的
原子距离最近的 的坐标参数为
的坐标参数为_______ ;若晶胞边长为 ,则该晶体的密度为
,则该晶体的密度为_______  (用代数式表示,设
(用代数式表示,设 为阿伏加德罗常数的值)。
为阿伏加德罗常数的值)。
(1)石青,又名蓝矿石,化学式为
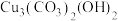 。基态
。基态 原子的价电子排布式为
原子的价电子排布式为 和
和 表示,称为电子的自旋磁量子数,则
表示,称为电子的自旋磁量子数,则 中电子自旋磁量子数的代数和为
中电子自旋磁量子数的代数和为(2)亚铁氰化钾,呈黄色结晶性粉末,化学式为
 。
。 中配体
中配体 的配位原子是
的配位原子是 中
中 原子的杂化方式
原子的杂化方式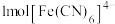 中含
中含 键为
键为 。
。(3)
 呈黑色或灰黑色,已知:晶胞中
呈黑色或灰黑色,已知:晶胞中 的位置如图1所示,
的位置如图1所示, 位于
位于 所构成的四面体中心,晶胞的侧视图如图2所示。
所构成的四面体中心,晶胞的侧视图如图2所示。
 填充了晶胞中四面体空隙的百分率是
填充了晶胞中四面体空隙的百分率是 配位数为
配位数为 原子的坐标参数为
原子的坐标参数为 ,则与
,则与 原子距离最近的
原子距离最近的 的坐标参数为
的坐标参数为 ,则该晶体的密度为
,则该晶体的密度为 (用代数式表示,设
(用代数式表示,设 为阿伏加德罗常数的值)。
为阿伏加德罗常数的值)。
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐3】按要求回答下列问题:
(1)Fe、Co、Ni是三种重要的金属元素,探究其结构有重要意义。
①Fe、Co、Ni在元素周期表中的位置为___________ ,请写出基态镍原子的核外电子排布式___________ 。
②按照核外电子排布,可把元素周期表划分为5个区,Co在元素周期表中属于___________ 区。
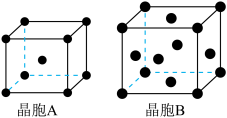
③用X射线衍射测定,得到Fe的两种晶胞A、B,其结构如图所示。晶胞A中每个Fe原子紧邻的原子数为___________ 。每个晶胞B中含Fe原子数为___________ 。
(2)[Co(NH3)5Cl] Cl2是Co3+的一种重要配合物。
①1mol [Co(NH3)5Cl] Cl2与足量的硝酸银溶液反应产生___________ molAgCl沉淀。
②Co3+的价层电子轨道表示式是___________ 。
③1mol[Co(NH3)5Cl]2+中含有的 键的数目为
键的数目为___________ 。
(3)第ⅤA族元素及其化合物的结构和性质如下:
①NH3、PH3、AsH3的沸点由高到低的顺序为___________ (填化学式,下同),键角由大到小的顺序为___________ 。
②某种氮化硼晶体的立方晶胞结构如图,该物质熔沸点高、硬度大与金刚石类似:
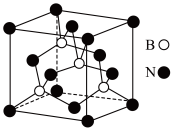
i.氮化硼属___________ 晶体;该种氮化硼的熔点___________ SiC (填“>”或“<”或“=”)。
ii.已知氮化硼晶胞的边长为a nm,则晶胞密度为___________ g·cm-3 (用含有a、NA的代数式表示)。
(1)Fe、Co、Ni是三种重要的金属元素,探究其结构有重要意义。
①Fe、Co、Ni在元素周期表中的位置为
②按照核外电子排布,可把元素周期表划分为5个区,Co在元素周期表中属于
③用X射线衍射测定,得到Fe的两种晶胞A、B,其结构如图所示。晶胞A中每个Fe原子紧邻的原子数为

(2)[Co(NH3)5Cl] Cl2是Co3+的一种重要配合物。
①1mol [Co(NH3)5Cl] Cl2与足量的硝酸银溶液反应产生
②Co3+的价层电子轨道表示式是
③1mol[Co(NH3)5Cl]2+中含有的
 键的数目为
键的数目为(3)第ⅤA族元素及其化合物的结构和性质如下:
①NH3、PH3、AsH3的沸点由高到低的顺序为
②某种氮化硼晶体的立方晶胞结构如图,该物质熔沸点高、硬度大与金刚石类似:

i.氮化硼属
ii.已知氮化硼晶胞的边长为a nm,则晶胞密度为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐1】NH3具有易液化、含氢密度高、应用广泛等优点,NH3的合成及应用一直是科学研究的重要课题。
(1)以H2、N2合成NH3,Fe是常用的催化剂。
①基态Fe原子的电子排布式为_______ 。
②实际生产中采用铁的氧化物Fe2O3、FeO,使用前用H2和N2的混合气体将它们还原为具有活性的金属铁。铁的两种晶胞(所示图形为正方体)结构示意如下:
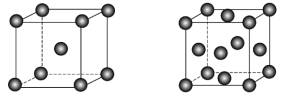
i.两种晶胞所含铁原子个数比为_______ 。
ii.图1晶胞的棱长为apm(1pm=1×10-10cm),则其密度ρ=_______ g·cm-3。
③我国科学家开发出Fe-LiH等双中心催化剂,在合成NH3中显示出高催化活性。第一电离能(I1):I1(H)>I1(Li)>I1(Na),原因是_______ 。
(2)化学工业科学家侯德榜利用下列反应最终制得了高质量的纯碱:NaCl+NH3+CO2+H2O=NaHCO3↓+NH4Cl
①1体积水可溶解1体积CO2,1体积水可溶解约700体积NH3,NH3极易溶于水的原因是_______ 。
②NaHCO3分解得Na2CO3, 空间结构为
空间结构为_______ 。
(3)NH3、NH3BH3(氨硼烷)储氢量高,是具有广泛应用前景的储氢材料。
①NH3BH3存在配位键,提供空轨道的是_______ 。
②比较熔点:NH3BH3_______ CH3CH3(填“>”或“<”)。
(1)以H2、N2合成NH3,Fe是常用的催化剂。
①基态Fe原子的电子排布式为
②实际生产中采用铁的氧化物Fe2O3、FeO,使用前用H2和N2的混合气体将它们还原为具有活性的金属铁。铁的两种晶胞(所示图形为正方体)结构示意如下:

i.两种晶胞所含铁原子个数比为
ii.图1晶胞的棱长为apm(1pm=1×10-10cm),则其密度ρ=
③我国科学家开发出Fe-LiH等双中心催化剂,在合成NH3中显示出高催化活性。第一电离能(I1):I1(H)>I1(Li)>I1(Na),原因是
(2)化学工业科学家侯德榜利用下列反应最终制得了高质量的纯碱:NaCl+NH3+CO2+H2O=NaHCO3↓+NH4Cl
①1体积水可溶解1体积CO2,1体积水可溶解约700体积NH3,NH3极易溶于水的原因是
②NaHCO3分解得Na2CO3,
 空间结构为
空间结构为(3)NH3、NH3BH3(氨硼烷)储氢量高,是具有广泛应用前景的储氢材料。
| 元素 | H | B | N |
| 电负性 | 2.1 | 2.0 | 3.0 |
①NH3BH3存在配位键,提供空轨道的是
②比较熔点:NH3BH3
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】已知A、B、C、D、E、F是原子序数依次增大的前四周期元素。其中A是宇宙中含量最多的元素;B元素原子最高能级的不同轨道都有电子,并且自旋方向相同;C元素原子的价层电子排布是 ;D元素原子中只有两种形状的电子云,最外层只有一种自旋方向的电子;E与D的最高能层数相同,但其最外层电子数等于其能层数。F元素原子的最外层只有一个电子,其次外层内的所有轨道的电子均成对。
;D元素原子中只有两种形状的电子云,最外层只有一种自旋方向的电子;E与D的最高能层数相同,但其最外层电子数等于其能层数。F元素原子的最外层只有一个电子,其次外层内的所有轨道的电子均成对。
(1)请用元素符号完成下列空白:
①A、B、C三种元素的电负性由大到小顺序为:___________ 。
②B、C、D、E 4种元素的第一电离能由大到小顺序为:___________ 。
(2)下面是A~F元素中某种元素的部分电离能,由此可判断该元素是___________ 。
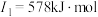
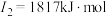
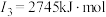
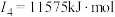
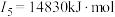
(3)F在周期表中的位置___________ ,位于周期表的___________ 区。
(4)BA3是一种很好的配体,BA3的沸点___________ (填“>”“=”或“<”)AsA3。
(5)B原子核外有___________ 种不同运动状态的电子;基态B原子中,能量最高的电子所占据的原子轨道的形状为___________ ;F原子核外电子占据的最高能层的符号是___________ 。
 ;D元素原子中只有两种形状的电子云,最外层只有一种自旋方向的电子;E与D的最高能层数相同,但其最外层电子数等于其能层数。F元素原子的最外层只有一个电子,其次外层内的所有轨道的电子均成对。
;D元素原子中只有两种形状的电子云,最外层只有一种自旋方向的电子;E与D的最高能层数相同,但其最外层电子数等于其能层数。F元素原子的最外层只有一个电子,其次外层内的所有轨道的电子均成对。(1)请用元素符号完成下列空白:
①A、B、C三种元素的电负性由大到小顺序为:
②B、C、D、E 4种元素的第一电离能由大到小顺序为:
(2)下面是A~F元素中某种元素的部分电离能,由此可判断该元素是
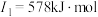
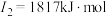
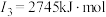
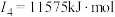
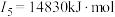
(3)F在周期表中的位置
(4)BA3是一种很好的配体,BA3的沸点
(5)B原子核外有
您最近一年使用:0次
【推荐3】石油裂解产生的乙烯含有0.5%~3%乙炔,乙炔在Ziegler-Natta催化剂中会使乙烯聚合失活。乙炔选择性加氢已经被证明是提纯乙烯最有效的技术之一。回答下列问题:
(1)已知25℃、101kPa下,相关物质的燃烧热数据如下表:
乙炔半氢化反应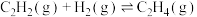 的
的 =
=_____________ 。
(2)在其他条件相同时,在不同的Pd基催化剂作用下,乙炔的转化率及乙烯的选择性随反应温度的变化如图a、b所示。已知:乙烯的选择性=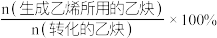 。
。______________ 。
②为保证该转化过程,需要过量的氢气,缺点是________________ 。
③某温度下,在刚性容器中发生乙炔半氢化反应,已知 与
与 的初始投料比[
的初始投料比[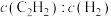 ]为1∶10,
]为1∶10, 的平衡转化率为90%(忽略其他副反应的发生)。若初始的总压强为
的平衡转化率为90%(忽略其他副反应的发生)。若初始的总压强为 ;则平衡时体系的压强=
;则平衡时体系的压强=___________ (用 列出计算式即可,下同);该反应的平衡常数
列出计算式即可,下同);该反应的平衡常数
___________ 。(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)
④制备基于MOFs(金属有机框架)薄膜材料为 /
/ 混合气体分离提供了一种经济高效的技术。该材料孔径大小和形状恰好将
混合气体分离提供了一种经济高效的技术。该材料孔径大小和形状恰好将 “固定”,能高效选择性吸附
“固定”,能高效选择性吸附 ,原理示意如图。
,原理示意如图。 最接近的是
最接近的是__________ 。(填标号)
A.利用 萃取碘水
萃取碘水
B.利用“杯酚”分离 和
和
C.利用饱和碳酸钠溶液除去乙酸乙酯中的少量乙酸
(3)在工业领域也可用N,N-二甲基甲酰胺(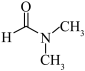 )粗乙烯中回收乙炔。N,N-二甲基甲酰胺是极性亲水性溶剂,其可与水任意比互溶的原因是
)粗乙烯中回收乙炔。N,N-二甲基甲酰胺是极性亲水性溶剂,其可与水任意比互溶的原因是__________________________ 。
(1)已知25℃、101kPa下,相关物质的燃烧热数据如下表:
物质 |
|
|
|
燃烧热(△H)/ | -1299.6 | -285.8 | -1411.0 |
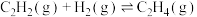 的
的 =
=(2)在其他条件相同时,在不同的Pd基催化剂作用下,乙炔的转化率及乙烯的选择性随反应温度的变化如图a、b所示。已知:乙烯的选择性=
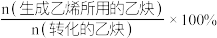 。
。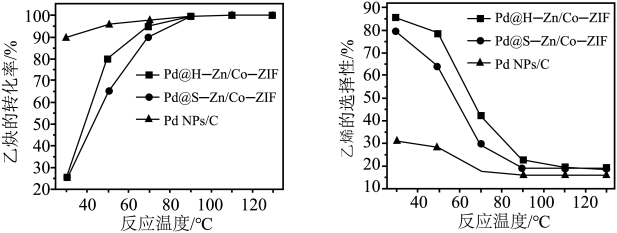
图a 图b
①若在实际生产中,选择Pd@H-Zn/Co-ZIF催化剂、50~60℃的反应条件,其依据是:②为保证该转化过程,需要过量的氢气,缺点是
③某温度下,在刚性容器中发生乙炔半氢化反应,已知
 与
与 的初始投料比[
的初始投料比[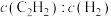 ]为1∶10,
]为1∶10, 的平衡转化率为90%(忽略其他副反应的发生)。若初始的总压强为
的平衡转化率为90%(忽略其他副反应的发生)。若初始的总压强为 ;则平衡时体系的压强=
;则平衡时体系的压强= 列出计算式即可,下同);该反应的平衡常数
列出计算式即可,下同);该反应的平衡常数
④制备基于MOFs(金属有机框架)薄膜材料为
 /
/ 混合气体分离提供了一种经济高效的技术。该材料孔径大小和形状恰好将
混合气体分离提供了一种经济高效的技术。该材料孔径大小和形状恰好将 “固定”,能高效选择性吸附
“固定”,能高效选择性吸附 ,原理示意如图。
,原理示意如图。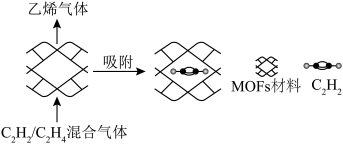
 最接近的是
最接近的是A.利用
 萃取碘水
萃取碘水B.利用“杯酚”分离
 和
和
C.利用饱和碳酸钠溶液除去乙酸乙酯中的少量乙酸
(3)在工业领域也可用N,N-二甲基甲酰胺(
 )粗乙烯中回收乙炔。N,N-二甲基甲酰胺是极性亲水性溶剂,其可与水任意比互溶的原因是
)粗乙烯中回收乙炔。N,N-二甲基甲酰胺是极性亲水性溶剂,其可与水任意比互溶的原因是
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】 广泛应用于太阳能电池领域。以
广泛应用于太阳能电池领域。以 、NaOH和抗坏血酸为原料,可制备
、NaOH和抗坏血酸为原料,可制备 。
。
(1)S、O两种元素可以形成多种阴离子,如 、
、 等,这两种离子的空间结构分别为:
等,这两种离子的空间结构分别为:_______ ,_______ 。
(2) 可用于制备
可用于制备 晶体,实验如下:
晶体,实验如下:
步骤1:向盛有硫酸铜水溶液的试管中边振荡边滴加氨水,观察到蓝色沉淀。
步骤2:继续滴加氨水至产生蓝色沉淀全部溶解,得到深蓝色的透明溶液。
步骤3:再向其中加入乙醇,析出深蓝色晶体。
①步骤1中生成的沉淀是_______ 。
② 中含有的
中含有的 键数为
键数为_______ 。
③步骤3中加入乙醇的作用是_______ 。
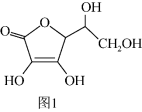
(3)抗坏血酸的分子结构如图1所示,分子中碳原子的轨道杂化类型为_______ ;根据电负性大小,抗坏血酸中显+1价的碳原子有_______ 个。
(4)一个 晶胞(见图2)中,Cu原子的数目为
晶胞(见图2)中,Cu原子的数目为_______ 。

 广泛应用于太阳能电池领域。以
广泛应用于太阳能电池领域。以 、NaOH和抗坏血酸为原料,可制备
、NaOH和抗坏血酸为原料,可制备 。
。(1)S、O两种元素可以形成多种阴离子,如
 、
、 等,这两种离子的空间结构分别为:
等,这两种离子的空间结构分别为:(2)
 可用于制备
可用于制备 晶体,实验如下:
晶体,实验如下:步骤1:向盛有硫酸铜水溶液的试管中边振荡边滴加氨水,观察到蓝色沉淀。
步骤2:继续滴加氨水至产生蓝色沉淀全部溶解,得到深蓝色的透明溶液。
步骤3:再向其中加入乙醇,析出深蓝色晶体。
①步骤1中生成的沉淀是
②
 中含有的
中含有的 键数为
键数为③步骤3中加入乙醇的作用是
(3)抗坏血酸的分子结构如图1所示,分子中碳原子的轨道杂化类型为

(4)一个
 晶胞(见图2)中,Cu原子的数目为
晶胞(见图2)中,Cu原子的数目为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】常见的太阳能电池有硅太阳能电池、镓(Ga)砷(As)太阳能电池及铜铟镓硒薄膜太阳能电池等。下列有关它们的化合物的问题,请回答:
(1)基态Ga原子的电子排布式为________ ;H2O的沸点高于H2Se的沸点(-42℃),其原因是__________ 。
(2)Na3AsO4中阴离子的空间构型为________ ,As原子采取________ 杂化。
(3)晶体Si、SiC、SiO2都属于原子晶体,请写出它们的熔点从高到低的顺序排列________ 。
(4)高温下CuO容易转化为Cu2O,试从原子结构角度解释原因______________ 。
(5)银与铜位于同一副族。氟化银具有氯化钠型结构,其中的阴离子采用面心立方最密堆积方式,氯化钠的晶胞结构如图所示。则Ag+周围等距离且最近的F−在空间围成的几何构型为_______ ,已知氟化银的密度为d g·cm−3,则氟化银晶胞的晶胞参数为_______ nm(不必简化)。

(1)基态Ga原子的电子排布式为
(2)Na3AsO4中阴离子的空间构型为
(3)晶体Si、SiC、SiO2都属于原子晶体,请写出它们的熔点从高到低的顺序排列
(4)高温下CuO容易转化为Cu2O,试从原子结构角度解释原因
(5)银与铜位于同一副族。氟化银具有氯化钠型结构,其中的阴离子采用面心立方最密堆积方式,氯化钠的晶胞结构如图所示。则Ag+周围等距离且最近的F−在空间围成的几何构型为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】A、B、C、D、E代表前四周期原子序数依次增大的五种元素。A、D同主族且有两种常见化合物DA2和DA3;工业上电解熔融C2A3制取单质C;B、E除最外层均只有2个电子外,其余各层全充满,E位于元素周期表的ds区。回答下列问题:
(1)B、C中第一电离能较大的是___ ,基态D原子价电子的轨道表达式为___ ,DA2分子的VSEPR模型是___ 。
(2)实验测得C与氯元素形成化合物的实际组成为C2Cl6,其球棍模型如图1所示。已知C2Cl6在加热时易升华,与过量的NaOH溶液反应可生成Na[C(OH)4]。
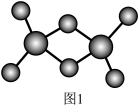
①C2Cl6属于___ 晶体(填晶体类型),其中C原子的杂化轨道类型为___ 杂化。
②[C(OH)4]-中存在的化学键有___ 。
③C2Cl6与过量的NaOH溶液反应的化学方程式为___ 。
(3)B、C的氟化物晶格能分别是2957kJ•mol-1、5492kJ•mol-1,二者相差很大的原因是___ 。
(4)D与E所形成化合物晶体的晶胞如图2所示。
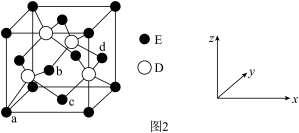
①在该晶胞中,E的配位数为___ 。
②已知该晶胞的密度为ρg/cm3,则其中两个D原子之间的距离为___ pm(列出计算式即可)。
(1)B、C中第一电离能较大的是
(2)实验测得C与氯元素形成化合物的实际组成为C2Cl6,其球棍模型如图1所示。已知C2Cl6在加热时易升华,与过量的NaOH溶液反应可生成Na[C(OH)4]。

①C2Cl6属于
②[C(OH)4]-中存在的化学键有
③C2Cl6与过量的NaOH溶液反应的化学方程式为
(3)B、C的氟化物晶格能分别是2957kJ•mol-1、5492kJ•mol-1,二者相差很大的原因是
(4)D与E所形成化合物晶体的晶胞如图2所示。

①在该晶胞中,E的配位数为
②已知该晶胞的密度为ρg/cm3,则其中两个D原子之间的距离为
您最近一年使用:0次




