资料显示, 可以将
可以将 氧化为
氧化为 。某小组同学设计实验探究
。某小组同学设计实验探究 被
被 氧化的产物及铜元素的价态。
氧化的产物及铜元素的价态。
已知: 易溶于
易溶于 溶液,发生反应
溶液,发生反应 (红棕色);
(红棕色); 和
和 氧化性几乎相同。
氧化性几乎相同。
I.将等体积的 溶液加入到
溶液加入到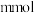 铜粉和
铜粉和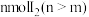 的固体混合物中,振荡。
的固体混合物中,振荡。
实验记录如下:
实验Ⅲ所得溶液中,被氧化的铜元素的可能存在形式有 (蓝色)或
(蓝色)或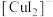 (无色),进行以下实验探究:
(无色),进行以下实验探究:
步骤a.取实验Ⅲ的深红棕色溶液,加入 ,多次萃取、分液。
,多次萃取、分液。
步骤b.取分液后的无色水溶液,滴入浓氨水。溶液颜色变浅蓝色,并逐渐变深。
ⅰ.步骤a的目的是_______ 。
ⅱ.查阅资料, ,
, (无色)容易被空气氧化。用离子方程式解释步骤
(无色)容易被空气氧化。用离子方程式解释步骤 的溶液中发生的变化:
的溶液中发生的变化:_______ 。
 可以将
可以将 氧化为
氧化为 。某小组同学设计实验探究
。某小组同学设计实验探究 被
被 氧化的产物及铜元素的价态。
氧化的产物及铜元素的价态。已知:
 易溶于
易溶于 溶液,发生反应
溶液,发生反应 (红棕色);
(红棕色); 和
和 氧化性几乎相同。
氧化性几乎相同。I.将等体积的
 溶液加入到
溶液加入到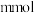 铜粉和
铜粉和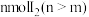 的固体混合物中,振荡。
的固体混合物中,振荡。实验记录如下:
 | 实验现象 | |
| 实验Ⅰ |  | 极少量 溶解,溶液为淡红色;充分反应后,红色的铜粉转化为白色沉淀,溶液仍为淡红色 溶解,溶液为淡红色;充分反应后,红色的铜粉转化为白色沉淀,溶液仍为淡红色 |
| 实验Ⅱ |  | 部分 溶解,溶液为红棕色;充分反应后,红色的铜粉转化为白色沉淀,溶液仍为红棕色 溶解,溶液为红棕色;充分反应后,红色的铜粉转化为白色沉淀,溶液仍为红棕色 |
| 实验Ⅲ |  |  完全溶解,溶液为深红棕色;充分反应后,红色的铜粉完全溶解,溶液为深红棕色 完全溶解,溶液为深红棕色;充分反应后,红色的铜粉完全溶解,溶液为深红棕色 |
 (蓝色)或
(蓝色)或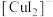 (无色),进行以下实验探究:
(无色),进行以下实验探究:步骤a.取实验Ⅲ的深红棕色溶液,加入
 ,多次萃取、分液。
,多次萃取、分液。步骤b.取分液后的无色水溶液,滴入浓氨水。溶液颜色变浅蓝色,并逐渐变深。
ⅰ.步骤a的目的是
ⅱ.查阅资料,
 ,
, (无色)容易被空气氧化。用离子方程式解释步骤
(无色)容易被空气氧化。用离子方程式解释步骤 的溶液中发生的变化:
的溶液中发生的变化:
2024高三下·全国·专题练习 查看更多[1]
(已下线)大题02 化学实验综合题(逐空突破)-【大题精做】冲刺2024年高考化学大题突破+限时集训(新高考专用)
更新时间:2024-04-20 06:34:12
|
相似题推荐
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】配位化合物在生产生活中有重要应用,请根据要求回答下列问题:
(1)Ni2+可以形成多种配离子,如[Ni(NH3)4]2+、[Ni(CN)4]2-、丁二酮肟镍分子(见图)等。

①1mol[Ni(NH3)4]2+中含有_____ molσ键。
②[Ni(NH3)4]2+中H-N-H键角比NH3分子中H-N-H键角______ (填“大”或“小”)。
③丁二酮肟镍分子内含有的作用力有______ (填字母)。
a.配位键 b.离子键 c.氢键 d.范德华力
(2)Co(NH3)5BrSO4可形成两种钴的配合物,已知Co3+的配位数是6,为确定钴的配合物的结构,现对两种配合物进行了如下实验:在第一种配合物的溶液中加BaCl2溶液时,产生白色沉淀,在第二种配合物的溶液中加BaCl2溶液时,则无明显现象。则第一种配合物的结构式可表示为______ ,第二种配合物的结构式可表示为______ 。若在第二种配合物的溶液中滴加AgNO3溶液,则产生的现象是______ 。
(3)关于[Ti(NH3)5Cl]Cl2的说法中错误的是______ 。
A.中心原子的化合价为+3价
B.中心原子的配位数是6
C.含1mol[Ti(NH3)5Cl]Cl2的水溶液中加入足量AgNO3溶液,产生3mol白色沉淀
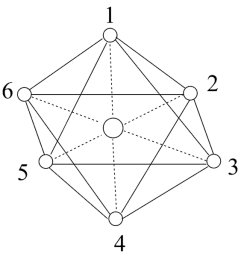
(4)已知[Co(NH3)6]3+的立体结构如图,其中1~6处的小圆圈表示NH3分子,且各相邻的NH3分子间的距离相等(图中虚线长度相等)。Co3+位于八面体的中心,若其中两个NH3被Cl-取代,所形成的[Co(NH3)4Cl2]+的结构的数目为______ 。
(1)Ni2+可以形成多种配离子,如[Ni(NH3)4]2+、[Ni(CN)4]2-、丁二酮肟镍分子(见图)等。

①1mol[Ni(NH3)4]2+中含有
②[Ni(NH3)4]2+中H-N-H键角比NH3分子中H-N-H键角
③丁二酮肟镍分子内含有的作用力有
a.配位键 b.离子键 c.氢键 d.范德华力
(2)Co(NH3)5BrSO4可形成两种钴的配合物,已知Co3+的配位数是6,为确定钴的配合物的结构,现对两种配合物进行了如下实验:在第一种配合物的溶液中加BaCl2溶液时,产生白色沉淀,在第二种配合物的溶液中加BaCl2溶液时,则无明显现象。则第一种配合物的结构式可表示为
(3)关于[Ti(NH3)5Cl]Cl2的说法中错误的是
A.中心原子的化合价为+3价
B.中心原子的配位数是6
C.含1mol[Ti(NH3)5Cl]Cl2的水溶液中加入足量AgNO3溶液,产生3mol白色沉淀
(4)已知[Co(NH3)6]3+的立体结构如图,其中1~6处的小圆圈表示NH3分子,且各相邻的NH3分子间的距离相等(图中虚线长度相等)。Co3+位于八面体的中心,若其中两个NH3被Cl-取代,所形成的[Co(NH3)4Cl2]+的结构的数目为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】(1)Co的氯化物与氨水反应可形成配合物[CoCl(NH3)5]Cl2 ,1 mol该配合物中含有σ键的数目为_____ ,含1 mol [CoCl(NH3)5]Cl2的溶液中加入足量AgNO3溶液,生成______ mol AgCl沉淀。
(2)关于化合物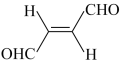 ,下列叙述正确的有
,下列叙述正确的有________ 。
A.分子间可形成氢键 B.分子中既有极性键又有非极性键
C.分子中有7个σ键和1个π键 D.该分子在水中的溶解度大于2-丁烯
(3) Al2O3、SiC、Si、金刚石中属于原子晶体的有______________ ,其熔点高低顺序为___________ ,其理由是__________ 。
(4)H3O+中H—O—H键角比H2O中H—O—H 键角_____ (填“大”或“小”),原因为________ 。
(2)关于化合物
 ,下列叙述正确的有
,下列叙述正确的有A.分子间可形成氢键 B.分子中既有极性键又有非极性键
C.分子中有7个σ键和1个π键 D.该分子在水中的溶解度大于2-丁烯
(3) Al2O3、SiC、Si、金刚石中属于原子晶体的有
(4)H3O+中H—O—H键角比H2O中H—O—H 键角
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】氟元素可形成多种有工业价值和科研价值的化合物,如OF2、(CF)x、XeF2、HF、NH4BF4、CaF2等。
(1)基态F原子核外电子有______ 种空间运动状态,下列为氟原子激发态的电子排布式的是_____ (填序号)。
A.1s22s22p43s1 B.1s22s22p43d2 C.1s22s12p2 D.1s22s22p33p2
(2)F2通入稀NaOH溶液中可生成OF2,其中氧原子的杂化方式为_________ 。
(3)AlF3的熔点为1090℃,远高于AlCl3的熔点(192℃),其原因是___________ 。
(4)石墨与F2在450℃反应,石墨层间插入F得到层状结构化合物(CF)x,该物质仍具有润滑性,其单层局部结构如图所示。与石墨相比,(CF)x的导电性________ (填“增强”或“减弱”),(CF)x中C-C键的键长比石墨中C-C键的_______ (填“长”或“短”)。

(5)芯片制造会经过六个最为关键的步骤:沉积、光刻胶涂覆、光刻、刻蚀、离子注入和封装。其中“刻蚀”过程可能用到刻蚀剂HF、NH4BF4及清洗剂CH3CH(OH)CH3,三种物质中除H外的各元素的电负性由大到小的顺序为________ ,1mol氟硼酸铵(NH4BF4)中含有_______ mol配位键。
(1)基态F原子核外电子有
A.1s22s22p43s1 B.1s22s22p43d2 C.1s22s12p2 D.1s22s22p33p2
(2)F2通入稀NaOH溶液中可生成OF2,其中氧原子的杂化方式为
(3)AlF3的熔点为1090℃,远高于AlCl3的熔点(192℃),其原因是
(4)石墨与F2在450℃反应,石墨层间插入F得到层状结构化合物(CF)x,该物质仍具有润滑性,其单层局部结构如图所示。与石墨相比,(CF)x的导电性

(5)芯片制造会经过六个最为关键的步骤:沉积、光刻胶涂覆、光刻、刻蚀、离子注入和封装。其中“刻蚀”过程可能用到刻蚀剂HF、NH4BF4及清洗剂CH3CH(OH)CH3,三种物质中除H外的各元素的电负性由大到小的顺序为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】化学兴趣小组的同学们设计了如图装置验证乙醇催化氧化的产物(加热仪器、夹持装置已略去)。
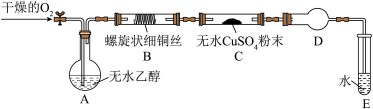
已知:乙醇的沸点为78℃,易溶于水;乙醛的沸点为20.8℃,易溶于水。
(1)乙醇催化氧化反应的化学方程式是________ 。
(2)实验时上述装置中需要加热的是_______ (填序号,下同),其中应该先加热的是____ ,为使装置A中的乙醇成为蒸气,最简单的加热方法是______ 。
(3)实验室制取氧气的化学方程式是________ 。
(4)实验开始后,装置B中能观察到的现象是______ ;装置C中能观察到的现象是______ ,由此得出的结论是_______ 。
(5)装置E的作用是_______ ,能初步判定反应后有乙醛生成的依据是________ 。
(6)装置D中的药品是______ ,其作用是_______ 。

已知:乙醇的沸点为78℃,易溶于水;乙醛的沸点为20.8℃,易溶于水。
(1)乙醇催化氧化反应的化学方程式是
(2)实验时上述装置中需要加热的是
(3)实验室制取氧气的化学方程式是
(4)实验开始后,装置B中能观察到的现象是
(5)装置E的作用是
(6)装置D中的药品是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】如图是实验室制备氯气并进行一系列相关实验的装置(夹持及加热仪器已略)。
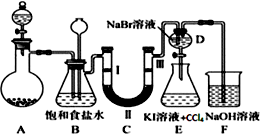
(1)装置 A 中反应的化学反应方程式为:________________________________ 。装置 B 中饱和食盐水的作用是___________________ ;同时装置 B 亦是安全瓶,监测实验进行时C中是否发生堵塞,请写出发生堵塞时 B 中的现象________________________________ 。
(2)装置 C 的实验目的是验证氯气是否具有漂白性,为此 C 中Ⅰ、Ⅱ、Ⅲ依次放入_____________ 。(填序号)
(3)设计装置 D、 E 的目的是验证氯、溴、碘单质的氧化性强弱(Cl2> Br2>I2),当向D中缓缓通入少量氯气时,可以看到无色溶液逐渐变为橙黄色,说明Cl2氧化性>Br2,打开活塞,将装置D中少量溶液加入装置 E中,振荡,观察到的现象是________________________________ 。
(4)工业上将氯气通入石灰乳制取漂白粉, 化学反应方程式为_____________________________ ,漂白粉敞放于空气中会失效,请写出失效所发生反应的化学方程式_____________________________ 。

(1)装置 A 中反应的化学反应方程式为:
(2)装置 C 的实验目的是验证氯气是否具有漂白性,为此 C 中Ⅰ、Ⅱ、Ⅲ依次放入
| a | b | c | d | |
| Ⅰ | 干燥的有色布条 | 干燥的有色布条 | 湿润的有色布条 | 湿润的有色布条 |
| Ⅱ | 碱石灰 | 硅胶 | 浓硫酸 | 无水氯化钙 |
| Ⅲ | 湿润的有色布条 | 湿润的有色布条 | 干燥的有色布条 | 干燥的有色布条 |
(4)工业上将氯气通入石灰乳制取漂白粉, 化学反应方程式为
您最近一年使用:0次
【推荐3】为了检验淀粉水解的产物,设计如下实验方案:
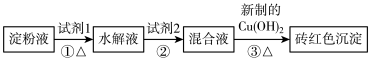
请回答下列问题:
(1)试剂1为20%的H2SO4溶液,其作用是____________________________________ 。
(2)试剂2为______________ ,其作用是__________________ ,使检验水解产物的实验得以顺利进行。
(3)反应①的化学方程式为__________________________________________________ 。
(4)为检验淀粉液是否已完全水解,取少量水解液于试管中,加入碘水,则证明淀粉未完全水解的现象是__________ 。
(5)如果实验过程中没有加入试剂2而直接加入试剂3,能否实现实验目的________ (填”能”或”否”),若不能,其原因是_____________________________ 。

请回答下列问题:
(1)试剂1为20%的H2SO4溶液,其作用是
(2)试剂2为
(3)反应①的化学方程式为
(4)为检验淀粉液是否已完全水解,取少量水解液于试管中,加入碘水,则证明淀粉未完全水解的现象是
(5)如果实验过程中没有加入试剂2而直接加入试剂3,能否实现实验目的
您最近一年使用:0次



