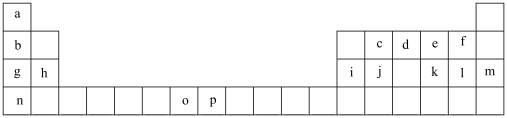
下表是元素周期表的一部分,表中所列的字母分别代表一种化学元素。试回答下列问题。_______ (用元素符号表示),1和n的离子半径较大的是_______ (填离子符号)。
(2)h的单质在空气中燃烧发出耀眼的白光,从原子结构角度解释是涉及电子从能量较高的轨道跃迁到能量较低的轨道时,以光(子)的形式释放能量,以下现象与该原理一样的是_______ (填字母)。
A.燃放焰火 B.棱镜分出的光 C.霓虹灯射出五颜六色的光
(3)o、p两元素的部分电离能数据如下表所示。
比较两元素的 、
、 可知,气态
可知,气态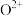 再失去一个电子比气态
再失去一个电子比气态 再失去一个电子难。对此,你认为原因可能是
再失去一个电子难。对此,你认为原因可能是_______ 。
(4)第三周期8种元素其中电负性最大的是_______ (填图中的序号)。
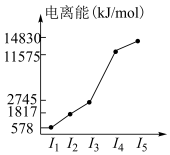
(5)表中所列的某主族元素的电离能情况如图所示,写出该元素的最高价氧化物对应的水化物与g的最高价氧化物对应的水化物反应的离子方程式:_______ 。
(2)h的单质在空气中燃烧发出耀眼的白光,从原子结构角度解释是涉及电子从能量较高的轨道跃迁到能量较低的轨道时,以光(子)的形式释放能量,以下现象与该原理一样的是
A.燃放焰火 B.棱镜分出的光 C.霓虹灯射出五颜六色的光
(3)o、p两元素的部分电离能数据如下表所示。
电离能/ |  |  |  |
| o | 717 | 1509 | 3248 |
| p | 759 | 1561 | 2957 |
 、
、 可知,气态
可知,气态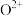 再失去一个电子比气态
再失去一个电子比气态 再失去一个电子难。对此,你认为原因可能是
再失去一个电子难。对此,你认为原因可能是(4)第三周期8种元素其中电负性最大的是
(5)表中所列的某主族元素的电离能情况如图所示,写出该元素的最高价氧化物对应的水化物与g的最高价氧化物对应的水化物反应的离子方程式:
更新时间:2024-05-05 16:37:44
|
相似题推荐
解答题-结构与性质
|
适中
(0.65)
名校
【推荐1】A、X、Y、Z、Q、R、T分别代表原子序数依次增大的短周期元素。元素A是原子半径最小的元素;X、Y、Z同周期且相邻,都是蛋白质的组成元素;X、R同族,Q与T原子的最外层电子数之和是R原子最外层电子数的2倍,T单质为淡黄色固体。U是d区元素,U2+的核外最高能级有2对成对电子。请回答下列问题:
(1)Y元素在周期表中的位置____________ ,位于周期表_____ 区;Q原子的核外电子排布式为________ 。
(2)X、Y、Z元素的第一电离能由大到小的顺序是________________ 。
(3)TZ3分子为________ 分子(填“极性”或“非极性”),YZ2-离子的VSEPR模型名称是________ 。
(4)Z和T的简单气态氢化物稳定性好的是_______ (填化学式),原因是________________________________________________________________ 。
(5)A、X、Z、可形成分子式为A2XZ的有机物,则该化合物分子中B原子的轨道杂化类型是________ ;1mol该分子中含有π键的数目是________ 。
(6)通常情况下,U2+的溶液很稳定,它与YH3形成的配位数为6的配离子却不稳定,在空气中易被氧化为配位数不变的+3价配离子.该反应的离子方程式是________________________________________________________________________ 。
(1)Y元素在周期表中的位置
(2)X、Y、Z元素的第一电离能由大到小的顺序是
(3)TZ3分子为
(4)Z和T的简单气态氢化物稳定性好的是
(5)A、X、Z、可形成分子式为A2XZ的有机物,则该化合物分子中B原子的轨道杂化类型是
(6)通常情况下,U2+的溶液很稳定,它与YH3形成的配位数为6的配离子却不稳定,在空气中易被氧化为配位数不变的+3价配离子.该反应的离子方程式是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】根据信息回答问题:
(1)实验测得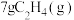 在氧气中充分燃烧生成二氧化碳气体和液态水时释放出352.75kJ的热量,试写出
在氧气中充分燃烧生成二氧化碳气体和液态水时释放出352.75kJ的热量,试写出 燃烧热的热化学方程式:
燃烧热的热化学方程式:_________________________________________ 。
(2)已知反应: .有关键能数据如下:
.有关键能数据如下: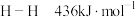 ,
,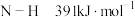 ,
,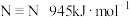 ,根据键能数据计算
,根据键能数据计算
___________ 。
(3)已知: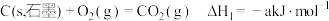 ;
;
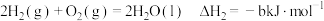 ;
;
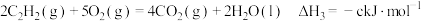 ;
;
根据盖斯定律,计算 时由
时由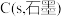 和
和 生成
生成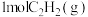 反应的反应热为:
反应的反应热为:
____________  。
。
(4)已知:A,B,C,D四种短周期元素的原子半径依次减小,D能分别与A,B,C形成电子总数相等的分子X、Y、Z。C原子的最外层电子排布为 。E的原子序数为29.回答下列问题:
。E的原子序数为29.回答下列问题:
①A,B,C的第一电离能由小到大的顺序为____________________ (用元素符号表示)。
②C元素原子核外有_______ 个原子轨道。
③E元素在周期表中属于_______ 区元素。写出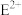 的电子排布式
的电子排布式_______________________ 。
(1)实验测得
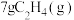 在氧气中充分燃烧生成二氧化碳气体和液态水时释放出352.75kJ的热量,试写出
在氧气中充分燃烧生成二氧化碳气体和液态水时释放出352.75kJ的热量,试写出 燃烧热的热化学方程式:
燃烧热的热化学方程式:(2)已知反应:
 .有关键能数据如下:
.有关键能数据如下: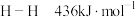 ,
,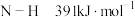 ,
,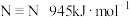 ,根据键能数据计算
,根据键能数据计算
(3)已知:
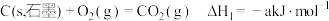 ;
;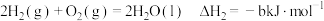 ;
;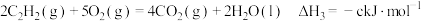 ;
;根据盖斯定律,计算
 时由
时由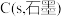 和
和 生成
生成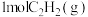 反应的反应热为:
反应的反应热为:
 。
。(4)已知:A,B,C,D四种短周期元素的原子半径依次减小,D能分别与A,B,C形成电子总数相等的分子X、Y、Z。C原子的最外层电子排布为
 。E的原子序数为29.回答下列问题:
。E的原子序数为29.回答下列问题:①A,B,C的第一电离能由小到大的顺序为
②C元素原子核外有
③E元素在周期表中属于
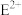 的电子排布式
的电子排布式
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】A、B、C、D、E、F均为36号以前的元素且原子序数依次增大。请完成下列空白:
(1)A元素基态原子的最外层有2个未成对电子,次外层有2个电子,它的原子核外电子共与_____ 种不同的运动状态,原子轨道数目为_______ 。
(2)B元素的原子最外层电子排布式为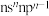 ,其简单氢化物的电子式为
,其简单氢化物的电子式为______ 。
(3)C、D原子核外s能级上的电子总数与p能级上的电子总数均相等。C、D简单离子的半径由大小到的顺序是______ (用离子符号填空)。A、B、C、D四种元素的原子半径由大到小的顺序是_______ (用元素符号填空,下同),四种元素的电负性由到大到小的顺序是________ ,四种元素的第一电离能由大到小的顺序是_______ 。
(4)E、F均位于ds区。则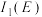
_____ 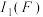 (填“>”或“<”),理由是
(填“>”或“<”),理由是___________ 。
(1)A元素基态原子的最外层有2个未成对电子,次外层有2个电子,它的原子核外电子共与
(2)B元素的原子最外层电子排布式为
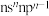 ,其简单氢化物的电子式为
,其简单氢化物的电子式为(3)C、D原子核外s能级上的电子总数与p能级上的电子总数均相等。C、D简单离子的半径由大小到的顺序是
(4)E、F均位于ds区。则
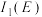
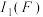 (填“>”或“<”),理由是
(填“>”或“<”),理由是
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】铬、铁、钴、铜等金属及其化合物在工业上有重要用途。请回答:
(1)基态铬原子的价电子排布图为___________ 。
(2)CrO2Cl2和NaClO均可作化工生产的氧化剂或氯化剂。制备CrO2Cl2的反应为K2Cr2O2+3CCl4=2KCl +2CrO2Cl2+3COCl2↑。
①上述反应式中非金属元素电负性由大到小的顺序是__________ (用元素符号表示)。
②常温时CrO2Cl2是一种易溶于CCl4的液体,则固态CrO2Cl2属于__________ 晶体。
③配合物CrCl3·6H2O中心离子Cr3+的配位数为6,向含0.1molCrCl3·6H2O 的溶液中滴加2mol·L-1 AgNO3溶液,反应完全后共消耗AgNO3溶液50mL,则配离子的化学式为___________ 。
(3)Co3+与NO2―形成的配合物与K+生成黄色沉淀检验溶液中的K+。配体NO2―的立体构型为__________ ,某常见气体化合物为NO2―的等电子体,该化合物的分子式为__________ 。
(4)氯和钾与+2价的铜可生成一种催化乙炔聚合反应的化合物,其阴离子为无限长链结构(如下图),a位置上Cl原子的杂化轨道类型为________ 杂化,这种化合物的化学式为_________

(5)铁和氨气在640 ℃可发生置换反应,产物之一的晶胞结构如图所示,写出该反应的化学方程式:_____ 。若两个最近的Fe原子间的距离为a cm,则该晶体的密度是_____ g/cm3(设阿伏加 德罗常数的值为NA)。

(1)基态铬原子的价电子排布图为
(2)CrO2Cl2和NaClO均可作化工生产的氧化剂或氯化剂。制备CrO2Cl2的反应为K2Cr2O2+3CCl4=2KCl +2CrO2Cl2+3COCl2↑。
①上述反应式中非金属元素电负性由大到小的顺序是
②常温时CrO2Cl2是一种易溶于CCl4的液体,则固态CrO2Cl2属于
③配合物CrCl3·6H2O中心离子Cr3+的配位数为6,向含0.1molCrCl3·6H2O 的溶液中滴加2mol·L-1 AgNO3溶液,反应完全后共消耗AgNO3溶液50mL,则配离子的化学式为
(3)Co3+与NO2―形成的配合物与K+生成黄色沉淀检验溶液中的K+。配体NO2―的立体构型为
(4)氯和钾与+2价的铜可生成一种催化乙炔聚合反应的化合物,其阴离子为无限长链结构(如下图),a位置上Cl原子的杂化轨道类型为

(5)铁和氨气在640 ℃可发生置换反应,产物之一的晶胞结构如图所示,写出该反应的化学方程式:

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】海军成立68周年时,我国第一艘国产航母成功下水。建造航母需要大量的新型材料。航母的龙骨要耐冲击,航母的甲板要耐高温,航母的外壳要耐腐蚀。
(1)镍铬钢就是抗腐蚀性能强的新型材料。
①基态Ni原子的电子排布式为________________ ,铬元素在周期表中____ 区。
②Ni能与CO形成正四面体形的配合物Ni(CO)4,1 mol Ni(CO)4中含有________ mol σ键。
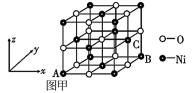
③NiO的晶体结构如图甲所示,其中离子坐标参数 A 为(0,0,0),B为(1,1,0),则C离子坐标参数为____ 。
(2)海洋底部有储量丰富的可燃冰,一定条件下,CH4、CO2都能与H2O形成笼状结构(如下图所示)的水合物晶体,其相关参数见下表。CH4与H2O形成的水合物晶体俗称“可燃冰”。
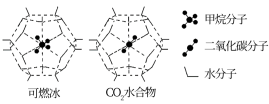
①“可燃冰”中分子间存在的2种作用力是_____________________ 。
②为开采深海海底的“可燃冰”,有科学家提出用CO2置换CH4的设想。已知如图中笼状结构的空腔直径为0.586 nm,根据上述图表,从物质结构及性质的角度分析,该设想的依据是___________________________________ 。

(3)①CH4和CO2所含的三种元素电负性从小到大的顺序为_______________
②碳的另一种同素异形体——石墨,其晶体结构如图所示,则石墨晶胞含碳原子个数为____ 个.已知石墨的密度为ρ g·cm—3,C—C键长为r cm,阿伏加 德罗常数的值为NA,计算石墨晶体的层间距为__________ cm。

(1)镍铬钢就是抗腐蚀性能强的新型材料。
①基态Ni原子的电子排布式为
②Ni能与CO形成正四面体形的配合物Ni(CO)4,1 mol Ni(CO)4中含有
③NiO的晶体结构如图甲所示,其中离子坐标参数 A 为(0,0,0),B为(1,1,0),则C离子坐标参数为
(2)海洋底部有储量丰富的可燃冰,一定条件下,CH4、CO2都能与H2O形成笼状结构(如下图所示)的水合物晶体,其相关参数见下表。CH4与H2O形成的水合物晶体俗称“可燃冰”。

| 参数 分子 | 分子直径/nm | 分子与H2O的结合能 E/kJ·mol-1 |
| CH4 | 0.436 | 16.40 |
| CO2 | 0.512 | 29.91 |
①“可燃冰”中分子间存在的2种作用力是
②为开采深海海底的“可燃冰”,有科学家提出用CO2置换CH4的设想。已知如图中笼状结构的空腔直径为0.586 nm,根据上述图表,从物质结构及性质的角度分析,该设想的依据是

(3)①CH4和CO2所含的三种元素电负性从小到大的顺序为
②碳的另一种同素异形体——石墨,其晶体结构如图所示,则石墨晶胞含碳原子个数为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】不同元素的原子在分子内吸引电子的能力大小可用一定数值x来表示,该数值称为电负性。若x越大,其原子吸引电子的能力越强,在所形成的分子中成为带负电荷的一方。下面是某些短周期元素的x值:
(1)推测在同周期的元素中x值与原子半径的关系是________________ 。短周期元素x值的变化特点,体现了元素性质的________ 变化规律。
(2)通过分析x值的变化规律,确定Mg、N的x值范围:________ <x(Mg)<______ ,______ <x(N)<________ 。
(3)在P—N键中,共用电子对偏向________ 原子。
(4)根据Be和Al在元素周期表中的位置及其电负性的大小,二者符合对角线规则。试写出Be(OH)2分别与盐酸、氢氧化钠溶液反应的离子方程式_________ 、___________ 。
(5)经验规律告诉我们:当成键的两原子相应元素的x差值即Δx>1.7时,一般为离子键;Δx<1.7时,一般为共价键。试推断:AlBr3中化学键类型是________ 。请设计一个实验方案证明上述所得到的结论:________________
| 元素符号 | Li | Be | B | C | O | F |
| x值 | 0.98 | 1.57 | 2.04 | 2.25 | 3.44 | 3.98 |
| 元素符号 | Na | Al | Si | P | S | Cl |
| x值 | 0.93 | 1.61 | 1.90 | 2.19 | 2.58 | 3.16 |
(1)推测在同周期的元素中x值与原子半径的关系是
(2)通过分析x值的变化规律,确定Mg、N的x值范围:
(3)在P—N键中,共用电子对偏向
(4)根据Be和Al在元素周期表中的位置及其电负性的大小,二者符合对角线规则。试写出Be(OH)2分别与盐酸、氢氧化钠溶液反应的离子方程式
(5)经验规律告诉我们:当成键的两原子相应元素的x差值即Δx>1.7时,一般为离子键;Δx<1.7时,一般为共价键。试推断:AlBr3中化学键类型是
您最近一年使用:0次



