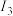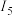海军成立68周年时,我国第一艘国产航母成功下水。建造航母需要大量的新型材料。航母的龙骨要耐冲击,航母的甲板要耐高温,航母的外壳要耐腐蚀。
(1)镍铬钢就是抗腐蚀性能强的新型材料。
①基态Ni原子的电子排布式为________________ ,铬元素在周期表中____ 区。
②Ni能与CO形成正四面体形的配合物Ni(CO)4,1 mol Ni(CO)4中含有________ mol σ键。
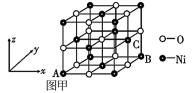
③NiO的晶体结构如图甲所示,其中离子坐标参数 A 为(0,0,0),B为(1,1,0),则C离子坐标参数为____ 。
(2)海洋底部有储量丰富的可燃冰,一定条件下,CH4、CO2都能与H2O形成笼状结构(如下图所示)的水合物晶体,其相关参数见下表。CH4与H2O形成的水合物晶体俗称“可燃冰”。
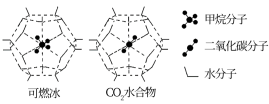
①“可燃冰”中分子间存在的2种作用力是_____________________ 。
②为开采深海海底的“可燃冰”,有科学家提出用CO2置换CH4的设想。已知如图中笼状结构的空腔直径为0.586 nm,根据上述图表,从物质结构及性质的角度分析,该设想的依据是___________________________________ 。

(3)①CH4和CO2所含的三种元素电负性从小到大的顺序为_______________
②碳的另一种同素异形体——石墨,其晶体结构如图所示,则石墨晶胞含碳原子个数为____ 个.已知石墨的密度为ρ g·cm—3,C—C键长为r cm,阿伏加 德罗常数的值为NA,计算石墨晶体的层间距为__________ cm。

(1)镍铬钢就是抗腐蚀性能强的新型材料。
①基态Ni原子的电子排布式为
②Ni能与CO形成正四面体形的配合物Ni(CO)4,1 mol Ni(CO)4中含有
③NiO的晶体结构如图甲所示,其中离子坐标参数 A 为(0,0,0),B为(1,1,0),则C离子坐标参数为
(2)海洋底部有储量丰富的可燃冰,一定条件下,CH4、CO2都能与H2O形成笼状结构(如下图所示)的水合物晶体,其相关参数见下表。CH4与H2O形成的水合物晶体俗称“可燃冰”。

| 参数 分子 | 分子直径/nm | 分子与H2O的结合能 E/kJ·mol-1 |
| CH4 | 0.436 | 16.40 |
| CO2 | 0.512 | 29.91 |
①“可燃冰”中分子间存在的2种作用力是
②为开采深海海底的“可燃冰”,有科学家提出用CO2置换CH4的设想。已知如图中笼状结构的空腔直径为0.586 nm,根据上述图表,从物质结构及性质的角度分析,该设想的依据是

(3)①CH4和CO2所含的三种元素电负性从小到大的顺序为
②碳的另一种同素异形体——石墨,其晶体结构如图所示,则石墨晶胞含碳原子个数为
更新时间:2020-06-15 15:54:38
|
相似题推荐
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】自然界中存在大量的金属元素,其中钠、镁、铁、铜等在工农业生产中有广泛的应用。回答下列问题:
(1)合成氨是人类科学技术上的一项重大突破,工业合成氨生产中常用铁触媒作催化剂, 元素的基态原子的价电子共占据
元素的基态原子的价电子共占据____ 个轨道,未成对电子数为____ 个。
(2)合成氨工业中,原料气( 、
、 及少量
及少量 、
、 的混合气)在进入合成塔前常用醋酸二氨合铜(I)溶液来吸收原料气体中的
的混合气)在进入合成塔前常用醋酸二氨合铜(I)溶液来吸收原料气体中的 (
( ),其反应是
),其反应是 [醋酸羰基三氨合铜(I)]。
[醋酸羰基三氨合铜(I)]。
①C、N、O三种元素的第一电离能由小到大的顺序为___ ,CO分子中σ键和π键数目之比为___ 。
② 中存在的化学键类型有
中存在的化学键类型有____ (填标号)。
A.配位键 B.离子键 C.极性共价键 D.非极性共价键
③醋酸分子中碳原子的杂化方式为____ 。
(3) 和
和 都属于离子化合物,
都属于离子化合物, 的熔点为801.3℃,
的熔点为801.3℃, 的熔点高达2800℃。造成两种晶体熔点差距的主要原因是
的熔点高达2800℃。造成两种晶体熔点差距的主要原因是____ 。
(4)下图是铜的一种氯化物晶体的晶胞结构,则它的化学式是____ ;已知晶胞边长为apm,位于晶胞中的4个铜原子构成的四面体的棱长为____ pm。

(1)合成氨是人类科学技术上的一项重大突破,工业合成氨生产中常用铁触媒作催化剂,
 元素的基态原子的价电子共占据
元素的基态原子的价电子共占据(2)合成氨工业中,原料气(
 、
、 及少量
及少量 、
、 的混合气)在进入合成塔前常用醋酸二氨合铜(I)溶液来吸收原料气体中的
的混合气)在进入合成塔前常用醋酸二氨合铜(I)溶液来吸收原料气体中的 (
( ),其反应是
),其反应是 [醋酸羰基三氨合铜(I)]。
[醋酸羰基三氨合铜(I)]。①C、N、O三种元素的第一电离能由小到大的顺序为
②
 中存在的化学键类型有
中存在的化学键类型有A.配位键 B.离子键 C.极性共价键 D.非极性共价键
③醋酸分子中碳原子的杂化方式为
(3)
 和
和 都属于离子化合物,
都属于离子化合物, 的熔点为801.3℃,
的熔点为801.3℃, 的熔点高达2800℃。造成两种晶体熔点差距的主要原因是
的熔点高达2800℃。造成两种晶体熔点差距的主要原因是(4)下图是铜的一种氯化物晶体的晶胞结构,则它的化学式是

您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】有短周期主族元素A、B、C、D、E,其中A为地壳中含量最高的金属元素,B元素原子的M层电子数为最内层电子数的2倍,C的气态氢化物的水溶液呈碱性,D元素的最外层电子数是电子层数的3倍,E的单质为黄绿色气体,是制备漂白粉的原料。
请回答下列问题:
(1)D元素在周期表中的位置:______ .
(2)A、D、E元素简单离子半径由大到小的顺序为________________ (用微粒符号填).
(3)F与D同主族且相邻,其气态氢化物稳定性由大到小为___________ (填化学式).
(4)用高能射线照射含有10电子的D元素氢化物分子时,一个分子能释放一个电子,同时产生一种具有较高氧化性的阳离子,试写出该阳离子的电子式______ ,该阳离子中存在的化学键有______ .
(5)C元素的简单气态氢化物与E元素的单质反应有白烟生成,化学方程式为______ .
(6)B的单质与强碱反应的离子方程式为______ .
请回答下列问题:
(1)D元素在周期表中的位置:
(2)A、D、E元素简单离子半径由大到小的顺序为
(3)F与D同主族且相邻,其气态氢化物稳定性由大到小为
(4)用高能射线照射含有10电子的D元素氢化物分子时,一个分子能释放一个电子,同时产生一种具有较高氧化性的阳离子,试写出该阳离子的电子式
(5)C元素的简单气态氢化物与E元素的单质反应有白烟生成,化学方程式为
(6)B的单质与强碱反应的离子方程式为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】C、N、F、Cu及其化合物在化工、医药、材料等方面应用十分广泛。回答下列有关问题:
(1)基态铜原子的价电子排布式为_________ ;C、N、F、Cu四种元素第一电离能从小到大的顺序为_______ 。
(2)化合物 常温下均为气体,沸点较高的是
常温下均为气体,沸点较高的是_________ ;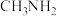 中氮原子的杂化方式是
中氮原子的杂化方式是___________ 。
(3)将无水硫酸铜溶解在一定量的水中,再加入过量氨水,溶液变为深蓝色,该深蓝色离子 内存在的化学键有
内存在的化学键有___________ 。
A.氢键 B.离子键 C.共价键 D.配位键 E.金属键
(4)氮、铜形成的一种化合物,为立方晶系晶体,晶胞参数为 ,沿面对角线投影如图所示。已知该晶胞中原子的分数坐标为:
,沿面对角线投影如图所示。已知该晶胞中原子的分数坐标为: 则该晶胞中,与Cu原子等距且最近的Cu原子有
则该晶胞中,与Cu原子等距且最近的Cu原子有_______ 个。

(1)基态铜原子的价电子排布式为
(2)化合物
 常温下均为气体,沸点较高的是
常温下均为气体,沸点较高的是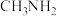 中氮原子的杂化方式是
中氮原子的杂化方式是(3)将无水硫酸铜溶解在一定量的水中,再加入过量氨水,溶液变为深蓝色,该深蓝色离子
 内存在的化学键有
内存在的化学键有A.氢键 B.离子键 C.共价键 D.配位键 E.金属键
(4)氮、铜形成的一种化合物,为立方晶系晶体,晶胞参数为
 ,沿面对角线投影如图所示。已知该晶胞中原子的分数坐标为:
,沿面对角线投影如图所示。已知该晶胞中原子的分数坐标为: 则该晶胞中,与Cu原子等距且最近的Cu原子有
则该晶胞中,与Cu原子等距且最近的Cu原子有
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】很多元素在生产生活中有很多应用,请回答下列问题:
(1)基态Fe原子的价电子排布图为___________
(2)Zn2+和CN-、K+可组成化合物K2Zn(CN)4,其中Zn(CN) 中的配体为
中的配体为___________ ,配位原子为___________ ,与该配离子中配体等电子体的分子为___________
(3)Fe-Cr-Al合金可作为汽车尾气催化剂的载体,汽车尾气催化剂可将NO2还原为无毒害的气体,防止HNO3型酸雨的形成,NO2的空间构型为___________ 。HNO3的酸性强于HNO2的原因为___________
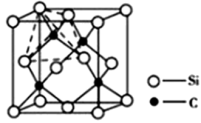
(4)金刚砂(SiC)的硬度为9.5,其晶胞结构如下图所示,则金刚砂晶体类型为___________ ,在SiC中,每个C原子周围最近的C原子数目为______ 个;若晶胞的边长为apm,则金刚砂的密度为_______ g/cm3(用NA表示阿伏加德罗常数的值)。
(1)基态Fe原子的价电子排布图为
(2)Zn2+和CN-、K+可组成化合物K2Zn(CN)4,其中Zn(CN)
 中的配体为
中的配体为(3)Fe-Cr-Al合金可作为汽车尾气催化剂的载体,汽车尾气催化剂可将NO2还原为无毒害的气体,防止HNO3型酸雨的形成,NO2的空间构型为
(4)金刚砂(SiC)的硬度为9.5,其晶胞结构如下图所示,则金刚砂晶体类型为

您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】已知W、X、Y、Z、M、N是原子序数依次递增的前四周期元素。其元素性质或原子结构特征如下:
请回答下列问题:
(1)元素M的核外电子排布式为__________ ;元素N的价层电子的轨道表示式为__________ 。
(2)化合物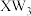 的VSEPR模型名称为
的VSEPR模型名称为__________ ,
(3)元素W和Y可以形成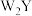 、
、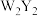 、
、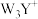 等微粒。
等微粒。
①下列说法不正确的是__________ 。
A.物质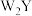 难以分解,主要是因为分子间存在氢键
难以分解,主要是因为分子间存在氢键
B.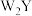 的空间结构为直线型
的空间结构为直线型
C.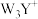 的中心原子采用
的中心原子采用 杂化
杂化
D.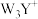 中W—Y—W键角比
中W—Y—W键角比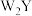 中的大
中的大
②物质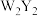 能与水混溶,却不溶于
能与水混溶,却不溶于 ,原因是
,原因是__________ 。
(4)下表是W—N元素中某种元素的部分电离能,由此可判断该元素是__________ 。
元素 | 元素性质或原子结构特征 |
W | 是宇宙中含量最多的元素 |
X | 元素原子最高能级的不同轨道都有电子,且自旋方向相同 |
Y | 原子核外s能级上的电子总数与p能级上的电子总数相等,但第一电离能都低于同周期相邻元素 |
Z | 价层电子数等于其电子层数 |
M | 其价电子中,在不同形状的原子轨道中运动的电子数相等 |
N | 核电荷数为25 |
(1)元素M的核外电子排布式为
(2)化合物
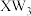 的VSEPR模型名称为
的VSEPR模型名称为(3)元素W和Y可以形成
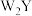 、
、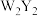 、
、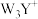 等微粒。
等微粒。①下列说法不正确的是
A.物质
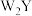 难以分解,主要是因为分子间存在氢键
难以分解,主要是因为分子间存在氢键B.
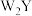 的空间结构为直线型
的空间结构为直线型C.
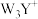 的中心原子采用
的中心原子采用 杂化
杂化D.
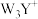 中W—Y—W键角比
中W—Y—W键角比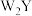 中的大
中的大②物质
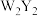 能与水混溶,却不溶于
能与水混溶,却不溶于 ,原因是
,原因是(4)下表是W—N元素中某种元素的部分电离能,由此可判断该元素是
元素 | 电离能/(kJ/mol) | ||||
|
|
|
|
| |
某种元素 | 578 | 1817 | 2745 | 11575 | 14830 |
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】铂(Pt)的单质是一种重要的催化剂,其化合物可用于医药领域。
(1)基态Pt的价层电子排布式是5d96s1,该元素在元素周期表中位于第______ 周期。
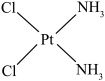
(2)Pt(NH3)2Cl2是铂的重要配位化合物,它有两种同分异构体,结构和性质如表。
①推测Pt(NH3)2Cl2中Pt的杂化轨道类型不是sp3,依据是______ 。
②顺铂在水中的溶解度大于反铂的原因是______ 。
(3)顺铂是临床使用的第一代铂类抗癌药物,其抗癌机理:在铜转运蛋白的作用下,顺铂进入人体细胞发生水解,生成的Pt(NH3)2(OH)Cl与DNA结合,破坏DNA的结构,阻止癌细胞增殖。如:______ 。
②在Pt(NH3)2Cl2中,配体与铂(Ⅱ)的结合能力:Cl-______ NH3(填“>”或“<”)。此外,顺铂还能躲避癌细胞对受损DNA的修复,使癌细胞彻底死亡。
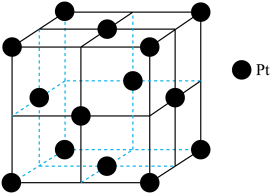
(4)顺铂的发现与铂电极使用有关。铂晶胞为正方体,边长为anm,结构如图。______ m3•mol-1(阿伏加德罗常数为NA)。
②通常情况下铂电极为惰性电极,但在NaCl溶液中使用会产生[PtCl6]2-而略有损耗,分析原因:______ 。
资料:i.单位物质的量的物质所具有的体积叫做摩尔体积
ii.1nm=1×10−9m
(1)基态Pt的价层电子排布式是5d96s1,该元素在元素周期表中位于第
(2)Pt(NH3)2Cl2是铂的重要配位化合物,它有两种同分异构体,结构和性质如表。
| 顺铂 | 反铂 | |
| 结构 |
|
|
| 25℃时溶解度/g | 0.2577 | 0.0366 |
②顺铂在水中的溶解度大于反铂的原因是
(3)顺铂是临床使用的第一代铂类抗癌药物,其抗癌机理:在铜转运蛋白的作用下,顺铂进入人体细胞发生水解,生成的Pt(NH3)2(OH)Cl与DNA结合,破坏DNA的结构,阻止癌细胞增殖。如:
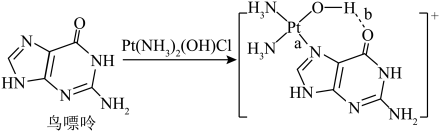
②在Pt(NH3)2Cl2中,配体与铂(Ⅱ)的结合能力:Cl-
(4)顺铂的发现与铂电极使用有关。铂晶胞为正方体,边长为anm,结构如图。
②通常情况下铂电极为惰性电极,但在NaCl溶液中使用会产生[PtCl6]2-而略有损耗,分析原因:
资料:i.单位物质的量的物质所具有的体积叫做摩尔体积
ii.1nm=1×10−9m
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐1】钙钛矿(CaTiO3)型化合物是一类可用于生产太阳能电池、传感器、固体电阻器等的功能材料,回答下列问题:
(1)基态Ti原子的核外电子排布式为____________ 。
(2)Ti的四卤化物熔点如下表所示,TiF4熔点高于其他三种卤化物,自TiCl4至TiI4熔点依次升高,原因是____________ 。
(3)CaTiO3的晶胞如图(a)所示,其组成元素的电负性大小顺序是__________ ;金属离子与氧离子间的作用力为__________ ,Ca2+的配位数是__________ 。
(4)一种立方钙钛矿结构的金属卤化物光电材料的组成为Pb2+、I﹣和有机碱离子 ,其晶胞如图(b)所示。其中Pb2+与图(a)中
,其晶胞如图(b)所示。其中Pb2+与图(a)中__________ 的空间位置相同,有机碱 中,N原子的杂化轨道类型是
中,N原子的杂化轨道类型是__________ ;若晶胞参数为a nm,则晶体密度为_________ g·cm-3(列出计算式)。_______ 、_______ 。
(1)基态Ti原子的核外电子排布式为
(2)Ti的四卤化物熔点如下表所示,TiF4熔点高于其他三种卤化物,自TiCl4至TiI4熔点依次升高,原因是
| 化合物 | TiF4 | TiCl4 | TiBr4 | TiI4 |
| 熔点/℃ | 377 | ﹣24.12 | 38.3 | 155 |
(3)CaTiO3的晶胞如图(a)所示,其组成元素的电负性大小顺序是
(4)一种立方钙钛矿结构的金属卤化物光电材料的组成为Pb2+、I﹣和有机碱离子
 ,其晶胞如图(b)所示。其中Pb2+与图(a)中
,其晶胞如图(b)所示。其中Pb2+与图(a)中 中,N原子的杂化轨道类型是
中,N原子的杂化轨道类型是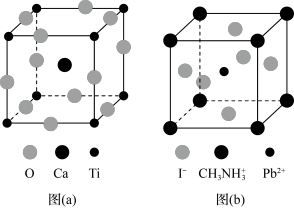
您最近一年使用:0次
【推荐2】元素A、B、C、D都是短周期元素,A元素原子的2p轨道上仅有两个未成对电子,B的3p轨道上有空轨道,A、B同主族,B、C同周期,C是同周期中电负性最大的,D的气态氢化物的水溶液能使无色酚酞试液变红。试回答:
(1)A的价电子轨道排布图为______________________________ ;B的电子排布式为 _________ ;C的价电子排布式为 ____________ ;D的原子结构示意图为 __________ 。
(2)已知D与H原子能形成一种高能量的分子D2H2,其中D原子满足8电子结构特征,则该分子的电子式为_____________ ,含有 _____ 个σ键和 _____ 个π键。
(3)B的原子核外电子运动状态________ 有多少种,原子轨道数为______ ,能级数__________ ,电子占据的最高能层符号为_________ 。
(4)四种元素最高价氧化物水化物酸性由强到弱的是(用对应化学式回答)____________________ 。
(1)A的价电子轨道排布图为
(2)已知D与H原子能形成一种高能量的分子D2H2,其中D原子满足8电子结构特征,则该分子的电子式为
(3)B的原子核外电子运动状态
(4)四种元素最高价氧化物水化物酸性由强到弱的是(用对应化学式回答)
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐3】前四周期元素X、Y、Z、M、N、O、P,原子序数逐渐增大,其中X、Y、Z、M、N为短周期元素,而X、Y、Z、M处于同周期的P区,且未成对电子数之比为1:2:3:2;N与Z同族。O、P分别位于周期表第2、4列,P的单质被称为“未来金属”,具有质量轻、强度大、耐腐蚀性好的优点。
(1)Y、Z、M三种元素的电负性由大到小的顺序:________ (用元素符号表示)。
(2)M的常见氢化物的氢键的键能小于HF的氢键的键能,但Z的常见氢化物常温下为液态而HF常温下为气态的原因是:__________ 。
(3)XN一种耐磨涂料,可用于金属表面保护层,该化合物可由X的三溴化物和N的三溴化物于高温下在氢气的氛围中合成。
①写出合成XN的化学方程式:_________ 。(各物质用化学式表示)
②XN的晶体的晶胞如图所示:
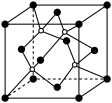
其中实心球为N,在一个晶胞中N原子空间堆积方式为______ ,N原子的配位数为______ ;该结构中有一个配位键,提供空轨道的原子是________ (写元素符号)。

(4)O和硫形成的某种晶体的晶胞如图a所示:该晶胞原子的坐标参数A为(0,0,0);B为(1,0,0)。则C原子的坐标参数为_______ 。
(5)图b为P的一种面心立方晶胞结构,若晶胞的边长为anm,则P的密度为_____ g·cm-3(用含a和NA的代数式表示)
(1)Y、Z、M三种元素的电负性由大到小的顺序:
(2)M的常见氢化物的氢键的键能小于HF的氢键的键能,但Z的常见氢化物常温下为液态而HF常温下为气态的原因是:
(3)XN一种耐磨涂料,可用于金属表面保护层,该化合物可由X的三溴化物和N的三溴化物于高温下在氢气的氛围中合成。
①写出合成XN的化学方程式:
②XN的晶体的晶胞如图所示:

其中实心球为N,在一个晶胞中N原子空间堆积方式为

(4)O和硫形成的某种晶体的晶胞如图a所示:该晶胞原子的坐标参数A为(0,0,0);B为(1,0,0)。则C原子的坐标参数为
(5)图b为P的一种面心立方晶胞结构,若晶胞的边长为anm,则P的密度为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】已知A、B、C、D是原子序数依次增大的四种短周期主族元素,A的周期数等于其主族序数,B原子的价电子排布为nsnnpn,D是地壳中含量最多的元素,E是第四周期的p区元素且最外层只有2对成对电子,F元素的基态原子第四能层只有一个电子,其它能层均已充满电子。
(1)基态E原子的价电子排布图________ 。
(2)B、C、D三元素第一电离能由大到小的顺序为________ (用元素符号表示)。
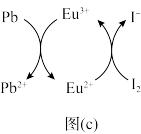
(3)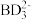 中心原子杂化轨道的类型为
中心原子杂化轨道的类型为________ 杂化;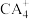 的空间构型为
的空间构型为________ 。
(4)化合物B2A4中含有σ键与π键的个数比为________ 。
(5)比较D、E元素最简单氢化物的沸点高低________ (用化学式表示),理由是________ (用文字表达)。
(6)C、F两元素形成的某化合物的晶胞结构如图所示,顶点为C原子,则该化合物的化学式是________ ,C原子的配位数是________ ,若相邻C原子和F原子间的距离为acm,阿伏加 德罗常数为NA,则该晶体的密度为________ g/cm3(用含a、NA的符号表示)。
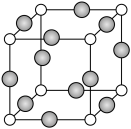
(1)基态E原子的价电子排布图
(2)B、C、D三元素第一电离能由大到小的顺序为
(3)
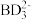 中心原子杂化轨道的类型为
中心原子杂化轨道的类型为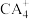 的空间构型为
的空间构型为(4)化合物B2A4中含有σ键与π键的个数比为
(5)比较D、E元素最简单氢化物的沸点高低
(6)C、F两元素形成的某化合物的晶胞结构如图所示,顶点为C原子,则该化合物的化学式是

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】硒化锌是一种透明黄色半导体,也可作红外光学材料,熔点1520℃。
(1)锌离子的电子排布式是_____________ 。
(2)根据元素周期律,电负性S______ Se,第一电离能Se______ As(填“>”或“<”)。
(3)H2O的沸点______________ (填“>”或“<”)H2Se的沸点,其原因是:______ 。
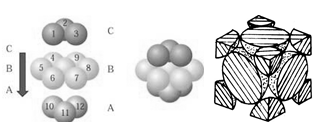
(4)NaCl晶胞如图所示,阴、阳离子都具有球型对称结构,它们都可以看做刚性圆球,并彼此“相切”。晶胞中Na+的配位数为____ ,若晶胞参数为a pm,阿伏伽德罗常数的值用NA表示,若晶体密度为_______ g·cm﹣3。(列出表达式)。
(5)铜晶体中铜原子的堆积方式如图所示,铜晶体中原子的堆积模型属于_______ 。若已知铜的原子半径为rcm,表示原子空间占有率的表达式为__________ 。
(1)锌离子的电子排布式是
(2)根据元素周期律,电负性S
(3)H2O的沸点
(4)NaCl晶胞如图所示,阴、阳离子都具有球型对称结构,它们都可以看做刚性圆球,并彼此“相切”。晶胞中Na+的配位数为
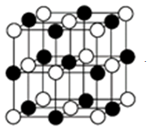
(5)铜晶体中铜原子的堆积方式如图所示,铜晶体中原子的堆积模型属于
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】钇(Y)是第一种被发现的稀土元素,位于元素周期表的第5周期第IIIB族,其在电子、激光、超导等领域均有广泛应用。回答下列问题:
(1)基态Y原子的价电子排布式为________________________ 。
(2)Y(NO3)3与水杨酸甲酯( )反应,可制得配合物同时生成HNO3,其中配合物能用于捕获NO。
)反应,可制得配合物同时生成HNO3,其中配合物能用于捕获NO。
①Y(NO3)3中所含三种元素的第一电离能由大到小的顺序为__________ (用元素符号表示); 的立体构型为
的立体构型为________________________ 。
②l mol HNO3中含有σ键的数目为_________ ,HNO3的酸性强于HNO2的原因为____ 。
③水杨酸甲酯中C原子的杂化方式为______ ;其沸点高于水杨酸的主要原因为______ 。
④NO分子中,N、O原子间形成共价键的电子云对称形式包括镜面对称和_______ 。
(3)Y、Cu、Ba、O形成的一种具有超导性的材料的晶胞结构如图所示。若NA表示阿伏加德罗常数的值, =β=γ=90°,则该晶体的化学式为
=β=γ=90°,则该晶体的化学式为__________ ,晶体密度 =
=_____ g•cm-3(用含a、c、NA的代数式表示)。

(1)基态Y原子的价电子排布式为
(2)Y(NO3)3与水杨酸甲酯(
 )反应,可制得配合物同时生成HNO3,其中配合物能用于捕获NO。
)反应,可制得配合物同时生成HNO3,其中配合物能用于捕获NO。①Y(NO3)3中所含三种元素的第一电离能由大到小的顺序为
 的立体构型为
的立体构型为②l mol HNO3中含有σ键的数目为
③水杨酸甲酯中C原子的杂化方式为
④NO分子中,N、O原子间形成共价键的电子云对称形式包括镜面对称和
(3)Y、Cu、Ba、O形成的一种具有超导性的材料的晶胞结构如图所示。若NA表示阿伏加德罗常数的值,
 =β=γ=90°,则该晶体的化学式为
=β=γ=90°,则该晶体的化学式为 =
=
您最近一年使用:0次