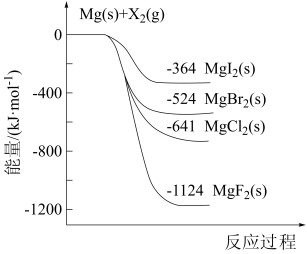
下列有关热化学方程式的叙述中正确的是
| A.中和热的离子方程式为:OH-(aq)+H+(aq)=H2O(g) ∆H=-57.3 kJ·mol-1 |
| B.已知C(s)+O2(g)=CO2(g) ∆H1,C(s)+O2(g)=CO2(s) ∆H2,则∆H1>∆H2 |
| C.已知2H2(g)+O2(g)=2H2O(l) ∆H=-571.6 kJ·mol-1,则H2的燃烧热为-571.6 kJ·mol-1 |
| D.已知C(石墨,s)=C(金刚石,s) ∆H=+1.9 kJ·mol-1,则金刚石比石墨稳定 |
更新时间:2024-05-09 07:48:38
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列依据热化学方程式得出的结论正确的是
热化学方程式 | 结论 | |
A | 2H2(g)+O2(g)=2H2O(g) ΔH=483.6kJ/mol | 氢气的燃烧热 △H=﹣483.6kJ/mol |
B | NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l) ΔH=-57.3kJ/mol | 含40.0gNaOH的稀溶液与稀醋酸完全中和,放出的热量小于57.3kJ |
C | 2C(s)+2O2(g)=2CO2(g) ΔH=-akJ/mol 2C(s)+O2(g)=2CO(g) ΔH=-bkJ/mol | b>a |
D | C(石墨,s)=C(金刚石,s)ΔH=+1.5kJ/mol | 金刚石比石墨稳定 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】合成尿素 是利用
是利用 的途径之一,工业上以
的途径之一,工业上以 和
和 为原料在一定温度和压强下合成尿素的反应历程分如下两步进行(假设每步均为基元反应):
为原料在一定温度和压强下合成尿素的反应历程分如下两步进行(假设每步均为基元反应):
反应a:
反应b:
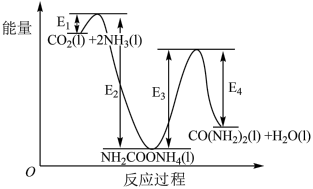
结合反应过程中的能量变化图,下列说法错误的是
 是利用
是利用 的途径之一,工业上以
的途径之一,工业上以 和
和 为原料在一定温度和压强下合成尿素的反应历程分如下两步进行(假设每步均为基元反应):
为原料在一定温度和压强下合成尿素的反应历程分如下两步进行(假设每步均为基元反应):反应a:

反应b:


结合反应过程中的能量变化图,下列说法错误的是
| A.反应a为放热反应,反应b为吸热反应 |
| B.反应a为快反应,反应b为慢反应 |
C.增大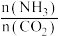 的投料比,二氧化碳的平衡转化率增大 的投料比,二氧化碳的平衡转化率增大 |
D.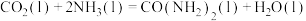 的 的 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】下列说法或表示方法中正确的是
| A.等质量的硫蒸气和硫固体分别完全燃烧,后者放出的热量多 |
| B.需要加热才能发生的反应一定是吸热反应 |
| C.在101Kpa时,2gH2完全燃烧生成液态水,放出285.8KJ热量,氢气燃烧的热化学方程式为:2H2(g)+O2(g)=2H2O(l);ΔH=+285.8KJ/mol |
| D.稀溶液中:H+(aq)+OH—(aq)=H2O(l);ΔH=—53.7KJ/mol ,若将含0.5 molH2SO4的浓溶液与含1 mol NaOH的溶液混合,放出的热量大于53.7KJ/mol |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列有关能量的判断和表示方法正确的是
| A.由C(s,石墨)=C(s,金刚石) ΔH=+1.9kJ·mol-1,可知:石墨比金刚石更稳定 |
| B.等质量的C2H5OH(g)和C2H5OH(l)分别完全燃烧,后者放出的热量更多 |
| C.由H+(aq)+OH-(aq)=H2O(l) ΔH= -57.3kJ·mol-1,可知:含1mol HCl的溶液与含1mol NH3•H2O的溶液混合,放出热量等于57.3kJ |
| D.已知2C(s)+2O2(g)=2CO2(g) ΔH1; 2C(s)+O2(g)=2CO(g) ΔH2,则ΔH1>ΔH2 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】已知反应:①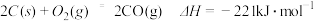 ,②
,②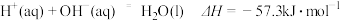 。下列结论正确的是
。下列结论正确的是
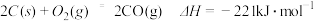 ,②
,②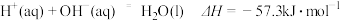 。下列结论正确的是
。下列结论正确的是A.碳的摩尔燃烧焓大于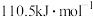 |
B.①的焓变为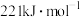 |
C.稀硫酸与稀 溶液反应的中和热为 溶液反应的中和热为 |
D.稀醋酸与稀 溶液反应生成 溶液反应生成 水,放出 水,放出 热量 热量 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】已知2H2(g)+O2(g)=2H2O(g) ΔH=-483.6 kJ/mol。下列说法正确的是( )
| A.在相同条件下,2L氢气与1L氧气化合生成2L水蒸气放出483.6kJ热量 |
B.H2(g)+ O2(g)=H2O(l) ΔH=-Q1 kJ/mol,则Q1>241.8 O2(g)=H2O(l) ΔH=-Q1 kJ/mol,则Q1>241.8 |
| C.H2的燃烧热为241.8kJ/mol |
| D.2mol氢气与1 mol氧气反应生成2mol水的反应热为483.6kJ/mol |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐3】目前,火箭的液体推进剂有液氢、液氧、偏二甲肼、四氧化二氮、硼烷等十几种,但比较理想的环境推进剂是液氢和液氧。由于储存、运输等技术的制约,液氢和液氧的使用受到很大程度的限制。化学反应2H2+O2=2H2O能量变化如图所示,则表示H2燃烧热的热化学方程式为
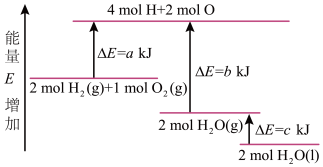

| A.2H2(g)+O2(g)=2H2O(g) ΔH=-(b-a)kJ·mol-1 |
B.H2(g)+ O2(g)=H2O(g) ΔH=- O2(g)=H2O(g) ΔH=- (b-a)kJ·mol-1 (b-a)kJ·mol-1 |
| C.2H2(g)+O2(g)=2H2O(l) ΔH=-(b+c-a)kJ·mol-1 |
D.H2(g)+ O2(g)=H2O(l) ΔH=- O2(g)=H2O(l) ΔH=- (b+c-a)kJ·mol-1 (b+c-a)kJ·mol-1 |
您最近一年使用:0次
【推荐1】下列说法正确的是
| A.镀锡的铁制品比镀锌的铁制品耐腐蚀 |
| B.用过量的稀盐酸与稀NaOH溶液测定中和热,在中和滴定实验中,用待测NaOH溶液润洗锥形瓶,测定结果将偏高 |
| C.已知:①2H2(g)+O2(g)=2H2O(g)△H1②2H2(g)+O2(g)=2H2O(1)△H2,则)△H1<)△H2 |
| D.用pH试纸测得溶液的pH值为2.3 |
您最近一年使用:0次
【推荐2】下列说法或表示法正确的是
| A.等量的白磷蒸气和白磷固体分别完全燃烧,后者放出热量多 |
| B.由C(s,石墨)=C(s,金刚石) ΔH=+1.19 kJ·mol-1可知,金刚石比石墨稳定 |
| C.应用盖斯定律,可计算某些难以直接测量的反应焓变 |
| D.在101 kPa时,2 g H2完全燃烧生成液态水,放出285.8 kJ热量,氢气燃烧的热化学方程式表示为:2H2(g)+O2(g)=2H2O(l) ΔH=-285.8 kJ·mol-1 |
您最近一年使用:0次