下列关于热化学反应的描述正确的是
| A.HCl和NaOH反应的反应热ΔH=-57.3 kJ·mol-1,则H2SO4和Ba(OH)2反应的反应热ΔH=2×(-57.3) kJ·mol-1 |
| B.甲烷的燃烧热ΔH=-890.3 kJ·mol-1,则CH4(g)+2O2(g)=CO2(g)+2H2O(g) ΔH<-890.3 kJ·mol-1 |
| C.CO(g)的燃烧热是283.0 kJ·mol-1,则2CO2(g)=2CO(g)+O2(g)反应的ΔH=+566.0 kJ·mol-1 |
D.已知:500 ℃、30 MPa下,N2(g)+3H2(g) 2NH3(g) ΔH=-92.4 kJ·mol-1;将3 mol H2和过量的N2在此条件下充分反应,会放出92.4 kJ热量 2NH3(g) ΔH=-92.4 kJ·mol-1;将3 mol H2和过量的N2在此条件下充分反应,会放出92.4 kJ热量 |
更新时间:2024-05-09 07:48:47
|
相似题推荐
单选题
|
较易
(0.85)
名校
【推荐1】强酸和强碱稀溶液的中和热可表示为:H+(aq)+OH-(aq)=H2O(l) ΔH=-57.3kJ·mol-1。已知①HCl(aq)+NH3·H2O(aq)=NH4Cl(aq)+H2O(l) ΔH=-akJ·mol-1 ②HCl(aq)+NaOH(s)===NaCl(aq)+H2O(l) ΔH=-bkJ·mol-1 ③HNO3(aq)+KOH(aq)===KNO3(aq)+H2O(l) ΔH=-ckJ·mol-1则a、b、c三者的大小关系为( )
| A.a>b>c | B.b>c>a | C.a=b=c | D.无法比较 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】已知: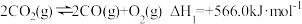
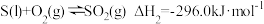 ,
,
已知某反应的平衡常数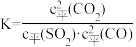 ,则该反应的
,则该反应的 等于
等于
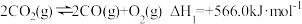
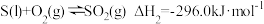 ,
,已知某反应的平衡常数
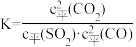 ,则该反应的
,则该反应的 等于
等于A.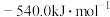 | B.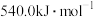 | C.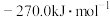 | D.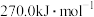 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐1】已知25℃、101kPa下,1g液态甲醇(CH3OH)完全燃烧生成液态水时放出23kJ的热量,则下列热化学方程式正确的是
A.CH3OH(l)+ O2(g)=CO2(g)+2H2O(l) △H=-23kJ•mol-1 O2(g)=CO2(g)+2H2O(l) △H=-23kJ•mol-1 |
| B.2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(g) △H=-1472kJ•mol-1 |
| C.2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(l) △H=-1472kJ•mol-1 |
| D.2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(l) △H=+1472kJ•mol-1 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】下列热化学方程式中的反应热下划线处表示燃烧热的是
A.NH3(g)+ O2(g)=NO(g)+ O2(g)=NO(g)+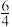 H2O(g) ΔH=-a kJ·mol-1 H2O(g) ΔH=-a kJ·mol-1 |
| B.C6H12O6(s)+6O2(g)=6CO2(g)+6H2O(l) ΔH=-b kJ·mol-1 |
| C.2CO(g)+O2(g)=2CO2(g) ΔH=-c kJ·mol-1 |
D.CH3CH2OH(l)+ O2(g)=CH3CHO(l)+H2O(l) ΔH=-d kJ·mol-1 O2(g)=CH3CHO(l)+H2O(l) ΔH=-d kJ·mol-1 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐1】下列说法正确的是
| A.增大压强,活化分子百分数增多,化学反应速率一定增大 |
| B.C(石墨,s)=C(金刚石,s) ∆H=+1.9 kJ/mol,则金刚石比石墨稳定 |
| C.CaCO3(s)=CaO(s)+CO2(g) ∆H>0,∆S>0,则不论在何种条件下都不可能自发进行 |
| D.用CH3COOH溶液和NaOH溶液反应测定中和热:CH3COOH(aq)+NaOH(aq)=CH3COONa(aq)+H2O(aq) ∆H>-57.3 kJ/mol |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐2】下列关于热化学方程式的说法正确的是
A.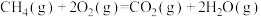 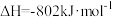 ,则 ,则 的燃烧热为 的燃烧热为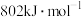 |
B.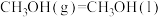  ,则该反应为放热反应 ,则该反应为放热反应 |
C.已知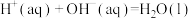 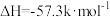 ,则 ,则 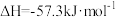 |
D. 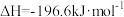 ,则 ,则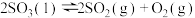 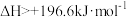 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐3】下列叙述正确的是
| A.甲烷的燃烧热为ΔH=-890.3kJ·mol-1,则甲烷燃烧的热化学方程式可表示为:CH4(g)+2O2(g)=CO2(g)+2H2O(g) ΔH=-890.3kJ·mol-1 |
| B.已知H+(aq)+OH-(aq)=H2O(l) ΔH=-57.3kJ·mol-1,则稀H2SO4溶液和稀Ba(OH)2溶液反应的反应热ΔH=2×(-57.3)kJ·mol-1 |
| C.CO(g)的燃烧热是283.0kJ/mol,则2CO2(g)=2CO(g)+O2(g)反应的ΔH=+(2×283.0)kJ/mol |
D.2SO2(g)+O2(g) 2SO3(g) ΔH=-196.3kJ·mol-1,则1mol SO2、0.5mol O2充分反应后,放出热量98.3kJ 2SO3(g) ΔH=-196.3kJ·mol-1,则1mol SO2、0.5mol O2充分反应后,放出热量98.3kJ |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐1】下列方程式书写正确的是( )
A.苏打溶液中加入过量石灰水: |
B.用硫酸酸化的橙色的重铬酸钾 溶液与乙醇作用生成乙酸和草绿色三价铬,可用于检测是否酒后驾驶: 溶液与乙醇作用生成乙酸和草绿色三价铬,可用于检测是否酒后驾驶: |
C.用铜为电极电解饱和食盐水: |
D.表示乙醇燃烧热的热化学方程式( 的绝对值正确): 的绝对值正确): |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐2】下列热化学方程式书写正确的是( 的绝对值均正确)
的绝对值均正确)
 的绝对值均正确)
的绝对值均正确)A.  (燃烧热) (燃烧热) |
B. 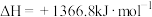 |
C. 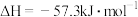 (中和热) (中和热) |
D.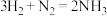 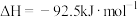 (反应热) (反应热) |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐3】标准生成热指的是在某温度下,由处于标准状态的各种元素的最稳定的单质生成标准状态下1mol某纯物质的热效应,单位常用kJ∙mol−1表示。已知在25℃的条件下:
Ag2O(s)+2HCl(g)=2AgCl(s)+H2O(l) △H1=-324.4 kJ∙mol−1
2Ag(s)+ O2(g)=Ag2O(s) △H2=-30.56 kJ∙mol−1
O2(g)=Ag2O(s) △H2=-30.56 kJ∙mol−1
 H2(g)+
H2(g)+ Cl2(g)=HCl(g) △H3=-92.21 kJ∙mol−1
Cl2(g)=HCl(g) △H3=-92.21 kJ∙mol−1
H2(g)+ O2(g)=H2O(l) △H4=-285.6 kJ∙mol−1
O2(g)=H2O(l) △H4=-285.6 kJ∙mol−1
则25℃时氯化银的标准生成热为
Ag2O(s)+2HCl(g)=2AgCl(s)+H2O(l) △H1=-324.4 kJ∙mol−1
2Ag(s)+
 O2(g)=Ag2O(s) △H2=-30.56 kJ∙mol−1
O2(g)=Ag2O(s) △H2=-30.56 kJ∙mol−1 H2(g)+
H2(g)+ Cl2(g)=HCl(g) △H3=-92.21 kJ∙mol−1
Cl2(g)=HCl(g) △H3=-92.21 kJ∙mol−1H2(g)+
 O2(g)=H2O(l) △H4=-285.6 kJ∙mol−1
O2(g)=H2O(l) △H4=-285.6 kJ∙mol−1则25℃时氯化银的标准生成热为
| A.-126.89kJ∙mol-1 | B.-324.4kJ∙mol-1 |
| C.-30.56kJ∙mol-1 | D.题中数据不足,无法计算 |
您最近一年使用:0次



