高铁酸钠(Na2FeO4)是一种优良的多功能水处理剂,具有很强的氧化性,工业上可采取干法和湿法制备Na2FeO4。回答下列问题:
(1)干法制备Na2FeO4,反应原理为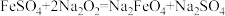 。
。
①Na2FeO4属于______________ (填“盐”“碱”或“氧化物”)。
②写出Na2O2的电子式:_______________ 。
③氧化性:Na2O2______________ (填“<”或“>”)Na2FeO4,每消耗1 mol FeSO4转移______________ mole-。
(2)湿法制备Na2FeO4,将Fe(OH)3固体加入含有一定浓度的NaClO和NaOH的混合溶液中,搅拌一段时间后,可得到Na2FeO4和NaCl。
①实验需要480mL0.2mol·L-1NaOH溶液,如图所示的仪器中配制溶液肯定不需要的是_______________ (填字母,下同)。_______________ 。
A.使用容量瓶之前应检查它是否漏水
B.容量瓶用蒸馏水洗净后,无需用待配溶液润洗
C.定容时,将蒸馏水小心倒入容量瓶中直至与刻度线齐平
D.配制溶液时,如果试样是液体,用量筒量取试样后直接倒入容量瓶中定容
③在配制NaOH溶液时,若NaOH固体溶解后立即移入容量瓶→洗烧杯→洗涤液移入容量瓶→定容,则所得溶液浓度_______________ (填“>”“<”或“=”)0.2mol·L-1。
④写出湿法制备Na2FeO4的化学方程式:_______________ 。
(3)如果以单位质量的氧化剂所得到的电子数来表示消毒的效率,Na2FeO4的消毒效率为______________ (用分数表示, →Fe3+)。
→Fe3+)。
(1)干法制备Na2FeO4,反应原理为
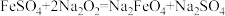 。
。①Na2FeO4属于
②写出Na2O2的电子式:
③氧化性:Na2O2
(2)湿法制备Na2FeO4,将Fe(OH)3固体加入含有一定浓度的NaClO和NaOH的混合溶液中,搅拌一段时间后,可得到Na2FeO4和NaCl。
①实验需要480mL0.2mol·L-1NaOH溶液,如图所示的仪器中配制溶液肯定不需要的是
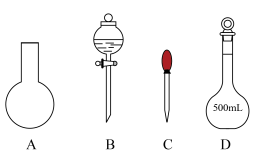
A.使用容量瓶之前应检查它是否漏水
B.容量瓶用蒸馏水洗净后,无需用待配溶液润洗
C.定容时,将蒸馏水小心倒入容量瓶中直至与刻度线齐平
D.配制溶液时,如果试样是液体,用量筒量取试样后直接倒入容量瓶中定容
③在配制NaOH溶液时,若NaOH固体溶解后立即移入容量瓶→洗烧杯→洗涤液移入容量瓶→定容,则所得溶液浓度
④写出湿法制备Na2FeO4的化学方程式:
(3)如果以单位质量的氧化剂所得到的电子数来表示消毒的效率,Na2FeO4的消毒效率为
 →Fe3+)。
→Fe3+)。
更新时间:2024-05-09 08:33:10
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】Ⅰ.现有以下物质:①NaCl溶液 ②NH3③冰醋酸(纯净的醋酸) ④铜 ⑤K2SO4固体 ⑥酒精
(1)其中能导电的是_______ (填序号,下同);属于电解质的是_______ ,属于非电解质的是_______ 。
(2)写出物质③溶于水的电离方程式_______ 。
(3)写出物质⑤溶于水的电离方程式_______ 。
Ⅱ.甘肃马家窑遗址出土的青铜刀,是我国最早冶炼的青铜器,由于时间久远,其表面有一层“绿锈”,“绿锈”俗称“铜绿”,是铜和空气中的水蒸气、CO2、O2作用产生的,其化学式为Cu2(OH)2CO3,“铜绿”能跟酸反应生成铜盐、CO2和H2O。回答下列问题:
(4)CO2属于_______ 氧化物。(填“酸性”或“碱性”)
(5)从物质分类标准看,“铜绿”属于哪类物质_______。(填选项)
(6)现代工业以黄铜矿为原料,在炼铜的过程中发生了多个反应,其中有如下两个反应:
反应Ⅰ:
反应Ⅱ:
①反应Ⅰ中,氧化产物是_______ ,还原产物是_______ 。
②反应Ⅱ中,Cu2O的作用是_______ 。(填“氧化剂”“还原剂”或“氧化剂和还原剂”)
(1)其中能导电的是
(2)写出物质③溶于水的电离方程式
(3)写出物质⑤溶于水的电离方程式
Ⅱ.甘肃马家窑遗址出土的青铜刀,是我国最早冶炼的青铜器,由于时间久远,其表面有一层“绿锈”,“绿锈”俗称“铜绿”,是铜和空气中的水蒸气、CO2、O2作用产生的,其化学式为Cu2(OH)2CO3,“铜绿”能跟酸反应生成铜盐、CO2和H2O。回答下列问题:
(4)CO2属于
(5)从物质分类标准看,“铜绿”属于哪类物质_______。(填选项)
| A.酸 | B.碱 | C.盐 | D.氧化物 |
反应Ⅰ:

反应Ⅱ:

①反应Ⅰ中,氧化产物是
②反应Ⅱ中,Cu2O的作用是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】请将下列物质前的编号按要求填入相应的空格中。
①空气 ②氧气 ③食盐水 ④H2SO4 ⑤铜 ⑥氢氧化钾 ⑦酒精 ⑧水 ⑨蔗糖 ⑩碳酸氢钠
(1)混合物:______ ;
(2)单质:______ ;
(3)酸:______ ;
(4)碱:______ ;
(5)盐:_______ ;
(6)氧化物:______ ;
(7)电解质:______ ;
(8)非电解质:______ 。
①空气 ②氧气 ③食盐水 ④H2SO4 ⑤铜 ⑥氢氧化钾 ⑦酒精 ⑧水 ⑨蔗糖 ⑩碳酸氢钠
(1)混合物:
(2)单质:
(3)酸:
(4)碱:
(5)盐:
(6)氧化物:
(7)电解质:
(8)非电解质:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】现有下列13种物质:①Fe;②CO2;③空气;④CaO;⑤HNO3;⑥Ca(OH)2;⑦碘酒;⑧CuSO4·5H2O;⑨乙醇;⑩NaHCO3;⑪Fe(OH)3胶体;⑫合金;⑬盐酸
(1)属于混合物的是__________ ((填序号,下同));
(2)属于氧化物的是__________ ;
(3)属于酸的是__________ ;
(4)属于碱的是__________ ;
(5)属于盐的是_______ ;
(6)可出现丁达尔效应的是_____ ;
(7)属于电解质的是______ ;属于非电解质的______ 。
(1)属于混合物的是
(2)属于氧化物的是
(3)属于酸的是
(4)属于碱的是
(5)属于盐的是
(6)可出现丁达尔效应的是
(7)属于电解质的是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】氮元素在海洋中的循环,是整个海洋生态系统的基础和关键。海洋中无机氮的循环过程可用下图表示。

(1)下列关于海洋中氮循环的说法不正确的是_______ (填字母)。
a.海洋中只存在游离态的氮
b.海洋中的氮循环起始于氮的氧化
c.②中的含氮物质转化属于氮的固定
d.向海洋排放含 的废水会影响海洋中
的废水会影响海洋中 的含量
的含量
(2)铜与稀硝酸反应的离子方程式为_______ ,该反应体现了稀硝酸的_______ 性。
(3)有氧时,在硝化细菌作用下 可实现过程④的转化,将过程④的离子方程式补充完整并配平
可实现过程④的转化,将过程④的离子方程式补充完整并配平______
_______NH +5O2=2NO
+5O2=2NO +_______H++_______+5H2O
+_______H++_______+5H2O
该反应中每消耗0.05molO2,转移电子的数目为_______ 。

(1)下列关于海洋中氮循环的说法不正确的是
a.海洋中只存在游离态的氮
b.海洋中的氮循环起始于氮的氧化
c.②中的含氮物质转化属于氮的固定
d.向海洋排放含
 的废水会影响海洋中
的废水会影响海洋中 的含量
的含量(2)铜与稀硝酸反应的离子方程式为
(3)有氧时,在硝化细菌作用下
 可实现过程④的转化,将过程④的离子方程式补充完整并配平
可实现过程④的转化,将过程④的离子方程式补充完整并配平_______NH
 +5O2=2NO
+5O2=2NO +_______H++_______+5H2O
+_______H++_______+5H2O该反应中每消耗0.05molO2,转移电子的数目为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】按要求填写下列空白:
(1)
___________ (填是或不是)碱性氧化物,78g 中含
中含___________ 个阴离子(用 表示);
表示);
(2)氯水中含氯粒子有___________ (填粒子的化学式),氯水长时间放置最终变为___________ ;
(3)配平离子方程式:___________
___________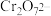 +___________
+___________ +
+ —___________
—___________ +___________
+___________ +___________
+___________
(4)标准状况下44.8mL的 气体恰好能与50mL
气体恰好能与50mL 的
的 溶液完全反应生
溶液完全反应生 ,该反应的还原产物中氯元素的化合价为
,该反应的还原产物中氯元素的化合价为___________
(5)“84消毒液”是种以 为主的高效消毒剂,被广泛用于宾馆、旅游、医院、食品加工行业、家庭等的卫生消毒。某“84消毒液”瓶体部分标签如图所示,该“84消毒液”通常稀释100倍(体积之比)后使用。某同学量取此“84消毒液”,按说明要求稀释后用于消毒,则稀释后的溶液中
为主的高效消毒剂,被广泛用于宾馆、旅游、医院、食品加工行业、家庭等的卫生消毒。某“84消毒液”瓶体部分标签如图所示,该“84消毒液”通常稀释100倍(体积之比)后使用。某同学量取此“84消毒液”,按说明要求稀释后用于消毒,则稀释后的溶液中
___________  (保留两位有效数字)
(保留两位有效数字)

(1)

 中含
中含 表示);
表示);(2)氯水中含氯粒子有
(3)配平离子方程式:
___________
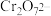 +___________
+___________ +
+ —___________
—___________ +___________
+___________ +___________
+___________
(4)标准状况下44.8mL的
 气体恰好能与50mL
气体恰好能与50mL 的
的 溶液完全反应生
溶液完全反应生 ,该反应的还原产物中氯元素的化合价为
,该反应的还原产物中氯元素的化合价为(5)“84消毒液”是种以
 为主的高效消毒剂,被广泛用于宾馆、旅游、医院、食品加工行业、家庭等的卫生消毒。某“84消毒液”瓶体部分标签如图所示,该“84消毒液”通常稀释100倍(体积之比)后使用。某同学量取此“84消毒液”,按说明要求稀释后用于消毒,则稀释后的溶液中
为主的高效消毒剂,被广泛用于宾馆、旅游、医院、食品加工行业、家庭等的卫生消毒。某“84消毒液”瓶体部分标签如图所示,该“84消毒液”通常稀释100倍(体积之比)后使用。某同学量取此“84消毒液”,按说明要求稀释后用于消毒,则稀释后的溶液中
 (保留两位有效数字)
(保留两位有效数字)
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】如图是硫酸试剂标签上的内容。
(1)该硫酸的物质的量浓度为_____ 。
(2)实验室用该硫酸配制 的稀硫酸,则
的稀硫酸,则
①需要用量筒量取该浓硫酸的体积为_____ mL。
②为完成实验,现有仪器:烧杯、10mL量筒、胶头滴管、玻璃棒,还必需的玻璃仪器有_____ 。
(3)下列操作中,容量瓶所具备的功能有_____。
(4)在下列配制过程示意图中,有错误的是(填写序号)_____ 。
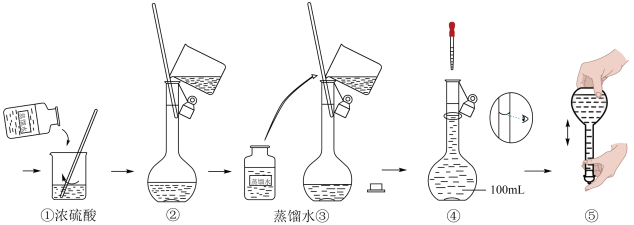
(5)在定容操作时,因不慎加水至凹液面最低处超过了刻度线,该如何处理:_____ 。
(6)下列说法正确的是_____ 。
A.洗涤烧杯和玻璃棒2-3次,并将洗涤液移入容量瓶以减少误差
B.将浓硫酸稀释后未冷却至室温便将溶液转移至容量瓶,所配溶液浓度会偏低
C.定容时仰视观察,所配溶液浓度会偏低
D.容量瓶使用前先要检查是否漏液,具体操作是向容量瓶中加蒸馏水,倒置不漏液即可
E.容量瓶在使用前未干燥,里面有少量蒸馏水,所配溶液浓度会偏低
硫酸化学纯(CP) (500 mL) 品名:硫酸 化学式:H2SO4 相对分子质量:98 密度:1.84 g/cm3 质量分数:98% |
(1)该硫酸的物质的量浓度为
(2)实验室用该硫酸配制
 的稀硫酸,则
的稀硫酸,则①需要用量筒量取该浓硫酸的体积为
②为完成实验,现有仪器:烧杯、10mL量筒、胶头滴管、玻璃棒,还必需的玻璃仪器有
(3)下列操作中,容量瓶所具备的功能有_____。
| A.配制一定体积准确浓度的标准溶液 |
| B.长期贮存溶液 |
| C.用来溶解固体溶质 |
| D.常用来代替烧杯作为反应容器 |
(4)在下列配制过程示意图中,有错误的是(填写序号)

(5)在定容操作时,因不慎加水至凹液面最低处超过了刻度线,该如何处理:
(6)下列说法正确的是
A.洗涤烧杯和玻璃棒2-3次,并将洗涤液移入容量瓶以减少误差
B.将浓硫酸稀释后未冷却至室温便将溶液转移至容量瓶,所配溶液浓度会偏低
C.定容时仰视观察,所配溶液浓度会偏低
D.容量瓶使用前先要检查是否漏液,具体操作是向容量瓶中加蒸馏水,倒置不漏液即可
E.容量瓶在使用前未干燥,里面有少量蒸馏水,所配溶液浓度会偏低
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】实验室欲配制250 mL 1 mol·L-1氢氧化钠溶液。
(1)实验步骤如下:
①计算:需要NaOH固体质量为___________ g。
②称量:用托盘天平称取NaOH固体,称量时要注意两个问题:一要装在烧杯里称,二要迅速。
③溶解:用量筒量取蒸馏水注入烧杯里,搅拌。
④冷却:将溶液冷却至室温。
⑤移液:将冷却溶液用___________ 引流到容量瓶中。
⑥洗涤:用适量蒸馏水洗涤烧杯和玻璃棒___________ ,并将洗涤液注入容量瓶里。
⑦振荡:手持容量瓶轻轻振荡,使溶液充分混合均匀。
⑧定容:继续加蒸馏水至距刻度线___________ 处,然后改用___________ 滴加蒸馏水至液面与刻度线相切。
⑨摇匀:盖好玻璃塞,反复上下颠倒,使溶液混合均匀。
(2)在配制过程中,下列实验操作对所配制的NaOH溶液的物质的量浓度有何影响?(在横线上填“偏大”“偏小”或“无影响”)。
①定容时俯视___________ 。
②定容后经振荡、摇匀、静置,发现液面下降,再加适量的蒸馏水___________ 。
③配制溶液前,所用的容量瓶还有少量水___________ 。
(1)实验步骤如下:
①计算:需要NaOH固体质量为
②称量:用托盘天平称取NaOH固体,称量时要注意两个问题:一要装在烧杯里称,二要迅速。
③溶解:用量筒量取蒸馏水注入烧杯里,搅拌。
④冷却:将溶液冷却至室温。
⑤移液:将冷却溶液用
⑥洗涤:用适量蒸馏水洗涤烧杯和玻璃棒
⑦振荡:手持容量瓶轻轻振荡,使溶液充分混合均匀。
⑧定容:继续加蒸馏水至距刻度线
⑨摇匀:盖好玻璃塞,反复上下颠倒,使溶液混合均匀。
(2)在配制过程中,下列实验操作对所配制的NaOH溶液的物质的量浓度有何影响?(在横线上填“偏大”“偏小”或“无影响”)。
①定容时俯视
②定容后经振荡、摇匀、静置,发现液面下降,再加适量的蒸馏水
③配制溶液前,所用的容量瓶还有少量水
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】实验室现需要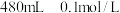 葡萄糖
葡萄糖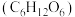 溶液。请根据所学知识回答下列问题:
溶液。请根据所学知识回答下列问题:
(1)葡萄糖的摩尔质量为___________ 。
(2)配制该溶液所需仪器有天平、量筒、烧杯、玻璃棒、胶头滴管、___________ 。
(3)需称量葡萄糖固体的质量为___________ g。
a.向容量瓶中直接加蒸馏水至离刻度线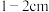 处
处
b.将溶液冷却至室温后转移到容量瓶中
c.将配制好的溶液转入准备好的试剂瓶中贮存备用
d.将称量好的葡萄糖用适量水在小烧杯内溶解
e.称量配制溶液所需的葡萄糖
f.盖上容量瓶塞子,上下颠倒容量瓶使溶液混合均匀
g.用胶头滴管小心加蒸馏水至刻度线
h.用少量蒸馏水洗涤小烧杯和玻璃棒 次,并将洗涤液转移到容量瓶中
次,并将洗涤液转移到容量瓶中
①容量瓶使用前应___________ 。
②正确的操作顺序是___________ (填标号)。
③此实验中两次用到玻璃棒,先后作用分别是___________ 、___________ 。
④判断下列操作对所配制溶液的浓度有何影响(填“偏高”、“偏低”或“无影响”):
i.转移溶液后的小烧杯,玻璃棒未洗涤___________ 。
ii.转移溶液前,容量瓶中有少量的蒸馏水___________ 。
iii.定容时俯视刻度线___________ 。
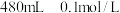 葡萄糖
葡萄糖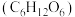 溶液。请根据所学知识回答下列问题:
溶液。请根据所学知识回答下列问题:(1)葡萄糖的摩尔质量为
(2)配制该溶液所需仪器有天平、量筒、烧杯、玻璃棒、胶头滴管、
(3)需称量葡萄糖固体的质量为
a.向容量瓶中直接加蒸馏水至离刻度线
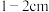 处
处b.将溶液冷却至室温后转移到容量瓶中
c.将配制好的溶液转入准备好的试剂瓶中贮存备用
d.将称量好的葡萄糖用适量水在小烧杯内溶解
e.称量配制溶液所需的葡萄糖
f.盖上容量瓶塞子,上下颠倒容量瓶使溶液混合均匀
g.用胶头滴管小心加蒸馏水至刻度线
h.用少量蒸馏水洗涤小烧杯和玻璃棒
 次,并将洗涤液转移到容量瓶中
次,并将洗涤液转移到容量瓶中①容量瓶使用前应
②正确的操作顺序是
③此实验中两次用到玻璃棒,先后作用分别是
④判断下列操作对所配制溶液的浓度有何影响(填“偏高”、“偏低”或“无影响”):
i.转移溶液后的小烧杯,玻璃棒未洗涤
ii.转移溶液前,容量瓶中有少量的蒸馏水
iii.定容时俯视刻度线
您最近一年使用:0次
【推荐1】氧化剂和还原剂在生产生活中广泛使用。
(1)高锰酸钾和氢溴酸溶液可以发生如下反应:2KMnO4+16HBr=2KBr+2MnBr2+8H2O+5Br2
①其中还原剂和氧化剂的物质的量之比为_______________ 。
②若消耗0.1mol氧化剂,则被氧化的还原剂的物质的量为_________ ,转移电子的数目是____ 。
(2)人体内所含铁元素以Fe2+和Fe3+的形式存在。市场出售的某种麦片中含有微量的颗粒细小的还原铁粉,这些铁粉在人体胃酸的作用下转化成亚铁盐,此反应的离子方程式为_________________________________________ ,但Fe2+在酸性条件下很容易被空气中的氧气氧化,写出该反应的离子方程式_________________________________ 。
(3)次磷酸(H3PO2)是一种精细化工产品,是一元中强酸,其电离方程式是:H3PO2 H++H2PO
H++H2PO ,具有较强还原性,回答下列问题:
,具有较强还原性,回答下列问题:
①H3PO2中,磷元素的化合价为_________ 。
②H3PO2及NaH2PO2均可将溶液中的银离子还原为银单质,从而用于化学镀银。利用(H3PO2)进行化学镀银反应中,氧化剂与还原剂的物质的量之比为4︰1,则氧化产物为:_________ 。
A.PH3 B.H3PO3 C.P D.H3PO4
③NaH2PO2是____________ (填正盐或酸式盐)
(1)高锰酸钾和氢溴酸溶液可以发生如下反应:2KMnO4+16HBr=2KBr+2MnBr2+8H2O+5Br2
①其中还原剂和氧化剂的物质的量之比为
②若消耗0.1mol氧化剂,则被氧化的还原剂的物质的量为
(2)人体内所含铁元素以Fe2+和Fe3+的形式存在。市场出售的某种麦片中含有微量的颗粒细小的还原铁粉,这些铁粉在人体胃酸的作用下转化成亚铁盐,此反应的离子方程式为
(3)次磷酸(H3PO2)是一种精细化工产品,是一元中强酸,其电离方程式是:H3PO2
 H++H2PO
H++H2PO ,具有较强还原性,回答下列问题:
,具有较强还原性,回答下列问题:①H3PO2中,磷元素的化合价为
②H3PO2及NaH2PO2均可将溶液中的银离子还原为银单质,从而用于化学镀银。利用(H3PO2)进行化学镀银反应中,氧化剂与还原剂的物质的量之比为4︰1,则氧化产物为:
A.PH3 B.H3PO3 C.P D.H3PO4
③NaH2PO2是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】高铁酸钠(Na2FeO4)是一种新型的净水剂,可以通过下述反应制取:2Fe(OH)3+4NaOH+3NaClO=2Na2FeO4+3NaCl+5H2O
(1)该反应中氧化剂是_______ (填化学式,下同),还原剂是_______ ,_______ 元素被氧化,还原产物为_______ 。
(2)用单线桥在方程式中标出电子转移情况:_______ 。
2Fe(OH)3+4NaOH+3NaClO=2Na2FeO4+3NaCl+5H2O
(3)当反应中有1个 离子生成时,转移的电子数是
离子生成时,转移的电子数是_______ 个。
(1)该反应中氧化剂是
(2)用单线桥在方程式中标出电子转移情况:
2Fe(OH)3+4NaOH+3NaClO=2Na2FeO4+3NaCl+5H2O
(3)当反应中有1个
 离子生成时,转移的电子数是
离子生成时,转移的电子数是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】为治理汽车尾气中的NO和CO对环境的污染,可在汽车排气管上安装催化转化器,发生的反应为2NO+2CO═N2+2CO2。
(1)碳元素的化合价_______ (填“升高”或“降低”),被_______ (填“氧化”或“还原”),CO是_______ 剂(填“氧化”或“还原”),NO是_______ 剂(填“氧化”或“还原”),发生_______ 反应。(填“氧化”或“还原”)
(2)用双线桥表示此反应中的电子得失情况2NO+2CO═N2+2CO2_______ 。
(3)用单线桥表示此反应中的电子转移情况2NO+2CO═N2+2CO2_______ 。
(4)若反应中消耗了2molCO,则生成N2的物质的量为_______ mol,转移电子的物质的量为_______ mol。
(1)碳元素的化合价
(2)用双线桥表示此反应中的电子得失情况2NO+2CO═N2+2CO2
(3)用单线桥表示此反应中的电子转移情况2NO+2CO═N2+2CO2
(4)若反应中消耗了2molCO,则生成N2的物质的量为
您最近一年使用:0次

 固体中混有的
固体中混有的 杂质的化学方程式:
杂质的化学方程式:


