A、B、C、D、E代表5种元素。请填空:
(1)A元素基态原子的最外层有3个未成对电子,次外层有2个电子,其基态原子的电子排布图为___________ 。
(2)B元素的负一价离子和C元素的正一价离子的电子层结构都与氩相同,B-的结构示意图为___________ ,C元素在元素周期表的___________ 区,写出常温下B的单质与C的最高价氧化物对应水化物反应的化学方程式:___________ 。
(3)D元素的正三价离子的3d能级为半充满状态,其基态原子的电子排布式为___________ 。
试根据原子核外电子排布所遵循的原理解释D的二价阳离子具有较强的还原性,易被氧化为正三价离子的原因:___________ 。
(4)E元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子,其基态原子的价电子排布式为___________ 。
(1)A元素基态原子的最外层有3个未成对电子,次外层有2个电子,其基态原子的电子排布图为
(2)B元素的负一价离子和C元素的正一价离子的电子层结构都与氩相同,B-的结构示意图为
(3)D元素的正三价离子的3d能级为半充满状态,其基态原子的电子排布式为
试根据原子核外电子排布所遵循的原理解释D的二价阳离子具有较强的还原性,易被氧化为正三价离子的原因:
(4)E元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子,其基态原子的价电子排布式为
更新时间:2024-05-09 17:31:18
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】下表为元素周期表一部分,请参照元素①-⑨在表中位置,用化学用语回答下列问题:
(1)写出⑧的原子结构示意图和周期表里的位置_______ ,_______ 。
(2)④、⑤、⑥的原子半径由大到小顺序为_______ (用元素符号回答)
(3)②、⑦、⑧的最高价含氧酸的酸性由强到弱的顺序是_______ (用化学式回答)
(4)②的氢化物和它的最高价含氧酸反应的化学方程式_______ 。
(5)⑤元素与⑧元素形成化合物中,化学键类型_______ 。
(6)元素①形成的单质和元素⑧形成的单质在点燃的条件下,发生反应的方程式:_______ ,现象是 _______ ,生成物的电子式: _______ 。
| ① | |||||||||||||||||
| ② | ③ | ④ | |||||||||||||||
| ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |||||||||||||
(1)写出⑧的原子结构示意图和周期表里的位置
(2)④、⑤、⑥的原子半径由大到小顺序为
(3)②、⑦、⑧的最高价含氧酸的酸性由强到弱的顺序是
(4)②的氢化物和它的最高价含氧酸反应的化学方程式
(5)⑤元素与⑧元素形成化合物中,化学键类型
(6)元素①形成的单质和元素⑧形成的单质在点燃的条件下,发生反应的方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】回答下列问题:
(1)①写出 Cl-的结构示意图_______ ;
②写出 NaHSO4 在水溶液中的电离方程式_______ 。
(2)写出电解饱和食盐水的离子方程式_______ ; 写出镁与 CO2 反应的化学方程式_______ 。
(3)已知阴离子 R2﹣的原子核内有 n 个中子,R 原子的质量数为 m,则 w 克 R2-所含有电子的物质的量是_______ 。
(1)①写出 Cl-的结构示意图
②写出 NaHSO4 在水溶液中的电离方程式
(2)写出电解饱和食盐水的离子方程式
(3)已知阴离子 R2﹣的原子核内有 n 个中子,R 原子的质量数为 m,则 w 克 R2-所含有电子的物质的量是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】呋喃(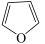 )、噻吩(
)、噻吩( )、吡咯(
)、吡咯(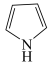 )和苯结构相似,所有的原子共平面,具有芳香性,是有机工业的重要基础原料。利用高粱秆生产呋喃过程中会用到锌、铬和锰的化合物作催化剂。请回答下列问题:
)和苯结构相似,所有的原子共平面,具有芳香性,是有机工业的重要基础原料。利用高粱秆生产呋喃过程中会用到锌、铬和锰的化合物作催化剂。请回答下列问题:
(1)基态Zn原子的价电子轨道表示式为_______ ;Cr在元素周期表中的位置是_______ ;Mn属于_______ 区。
(2)已知吡咯中含有大 键
键 (5个原子共用6个电子),则吡咯中N原子的价层孤电子对占据_______(填字母)。
(5个原子共用6个电子),则吡咯中N原子的价层孤电子对占据_______(填字母)。
(3) 、
、 的碱性随N原子电子云密度的增大而增强,其中碱性较强的是
的碱性随N原子电子云密度的增大而增强,其中碱性较强的是_______ 。
(4)呋喃的氢化饱和产物( )极易溶于水,可能的原因是
)极易溶于水,可能的原因是_______ 。
 )、噻吩(
)、噻吩( )、吡咯(
)、吡咯( )和苯结构相似,所有的原子共平面,具有芳香性,是有机工业的重要基础原料。利用高粱秆生产呋喃过程中会用到锌、铬和锰的化合物作催化剂。请回答下列问题:
)和苯结构相似,所有的原子共平面,具有芳香性,是有机工业的重要基础原料。利用高粱秆生产呋喃过程中会用到锌、铬和锰的化合物作催化剂。请回答下列问题:(1)基态Zn原子的价电子轨道表示式为
(2)已知吡咯中含有大
 键
键 (5个原子共用6个电子),则吡咯中N原子的价层孤电子对占据_______(填字母)。
(5个原子共用6个电子),则吡咯中N原子的价层孤电子对占据_______(填字母)。| A.2s轨道 | B.2p轨道 | C.sp杂化轨道 | D.sp2杂化轨道 |
 、
、 的碱性随N原子电子云密度的增大而增强,其中碱性较强的是
的碱性随N原子电子云密度的增大而增强,其中碱性较强的是(4)呋喃的氢化饱和产物(
 )极易溶于水,可能的原因是
)极易溶于水,可能的原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】原子序数小于36的X、Y、Z、M、N、W六种元素,原子序数依次增大。已知X是迄今为止形成化合物最多的元素。Y原子最外层电子数与核外电子总数之比为3∶4。M元素的常见氧化物有两种,其中一种常温下为气体,且是主要的大气污染物。Z、M、N 同周期,M2-、N-、Z+ 离子半径逐渐减小。W是第Ⅷ族元素中原子序数最小的元素。据此回答:
(1)写出W在周期表中位于哪一区:_____________ ,X与N按1:4形成的化合物中,X和N之间的σ键的类型:____________ ;
(2)用电子式表示Z与M形成化合物的过程_____________________________________ ;
(3)X、Y、M的电负性由小到大的顺序是____________________ 填元素符号);N3一与X、Y形成的一种化合物互为等电子体,则N3一的空间构型为________________ ;
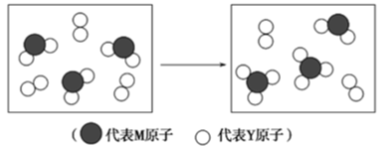
(4)下图表示由上述两种元素组成的气体分子在一定条件下的密闭容器中充分反应前后的转化关系,请写出该转化过程的化学方程式:____________________
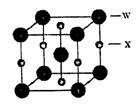
(5)X和W所形成的某种晶体结构如右图所示,写出: 基态W3+离子的结构示意图:_____________ ;
(6)N元素基态原子核外电子有_______ 种空间运动状态?
(1)写出W在周期表中位于哪一区:
(2)用电子式表示Z与M形成化合物的过程
(3)X、Y、M的电负性由小到大的顺序是
(4)下图表示由上述两种元素组成的气体分子在一定条件下的密闭容器中充分反应前后的转化关系,请写出该转化过程的化学方程式:


(5)X和W所形成的某种晶体结构如右图所示,写出: 基态W3+离子的结构示意图:
(6)N元素基态原子核外电子有
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】海水是资源宝库,蕴藏着丰富的化学元素,如氯、溴、碘等。完成下列填空:
(1)氯离子原子核外有___ 种不同运动状态的电子,有___ 种不同能量的电子,共占据了___ 个轨道。
(2)溴在周期表中的位置___ 。HI的稳定性比HBr___ (填写“强”或“弱”)。
(3)卤素单质及其化合物在许多性质上都存在递变规律,请说明下列递变规律的原因。
①熔点按F2、Cl2、Br2、I2的顺序依次升高,原因是___ 。
②还原性按Cl-、Br-、I-的顺序依次增大,原因是___ 。
(4)ClO2和碱溶液反应生成亚氯酸盐(阴离子是ClO2-)和氯酸盐,其离子方程式是___ ,氧化产物___ 。(填离子符号)
(5)HClO有很好的杀菌消毒效果,为增强氯水的杀菌消毒能力,可用饱和氯水与小苏打反应来达到目的,试用平衡移动原理解释其原因___ 。
(1)氯离子原子核外有
(2)溴在周期表中的位置
(3)卤素单质及其化合物在许多性质上都存在递变规律,请说明下列递变规律的原因。
①熔点按F2、Cl2、Br2、I2的顺序依次升高,原因是
②还原性按Cl-、Br-、I-的顺序依次增大,原因是
(4)ClO2和碱溶液反应生成亚氯酸盐(阴离子是ClO2-)和氯酸盐,其离子方程式是
(5)HClO有很好的杀菌消毒效果,为增强氯水的杀菌消毒能力,可用饱和氯水与小苏打反应来达到目的,试用平衡移动原理解释其原因
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】依据原子结构知识回答下列问题。
(1)基态Cr原子的电子排布式是___________ 。
(2)下列有关微粒性质的排列顺序错误的是___________。
(3)下列硼原子电子排布图表示的状态中,能量最高的为___________(填选项字母)。
(4)O的基态原子核外电子空间运动状态有___________ 种,其原子半径___________  (填“大于”或“小于”)。
(填“大于”或“小于”)。
(1)基态Cr原子的电子排布式是
(2)下列有关微粒性质的排列顺序错误的是___________。
A.元素的电负性: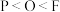 | B.元素的第一电离能: |
C.离子半径: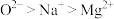 | D.原子的未成对电子数: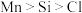 |
(3)下列硼原子电子排布图表示的状态中,能量最高的为___________(填选项字母)。
A. | B.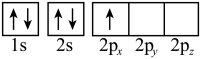 |
C.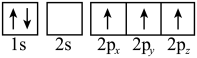 | D.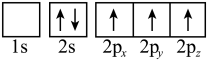 |
(4)O的基态原子核外电子空间运动状态有
 (填“大于”或“小于”)。
(填“大于”或“小于”)。
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】过渡金属元素在工农业生产和国防建设中有着广泛应用。回答下列问题:
(1)原子序数为21~30的元素基态原子中,未成对电子数最多的和成对电子数最多的元素在周期表中的位置分别是______ 和______ 。
(2)基态钒原子核外电子的运动状态有_____ 种。
(3)A元素M层电子数是N电子数7倍,其价层电子轨道表示式________ 。
(4)C元素基态原子的轨道表示式是下图中的_____ (填“①”或“②”),另一轨道表示式不能作为基态原子的轨道表示式是因为它不符合_____ (填“A”“B”或“C”)。
(5)第三周期元素的气态电中性基态原子失去最外层一个电子转化为气态基态正离子所需的最低能量叫作第一电离能(设为I1)。如图所示:_____ 。
②根据图中提供的信息,可推断出I1(N)_____ I1(O)(填“>”“<”或“=”);原因是_____ 。
(1)原子序数为21~30的元素基态原子中,未成对电子数最多的和成对电子数最多的元素在周期表中的位置分别是
(2)基态钒原子核外电子的运动状态有
(3)A元素M层电子数是N电子数7倍,其价层电子轨道表示式
(4)C元素基态原子的轨道表示式是下图中的
①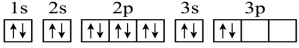
②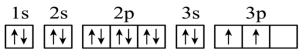
(5)第三周期元素的气态电中性基态原子失去最外层一个电子转化为气态基态正离子所需的最低能量叫作第一电离能(设为I1)。如图所示:
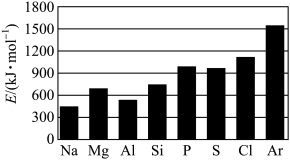
②根据图中提供的信息,可推断出I1(N)
您最近一年使用:0次

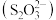 可看作是
可看作是 中的一个O原子被S原子取代的产物。
中的一个O原子被S原子取代的产物。 的空间结构是
的空间结构是 形成
形成 。分别判断
。分别判断

