高效氧化剂亚氯酸钠( )常用于烟气脱硝(
)常用于烟气脱硝( )和废水脱除氨氮。
)和废水脱除氨氮。
(1) 的制备。一种制备
的制备。一种制备 的过程可表示为
的过程可表示为_______ 。
②“反应1”的产物 经净化后常作为饮用水消毒剂替代传统的
经净化后常作为饮用水消毒剂替代传统的 ,从消毒后饮用水水质和消毒效率(单位质量消毒剂被还原时得电子数)的角度考虑,用
,从消毒后饮用水水质和消毒效率(单位质量消毒剂被还原时得电子数)的角度考虑,用 替代
替代 的原因是
的原因是_______ 。
(2) 溶液对烟气脱硝。
溶液对烟气脱硝。
①酸性条件下, 可催化溶液中的
可催化溶液中的 产生氧化性更强的
产生氧化性更强的 气体,总反应可表示为
气体,总反应可表示为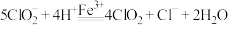 。请补充完整过程Ⅱ的离子方程式:
。请补充完整过程Ⅱ的离子方程式:
I.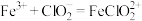 ;
;
Ⅱ._______ ;
Ⅲ.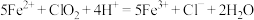 。
。
② 催化
催化 溶液脱硝。其他条件相同时,烟气中NO氧化率随
溶液脱硝。其他条件相同时,烟气中NO氧化率随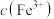 、反应温度的变化分别如图所示。
、反应温度的变化分别如图所示。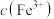 增大而增大的原因是
增大而增大的原因是_______ 。
ii.温度升高,NO氧化率先增大后减小的可能原因是_______ 。
(3) 溶液处理氨氮废水。向一定量酸性氨氮废水中加入一定体积已知浓度的
溶液处理氨氮废水。向一定量酸性氨氮废水中加入一定体积已知浓度的 溶液,用传感器测得溶液中
溶液,用传感器测得溶液中 与
与 含量随反应时间的变化如图所示。判断该实验中被氧化的
含量随反应时间的变化如图所示。判断该实验中被氧化的 是否全部转化为
是否全部转化为 的依据为
的依据为_______ 。
 )常用于烟气脱硝(
)常用于烟气脱硝( )和废水脱除氨氮。
)和废水脱除氨氮。(1)
 的制备。一种制备
的制备。一种制备 的过程可表示为
的过程可表示为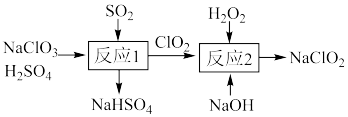
②“反应1”的产物
 经净化后常作为饮用水消毒剂替代传统的
经净化后常作为饮用水消毒剂替代传统的 ,从消毒后饮用水水质和消毒效率(单位质量消毒剂被还原时得电子数)的角度考虑,用
,从消毒后饮用水水质和消毒效率(单位质量消毒剂被还原时得电子数)的角度考虑,用 替代
替代 的原因是
的原因是(2)
 溶液对烟气脱硝。
溶液对烟气脱硝。①酸性条件下,
 可催化溶液中的
可催化溶液中的 产生氧化性更强的
产生氧化性更强的 气体,总反应可表示为
气体,总反应可表示为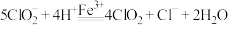 。请补充完整过程Ⅱ的离子方程式:
。请补充完整过程Ⅱ的离子方程式:I.
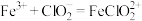 ;
;Ⅱ.
Ⅲ.
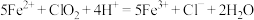 。
。②
 催化
催化 溶液脱硝。其他条件相同时,烟气中NO氧化率随
溶液脱硝。其他条件相同时,烟气中NO氧化率随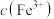 、反应温度的变化分别如图所示。
、反应温度的变化分别如图所示。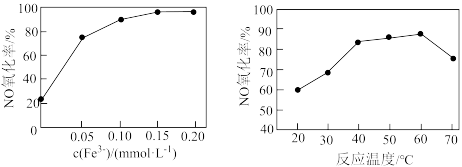
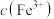 增大而增大的原因是
增大而增大的原因是ii.温度升高,NO氧化率先增大后减小的可能原因是
(3)
 溶液处理氨氮废水。向一定量酸性氨氮废水中加入一定体积已知浓度的
溶液处理氨氮废水。向一定量酸性氨氮废水中加入一定体积已知浓度的 溶液,用传感器测得溶液中
溶液,用传感器测得溶液中 与
与 含量随反应时间的变化如图所示。判断该实验中被氧化的
含量随反应时间的变化如图所示。判断该实验中被氧化的 是否全部转化为
是否全部转化为 的依据为
的依据为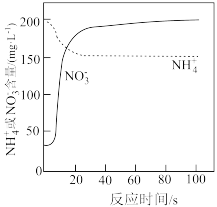
2024·江苏南京·二模 查看更多[2]
更新时间:2024-05-14 19:08:41
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】铋酸钠(NaBiO3)是分析化学中的重要试剂。某兴趣小组设计实验制取铋酸钠并探究其应用。回答下列问题:
Ⅰ、制取铋酸钠:制取装置如图(加热和夹持仪器已略去)。
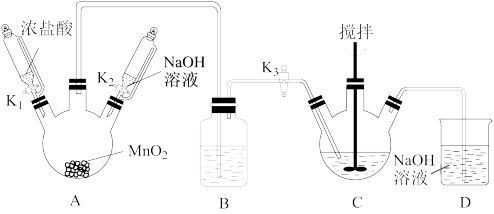
部分物质性质如下:
(1)反应开始时,打开K1和K3,写出A中反应的化学方程式_______ 。B装置的作用是_______ 。
(2)C中盛放Bi(OH)3与NaOH混合物,与Cl2反应生成NaBiO3,反应的离子方程式为_______ 。反应过程中观察到C中的主要现象是_______ 。
(3)反应结束后,为从装置C中获得尽可能多的产品,需要的操作是_______ ,过滤、洗涤、干燥。
(4)拆除装置前须先除去A中残留的Cl2以免污染空气,除去Cl2的操作是关闭_______ ,打开_______ 。
Ⅱ、铋酸钠的应用——检验Mn2+
(5)向待测液中加入铋酸钠晶体,加入硫酸酸化,溶液变为紫红色,证明待测液中存在Mn2+(铋酸钠转变为Bi3+),产生紫红色现象的离子方程式为_______ 。
Ⅰ、制取铋酸钠:制取装置如图(加热和夹持仪器已略去)。

部分物质性质如下:
| 物质 | NaBiO3 | Bi(OH)3 |
| 性质 | 不溶于冷水,浅黄色 | 难溶于水;白色 |
(2)C中盛放Bi(OH)3与NaOH混合物,与Cl2反应生成NaBiO3,反应的离子方程式为
(3)反应结束后,为从装置C中获得尽可能多的产品,需要的操作是
(4)拆除装置前须先除去A中残留的Cl2以免污染空气,除去Cl2的操作是关闭
Ⅱ、铋酸钠的应用——检验Mn2+
(5)向待测液中加入铋酸钠晶体,加入硫酸酸化,溶液变为紫红色,证明待测液中存在Mn2+(铋酸钠转变为Bi3+),产生紫红色现象的离子方程式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】某化学小组利用如图装置制备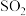 并探究其性质。
并探究其性质。
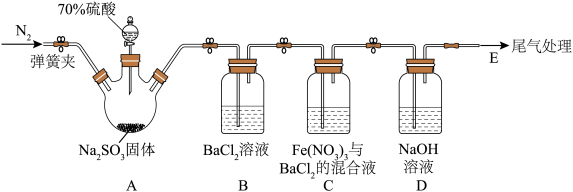
回答下列问题:
(1)盛放 固体的仪器名称为
固体的仪器名称为___________ 。
(2)实验前,检查装置气密性的方法为按图示连接好装置,___________ 。
(3)实验时,观察到装置B中无明显现象,装置C中有白色沉淀生成,据此推测装置C中白色沉淀的成分为___________ (填化学式)。该小组同学猜想产生该物质的原因可能有两种:
i. 氧化了
氧化了
ⅱ.___________
(4)为了验证猜想,小组同学进行了以下实验:
①为了验证猜想i,小组同学取少量装置B中反应后的溶液置于试管中,向其中滴加 溶液,产生了白色沉淀,写出该反应的离子方程式:
溶液,产生了白色沉淀,写出该反应的离子方程式:___________ 。
②为了验证猜想ⅱ,小组同学取少量装置B中反应后的溶液置于试管中,向其中滴加 溶液,也产生了白色沉淀,写出该反应的离子方程式:
溶液,也产生了白色沉淀,写出该反应的离子方程式:___________ 。
③据此小组同学认为猜想i和ⅱ均正确,为进一步检验装置中是否有猜想i的反应发生,还需要向反应后的装置C溶液中滴加___________ 进行验证。
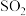 并探究其性质。
并探究其性质。
回答下列问题:
(1)盛放
 固体的仪器名称为
固体的仪器名称为(2)实验前,检查装置气密性的方法为按图示连接好装置,
(3)实验时,观察到装置B中无明显现象,装置C中有白色沉淀生成,据此推测装置C中白色沉淀的成分为
i.
 氧化了
氧化了
ⅱ.
(4)为了验证猜想,小组同学进行了以下实验:
①为了验证猜想i,小组同学取少量装置B中反应后的溶液置于试管中,向其中滴加
 溶液,产生了白色沉淀,写出该反应的离子方程式:
溶液,产生了白色沉淀,写出该反应的离子方程式:②为了验证猜想ⅱ,小组同学取少量装置B中反应后的溶液置于试管中,向其中滴加
 溶液,也产生了白色沉淀,写出该反应的离子方程式:
溶液,也产生了白色沉淀,写出该反应的离子方程式:③据此小组同学认为猜想i和ⅱ均正确,为进一步检验装置中是否有猜想i的反应发生,还需要向反应后的装置C溶液中滴加
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】孔雀石主要成分是 ,还含少量
,还含少量 及硅的氧化物,实验室以孔雀石为原料制备硫酸铜晶体的步骤如下:
及硅的氧化物,实验室以孔雀石为原料制备硫酸铜晶体的步骤如下:

有关物质沉淀的pH数据如下:
(1)步骤Ⅰ加稀硫酸充分反应,提高步骤Ⅰ反应速率的措施是_______ (写一条即可)。
(2)步骤Ⅱ中试剂①应选用试剂_______ (填代号)。
a. b.稀
b.稀 c.双氧水 d.氯水
c.双氧水 d.氯水
相关反应的离子方程式为:_______ 。
(3)步骤Ⅲ加入CuO调节溶液的pH至_______ (填写范围),目的是_______ 。
(4)从滤液3中获得干燥的硫酸铜晶体的操作是_______ 。
(5)常温下 的
的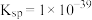 ,若要将溶液中的
,若要将溶液中的 转化为
转化为 沉淀,使溶液中
沉淀,使溶液中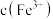 降低至
降低至 ,必须将溶液调节至
,必须将溶液调节至
_______ 。
(6)用 和孔雀石反应可以制得金属铜,已知1mol氨气通过灼热的
和孔雀石反应可以制得金属铜,已知1mol氨气通过灼热的 可以产生
可以产生 金属铜,则该反应的化学方程式为
金属铜,则该反应的化学方程式为_______ 。
 ,还含少量
,还含少量 及硅的氧化物,实验室以孔雀石为原料制备硫酸铜晶体的步骤如下:
及硅的氧化物,实验室以孔雀石为原料制备硫酸铜晶体的步骤如下:
有关物质沉淀的pH数据如下:
| 物质 |  开始沉淀 开始沉淀 |  完全沉淀 完全沉淀 |
 | 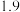 |  |
 | 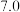 |  |
 |  | 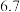 |
(1)步骤Ⅰ加稀硫酸充分反应,提高步骤Ⅰ反应速率的措施是
(2)步骤Ⅱ中试剂①应选用试剂
a.
 b.稀
b.稀 c.双氧水 d.氯水
c.双氧水 d.氯水相关反应的离子方程式为:
(3)步骤Ⅲ加入CuO调节溶液的pH至
(4)从滤液3中获得干燥的硫酸铜晶体的操作是
(5)常温下
 的
的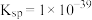 ,若要将溶液中的
,若要将溶液中的 转化为
转化为 沉淀,使溶液中
沉淀,使溶液中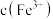 降低至
降低至 ,必须将溶液调节至
,必须将溶液调节至
(6)用
 和孔雀石反应可以制得金属铜,已知1mol氨气通过灼热的
和孔雀石反应可以制得金属铜,已知1mol氨气通过灼热的 可以产生
可以产生 金属铜,则该反应的化学方程式为
金属铜,则该反应的化学方程式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】下图为实验室制取氨气、二氧化硫气体及有关性质实验的组合装置。
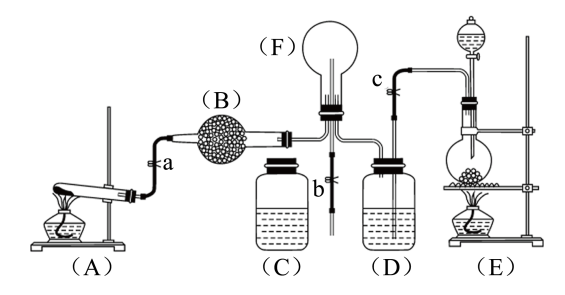
(1)如果A、E是气体制取装置,则按照题目要求,A中制取气体的化学反应方程式为____ ;
(2)实验中,B加入的药品是___ ;D中盛放的是____
(3)先加热A装置,使产生气体通入烧瓶F中,此时弹簧夹a、b打开、c关闭。当F中充满A中气体后,A停止制气,关闭a,打开弹簧夹c,使E中气体通入F中;
①如何测知F中已充满大量A中气体:____ ;
②E中气体进入F后,触发F中气体发生反应的操作是将烧瓶导管与塑料瓶C连接,并完成喷泉实验,F中气体发生反应的化学方程式为____ ;
(4)为了有效实现NO和NO2的相互转化,设计如下实验:按图组装好实验装置,并检查装置气密性,实验前用排水法收集半瓶NO气体。

①打开止水夹,推动针筒活塞,使氧气进入烧瓶。
②关上止水夹,轻轻摇动烧瓶,此时,观察到烧瓶中的现象为____
(5)可用酸性高锰酸钾溶液,吸收上述实验中的尾气,已知NO能与 在酸性条件下反应生成
在酸性条件下反应生成 和Mn2+,写出该反应的离子方程式
和Mn2+,写出该反应的离子方程式_____ 。

(1)如果A、E是气体制取装置,则按照题目要求,A中制取气体的化学反应方程式为
(2)实验中,B加入的药品是
(3)先加热A装置,使产生气体通入烧瓶F中,此时弹簧夹a、b打开、c关闭。当F中充满A中气体后,A停止制气,关闭a,打开弹簧夹c,使E中气体通入F中;
①如何测知F中已充满大量A中气体:
②E中气体进入F后,触发F中气体发生反应的操作是将烧瓶导管与塑料瓶C连接,并完成喷泉实验,F中气体发生反应的化学方程式为
(4)为了有效实现NO和NO2的相互转化,设计如下实验:按图组装好实验装置,并检查装置气密性,实验前用排水法收集半瓶NO气体。

①打开止水夹,推动针筒活塞,使氧气进入烧瓶。
②关上止水夹,轻轻摇动烧瓶,此时,观察到烧瓶中的现象为
(5)可用酸性高锰酸钾溶液,吸收上述实验中的尾气,已知NO能与
 在酸性条件下反应生成
在酸性条件下反应生成 和Mn2+,写出该反应的离子方程式
和Mn2+,写出该反应的离子方程式
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】实验室采用下列实验装置制取少量 并对其性质进行探究:
并对其性质进行探究:
(1)装置B中的现象是品红溶液___________ (填“褪色”或“不褪色”);
(2)装置C中溶液紫红色褪去,体现了 的
的___________ (填“漂白性”或“还原性”);
(3)装置E中倒置漏斗的作用是___________ ;
(4)若装置E中NaOH溶液足量,则E中发生反应的化学方程式为___________ ;
(5)欲制取2.24L(标准状况) ,至少需要
,至少需要 的质量为
的质量为___________ g。
 并对其性质进行探究:
并对其性质进行探究: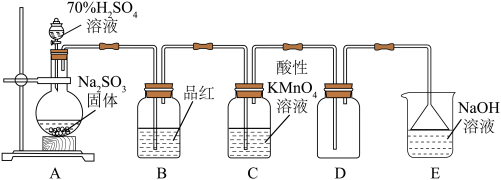

(1)装置B中的现象是品红溶液
(2)装置C中溶液紫红色褪去,体现了
 的
的(3)装置E中倒置漏斗的作用是
(4)若装置E中NaOH溶液足量,则E中发生反应的化学方程式为
(5)欲制取2.24L(标准状况)
 ,至少需要
,至少需要 的质量为
的质量为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】某研究小组探究SO2和Fe(NO3)3溶液的反应。

已知:1.0 mol/L的Fe(NO3)3溶液的pH=l;请回答:
(1)装置A中反应的化学方程式是_______ 。
(2)为排除空气对实验的干扰,滴加浓硫酸之前应进行的操作是_______ 。
(3)装置B中产生了白色沉淀,其成分是_______ ,说明SO2具有_______ 性。
(4)分析B中产生白色沉淀的原因:
观点1._______ ;
观点2:SO2与Fe3+反应;
观点3:在酸性条件下SO2与NO 反应;
反应;
①按观点2,装置B中反应的离子方程式是_______ ,为证明该观点应进一步检验生成的新物质,其实验操作及现象是_______ 。
②按观点3,只需将装置B中的Fe(NO3)3溶液替换为等体积的下列溶液,在相同条件下进行实验。应选择的试剂是(填序号)_______ 。
a.0.1 mol/L稀硝酸
b.1.5 mol/L Fe(NO3)2溶液
c.6.0 mol/L NaNO3和0.2 mol/L盐酸等体积混合的溶液

已知:1.0 mol/L的Fe(NO3)3溶液的pH=l;请回答:
(1)装置A中反应的化学方程式是
(2)为排除空气对实验的干扰,滴加浓硫酸之前应进行的操作是
(3)装置B中产生了白色沉淀,其成分是
(4)分析B中产生白色沉淀的原因:
观点1.
观点2:SO2与Fe3+反应;
观点3:在酸性条件下SO2与NO
 反应;
反应;①按观点2,装置B中反应的离子方程式是
②按观点3,只需将装置B中的Fe(NO3)3溶液替换为等体积的下列溶液,在相同条件下进行实验。应选择的试剂是(填序号)
a.0.1 mol/L稀硝酸
b.1.5 mol/L Fe(NO3)2溶液
c.6.0 mol/L NaNO3和0.2 mol/L盐酸等体积混合的溶液
您最近一年使用:0次



