已知25℃时,几种酸或碱的电离常数如表所示。对于下列实验,能正确描述其反应的离子方程式的是
物质 |
|
| HClO |
|
电离常数 |
|
|
|
|
|
|
A.用 溶液吸收少量 溶液吸收少量 : : |
B.向 溶液滴加少量 溶液滴加少量 溶液: 溶液: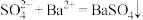 |
C.少量的 通入到NaClO溶液中: 通入到NaClO溶液中: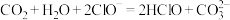 |
D.石墨电极电解 水溶液: 水溶液: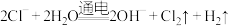 |
更新时间:2024-05-12 08:47:36
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】能正确表示下列变化的离子方程式是
| A.磁性氧化铁溶于足量稀盐酸:Fe3O4+8H+=2Fe2++Fe3++4H2O |
B.Na2O2溶于水产生O2:2 +2H2O=4OH-+O2↑ +2H2O=4OH-+O2↑ |
C.NH4HCO3溶液和过量Ca(OH)2溶液混合:Ca2++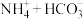 +2OH-=CaCO3↓+H2O+NH3·H2O +2OH-=CaCO3↓+H2O+NH3·H2O |
| D.氯化铝溶液中加入足量氨水Al3++3OH-=Al(OH)3↓ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列离子方程式书写正确的是
A.铁与稀硫酸反应: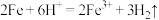 |
B.金属钠与水反应: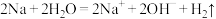 |
C.碳酸钙与盐酸反应: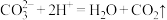 |
D.硫酸溶液和氢氧化钡溶液: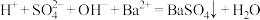 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】一种新型镁储备电池储存寿命长,电压平稳,电池反应为Mg+Cu2Cl2=2Cu+MgCl2。实验室以该电池为电源处理含Na2SO4废水,同时制备NaOH和H2SO4的装置如图所示。下列说法错误的是


| A.M电极材料为Mg |
| B.ab为阴离子交换膜 |
| C.N极的电极反应式为Cu2Cl2+2e-=2Cu+2Cl- |
| D.电路上每通过4mole-,阴阳两极总共产生67.2L气体 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】以完全非碳的Pd包覆纳米多孔金(NPG@Pd)为一体化催化剂的可再充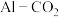 电池示意图如图所示,其正极采用纯
电池示意图如图所示,其正极采用纯 作为活性材料,放电时生成碳酸铝和碳。下列说法错误的是
作为活性材料,放电时生成碳酸铝和碳。下列说法错误的是
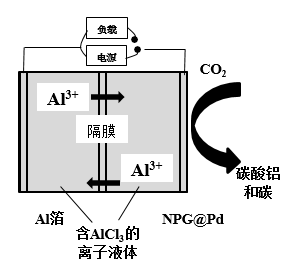
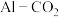 电池示意图如图所示,其正极采用纯
电池示意图如图所示,其正极采用纯 作为活性材料,放电时生成碳酸铝和碳。下列说法错误的是
作为活性材料,放电时生成碳酸铝和碳。下列说法错误的是
A.放电时,铝箔失去电子生成 , , 移向正极 移向正极 |
| B.放电时,电流由正极经负载、铝箔、电解质,回到NPG@Pd电极 |
C.充电时,阳极反应式为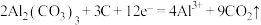 |
D.电池放电和充电时的总反应为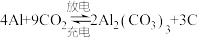 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐3】下列离子方程式书写正确的是
| A.NaClO溶液和FeCl2溶液混合:2ClO-+Fe2++2H2O=Fe(OH)2↓+2HClO |
B.苯酚浊液与纯碱溶液混合后变澄清:2C6H5OH+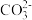 =2C6H5O-+CO2↑+H2O =2C6H5O-+CO2↑+H2O |
C.用过量氨水吸收工业尾气中的SO2:2NH3∙H2O+SO2=2 + + +H2O +H2O |
D.用铜制作电极电解CuSO4溶液:2Cu2++2H2O 2Cu↓+O2↑+4H+ 2Cu↓+O2↑+4H+ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】常温下,三种酸的电离平衡常数如下表,下列判断正确的是
| 酸 | HCN |  |  (一元酸) (一元酸) |
| 电离常数K | 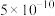 |  | 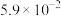 |
A.三种酸的强弱关系: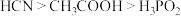 |
B.反应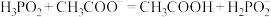 能够发生 能够发生 |
C.由电离常数可以判断, 属于强酸,HCN和 属于强酸,HCN和 属于弱酸 属于弱酸 |
| D.相同温度下,相同浓度的醋酸钠溶液pH大于氰化钠溶液pH |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】常温下,向碳酸溶液中逐滴加入NaOH溶液,所得溶液中pC(C微粒的浓度的负对数)与pH的关系如图所示。下列说法错误的是
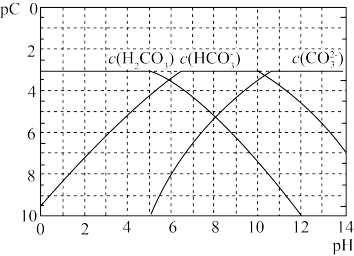

| A.由图中数据可以计算碳酸的电离常数Ka1的数量级为10-6 |
B.虽然H2CO3能与CO 能反应,但从图象中能看出这两种微粒在溶液中能够共存 能反应,但从图象中能看出这两种微粒在溶液中能够共存 |
C.pH=7的溶液中离子浓度大小关系为c( )>c(H2CO3)>c( )>c(H2CO3)>c( ) ) |
D.pH=10的溶液中离子浓度大小关系有c(Na+)<3c( ) ) |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】常温下,向一定浓度的H2X溶液中滴加NaOH溶液,混合溶液的pH与离子浓度变化的关系如图所示。下列叙述正确的是


| A.N点时,c(Na+)<3c(HX-) |
| B.水电离的c(H+):N点<M点 |
| C.H2X的电离平衡常数Ka2的数量级为10-2 |
| D.当混合溶液呈中性时,c(Na+)>c(HX-)>c(X2-)>c(H+)=c(OH-) |
您最近一年使用:0次




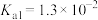





 +2C1-
+2C1- +2OH-=NH3↑+2H2O
+2OH-=NH3↑+2H2O

