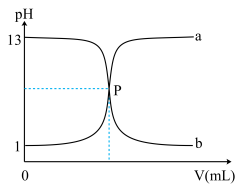
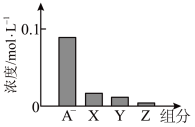
如图所示为常温下用0.1000mol·L-1NaOH溶液滴定10.00mL未知浓度的硫酸(用酚酞作指示剂)的滴定曲线。下列说法正确的是
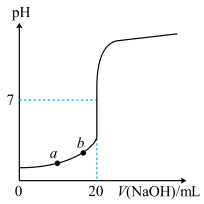
| A.水电离出的氢氧根离子浓度:a>b |
| B.硫酸的物质的量浓度为0.2000mol·L-1 |
| C.指示剂变色时,说明硫酸与NaOH恰好完全反应 |
D.当滴加NaOH溶液的体积为10.00mL时,该混合液的 =0.05mol·L-1 =0.05mol·L-1 |
更新时间:2024-05-12 16:56:37
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】室温下,柠檬水溶液的pH是3,则其中由水电离出的c(H+)是
| A.1×10-11mol·L-1 | B.1×10-3 mol·L-1 |
| C.1×10-7mol·L-1 | D.0.1mol·L-1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】常温下,在下列给定条件的溶液中,一定能大量共存的离子组是
A.澄清透明的溶液: 、 、 、 、 、 、 |
B. 的溶液: 的溶液: 、 、 、 、 、 、 |
C.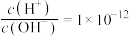 的溶液: 的溶液: 、 、 、 、 、 、 |
D.水电离出的氢离子为 的溶液: 的溶液: 、 、 、 、 、 、 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】常温下,将某一元酸HX和NaOH溶液等体积混合,两种溶液的浓度和混合后溶液的pH如下表:
下列说法不正确的是
| 实验编号 | c (HX) mol/L | c (NaOH) mol/L | 混合溶液的pH |
| 甲 | 0.1 | 0.1 | pH=a |
| 乙 | C1 | 0.1 | pH=7 |
| 丙 | 0.2 | 0.1 | pH<7 |
| 丁 | C2 | C2 | pH=10 |
| A.从甲组情况分析,若a=7,则HX为强酸;若a>7,则HX为弱酸 |
| B.在乙组混合溶液中,离子浓度c(Xˉ)=c(Na+) |
| C.从丙组实验结果分析,HX是强酸 |
| D.丁组实验所得混合溶液中,由水电离出的c(OHˉ)=10-4mol/L |
您最近一年使用:0次
【推荐1】下列装置图或曲线图与对应的叙述相符的是
A.如下图所示,用 0.1 mol·L-1 NaOH 溶液分别滴定相同物质的量浓度、相同体积的盐酸和醋酸,其中实线表示的是滴定盐酸的曲线 |
B.某温度下 FeS、CuS 的沉淀溶解平衡曲线如下图 所示。在物质的量浓度相等的 Fe2+和 Cu2+的溶液中滴加硫化钠溶液,首先沉淀的离子为 Fe2+ |
C.如下图 所示,用 0.1 mol·L-1CH3COOH 溶液滴定 20 mL 0.1 mol·L-1 NaOH 溶液的滴定曲线, 当 pH=7 时:c(Na+) = c(CH3COO-) > c(OH-) = c(H+)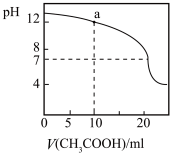 |
D.据下图,若除去CuSO4溶液中的 Fe3+可向溶液中加入适量CuO 至 pH 在 5.8 左右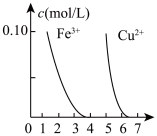 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列各组实验所选玻璃仪器和试剂,不能达到实验目的的是(不考虑存放试剂的容器)
| 实验目的 | 玻璃仪器 | 试剂 | |
| A | 测定某NaOH溶液的浓度 | 酸式滴定管、碱式滴定管、烧杯 |  HCl溶液、酚酞试剂、待测NaOH溶液、蒸馏水 HCl溶液、酚酞试剂、待测NaOH溶液、蒸馏水 |
| B | 探究浓度对化学平衡的影响 | 胶头滴管、试管、量筒 | 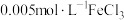 溶液、 溶液、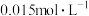 KSCN溶液、 KSCN溶液、 KSCN溶液 KSCN溶液 |
| C | 比较氯、溴、碘的非金属性 | 试管、胶头滴管 | 新制氯水、溴水、NaBr溶液、NaI溶液 |
| D | 验证铁盐的氧化性 | 试管、胶头滴管 |  溶液、KI溶液、淀粉溶液 溶液、KI溶液、淀粉溶液 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】下列说法正确的是
| A.镁与极稀硝酸反应生成硝酸铵的离子方程式为:4Mg+6H++NO3- =4Mg2++NH4++3H2O |
| B.25℃时,将20 mL 0.1mol·L-1H2SO4溶液和30 mL 0.15mol·L-1NaOH溶液混合,若混合后溶液体积不变,则混合溶液的pH为11 |
| C.将10 mL 0.1 mol·L-1KAl(SO4)2溶液和10 mL0.2 mol·L-1Ba(OH)2溶液混合,得到的沉淀中Al(OH)3和BaSO4的物质的量之比为1:2 |
| D.浓度均为0.1 mol·L-1的醋酸和CH3COONa溶液等体积混合,溶液中有下列关系:c(CH3COOH)+2c(H+)=c(CH3COO-)+2c(OH-) |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列溶液中微粒浓度关系一定正确的是
| A.氨水与氯化铵的pH=7的混合溶液中:c(Cl-)>c(NH4+) |
| B.0.1 mol ·L-1的硫酸铵溶液中:c(NH4+)> c(SO42-)> c(H+)> c(OH-) |
| C.pH=2的一元酸和pH=12的一元强碱等体积混合:c(OH-)= c(H+) |
| D.0.1 mol ·L-1的硫化钠溶液中:c(OH-)=c(H+) +c(HS-)+c(H2S) |
您最近一年使用:0次