根据实验操作及现象,得出的结论正确的是
| 选项 | 操作及现象 | 结论 |
| A | 木炭和浓硝酸共热,产生红棕色气体 |  一定是 一定是 和C反应的还原产物 和C反应的还原产物 |
| B | 向酸性 溶液中通入 溶液中通入 ,溶液褪色 ,溶液褪色 |  具有漂白性 具有漂白性 |
| C | 常温下,测定 溶液、HClO溶液pH,前者小于后者 溶液、HClO溶液pH,前者小于后者 | 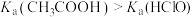 |
| D | 向碘的四氯化碳溶液中加入KI溶液,振荡,下层液体颜色变浅 |  在KI溶液中的溶解度大于在四氯化碳中的溶解度 在KI溶液中的溶解度大于在四氯化碳中的溶解度 |
| A.A | B.B | C.C | D.D |
更新时间:2024-05-22 16:47:42
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】下列化学反应的离子方程式不正确的是
A.将少量SO2气体通入足量的NaClO溶液中:SO2+ClO-+ H2O=SO +2HClO +2HClO |
B.向偏铝酸钠溶液中加入小苏打溶液:HCO +AlO +AlO +H2O=Al(OH)3↓ +CO +H2O=Al(OH)3↓ +CO |
C.向Ba(OH)2溶液中滴加NH 4HSO 4溶液至刚好沉淀完全: Ba2++ 2OH-+ NH + H++ SO + H++ SO = BaSO4↓+ NH3·H2O+ H2O = BaSO4↓+ NH3·H2O+ H2O |
D.稀硝酸中加入过量的铁屑:3Fe+ 8H+ +2NO = 3Fe2+ 2NO = 3Fe2+ 2NO + 4H2 O + 4H2 O |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列各组离子在指定溶液中一定能大量共存的是
A.明矾溶液中: 、 、 、 、 、 、 |
B.不能使酚酞变色的溶液中: 、 、 、 、 、 、 |
C. 的溶液中: 的溶液中: 、 、 、 、 、 、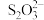 |
D.水电离出来的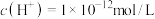 的溶液中: 的溶液中: 、 、 、 、 、 、 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】某兴趣小组为了探究SO2气体还原Fe3+的反应,他们使用的药品和装置如下图所示,下列说法不合理的是
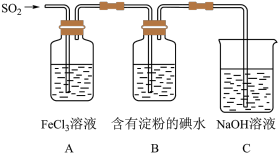
| A.能表明I-的还原性弱于SO2的现象是B中蓝色溶液褪色 |
| B.装置C的作用是吸收SO2尾气,防止污染空气 |
| C.为了验证A中发生了氧化还原反应,加入酸性KMnO4溶液,紫色褪去 |
| D.为了验证A中发生了氧化还原反应,加入用稀盐酸酸化的BaCl2溶液,产生白色沉淀 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列说法正确的是
| A.SO2能使酸性KMnO4溶液褪色,故SO2有漂白性 |
| B.NO2与水反应生成HNO3,故NO2是酸性氧化物 |
| C.H2SiO3的酸性弱于H2CO3,故非金属性C强于Si |
| D.CaCO3难溶于水,故CO2能与CaCl2溶液反应 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】根据下表提供的数据可知,在溶液中能大量共存的微粒是
| 化学式 | 电离常数 |
| CH3COOH | K=1.7×10-5 |
| HCN | K=4.9×10-10 |
| H2CO3 | K1=4.3×10-7,K2=5.6×10-11 |
| A.H2CO3、HCO3-、CH3COO-、CN- |
B.HCO3-、CH3COOH、CN-、CO |
C.HCN、HCO 、CN-、CO 、CN-、CO |
D.HCN、HCO 、CH3COO-、CN- 、CH3COO-、CN- |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】常温下,用蒸馏水稀释 的醋酸溶液至
的醋酸溶液至 ,随着溶液的稀释,下列各项中始终保持减小趋势的是
,随着溶液的稀释,下列各项中始终保持减小趋势的是
 的醋酸溶液至
的醋酸溶液至 ,随着溶液的稀释,下列各项中始终保持减小趋势的是
,随着溶液的稀释,下列各项中始终保持减小趋势的是A. | B. |
C.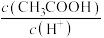 | D. |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】人体血液中存在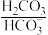 、
、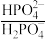 等缓冲对。常温下,水溶液中部分缓冲对的微粒浓度之比的对数值lgx[x表示
等缓冲对。常温下,水溶液中部分缓冲对的微粒浓度之比的对数值lgx[x表示 或
或 与溶液pH的关系如图所示。下列说法错误的是
与溶液pH的关系如图所示。下列说法错误的是
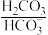 、
、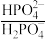 等缓冲对。常温下,水溶液中部分缓冲对的微粒浓度之比的对数值lgx[x表示
等缓冲对。常温下,水溶液中部分缓冲对的微粒浓度之比的对数值lgx[x表示 或
或 与溶液pH的关系如图所示。下列说法错误的是
与溶液pH的关系如图所示。下列说法错误的是
A.曲线I表示lg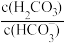 与溶液pH的变化关系 与溶液pH的变化关系 |
| B.Ka1(H2CO3)>Ka2(H3PO4) |
| C.a→b的过程中,水的电离程度逐渐减小 |
D.当pH增大时,lg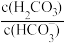 -lg -lg 的值逐渐增大 的值逐渐增大 |
您最近一年使用:0次

 反应生成气体:
反应生成气体:
 溶液中加入稀硫酸:
溶液中加入稀硫酸:
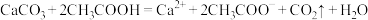


 可以循环利用
可以循环利用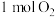 可氧化
可氧化


