分子的结构与物质性质之间存在紧密的联系。
(1)如图是部分主族元素氢化物的沸点变化趋势_______ ,其汽化过程中克服的作用力是 _______ 。
②氢化物b、c、d的沸点均高于同族其它元素氢化物的沸点,原因是_______ 。
③H2O的沸点高于HF,预测可能的原因是_______ 。
(2)如图是冰(H2O)和干冰(CO2)的结构模型。_______ (填字母序号)。
a.冰中氢键存在方向性,晶体有较大空隙,空间利用率低
b.水分子极性强,分子间作用力大
c.二氧化碳分子的质量大于水分子
d.干冰晶胞中二氧化碳分子堆积得更密集
(3)苯胺(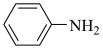 )与甲苯(
)与甲苯(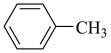 )的相对分子质量接近,但苯胺的熔点(﹣6.2℃)和沸点(184.4℃)高于甲苯的熔点(﹣95.0℃)和沸点(110.6℃),原因是
)的相对分子质量接近,但苯胺的熔点(﹣6.2℃)和沸点(184.4℃)高于甲苯的熔点(﹣95.0℃)和沸点(110.6℃),原因是 _______ 。
(1)如图是部分主族元素氢化物的沸点变化趋势
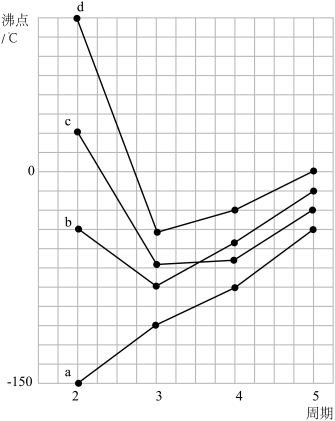
②氢化物b、c、d的沸点均高于同族其它元素氢化物的沸点,原因是
③H2O的沸点高于HF,预测可能的原因是
(2)如图是冰(H2O)和干冰(CO2)的结构模型。
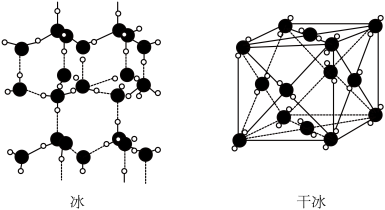
a.冰中氢键存在方向性,晶体有较大空隙,空间利用率低
b.水分子极性强,分子间作用力大
c.二氧化碳分子的质量大于水分子
d.干冰晶胞中二氧化碳分子堆积得更密集
(3)苯胺(
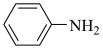 )与甲苯(
)与甲苯( )的相对分子质量接近,但苯胺的熔点(﹣6.2℃)和沸点(184.4℃)高于甲苯的熔点(﹣95.0℃)和沸点(110.6℃),原因是
)的相对分子质量接近,但苯胺的熔点(﹣6.2℃)和沸点(184.4℃)高于甲苯的熔点(﹣95.0℃)和沸点(110.6℃),原因是
更新时间:2024-05-22 21:04:32
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】(1)在①CaCl2、②KOH、③CO2、④NaHSO4、⑤Na2O2、⑥N2中,只含有离子键的是(填序号,下同)______ ,只含有极性键的是________________ ,含有非极性键的离子化合物是_______________ 。
(2)将NaHSO4溶于水,破坏的化学键是_____________ ,I2升华破坏的是_______________ 。
(2)将NaHSO4溶于水,破坏的化学键是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】范德华力
(1)存在:范德华力是一种普遍存在于___________ 分子之间的一种作用力。
(2)特点:与共价键相比,范德华力___________ ,一般___________ 饱和性和方向性。
(3)影响因素:
①分子的___________ 、___________ 以及分子中___________ 是否均匀。
②组成和结构相似的分子,其范德华力一般随着相对分子质量的增大而___________ 。
(4)对物质性质的影响:
主要影响物质的熔点、沸点、溶解度等___________ 性质。
①分子间范德华力越大,物质的熔、沸点___________ 。
②溶质与溶剂分子间的范德华力越大,物质的溶解度___________ 。
(1)存在:范德华力是一种普遍存在于
(2)特点:与共价键相比,范德华力
(3)影响因素:
①分子的
②组成和结构相似的分子,其范德华力一般随着相对分子质量的增大而
(4)对物质性质的影响:
主要影响物质的熔点、沸点、溶解度等
①分子间范德华力越大,物质的熔、沸点
②溶质与溶剂分子间的范德华力越大,物质的溶解度
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】下表所列是A、B、C、D、E五种短周期元素的相关数据:
(1)元素A是形成有机物的主要元素,下列分子中含有sp和sp3杂化方式的是________ 。
A.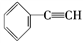 B.CH4
B.CH4
C.CH2==CHCH3 D.CH3CH2C≡CH E.CH3CH3
(2)用氢键表示式写出E的氢化物的水溶液中存在的所有氢键:____________ 。
(3)相同条件下,AD2与BD2分子在水中的溶解度较大的是______ (化学式),理由是____ 。
(4)B、D形成的氢化物沸点:________ 更高,热稳定性________ 更强。(写化学式)
| A | B | C | D | E | |
| 化合价 | -4 | -2 | -1 | -2 | -1 |
| 电负性 | 2.55 | 2.58 | 3.16 | 3.44 | 3.98 |
(1)元素A是形成有机物的主要元素,下列分子中含有sp和sp3杂化方式的是
A.
 B.CH4
B.CH4 C.CH2==CHCH3 D.CH3CH2C≡CH E.CH3CH3
(2)用氢键表示式写出E的氢化物的水溶液中存在的所有氢键:
(3)相同条件下,AD2与BD2分子在水中的溶解度较大的是
(4)B、D形成的氢化物沸点:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】锌在工业中有重要作用,也是人体必需的微量元素。回答下列问题:
(1)Zn原子核外电子排布式为________________ 。
(2)黄铜是人类最早使用的合金之一,主要由Zn和Cu组成。第一电离能Ⅰ1(Zn)_____ Ⅰ1(Cu)(填“大于”或“小于”)。原因是_____________________________ 。
(3)《中华本草》等中医典籍中,记载了炉甘石(ZnCO3)入药,可用于治疗皮肤炎症或表面创伤。ZnCO3中,阴离子空间构型为________________ ,C原子的杂化形式为________________ ,SO42-、CS2、CO32-键角由大到小的顺序是______________________
(4)锌冶炼过程中会产生污染性气体二氧化硫,已知液态二氧化硫也可以发生类似水的自身电离2SO2 SO2++SO32-,S和O两种元素中电负性较强的是
SO2++SO32-,S和O两种元素中电负性较强的是______________ ,与SO2+互为等电子体的单质分子是________ (填化学式),SO2+中σ键和Π键数目比为___________ 。
(5)分析并比较物质A: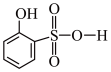 与B:
与B: 的沸点高低及其原因:
的沸点高低及其原因:__
(1)Zn原子核外电子排布式为
(2)黄铜是人类最早使用的合金之一,主要由Zn和Cu组成。第一电离能Ⅰ1(Zn)
(3)《中华本草》等中医典籍中,记载了炉甘石(ZnCO3)入药,可用于治疗皮肤炎症或表面创伤。ZnCO3中,阴离子空间构型为
(4)锌冶炼过程中会产生污染性气体二氧化硫,已知液态二氧化硫也可以发生类似水的自身电离2SO2
 SO2++SO32-,S和O两种元素中电负性较强的是
SO2++SO32-,S和O两种元素中电负性较强的是(5)分析并比较物质A:
 与B:
与B: 的沸点高低及其原因:
的沸点高低及其原因:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】教材插图具有简洁而又内涵丰富的特点。请回答以下问题:
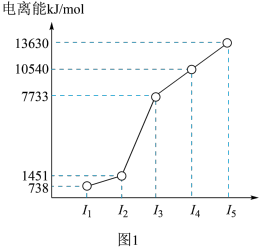
(1)第三周期的某主族元素,其第一至第五电离能数据如图1所示,则该元素对应的原子有___ 种不同运动状态的电子。

(2)如图2所示,每条折线表示周期表ⅣA-ⅦA中的某一族元素氢化物的沸点变化。每个小黑点代表一种氢化物,其中a点代表的是___ 。
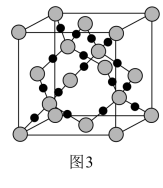
(3)CO2在高温高压下所形成的晶体其晶胞如图3所示。则该晶体的类型属于___ 晶体。
(4)第一电离能介于Al、P之间的第三周期元素有___ 种。GaCl3原子的杂化方式为___ 。
(5)冰、干冰、碘都是分子晶体,冰的结构具有特殊性,而干冰、碘的晶体具有相似的结构特征,干冰分子中一个分子周围有___ 个紧邻分子。D的醋酸盐晶体局部结构如图,该晶体中含有的化学键是___ (填字母标号)。

a.极性键 b.非极性键 c.配位键 d.金属键
(1)第三周期的某主族元素,其第一至第五电离能数据如图1所示,则该元素对应的原子有



(2)如图2所示,每条折线表示周期表ⅣA-ⅦA中的某一族元素氢化物的沸点变化。每个小黑点代表一种氢化物,其中a点代表的是
(3)CO2在高温高压下所形成的晶体其晶胞如图3所示。则该晶体的类型属于
(4)第一电离能介于Al、P之间的第三周期元素有
(5)冰、干冰、碘都是分子晶体,冰的结构具有特殊性,而干冰、碘的晶体具有相似的结构特征,干冰分子中一个分子周围有

a.极性键 b.非极性键 c.配位键 d.金属键
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】C60、金刚石、石墨、二氧化碳和氯化铯的结构模型如图所示(石墨仅表示出其中的一层结构):_______ 晶体,固态时,C60属于_______ (填“原子”或“分子”或“离子”)晶体。
(2)1mol金刚石中含有C—C单键的数目约是_______ NA。
(3)石墨层状结构中,平均每个正六边形占有的碳原子数是_______ 。
(4)CO2分子晶体中,每个CO2分子周围有_______ 个与之紧邻且等距的CO2分子。上图晶胞中有_______ 个CO2分子。
(5)CsCl晶体中每个Cl-周围紧邻且等距的Cs+数目为_______ 。

(2)1mol金刚石中含有C—C单键的数目约是
(3)石墨层状结构中,平均每个正六边形占有的碳原子数是
(4)CO2分子晶体中,每个CO2分子周围有
(5)CsCl晶体中每个Cl-周围紧邻且等距的Cs+数目为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】下图表示一些晶体中的某些结构,请回答下列问题:
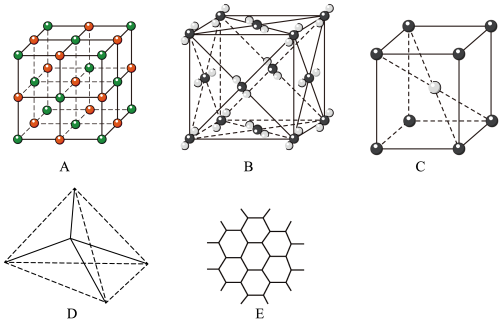
(1)代表金刚石的是(填编号字母,下同)_____ ,其中每个碳原子与_____ 个碳原子最近且距离相等。
(2)代表石墨的是_____ ,每个正六边形占有的碳原子数平均为_____ 个。
(3)代表 NaCl 的是_________ ,每个 Na+周围与它最近且距离相等的 Cl-有_____ 个。
(4)代表 CsCl 的是_____ ,每个 Cs+与_____ 个 Cl-紧邻。
(5)代表干冰的是_____ ,每个 CO2分子与_____ 个 CO2分子紧邻。
(6)已知石墨中碳碳键的键长比金刚石中碳碳键的键长短,则上述五种物质熔点由高到低的排列顺序为_____ 。

(1)代表金刚石的是(填编号字母,下同)
(2)代表石墨的是
(3)代表 NaCl 的是
(4)代表 CsCl 的是
(5)代表干冰的是
(6)已知石墨中碳碳键的键长比金刚石中碳碳键的键长短,则上述五种物质熔点由高到低的排列顺序为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】观察下列部分图形,并按要求回答下列问题
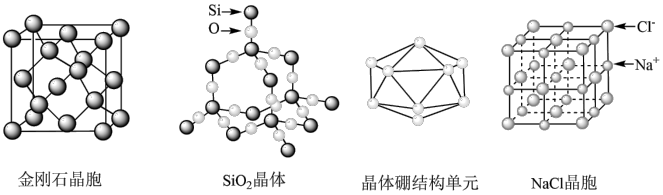
(1)由金刚石晶体结构和晶胞图知,金刚石是原子晶体,晶体中碳原子取_______ ,杂化轨道形成σ键,每个晶胞中含碳原子数为_______ 个。
(2)白磷分子(P4)中键角为________ ,分子的空间结构为_________ ,每1mol白磷分子含_________ mol P-P共价键。若将1分子白磷中所有P-P键打开并各插入一个氧原子所得氧化物的分子式为________ ,若每个P原子的孤对电子再与氧原子配位,就可得到磷的另一种氧化物________ (填分子式)。
(3)由SiO2晶体结构知SiO2晶体是_______ 晶体,每1mol SiO2晶体含________ mol Si-O共价键。
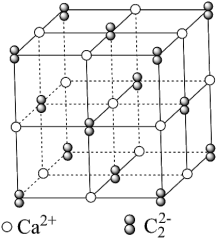
(4)已知CaC2晶体的晶胞结构与NaCl晶体相似,(如图)但CaC2晶体中哑铃形C22-的存在,使晶胞沿一个方向拉长,则CaC2晶体中Ca2+配位数(C.N)为_________ 。C22-与O22+互为等电子体,O22+的电子式为_______ ,1molO22+中含π键数目为________ 。
(5)晶体硼的基本结构单元都是由硼原子组成的正二十面体的原子晶体。其中含有20个等边三角形和一定数目的顶角,每个顶角各有一个原子,观察图形回答。这个基本结构单元由______ 个硼原子组成,共含有____ 个B-B键。
(6)若测得mg NaCl固体的体积为Vcm3,已知NaCl晶体中,靠得最近的Na+、Cl-间的距离为a cm,则阿伏伽德罗常数NA的表达式为________ 。

(1)由金刚石晶体结构和晶胞图知,金刚石是原子晶体,晶体中碳原子取
(2)白磷分子(P4)中键角为
(3)由SiO2晶体结构知SiO2晶体是
(4)已知CaC2晶体的晶胞结构与NaCl晶体相似,(如图)但CaC2晶体中哑铃形C22-的存在,使晶胞沿一个方向拉长,则CaC2晶体中Ca2+配位数(C.N)为

(5)晶体硼的基本结构单元都是由硼原子组成的正二十面体的原子晶体。其中含有20个等边三角形和一定数目的顶角,每个顶角各有一个原子,观察图形回答。这个基本结构单元由
(6)若测得mg NaCl固体的体积为Vcm3,已知NaCl晶体中,靠得最近的Na+、Cl-间的距离为a cm,则阿伏伽德罗常数NA的表达式为
您最近一年使用:0次

 的熔点(1291℃)比
的熔点(1291℃)比 的熔点(190℃)高很多的原因是
的熔点(190℃)高很多的原因是 溶于水克服的微粒间作用力有
溶于水克服的微粒间作用力有 )与邻羟基苯甲酸(
)与邻羟基苯甲酸( )熔点高低并解释产生这种现象的原因是
)熔点高低并解释产生这种现象的原因是

