(1)I.短周期某主族元素M的电离能情况如图(A)所示,则M元素位于周期表的第____ 族;
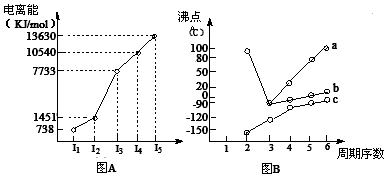
Ⅱ.图B折线c可以表达出第____________ 族元素氢化物的沸点的变化规律。两位同学对某主族元素氢化物的沸点的变化趋势画出了两条折线a和b,你认为正确的是:________________ (填“a”或 “b”);
Ⅲ.部分有机物的熔沸点见下表:
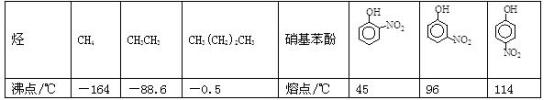
根据物质结构理论,由这些数据你能得出的相关结论是(至少写2条):____________________ ;_________________________________
(2)COCl2俗称光气,分子中C原子采取__________ 杂化成键;其中碳氧原子之间共价键含有___________ (填字母):
a.2个σ键
b.2个π键
c.1个σ键.1个π键;
(3)金属是钛(22Ti) 将是继铜.铁.铝之后人类广泛使用的第四种金属,试回答:
I.Ti元素的基态原子的价电子层排布式为_________________________ ;
Ⅱ.已知Ti3+可形成配位数为6的配合物。现有紫色和绿色两种含钛晶体,其组成均为TiCl3·6H2O。为测定这两种晶体的化学式,设计了如下实验:
a.分别取等质量的两种晶体的样品配成溶液;
b.向两种溶液中分别滴入AgNO3溶液,均产生白色沉淀;
c.沉淀完全后分别过滤得两份沉淀,经洗涤干燥后称量发现产生的沉淀质量关系为:绿色晶体为紫色晶体的 ,则绿色晶体配合物的化学式为
,则绿色晶体配合物的化学式为_________________________ 。

Ⅱ.图B折线c可以表达出第
Ⅲ.部分有机物的熔沸点见下表:

根据物质结构理论,由这些数据你能得出的相关结论是(至少写2条):
(2)COCl2俗称光气,分子中C原子采取
a.2个σ键
b.2个π键
c.1个σ键.1个π键;
(3)金属是钛(22Ti) 将是继铜.铁.铝之后人类广泛使用的第四种金属,试回答:
I.Ti元素的基态原子的价电子层排布式为
Ⅱ.已知Ti3+可形成配位数为6的配合物。现有紫色和绿色两种含钛晶体,其组成均为TiCl3·6H2O。为测定这两种晶体的化学式,设计了如下实验:
a.分别取等质量的两种晶体的样品配成溶液;
b.向两种溶液中分别滴入AgNO3溶液,均产生白色沉淀;
c.沉淀完全后分别过滤得两份沉淀,经洗涤干燥后称量发现产生的沉淀质量关系为:绿色晶体为紫色晶体的
 ,则绿色晶体配合物的化学式为
,则绿色晶体配合物的化学式为
更新时间:2016-12-08 23:10:21
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】依据元素周期表与元素周期律回答以下问题:
(1)根据元素周期表对角线规则,金属Be与Al单质及其化合物性质相似。写出Be与 溶液反应离子方程式:
溶液反应离子方程式:_______ 。
(2)硒(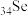 )和S位于同一主族。
)和S位于同一主族。 的稳定性比
的稳定性比 的
的_______ (填“强”或“弱”,断开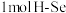 键吸收的能量比断开
键吸收的能量比断开 键吸收的能量
键吸收的能量_______ (填“多”或“少”)。用原子结构解释原因:同主族元素最外层电子数相同,从上到下_______ 。
(3)氮(N)、磷(P)、砷(As)、锑(Sb)、铋(Bi)为元素周期表原子序数依次增大的同族元素。回答下列问题:
①砷在元素周期表中的位置_______ 。
② 的电子式为
的电子式为_______ ,沸点:
_______ 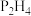 (填“>”或“<”),判断依据是
(填“>”或“<”),判断依据是_______ 。
③ 和
和 与卤化氢的反应相似,产物的结构和性质也相似。下列对
与卤化氢的反应相似,产物的结构和性质也相似。下列对 与
与 反应所得产物的推断正确的是
反应所得产物的推断正确的是_______ (填序号)。
a.只含共价键 b.难于水 c.受热易分解 d.能与 溶液反应
溶液反应
(1)根据元素周期表对角线规则,金属Be与Al单质及其化合物性质相似。写出Be与
 溶液反应离子方程式:
溶液反应离子方程式:(2)硒(
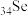 )和S位于同一主族。
)和S位于同一主族。 的稳定性比
的稳定性比 的
的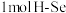 键吸收的能量比断开
键吸收的能量比断开 键吸收的能量
键吸收的能量(3)氮(N)、磷(P)、砷(As)、锑(Sb)、铋(Bi)为元素周期表原子序数依次增大的同族元素。回答下列问题:
①砷在元素周期表中的位置
②
 的电子式为
的电子式为
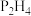 (填“>”或“<”),判断依据是
(填“>”或“<”),判断依据是③
 和
和 与卤化氢的反应相似,产物的结构和性质也相似。下列对
与卤化氢的反应相似,产物的结构和性质也相似。下列对 与
与 反应所得产物的推断正确的是
反应所得产物的推断正确的是a.只含共价键 b.难于水 c.受热易分解 d.能与
 溶液反应
溶液反应
您最近一年使用:0次
填空题
|
适中
(0.64)
名校
【推荐2】原子序数小于36的X、Y、Z、W四种元素,其中X是原子半径最小的元素,Y原子基态时最外层电子数是其内层电子数的2倍,Z原子基态时2p原子轨道上有3个未成对的电子,W的原子序数为29.回答下列问题:
(1)1mol Y2X2含有σ键的数目为______ 。
(2)X和Z形成的化合物为M,Y和X形成的化合物为N,则M、N中其VSEPR模型和分子立体构型相同的是______ (写化学式)。
(3)W原子价电子排布式为______ ,向其硫酸盐(WSO4)溶液中逐滴加入氨水至过量,发生的现象是______ ,反应后的溶液中W形成的配离子的化学式为______ 。
(1)1mol Y2X2含有σ键的数目为
(2)X和Z形成的化合物为M,Y和X形成的化合物为N,则M、N中其VSEPR模型和分子立体构型相同的是
(3)W原子价电子排布式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】C、N、O、Na、Al、Si、S、Cl是常见的八种元素。请回答下列问题:
(1)Si在元素周期表中的位置为___________ ;CO2的电子式是___________ 。
(2)上述元素中原子半径最大的是(写元素符号)___________ ;最高价氧化物对应的水化物酸性最强的是___________ (写化学式)。
(3)下列事实能说明O元素的非金属性比S元素的非金属性强的是___________ 。
a.O2与H2S溶液反应,溶液变浑浊
b.O和S两元素的简单氢化物受热分解,前者的分解温度高
c.在氧化还原反应中,1molO2比1molS得电子多
(4)金刚石具有优良的耐磨,耐腐蚀性,应用广泛。一定条件下,Na还原CCl4可制备金刚石。反应结束冷却至室温后,回收其中的CCl4的实验操作名称为___________ ,除去粗产品中少里钠的试剂为___________ 。
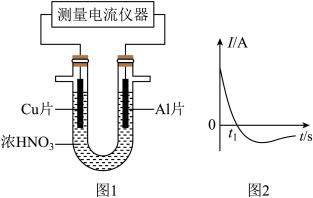
(5)常温下,将除去表面氧化膜的Al、Cu片插入浓HNO3中组成原电池(图l),测得原电池的电流强度(I)随时间(t)的变化如图2所示,反应过程中有红棕色气体产生。0~t1时,原电池的负极是Al片,此时,正极的电极反应式是___________ ,溶液中的H+向___________ 极移动。t1时,原电池中电子流动方向发生改变,其原因是:___________ 。
(1)Si在元素周期表中的位置为
(2)上述元素中原子半径最大的是(写元素符号)
(3)下列事实能说明O元素的非金属性比S元素的非金属性强的是
a.O2与H2S溶液反应,溶液变浑浊
b.O和S两元素的简单氢化物受热分解,前者的分解温度高
c.在氧化还原反应中,1molO2比1molS得电子多
(4)金刚石具有优良的耐磨,耐腐蚀性,应用广泛。一定条件下,Na还原CCl4可制备金刚石。反应结束冷却至室温后,回收其中的CCl4的实验操作名称为
(5)常温下,将除去表面氧化膜的Al、Cu片插入浓HNO3中组成原电池(图l),测得原电池的电流强度(I)随时间(t)的变化如图2所示,反应过程中有红棕色气体产生。0~t1时,原电池的负极是Al片,此时,正极的电极反应式是

您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】经研究表明,Fe(SCN)3是配合物,Fe3+与SCN-不仅能以1∶3的个数比配合,还可以其他个数比配合。请按要求填空:
(1)若所得的Fe3+和SCN-的配合物中,主要是Fe3+与SCN-以个数比1∶1配合所得离子显红色。该离子的离子符号是________ 。
(2)若Fe3+与SCN-以个数比1∶5配合,则FeCl3与KSCN在水溶液中发生反应的化学方程式可以表示为____________________ 。
(1)若所得的Fe3+和SCN-的配合物中,主要是Fe3+与SCN-以个数比1∶1配合所得离子显红色。该离子的离子符号是
(2)若Fe3+与SCN-以个数比1∶5配合,则FeCl3与KSCN在水溶液中发生反应的化学方程式可以表示为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】高温陶瓷材料Si3N4晶体中键角N-Si-N_______ Si-N-Si(填“>“<”或“=”),原因是_______ 。
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】铜是人类广泛使用的第一种金属,含铜物质在生产生活中有着广泛应用。回答下列问题:
一种含有Fe、Cu、S三种元素的矿物的晶胞(如图所示),属于四方晶系(晶胞底面为正方形),则该化合物的化学式为_______ ;若晶胞的底面边长为a nm,晶体的密度为p g·cm-3,阿伏加德罗常数为NA,则该晶胞的高为_______ nm。

一种含有Fe、Cu、S三种元素的矿物的晶胞(如图所示),属于四方晶系(晶胞底面为正方形),则该化合物的化学式为

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】回答下列问题:
(1)请写出下列基态粒子的简化电子排布式和价层电子的轨道表示式:Cu:_______ ,_______ 。
(2)在配合物 中,
中,_______ 是中心离子,_______ 是配位原子,_______ 是配位体; 的结构式为
的结构式为_______ 。
(3)下图为几种晶体或晶胞的示意图:

请回答下列问题:
①上述晶体中,粒子之间以共价键结合形成的晶体是_______ 。
②冰、金刚石、MgO、干冰4种晶体的熔点由高到低的顺序为_______ 。
③每个Cu晶胞中实际占有_______ 个铜原子,干冰晶体中一个分子周围有_______ 个紧邻分子。
(1)请写出下列基态粒子的简化电子排布式和价层电子的轨道表示式:Cu:
(2)在配合物
 中,
中, 的结构式为
的结构式为(3)下图为几种晶体或晶胞的示意图:

请回答下列问题:
①上述晶体中,粒子之间以共价键结合形成的晶体是
②冰、金刚石、MgO、干冰4种晶体的熔点由高到低的顺序为
③每个Cu晶胞中实际占有
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】已知肼(N2H4)和强氧化剂过氧化氢常用作火箭燃料,火箭部分构件采用钛合金材料。请回答下列问题:
(1)N2H4、H2O2的组成元素中第一电离能最大的是______ 。
(2)钛元素基态原子的核外电子排布式为_____________________ 。
(3)1 mol N2H4分子中所含极性键的数目为___________ 。
(4)H2O2受热易分解为H2O,H2O的空间构型为_______ ,其中心原子的杂化轨道类型为_________ 。
(5)H2S和H2O2的主要物理性质如下表所示:
造成上述熔沸点和溶解度差异的主要原因分别是_______________ 和________________ 。
(6)氧化镁和氮化硼均可用作返回舱的热屏蔽材料,晶格能:氧化镁_______ (填“大于”或“小于”)氧化钙。
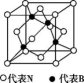
(7)立方氮化硼的晶胞如图所示。处于晶胞顶点的原子的配位数为______ 。若晶胞边长为a cm,则立方氮化硼的密度是________________ g·cm-3。(只要求列出算式,设阿伏伽德罗常数的值为NA)
(1)N2H4、H2O2的组成元素中第一电离能最大的是
(2)钛元素基态原子的核外电子排布式为
(3)1 mol N2H4分子中所含极性键的数目为
(4)H2O2受热易分解为H2O,H2O的空间构型为
(5)H2S和H2O2的主要物理性质如下表所示:
| 物质 | 熔点/K | 沸点/K | 水中溶解度(标准状况) |
| H2S | 187 | 202 | 每升水中溶解2.6 L |
| H2O2 | 272 | 423 | 以任意比互溶 |
造成上述熔沸点和溶解度差异的主要原因分别是
(6)氧化镁和氮化硼均可用作返回舱的热屏蔽材料,晶格能:氧化镁
(7)立方氮化硼的晶胞如图所示。处于晶胞顶点的原子的配位数为

您最近一年使用:0次



