油脂是高级脂肪酸的甘油酯,在工业上用途广泛。
实验一:用地沟油制肥皂(高级脂肪酸钠盐)和甘油(常压下甘油的沸点为290℃)。
32.将约6g地沟油、10mL 40%的烧碱溶液、5mL液体A混合后在烧杯中加热约0.5小时。A可以增大反应物间的接触,则A可以是_____ (选填编号)。
a.四氯化碳 b.汽油 c.乙醇
33.从皂化反应后的溶液中提取肥皂和甘油的过程如下:
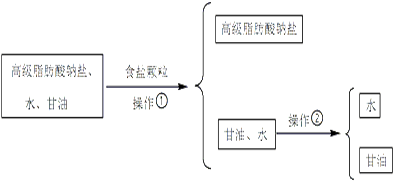
加入食盐颗粒后,液体表面析出白色固体,则食盐的作用是_____________________ 。
操作②必须用到的玻璃仪器是_____ (选填编号)。
a.漏斗 b.分液漏斗 c.蒸馏烧瓶
34.若甘油的产率明显低于高级脂肪酸钠盐的产率,可能的原因是_____ (选填编号)。
a.油脂水解不充分 b.部分甘油挥发 c.甘油中混有水
实验二:测定油脂的碘值。碘值是指100g油脂中所能吸收(加成)碘的克数。
称取a g某油脂,加入含bmol I2的溶液(韦氏液),充分振荡;过量的I2用cmol/L Na2S2O3溶液滴定(以淀粉为指示剂):2Na2S2O3+ I2 →Na2S4O6+ 2NaI用去vmL。
35.配制韦氏液,溶剂选用冰醋酸而不选用水的原因是______ 。滴定终点时颜色的变化是_________ 。
36.该油脂的碘值为(用相关字母表示)__________________________ 。
37.冰醋酸也会消耗Na2S2O3,所以还要做相关实验进行校正,否则会引起测得的碘值偏_____ (选填“高”或“低”)。
实验一:用地沟油制肥皂(高级脂肪酸钠盐)和甘油(常压下甘油的沸点为290℃)。
32.将约6g地沟油、10mL 40%的烧碱溶液、5mL液体A混合后在烧杯中加热约0.5小时。A可以增大反应物间的接触,则A可以是
a.四氯化碳 b.汽油 c.乙醇
33.从皂化反应后的溶液中提取肥皂和甘油的过程如下:

加入食盐颗粒后,液体表面析出白色固体,则食盐的作用是
操作②必须用到的玻璃仪器是
a.漏斗 b.分液漏斗 c.蒸馏烧瓶
34.若甘油的产率明显低于高级脂肪酸钠盐的产率,可能的原因是
a.油脂水解不充分 b.部分甘油挥发 c.甘油中混有水
实验二:测定油脂的碘值。碘值是指100g油脂中所能吸收(加成)碘的克数。
称取a g某油脂,加入含bmol I2的溶液(韦氏液),充分振荡;过量的I2用cmol/L Na2S2O3溶液滴定(以淀粉为指示剂):2Na2S2O3+ I2 →Na2S4O6+ 2NaI用去vmL。
35.配制韦氏液,溶剂选用冰醋酸而不选用水的原因是
36.该油脂的碘值为(用相关字母表示)
37.冰醋酸也会消耗Na2S2O3,所以还要做相关实验进行校正,否则会引起测得的碘值偏
更新时间:2016-12-09 07:15:08
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】某化学课外小组的同学通过实验探究认识化学反应速率和化学反应限度。
I.实验一:探究温度和浓度对反应速率的影响。
实验原理及方案:在酸性溶液中,碘酸钾( )和亚硫酸钠可发生反应生成碘,反应原理是
)和亚硫酸钠可发生反应生成碘,反应原理是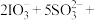
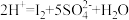 ,生成的碘可用淀粉溶液检验,根据出现蓝色所需的时间来衡量该反应的速率。实验出现蓝
,生成的碘可用淀粉溶液检验,根据出现蓝色所需的时间来衡量该反应的速率。实验出现蓝
(1)则
_______ mL,
_______ mL。
Ⅱ.实验二:探究KI和 混合时生成KCl、I2和
混合时生成KCl、I2和 的反应存在一定的限度。
的反应存在一定的限度。
实验原理: 。
。
实验步骤:向5mL 0.1 KI溶液中滴加5~6滴0.1
KI溶液中滴加5~6滴0.1
 溶液,充分反应后,将所得溶液分成甲、乙、丙三等份。
溶液,充分反应后,将所得溶液分成甲、乙、丙三等份。
(2)向甲中滴加 ,充分振荡、静置,下层溶液出现紫红色,说明有
,充分振荡、静置,下层溶液出现紫红色,说明有 生成;向乙中滴加试剂
生成;向乙中滴加试剂_______ ,若现象为_______ ,则说明该反应有一定的限度。
Ⅲ.800℃时A、B、C三种气体在恒容密闭容器中反应时的浓度变化如图,分析图像回答问题:

(3)该反应的化学方程式为_______ 。
(4)2min内,用C来表示的化学反应速率为_______ 。
(5)在其他条件下,测得A的反应速率为0.05 ,此时的反应与800℃时相比,
,此时的反应与800℃时相比,_______ (填字母)。
A.比800℃时快B.比800℃时慢C.和800℃时速率一样
I.实验一:探究温度和浓度对反应速率的影响。
实验原理及方案:在酸性溶液中,碘酸钾(
 )和亚硫酸钠可发生反应生成碘,反应原理是
)和亚硫酸钠可发生反应生成碘,反应原理是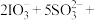
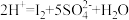 ,生成的碘可用淀粉溶液检验,根据出现蓝色所需的时间来衡量该反应的速率。实验出现蓝
,生成的碘可用淀粉溶液检验,根据出现蓝色所需的时间来衡量该反应的速率。实验出现蓝| 实验序号 | 0.01  酸性溶液(含淀粉)的体积/mL 酸性溶液(含淀粉)的体积/mL | 0.01  溶液的体积/mL 溶液的体积/mL | 水的体积/mL | 实验温度/℃ | 出现蓝色的时间/s |
| ① | 5 | 5 |  | 0 | |
| ② | 5 | 5 | 40 | 25 | |
| ③ | 5 |  | 35 | 25 |


Ⅱ.实验二:探究KI和
 混合时生成KCl、I2和
混合时生成KCl、I2和 的反应存在一定的限度。
的反应存在一定的限度。实验原理:
 。
。实验步骤:向5mL 0.1
 KI溶液中滴加5~6滴0.1
KI溶液中滴加5~6滴0.1
 溶液,充分反应后,将所得溶液分成甲、乙、丙三等份。
溶液,充分反应后,将所得溶液分成甲、乙、丙三等份。(2)向甲中滴加
 ,充分振荡、静置,下层溶液出现紫红色,说明有
,充分振荡、静置,下层溶液出现紫红色,说明有 生成;向乙中滴加试剂
生成;向乙中滴加试剂Ⅲ.800℃时A、B、C三种气体在恒容密闭容器中反应时的浓度变化如图,分析图像回答问题:

(3)该反应的化学方程式为
(4)2min内,用C来表示的化学反应速率为
(5)在其他条件下,测得A的反应速率为0.05
 ,此时的反应与800℃时相比,
,此时的反应与800℃时相比,A.比800℃时快B.比800℃时慢C.和800℃时速率一样
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】酯化反应是高中化学的重要考察对象。某科研单位对乙酸乙酯的合成实验作了绿色化改进,探究酯化反应的最佳条件。实验结果与讨论:
(1)催化剂对酯化反应的影响
选用一定量的浓硫酸和耐水固体酸 两种不同的催化剂来探究催化剂对酯化反应的影响结果如图所示。则催化效果更好的是
两种不同的催化剂来探究催化剂对酯化反应的影响结果如图所示。则催化效果更好的是______
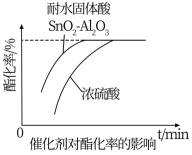

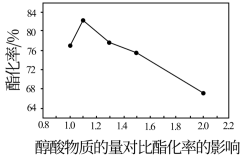
A.浓硫酸 B.耐水固体酸
(2)吸水剂 的用量对酯化反应的影响
的用量对酯化反应的影响
由表中数据可知,应选择吸水剂的用量为______ g,加入吸水剂的作用是______ 。
(3)根据上图曲线,得出结论:酯化反应的最佳反应时间为______ ,最佳醇酸物质的量比为______ 。
(4)写出乙酸与乙醇酯化反应的化学方程式______ 。
(5)写出上述反应平衡常数表达式K=______ 。
(1)催化剂对酯化反应的影响
选用一定量的浓硫酸和耐水固体酸
 两种不同的催化剂来探究催化剂对酯化反应的影响结果如图所示。则催化效果更好的是
两种不同的催化剂来探究催化剂对酯化反应的影响结果如图所示。则催化效果更好的是


A.浓硫酸 B.耐水固体酸
(2)吸水剂
 的用量对酯化反应的影响
的用量对酯化反应的影响| 吸水剂用量/g | 0.7 | 0.9 | 1.4 | 2.0 |
| 酯化率/% | 55.0 | 64.0 | 71.1 | 72.0 |
(3)根据上图曲线,得出结论:酯化反应的最佳反应时间为
(4)写出乙酸与乙醇酯化反应的化学方程式
(5)写出上述反应平衡常数表达式K=
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐3】目前正研究利用催化技术将尾气中的NO和CO转变成CO2和N2,化学方程式如下:2NO+2CO 2CO2+N2+Q为了测定在某种催化剂作用下的反应速率,在某温度下用气体传感器测得不同时间的NO和CO浓度如下表
2CO2+N2+Q为了测定在某种催化剂作用下的反应速率,在某温度下用气体传感器测得不同时间的NO和CO浓度如下表
请回答下列问题(均不考虑温度变化对催化剂催化效率的影响):
(1)前2s内的平均反应速率v(N2)=____________ ;
(2)假设在密闭容器中发生上述反应,达到平衡时下列措施能提高CO转化率的是_______ ;
A. 选用更有效的催化剂 B. 升高反应体系的温度
C. 降低反应体系的温度 D. 缩小容器的体积
(3)研究表明:在使用等质量催化剂时,增大催化剂比表面积可提高化学反应速率。为了分别验证温度、催化剂比表面积对化学反应速率的影响规律,某同学设计了三组实验,部分实验条件已经填在下面实验设计表中;请在下表空格中填入剩余的实验条件数据。
(4)请画出题表中的三个实验条件下混合气体中CO浓度随时间变化的趋势曲线图 ,并标明各条曲线的实验编号。______________

(5)消除一氧化氮可以用在水的存在下通入氧气加以除去。现将标准状况下的一试管一氧化氮气体倒置于水中,慢慢通入氧气,溶液充满整个试管,若不考虑溶质的扩散,则试管内稀硝酸的浓度为_________ mol/L;若继续通入氧气,将试管内溶液排除一半,则剩余稀硝酸的浓度为__________ mol/L。
(6)利用氨气的还原性也可以除去氮氧化合物(NOx),当氨气与NOx等物质的量恰好反应生成氮气和水,则x=_________ 。
 2CO2+N2+Q为了测定在某种催化剂作用下的反应速率,在某温度下用气体传感器测得不同时间的NO和CO浓度如下表
2CO2+N2+Q为了测定在某种催化剂作用下的反应速率,在某温度下用气体传感器测得不同时间的NO和CO浓度如下表时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
| c(NO)/mol·L-1 | 1.00×10-3 | 4.50×10-4 | 2.50×10-4 | 1.50×10-4 | 1.00×10-4 | 1.00×10-4 |
| c(CO)/mol·L-1 | 3.60×10-3 | 3.05×10-3 | 2.85×10-3 | 2.75×10-3 | 2.70×10-3 | 2.70×10-3 |
(1)前2s内的平均反应速率v(N2)=
(2)假设在密闭容器中发生上述反应,达到平衡时下列措施能提高CO转化率的是
A. 选用更有效的催化剂 B. 升高反应体系的温度
C. 降低反应体系的温度 D. 缩小容器的体积
(3)研究表明:在使用等质量催化剂时,增大催化剂比表面积可提高化学反应速率。为了分别验证温度、催化剂比表面积对化学反应速率的影响规律,某同学设计了三组实验,部分实验条件已经填在下面实验设计表中;请在下表空格中填入剩余的实验条件数据。
| 实验编号 | T/℃ | NO初始浓度(mol/L) | CO初始浓度(mol/L) | 催化剂的比表面积(m2/g) |
| Ⅰ | 280 | 1.20×10-3 | 5.80×10-3 | 82 |
| Ⅱ | 124 | |||
| Ⅲ | 350 | 124 |
(4)请画出题表中的三个实验条件下混合气体中CO浓度随时间变化的趋势

(5)消除一氧化氮可以用在水的存在下通入氧气加以除去。现将标准状况下的一试管一氧化氮气体倒置于水中,慢慢通入氧气,溶液充满整个试管,若不考虑溶质的扩散,则试管内稀硝酸的浓度为
(6)利用氨气的还原性也可以除去氮氧化合物(NOx),当氨气与NOx等物质的量恰好反应生成氮气和水,则x=
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】硬脂酸甘油酯在碱性条件下水解的装置如图所示。
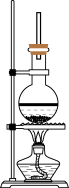
进行皂化反应实验的操作步骤如下:
(1)在圆底烧瓶中加入7~8g硬脂酸甘油酯,然后加入2~3gNaOH、5mL水和10mL酒精,其中加入酒精的作用是___ 。
(2)加热反应混合物约10min,皂化反应基本完成,所得的混合物为___ (填“悬浊液”、“乳浊液”、“溶液”或“胶体”)。
(3)向所得混合物中加入食盐细粒,静置一段时间,溶液分为上下两层,高级脂肪酸钠盐在___ 层,这个过程称为___ 。
(4)装置中长玻璃导管的作用为___ 。

进行皂化反应实验的操作步骤如下:
(1)在圆底烧瓶中加入7~8g硬脂酸甘油酯,然后加入2~3gNaOH、5mL水和10mL酒精,其中加入酒精的作用是
(2)加热反应混合物约10min,皂化反应基本完成,所得的混合物为
(3)向所得混合物中加入食盐细粒,静置一段时间,溶液分为上下两层,高级脂肪酸钠盐在
(4)装置中长玻璃导管的作用为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】硬脂酸甘油酯在碱性条件下水解的装置如图所示。试回答下列问题:
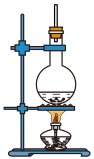
(1)在圆底烧瓶中装入7~8g硬脂酸甘油酯,然后加入2~3g氢氧化钠、5mL水、10mL酒精。加入酒精的作用是__ ;加入NaOH溶液的作用是__ 。
(2)给反应混合物加热约10min,皂化反应基本完成。证明皂化反应进行完全的方法和现象是__ 。
(3)皂化反应完成后,加入饱和NaCl溶液的作用是__ 。
(4)图中长玻璃导管的作用是__ 。
(5)写出该反应的化学方程式:__ 。

(1)在圆底烧瓶中装入7~8g硬脂酸甘油酯,然后加入2~3g氢氧化钠、5mL水、10mL酒精。加入酒精的作用是
(2)给反应混合物加热约10min,皂化反应基本完成。证明皂化反应进行完全的方法和现象是
(3)皂化反应完成后,加入饱和NaCl溶液的作用是
(4)图中长玻璃导管的作用是
(5)写出该反应的化学方程式:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】油脂是高级脂肪酸的甘油酯,在工业上用途广泛。
实验一:用地沟油制肥皂(高级脂肪酸钠盐)和甘油(常压下甘油的沸点为290℃)。
(1)将约6g地沟油、10mL 40%的烧碱溶液、5mL液体A混合后在烧杯中加热约0.5小时。A可以增大反应物间的接触,则A可以是_____ (选填编号)。
a.四氯化碳 b.汽油 c.乙醇
(2)从皂化反应后的溶液中提取肥皂和甘油的过程如下:
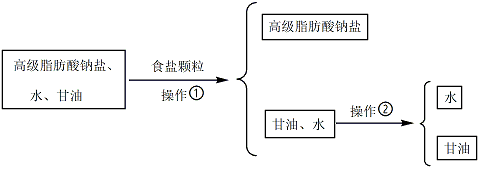
加入食盐颗粒后,液体表面析出白色固体,则食盐的作用是_____________________ 。操作②必须用到的玻璃仪器是_____ (选填编号)。
a.漏斗 b.分液漏斗 c.蒸馏烧瓶
(3)若甘油的产率明显低于高级脂肪酸钠盐的产率,可能的原因是_____ (选填编号)。
a.油脂水解不充分 b.部分甘油挥发 c.甘油中混有水
实验二:测定油脂的碘值。碘值是指100g油脂中所能吸收(加成)碘的克数。
称取a g某油脂,加入含bmol I2的溶液(韦氏液),充分振荡;过量的I2用cmol/L Na2S2O3溶液滴定(以淀粉为指示剂):2Na2S2O3+ I2 =Na2S4O6+ 2NaI用去vmL。
(4)配制韦氏液,溶剂选用冰醋酸而不选用水的原因是___________________ 。滴定终点时颜色的变化是__________________________ 。
(5)该油脂的碘值为(用相关字母表示)__________________________ 。
(6)冰醋酸也会消Na2S2O3,所以还要做相关实验进行校正,否则会引起测得的碘值偏_____ (选填“高”或“低”)。
实验一:用地沟油制肥皂(高级脂肪酸钠盐)和甘油(常压下甘油的沸点为290℃)。
(1)将约6g地沟油、10mL 40%的烧碱溶液、5mL液体A混合后在烧杯中加热约0.5小时。A可以增大反应物间的接触,则A可以是
a.四氯化碳 b.汽油 c.乙醇
(2)从皂化反应后的溶液中提取肥皂和甘油的过程如下:

加入食盐颗粒后,液体表面析出白色固体,则食盐的作用是
a.漏斗 b.分液漏斗 c.蒸馏烧瓶
(3)若甘油的产率明显低于高级脂肪酸钠盐的产率,可能的原因是
a.油脂水解不充分 b.部分甘油挥发 c.甘油中混有水
实验二:测定油脂的碘值。碘值是指100g油脂中所能吸收(加成)碘的克数。
称取a g某油脂,加入含bmol I2的溶液(韦氏液),充分振荡;过量的I2用cmol/L Na2S2O3溶液滴定(以淀粉为指示剂):2Na2S2O3+ I2 =Na2S4O6+ 2NaI用去vmL。
(4)配制韦氏液,溶剂选用冰醋酸而不选用水的原因是
(5)该油脂的碘值为(用相关字母表示)
(6)冰醋酸也会消Na2S2O3,所以还要做相关实验进行校正,否则会引起测得的碘值偏
您最近一年使用:0次



