工业上用铝土矿(主要成分是Al2O3,还含有Fe2O3、SiO2)提取氧化铝冶炼铝的原料(纯净的Al2O3),提取操作过程如下:
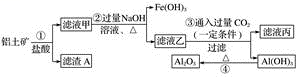
请回答下列问题:
(1)请写主要成分的化学式:滤渣A________ ,滤液丙中的溶质是NaCl和________ 。
(2)反应②中Al3+反应的离子方程式为_________________ ;反应③的离子方程式为____________ ;反应④的化学方程式为______________________________ 。

请回答下列问题:
(1)请写主要成分的化学式:滤渣A
(2)反应②中Al3+反应的离子方程式为
更新时间:2016-12-09 07:21:47
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】聚合氯化铝铁(PAFC)是一种高效净水剂,其组成可表示为[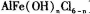 ]。
]。
为检测PAFC中Al的含量,采用下图所示流程。
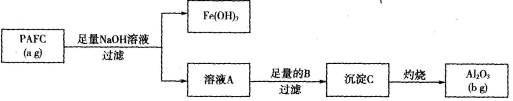
(1)PAFC中铁元素的化合价为_______ .
(2)溶液A中含铝元素的溶质是______ ,它属于____ (填“酸”、“碱”、“盐”)。
(3)如图所示,过滤操作中的一处错误是__________________ .
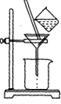
(4)物质B可能是下列试剂中的_______ (填代号)。
a.NH3 b.CO2 c.NaOH溶液 d.HNO3溶液
判断流程中沉淀C是否洗净的方法是______________________ (描述操作、现象和结论)。
(5)PAFC中A1元素的质量分数为____________ (用含有a、b的代数式表示)。
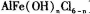 ]。
]。为检测PAFC中Al的含量,采用下图所示流程。

(1)PAFC中铁元素的化合价为
(2)溶液A中含铝元素的溶质是
(3)如图所示,过滤操作中的一处错误是

(4)物质B可能是下列试剂中的
a.NH3 b.CO2 c.NaOH溶液 d.HNO3溶液
判断流程中沉淀C是否洗净的方法是
(5)PAFC中A1元素的质量分数为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】铁、铝、铜等金属及其化合物在日常生活中应用广泛,请回答下列问题。
(1)生铁中含有一种铁碳化合物X(Fe3C)。X在足量的空气中高温煅烧,生成有磁性的固体Y,将Y溶于过量盐酸,离子方程式为_______________________________________________________ ;Y与过量浓硝酸反应后溶液中含有的盐的化学式为____________ ;
(2)某溶液中含有Mg2+、Fe2+、Al3+、Cu2+等离子,向其中加入过量的NaOH溶液后,过滤,将滤渣高温灼烧并将灼烧后的固体投入到过量的稀盐酸中,所得溶液与原溶液相比,溶液中大量减少的阳离子是___________ (填编号)。
A.Mg2+ B.Fe2+ C.Al3+ D.Cu2+
(3)氧化铁是重要的工业颜料,用废铁屑制备它的流程如下:
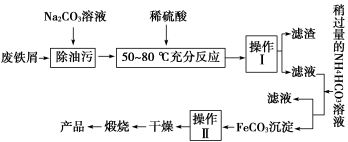
①Na2CO3溶液可以除油污,原因是(用离子方程式表示)________________________________ ;
②操作Ⅱ中沉淀的洗涤方法是___________________________________________________________
③请写出生成FeCO3沉淀的离子方程式_______________________________________________ 。
(1)生铁中含有一种铁碳化合物X(Fe3C)。X在足量的空气中高温煅烧,生成有磁性的固体Y,将Y溶于过量盐酸,离子方程式为
(2)某溶液中含有Mg2+、Fe2+、Al3+、Cu2+等离子,向其中加入过量的NaOH溶液后,过滤,将滤渣高温灼烧并将灼烧后的固体投入到过量的稀盐酸中,所得溶液与原溶液相比,溶液中大量减少的阳离子是
A.Mg2+ B.Fe2+ C.Al3+ D.Cu2+
(3)氧化铁是重要的工业颜料,用废铁屑制备它的流程如下:

①Na2CO3溶液可以除油污,原因是(用离子方程式表示)
②操作Ⅱ中沉淀的洗涤方法是
③请写出生成FeCO3沉淀的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】从铝土矿(主要成分是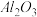 ,含
,含 、
、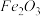 、MgO等杂质)中提取两种工艺品的流程如下:
、MgO等杂质)中提取两种工艺品的流程如下:
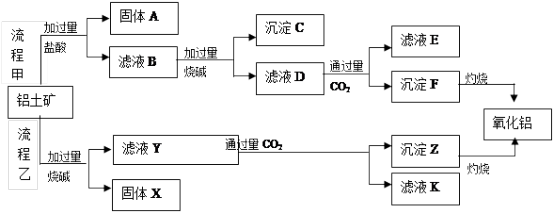
请回答下列问题:
(1)流程乙加入烧碱后的离子方程式为_________________________________________ .
(2)固体A的应用_________________________________________ .(两点)
(3)滤液D与少量CO2反应的离子方程式为__________________________________ ,
向该滤液K中加入足量石灰水的离子方程式是________
(4)流程乙制氧化铝的优点是所用的试剂较经济,缺点是__________________________
(5)已知298K时, 的溶度积常数
的溶度积常数 =10-11,取适量的滤液B,加入一定量的烧碱恰使镁离子沉淀完全,则溶液的pH最小为
=10-11,取适量的滤液B,加入一定量的烧碱恰使镁离子沉淀完全,则溶液的pH最小为_______ .
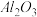 ,含
,含 、
、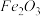 、MgO等杂质)中提取两种工艺品的流程如下:
、MgO等杂质)中提取两种工艺品的流程如下:
请回答下列问题:
(1)流程乙加入烧碱后的离子方程式为
(2)固体A的应用
(3)滤液D与少量CO2反应的离子方程式为
向该滤液K中加入足量石灰水的离子方程式是
(4)流程乙制氧化铝的优点是所用的试剂较经济,缺点是
(5)已知298K时,
 的溶度积常数
的溶度积常数 =10-11,取适量的滤液B,加入一定量的烧碱恰使镁离子沉淀完全,则溶液的pH最小为
=10-11,取适量的滤液B,加入一定量的烧碱恰使镁离子沉淀完全,则溶液的pH最小为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】铝土矿的主要成分是Al2O3,含有杂质SiO2、Fe2O3、MgO。工业上从铝土矿中提取铝可采用如下工艺流程:

请回答下列问题:
⑴图中涉及分离溶液与沉淀的实验方法是__________ (填操作名称)。
⑵沉淀B的成分是___________ (填化学式,下同);沉淀C的成分是___________ ;溶液D中大量存在的阴离子是___________ 。
⑶沉淀F转化为物质M的化学方程式为___________ ;由物质M制取铝的化学方程式为___________ ;溶液D中通入过量CO2生成沉淀F的离子方程式为__________ 。

请回答下列问题:
⑴图中涉及分离溶液与沉淀的实验方法是
⑵沉淀B的成分是
⑶沉淀F转化为物质M的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】聚合铝(PAC)是一种新型高效的无机高分子絮凝剂,广泛用于水的处理。用铝灰、铝土矿、铝渣等为原料(主要成分为Al、Al2O3)可制取聚合铝。实验步骤如下:

聚合铝(PAC)的分子式为[Al2(OH)aCl b]m,聚合铝中OH-与Al3+的比值对净水效果有很大影响,定义盐基度B= ,当B=
,当B=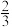 时,b = (填入合适数字)。
时,b = (填入合适数字)。

聚合铝(PAC)的分子式为[Al2(OH)aCl b]m,聚合铝中OH-与Al3+的比值对净水效果有很大影响,定义盐基度B=
 ,当B=
,当B=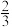 时,b = (填入合适数字)。
时,b = (填入合适数字)。
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】工业上用铝土矿(主要成分为Al2O3,还有少量的Fe2O3,SiO2等杂质)提取氧化铝作冶炼铝的原料,提取的操作过程如下:

(1)Ⅰ和Ⅱ步骤中分离溶液和沉淀的操作是:_____________ 。
(2)沉淀M中除含有泥沙外,一定还含有_________ (填化学式),生成固体N反应的化学方程式为_________ 。
(3)滤液X中,含铝元素的溶质的化学式为___________ ,它属于__________ (填“酸”、“碱”或“盐”)类物质。
(4)实验室里常往AlCl3溶液中加入___________ (填“氨水”或“NaOH溶液”)来制取Al(OH)3,该反应的离子方程式为__________________________ 。
(5)滤液Y中除了含有Na2CO3或NaHCO3外,一定还含有__________________ 。

(1)Ⅰ和Ⅱ步骤中分离溶液和沉淀的操作是:
(2)沉淀M中除含有泥沙外,一定还含有
(3)滤液X中,含铝元素的溶质的化学式为
(4)实验室里常往AlCl3溶液中加入
(5)滤液Y中除了含有Na2CO3或NaHCO3外,一定还含有
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】1929年,吴蕴初先生在上海创建了天原化工厂,它是中国最早的氯碱工业,如图给出了部分生产流程:


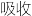
(1)为了除去粗盐中Ca2+、Mg2+、SO 及泥沙,可将粗盐溶于水,然后进行下列操作。
及泥沙,可将粗盐溶于水,然后进行下列操作。
①过滤②加过量的NaOH溶液③加适量盐酸④加过量Na2CO3溶液⑤加过量BaCl2溶液。其中正确的操作顺序是____ 。
A.②④⑤①③ B.①⑤④②③ C.⑤②④①③ D.②⑤④①③
操作①过滤所需要的玻璃仪器是____ ,操作③加适量盐酸所发生的化学反应____ 。
(2)在电解过程中,与电源正极相连的电极称____ 极,另一电极产生的物质____ 。氯碱厂电解饱和食盐水的化学方程式为:____ ;阳极产物检验的方法是____ 。电解饱和食盐水得到的气体物质,在合成塔中发生反应生成X,X溶于水可得到重要的化工原料,合成X的化学方程式是____ 。


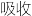
(1)为了除去粗盐中Ca2+、Mg2+、SO
 及泥沙,可将粗盐溶于水,然后进行下列操作。
及泥沙,可将粗盐溶于水,然后进行下列操作。①过滤②加过量的NaOH溶液③加适量盐酸④加过量Na2CO3溶液⑤加过量BaCl2溶液。其中正确的操作顺序是
A.②④⑤①③ B.①⑤④②③ C.⑤②④①③ D.②⑤④①③
操作①过滤所需要的玻璃仪器是
(2)在电解过程中,与电源正极相连的电极称
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】钯(Pd)是一种不活泼金属,含钯催化剂在工业、科研上用量较大。某废钯催化剂(钯碳)中含有钯(5%~6%)、碳(93%~94%)、铁(1%~2%)以及其他杂质,故钯碳具有很高的回收价值。如图是利用钯碳制备氯化钯(PdCl2)和Pd的流程,回答下列问题:___________

您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】碱式硫酸铝[(1-x)Al2(SO4)3·xAl(OH)3]溶液可用于烟气脱硫。实验室用粉煤灰(主要含Al2O3、SiO2等)制备碱式硫酸铝溶液,实验流程如下:
已知“调pH”的反应为(2-x)Al2(SO4)3+3xCaCO3+3xH2O=2[(1-x)Al2(SO4)3·xAl(OH)3]+3xCaSO4+3xCO2↑
“酸浸”时应控制H2SO4溶液的用量,H2SO4溶液用量不能过量太多的原因是___________ 。

已知“调pH”的反应为(2-x)Al2(SO4)3+3xCaCO3+3xH2O=2[(1-x)Al2(SO4)3·xAl(OH)3]+3xCaSO4+3xCO2↑
“酸浸”时应控制H2SO4溶液的用量,H2SO4溶液用量不能过量太多的原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
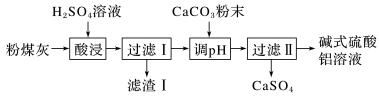
【推荐1】某再回收利用公司对一厨房铁铝合金废旧家具进行回收利用,其流程如下图所示:
请回答下列问题:
(1)流程中加碳酸钠溶液浸泡的目的是_______________ ;在空气中久置的目的是_________________ 。
(2)同条件下Na2FeO4溶解度__________ K2FeO4溶解度(填“低于”,“高于”, “不确定”),推测K2FeO4在净水方面的作用_______________ 。(至少答两条)
(3)已知K2FeO4水解显碱性。在洗涤K2FeO4固体时最好选用__________ 。
A.水 B.亚硫酸氢钠溶液 C.氢氧化钠溶液 D.先氢氧化钠溶液后乙醇
(4)熔融盐电镀中铝元素和氯元素主要以AlCl4-和Al2Cl7-形式存在,铝电镀的主要电极反应式为___________________ 。(写出一个电极反应即可)
(5)已知氯化铝受热易升华,气态氯化铝的密度为11.92g/L(已转化为标准状况),则气态氯化铝的分子式为______________________ 。
(6)氢氧化铝经常用于做药品,有两种溶解方式:可以溶解为Al3+或[Al(OH)4]-。已知25℃时氢氧化铝在pH=3和pH=10的两溶液中溶解度均为7.8×10-3g(溶液密度近似为1g/mL),则25℃下氢氧化铝的两种溶解方式的溶度积之比为____________ 。

请回答下列问题:
(1)流程中加碳酸钠溶液浸泡的目的是
(2)同条件下Na2FeO4溶解度
(3)已知K2FeO4水解显碱性。在洗涤K2FeO4固体时最好选用
A.水 B.亚硫酸氢钠溶液 C.氢氧化钠溶液 D.先氢氧化钠溶液后乙醇
(4)熔融盐电镀中铝元素和氯元素主要以AlCl4-和Al2Cl7-形式存在,铝电镀的主要电极反应式为
(5)已知氯化铝受热易升华,气态氯化铝的密度为11.92g/L(已转化为标准状况),则气态氯化铝的分子式为
(6)氢氧化铝经常用于做药品,有两种溶解方式:可以溶解为Al3+或[Al(OH)4]-。已知25℃时氢氧化铝在pH=3和pH=10的两溶液中溶解度均为7.8×10-3g(溶液密度近似为1g/mL),则25℃下氢氧化铝的两种溶解方式的溶度积之比为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】
(1)H3PO2的工业制法是:将白磷(P4)与Ba(OH)2溶液反应生成PH3气体和Ba(H2PO2)2,后者再与H2SO4反应制得H3PO2,写出白磷与Ba(OH)2溶液反应的化学方程式:____________________ 。
(2)①PbO2与浓盐酸共热生成黄绿色气体,反应的化学方程式为_________________ 。
②PbO2可由PbO与次氯酸钠溶液反应制得,反应的离子方程式为____________________ 。
(1)H3PO2的工业制法是:将白磷(P4)与Ba(OH)2溶液反应生成PH3气体和Ba(H2PO2)2,后者再与H2SO4反应制得H3PO2,写出白磷与Ba(OH)2溶液反应的化学方程式:
(2)①PbO2与浓盐酸共热生成黄绿色气体,反应的化学方程式为
②PbO2可由PbO与次氯酸钠溶液反应制得,反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
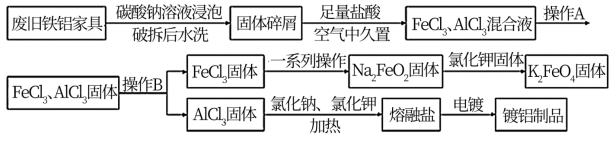
【推荐3】高铁酸钾是一种重要的绿色净水剂,具有净水和消毒双重功能。某课外学习小组设计如下方案制备高铁酸钾:
(1)高铁酸钾中铁元素的化合价为________ ,推测它具有的化学性质是__________________ 。
(2)已知Fe2O3与KNO3和KOH的混合物加热共融也可制得高铁酸钾。完成并配平下列化学方程式:
( ) Fe2O3+( ) KNO3+( ) KOH
( ) +( ) KNO2+( )
(3)将KOH加入含Na2FeO4的溶液中搅拌半小时,静置,过滤粗产品,该过程发生的反应为2KOH+Na2FeO4===K2FeO4+2NaOH,根据复分解反应原理,高铁酸钠的溶解度________ (填“大于”、“小于”或“等于”)高铁酸钾的溶解度。
(4)为测定含铁溶液中铁元素的总含量,实验操作:
①准确量取20.00mL含铁溶液于带塞锥形瓶中,加入足量H2O2,待充分反应后,加热除去过量H2O2;
②加入过量KI充分反应后,再用0.1000 mol·L-1Na2S2O3标准溶液滴定至终点,消耗标准溶液20.00 ml。已知: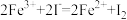
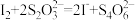
①写出滴定选用的指示剂________ ,滴定终点观察到的现象________ 。
②溶液Ⅰ中铁元素的总含量为_______________ g·L-1。若滴定前溶液中H2O2没有除尽,所测定的铁元素的含量将会______ (填“偏高”“偏低”“不变”)。

(1)高铁酸钾中铁元素的化合价为
(2)已知Fe2O3与KNO3和KOH的混合物加热共融也可制得高铁酸钾。完成并配平下列化学方程式:

(3)将KOH加入含Na2FeO4的溶液中搅拌半小时,静置,过滤粗产品,该过程发生的反应为2KOH+Na2FeO4===K2FeO4+2NaOH,根据复分解反应原理,高铁酸钠的溶解度
(4)为测定含铁溶液中铁元素的总含量,实验操作:
①准确量取20.00mL含铁溶液于带塞锥形瓶中,加入足量H2O2,待充分反应后,加热除去过量H2O2;
②加入过量KI充分反应后,再用0.1000 mol·L-1Na2S2O3标准溶液滴定至终点,消耗标准溶液20.00 ml。已知:
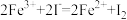
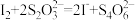
①写出滴定选用的指示剂
②溶液Ⅰ中铁元素的总含量为
您最近一年使用:0次



