由熔盐电解法获得的粗铝含一定量的金属钠和氢气,这些杂质可采用吹气精炼法除去,产生的尾气经处理后可用于钢材镀铝。工艺流程如下:
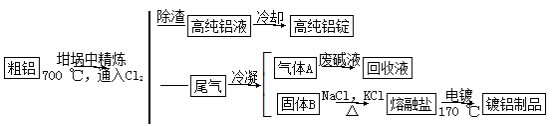
(注:NaCl熔点为801 ℃;AlCl3在181 ℃升华)
(1)精炼前,需清除坩埚表面的氧化铁和石英砂,防止精炼时它们分别与铝发生置换反应产生新的杂质,相关的化学方程式为:
①____________
②____________ 。
(2)将Cl2连续通入坩埚中的粗铝熔体,杂质随气泡上浮除去。气泡的主要成分除Cl2外还含有_________ ;固态杂质粘附于气泡上,在熔体表面形成浮渣,浮渣中肯定存在__________ 。
(3)在用废碱液处理气体A的过程中,所发生反应的离子方程式为:________________ 。
(4)镀铝电解池中,金属铝为________ 极。熔融盐电镀液中铝元素和氯元素主要以AlCl4-和Al2Cl7-形式存在,铝电极的主要电极反应式为___________ 。
(5)钢材镀铝后,表面形成的致密氧化铝膜能防止钢材腐蚀,其原因是______________ 。

(注:NaCl熔点为801 ℃;AlCl3在181 ℃升华)
(1)精炼前,需清除坩埚表面的氧化铁和石英砂,防止精炼时它们分别与铝发生置换反应产生新的杂质,相关的化学方程式为:
①
②
(2)将Cl2连续通入坩埚中的粗铝熔体,杂质随气泡上浮除去。气泡的主要成分除Cl2外还含有
(3)在用废碱液处理气体A的过程中,所发生反应的离子方程式为:
(4)镀铝电解池中,金属铝为
(5)钢材镀铝后,表面形成的致密氧化铝膜能防止钢材腐蚀,其原因是
更新时间:2016-12-09 00:39:06
|
相似题推荐
填空题
|
较难
(0.4)
名校
解题方法
【推荐1】绿色化学,体现了人类可持续发展的客观要求。尿素电氧化法在碱性条件下将工业废水和生活污水富含的尿素转化为对环境无害的物质,并将化学能转化电能(图1),由尿素电氧化法产生的电能可供治理硫化氢(图2)。


(1)写出CO(NH2)2的电子式:___ 。
(2)尿素电氧化法负极发生的反应为:___ ,隔膜为___ (填“阴”或“阳”)离子交换膜。
(3)先用FeCl3溶液吸收含H2S的工业废气,所得溶液用惰性电极电解,阳极区所得溶液循环利用,见图1。
①处理掉废水中尿素,消耗22.4L O2(标准状况下)时,可供治理硫化氢,产生___ gS沉淀;电解池的溶液中,溶质是___ 。
②阳极的电极反应式为___ 。
③电解总反应的离子方程式是___ 。


(1)写出CO(NH2)2的电子式:
(2)尿素电氧化法负极发生的反应为:
(3)先用FeCl3溶液吸收含H2S的工业废气,所得溶液用惰性电极电解,阳极区所得溶液循环利用,见图1。
①处理掉废水中尿素,消耗22.4L O2(标准状况下)时,可供治理硫化氢,产生
②阳极的电极反应式为
③电解总反应的离子方程式是
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐2】回答下列问题
(1)汽车尾气中 生成过程的能量变化如图所示。
生成过程的能量变化如图所示。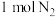 和
和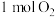 完全反应生成
完全反应生成 会
会_______ (填“吸收”或“放出”)_______ kJ能量。 和
和 组合形成的质子交换膜燃料电池的结构示意图如下图所示:
组合形成的质子交换膜燃料电池的结构示意图如下图所示: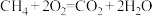 ,则c电极是
,则c电极是 _______ (填“正极”或“负极”),d电极的电极反应式:_______ 。若线路中转移 电子,则上述
电子,则上述 燃料电池消耗的
燃料电池消耗的 在标准状况下的体积为
在标准状况下的体积为_______ L。
(3)一种新型催化用于 和
和 的反应:
的反应: 。已知增大催化剂的表面积可提高该反应速率,为了验证温度、催化剂的比表面积对化学反应速率的影响规律,某同学设计了三组实验,部分条件已经填在下表中。
。已知增大催化剂的表面积可提高该反应速率,为了验证温度、催化剂的比表面积对化学反应速率的影响规律,某同学设计了三组实验,部分条件已经填在下表中。
①请将表中数据补充完整:a=_______ 。
②能验证温度对化学反应速率影响规律的是实验_______ (填序号)。
③实验I和实验II中, 的物质的量浓度
的物质的量浓度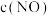 随时间
随时间 的变化曲线如图所示,其中表示实验II的是曲线
的变化曲线如图所示,其中表示实验II的是曲线 _______ (填“甲”或“乙”)。
(1)汽车尾气中
 生成过程的能量变化如图所示。
生成过程的能量变化如图所示。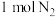 和
和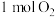 完全反应生成
完全反应生成 会
会
 和
和 组合形成的质子交换膜燃料电池的结构示意图如下图所示:
组合形成的质子交换膜燃料电池的结构示意图如下图所示:
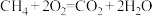 ,则c电极是
,则c电极是  电子,则上述
电子,则上述 燃料电池消耗的
燃料电池消耗的 在标准状况下的体积为
在标准状况下的体积为(3)一种新型催化用于
 和
和 的反应:
的反应: 。已知增大催化剂的表面积可提高该反应速率,为了验证温度、催化剂的比表面积对化学反应速率的影响规律,某同学设计了三组实验,部分条件已经填在下表中。
。已知增大催化剂的表面积可提高该反应速率,为了验证温度、催化剂的比表面积对化学反应速率的影响规律,某同学设计了三组实验,部分条件已经填在下表中。| 实验编号 | T/℃ | NO初始浓度/(mol∙L-1) | CO初始浓度/(mol∙L-1) | 催化剂的比表面积 (m2∙g-1) |
| I | 280 |  |  | 82 |
| II | 280 |  |  | 124 |
| III | 350 |  |  | 82 |
②能验证温度对化学反应速率影响规律的是实验
③实验I和实验II中,
 的物质的量浓度
的物质的量浓度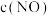 随时间
随时间 的变化曲线如图所示,其中表示实验II的是曲线
的变化曲线如图所示,其中表示实验II的是曲线 
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
解题方法
【推荐3】完成下列问题。
(1)已知:①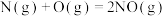

②

则表示氨气燃烧热的热化学方程式为___________ ,该反应可设计为碱性条件下的燃料电池,负极电极反应式为___________ 。
(2)已知几种化学键的键能和热化学方程式如下:

 ,则
,则
___________ 。
(3)4种不饱和烃分别与氢气发生加成反应生成1mol环己烷( )的能量变化如图所示。根据图示计算反应
)的能量变化如图所示。根据图示计算反应 (1)=
(1)=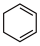 (1)的
(1)的
___________ 。

(4)利用多晶铜高效催化电解 制乙烯的原理如图所示。因电解前后电解液浓度几乎不变,故可实现
制乙烯的原理如图所示。因电解前后电解液浓度几乎不变,故可实现 的连续转化。
的连续转化。
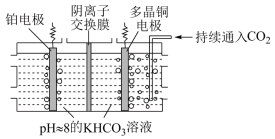
①电解过程中 向
向___________ (填“铂”或“多晶铜”)电极方向移动。
②铂电极产生的气体是___________ 。
③多晶铜电极上的电极反应式为___________ 。
(1)已知:①
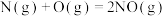

②


则表示氨气燃烧热的热化学方程式为
(2)已知几种化学键的键能和热化学方程式如下:
| 化学键 |  |  |  |  |  |
键能 | a | b | c | x | d |

 ,则
,则
(3)4种不饱和烃分别与氢气发生加成反应生成1mol环己烷(
 )的能量变化如图所示。根据图示计算反应
)的能量变化如图所示。根据图示计算反应 (1)=
(1)= (1)的
(1)的

(4)利用多晶铜高效催化电解
 制乙烯的原理如图所示。因电解前后电解液浓度几乎不变,故可实现
制乙烯的原理如图所示。因电解前后电解液浓度几乎不变,故可实现 的连续转化。
的连续转化。
①电解过程中
 向
向②铂电极产生的气体是
③多晶铜电极上的电极反应式为
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐1】钼酸钠晶体(Na2MoO4·2H2O)可用于制造生物碱、油墨、化肥、钼红颜料、催化剂等,也可用于制造阻燃剂和无公害型冷水系统的金属抑制剂。下图是利用钼精矿(主要成分是MoS2,含少量PbS等)为原料生产钼酸钠晶体的工艺流程图:

回答下列问题:
(1)Na2MoO4中Mo的化合价为____________ 。
(2)“焙烧”时,Mo元素转化为MoO3,反应的化学方程式为____________ ,氧化产物是________ (写化学式)。
(3)“碱浸”生成CO2和另外一种物质,CO2的电子式为_______ ,另外一种生成物的化学式为______ 。
(4)若“除重金属离子”时加入的沉淀剂为Na2S,则废渣成分的化学式为________ 。
(5)测得“除重金属离子”中部分离子的浓度:c(MoO42-)=0.40mol/L,c(SO42-)=0.04mol/L。“结晶”前需先除去SO42-,方法是加入Ba(OH)2固体。假设加入Ba(OH)2固体后溶液体积不变,当BaMoO4开始沉淀时,SO42-的去除率为______ %。(小数点后保留一位数字)[已知:Ksp(BaSO4)=1.1×10-10,Ksp(BaMoO4)=4.0×10-8]
(6)钼精矿在碱性条件下,加入NaClO溶液,也可以制备钼酸钠,同时有SO42-生成,该反应的离子方程式为___________________ 。

回答下列问题:
(1)Na2MoO4中Mo的化合价为
(2)“焙烧”时,Mo元素转化为MoO3,反应的化学方程式为
(3)“碱浸”生成CO2和另外一种物质,CO2的电子式为
(4)若“除重金属离子”时加入的沉淀剂为Na2S,则废渣成分的化学式为
(5)测得“除重金属离子”中部分离子的浓度:c(MoO42-)=0.40mol/L,c(SO42-)=0.04mol/L。“结晶”前需先除去SO42-,方法是加入Ba(OH)2固体。假设加入Ba(OH)2固体后溶液体积不变,当BaMoO4开始沉淀时,SO42-的去除率为
(6)钼精矿在碱性条件下,加入NaClO溶液,也可以制备钼酸钠,同时有SO42-生成,该反应的离子方程式为
您最近一年使用:0次
填空题
|
较难
(0.4)
解题方法
【推荐2】氧缺位体( )是热化学循环分解水制氢的催化剂。一种以黄铜矿主要成分是(
)是热化学循环分解水制氢的催化剂。一种以黄铜矿主要成分是( ,含
,含 、
、 等杂质)、为原料制备
等杂质)、为原料制备 的流程如下:
的流程如下: 、
、 、
、 和
和
②25℃时已知几种金属离子沉淀的pH如表所示:
请回答下列问题:
(1)加Cu“还原”的目是___________ 。
 )是热化学循环分解水制氢的催化剂。一种以黄铜矿主要成分是(
)是热化学循环分解水制氢的催化剂。一种以黄铜矿主要成分是( ,含
,含 、
、 等杂质)、为原料制备
等杂质)、为原料制备 的流程如下:
的流程如下: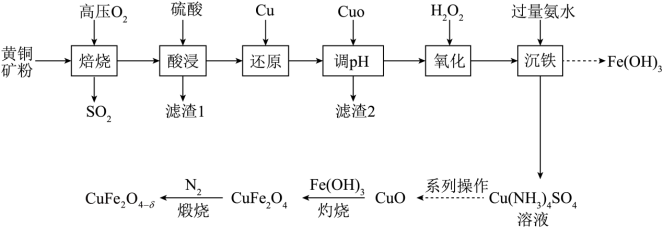
 、
、 、
、 和
和
②25℃时已知几种金属离子沉淀的pH如表所示:
| 金属氢氧化物 |  |  |  |  |
| 开始沉淀的pH | 1.9 | 3.4 | 6.4 | 7.0 |
| 完全沉淀的pH | 3.2 | 4.7 | 7.6 | 9.0 |
(1)加Cu“还原”的目是
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐3】污染物的有效去除和资源的充分利用是化学造福人类的重要研究课题。某研究小组利用软锰矿(主要成分为MnO2,另含少量铁,铝,铜等金属化合物)作脱硫剂,通过如下简化流程,既脱除燃煤尾气中的SO2,又制得电池材料MnO2(反应条件已省略)。

请回答下列问题:
38.上述流程脱硫实现了_________ (选填编号)。
a.废弃物的综合利用 b.白色污染的减少
c.酸雨的减少 d.臭氧层空洞的减少
39.步骤I生成无水MnSO4的化学方程式是_________________________________ 。
步骤IV生成无水MnO2的化学方程式是_________________________________ 。
40.步骤I中,用MnCO3能除去溶液中Al3+和Fe3+,其原因是__________________ 。滤渣M的成分是_________________ 。铜元素以______ 形式存在于滤渣N中。(写化学式)
41.产品MnO2可作超级电容材料。用惰性电极电解MnSO4溶液可以制得MnO2,则MnO2在_______ 生成(填电极名称)。
42.假设脱除的SO2只与软锰矿浆中MnO2反应。按照图示流程,将2.0 m3(标准状况)含SO2的体积分数为60%的尾气通入矿浆,若SO2的脱除率为89.6%,最终得到MnO2的质量10.44 kg。则在除去铁、铝、铜、镍等杂质的过程中,所引入的锰元素为________ kg。

请回答下列问题:
38.上述流程脱硫实现了
a.废弃物的综合利用 b.白色污染的减少
c.酸雨的减少 d.臭氧层空洞的减少
39.步骤I生成无水MnSO4的化学方程式是
步骤IV生成无水MnO2的化学方程式是
40.步骤I中,用MnCO3能除去溶液中Al3+和Fe3+,其原因是
41.产品MnO2可作超级电容材料。用惰性电极电解MnSO4溶液可以制得MnO2,则MnO2在
42.假设脱除的SO2只与软锰矿浆中MnO2反应。按照图示流程,将2.0 m3(标准状况)含SO2的体积分数为60%的尾气通入矿浆,若SO2的脱除率为89.6%,最终得到MnO2的质量10.44 kg。则在除去铁、铝、铜、镍等杂质的过程中,所引入的锰元素为
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐1】无水四氯化锡[ g/mol]常用于合成染色的媒染剂。实验室可用熔融的锡与氯气反应制备无水
g/mol]常用于合成染色的媒染剂。实验室可用熔融的锡与氯气反应制备无水 ,可选用的装置如下图所示:
,可选用的装置如下图所示:

已知: 常温时为无色液体,沸点(114℃);
常温时为无色液体,沸点(114℃); 易溶于
易溶于 ;
; 在空气中极易水解生成
在空气中极易水解生成 。
。
回答下列问题:
(1)A中盛放 晶体的仪器名称为
晶体的仪器名称为_______ ,在其中发生反应的化学方程式是_______ 。
(2)整个实验装置的连接顺序是A→_______ →BC→_______ 。
(3)装置E的作用是_______ ;若缺少装置F,则收集器C中发生反应的化学方程式为_______
(4)收集器C中收集到的液体略显黄色,原因是_______ ,C中上方冷水的作用是_______ 。
(5)除氯后测定最后产品的纯度。量取 mL,Ag/mL的样品,置于已称重含20mL水的称量瓶中,混合后,移入锥形瓶,加入200mL水和2滴1%甲基橙指示液,用B mol/L的NaOH标准液滴定,消耗标准液
mL,Ag/mL的样品,置于已称重含20mL水的称量瓶中,混合后,移入锥形瓶,加入200mL水和2滴1%甲基橙指示液,用B mol/L的NaOH标准液滴定,消耗标准液 mL(接近终点时,每滴加一滴标准液须待沉淀沉降后观察澄清液体的颜色)。滴定到达终点的实验现象为
mL(接近终点时,每滴加一滴标准液须待沉淀沉降后观察澄清液体的颜色)。滴定到达终点的实验现象为_______ ,产品的纯度为_______ %。
 g/mol]常用于合成染色的媒染剂。实验室可用熔融的锡与氯气反应制备无水
g/mol]常用于合成染色的媒染剂。实验室可用熔融的锡与氯气反应制备无水 ,可选用的装置如下图所示:
,可选用的装置如下图所示:
已知:
 常温时为无色液体,沸点(114℃);
常温时为无色液体,沸点(114℃); 易溶于
易溶于 ;
; 在空气中极易水解生成
在空气中极易水解生成 。
。回答下列问题:
(1)A中盛放
 晶体的仪器名称为
晶体的仪器名称为(2)整个实验装置的连接顺序是A→
(3)装置E的作用是
(4)收集器C中收集到的液体略显黄色,原因是
(5)除氯后测定最后产品的纯度。量取
 mL,Ag/mL的样品,置于已称重含20mL水的称量瓶中,混合后,移入锥形瓶,加入200mL水和2滴1%甲基橙指示液,用B mol/L的NaOH标准液滴定,消耗标准液
mL,Ag/mL的样品,置于已称重含20mL水的称量瓶中,混合后,移入锥形瓶,加入200mL水和2滴1%甲基橙指示液,用B mol/L的NaOH标准液滴定,消耗标准液 mL(接近终点时,每滴加一滴标准液须待沉淀沉降后观察澄清液体的颜色)。滴定到达终点的实验现象为
mL(接近终点时,每滴加一滴标准液须待沉淀沉降后观察澄清液体的颜色)。滴定到达终点的实验现象为
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐2】(1)已知用金属钠制取氧化钠,可有多种方法:
①4Na+O2===2Na2O
②4Na+CO2===2Na2O+C
③2NaNO2+6Na===4Na2O+N2↑
在上述三种方法中最好的是_______ ,原因是______________________________________ 。该反应中作氧化剂的是________ 。
(2)据资料介绍:过氧化钠是钠在空气中燃烧的主要产物,由于空气中还含有其他成分,因此还存在其他产物,如氮化钠。已知氮化钠与水反应能生成氢氧化钠和氨气,则氮化钠与水反应的化学方程式为____________________________ 。
①4Na+O2===2Na2O
②4Na+CO2===2Na2O+C
③2NaNO2+6Na===4Na2O+N2↑
在上述三种方法中最好的是
(2)据资料介绍:过氧化钠是钠在空气中燃烧的主要产物,由于空气中还含有其他成分,因此还存在其他产物,如氮化钠。已知氮化钠与水反应能生成氢氧化钠和氨气,则氮化钠与水反应的化学方程式为
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐3】A、B、C、D、E是中学常见的5种化合物,A、B是氧化物,元素X、Y、的单质是生活中常见的金属,相关物质间的关系如下图所示。
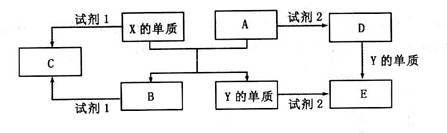
回答下列问题:
(1)X的单质与A反应的化学方程式是______ 。
(2)若C溶液显碱性,则试剂1是______ 溶液(写化学式);若C溶液显酸性,则显酸性的原因是(用离子方程式表示)______ 。
(3)若试剂1和试剂2均是稀硫酸。
①检验物质D的溶液中金属离子的方法是______ ;
②写出D—E反应的离子方程式______ ;
③某高效净水剂是由Y(OH)SO4聚合得到的。工业上以E、稀硫酸和亚硝酸钠为原料来制备Y(OH)SO4,反应中有NO生成,该反应的化学方程式是(不必配平):______ 。

回答下列问题:
(1)X的单质与A反应的化学方程式是
(2)若C溶液显碱性,则试剂1是
(3)若试剂1和试剂2均是稀硫酸。
①检验物质D的溶液中金属离子的方法是
②写出D—E反应的离子方程式
③某高效净水剂是由Y(OH)SO4聚合得到的。工业上以E、稀硫酸和亚硝酸钠为原料来制备Y(OH)SO4,反应中有NO生成,该反应的化学方程式是(不必配平):
您最近一年使用:0次



