氯化铁和高铁酸钾都是常见的水处理剂。下图为制备氯化铁及进一步氧化制备高铁酸钾的工艺流程。

请回答下列问题:
(1)氯化铁有多种用途,请用离子方程式表示下列用途的原理。
①氯化铁做净水剂______________________ ;
②用FeCl3溶液(32%~35%)腐蚀铜印刷线路板_________________________ 。
(2)吸收剂X的化学式为___________________ ;氧化剂Y的化学式为____________ 。
(3)碱性条件下反应①的离子方程式为____________________________________ 。
(4)过程②将混合溶液搅拌半小时,静置,抽滤获得粗产品。该反应的化学方程式为2KOH+Na2FeO4=K2FeO4+2NaOH,请根据复分解反应原理分析反应发生的原因________________ 。
(5)K2FeO4在水溶液中易发生反应:4FeO42+10H2O 4Fe(OH)3+8OH+3O2↑。在提纯K2FeO4时采用重结晶、洗涤、低温烘干的方法,则洗涤剂最好选用
4Fe(OH)3+8OH+3O2↑。在提纯K2FeO4时采用重结晶、洗涤、低温烘干的方法,则洗涤剂最好选用__________________ (填序号)。
(6)可用滴定分析法测定粗K2FeO4的纯度,有关反应离子方程式为:
①FeO42-+CrO2-+2H2O CrO42-+Fe(OH)3↓+OH-
CrO42-+Fe(OH)3↓+OH-
②2CrO42-+2H+ Cr2O72-+H2O
Cr2O72-+H2O
③Cr2O72-+6Fe2++14H+ 2Cr3++6Fe3++7H2O
2Cr3++6Fe3++7H2O
现称取1.980 g粗高铁酸钾样品溶于适量氢氧化钾溶液中,加入稍过量的KCrO2,充分反应后过滤滤液定容于250 mL容量瓶中。每次取25.00 mL加入稀硫酸酸化,用0.1000 mol/L的(NH4)2Fe(SO4)2标准溶液滴定,三次滴定消耗标准溶液的平均体积为18.93 mL。则上述样品中高铁酸钾的质量分数为____________ 。

请回答下列问题:
(1)氯化铁有多种用途,请用离子方程式表示下列用途的原理。
①氯化铁做净水剂
②用FeCl3溶液(32%~35%)腐蚀铜印刷线路板
(2)吸收剂X的化学式为
(3)碱性条件下反应①的离子方程式为
(4)过程②将混合溶液搅拌半小时,静置,抽滤获得粗产品。该反应的化学方程式为2KOH+Na2FeO4=K2FeO4+2NaOH,请根据复分解反应原理分析反应发生的原因
(5)K2FeO4在水溶液中易发生反应:4FeO42+10H2O
 4Fe(OH)3+8OH+3O2↑。在提纯K2FeO4时采用重结晶、洗涤、低温烘干的方法,则洗涤剂最好选用
4Fe(OH)3+8OH+3O2↑。在提纯K2FeO4时采用重结晶、洗涤、低温烘干的方法,则洗涤剂最好选用| A.H2O |
| B.稀KOH溶液、异丙醇 |
| C.NH4Cl溶液、异丙醇 |
| D.Fe(NO3)3溶液、异丙醇 |
(6)可用滴定分析法测定粗K2FeO4的纯度,有关反应离子方程式为:
①FeO42-+CrO2-+2H2O
 CrO42-+Fe(OH)3↓+OH-
CrO42-+Fe(OH)3↓+OH-②2CrO42-+2H+
 Cr2O72-+H2O
Cr2O72-+H2O③Cr2O72-+6Fe2++14H+
 2Cr3++6Fe3++7H2O
2Cr3++6Fe3++7H2O现称取1.980 g粗高铁酸钾样品溶于适量氢氧化钾溶液中,加入稍过量的KCrO2,充分反应后过滤滤液定容于250 mL容量瓶中。每次取25.00 mL加入稀硫酸酸化,用0.1000 mol/L的(NH4)2Fe(SO4)2标准溶液滴定,三次滴定消耗标准溶液的平均体积为18.93 mL。则上述样品中高铁酸钾的质量分数为
更新时间:2016-12-09 01:04:04
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】铁及其化合物在生产生活中有十分广泛的应用。铁的部分化合物的相互转化关系如框图所示,请回答相关问题。
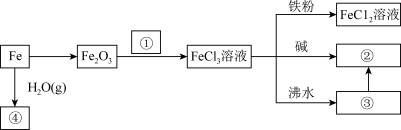
(1)图中①②③代表的物质所属不同分散系,③代表的物质所属的分散系名称是_______ ;
(2)写出生成④的化学反应方程式_______ ;
(3)写出 与①反应的离子方程式
与①反应的离子方程式_______ 。
(4)已知: 与铁粉反应生成
与铁粉反应生成 ,该反应中的氧化剂是
,该反应中的氧化剂是_______ 。若要实现 转化为
转化为 ,可以选用稀硫酸酸化的
,可以选用稀硫酸酸化的 溶液,请写出该反应的离子方程式
溶液,请写出该反应的离子方程式_______ 。

(1)图中①②③代表的物质所属不同分散系,③代表的物质所属的分散系名称是
(2)写出生成④的化学反应方程式
(3)写出
 与①反应的离子方程式
与①反应的离子方程式(4)已知:
 与铁粉反应生成
与铁粉反应生成 ,该反应中的氧化剂是
,该反应中的氧化剂是 转化为
转化为 ,可以选用稀硫酸酸化的
,可以选用稀硫酸酸化的 溶液,请写出该反应的离子方程式
溶液,请写出该反应的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】铁在一定条件下的反应如图所示。请回答下列问题:
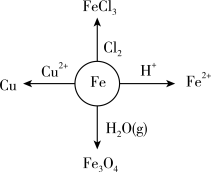
(1)晋代的《抱朴子》中有记载“以曾青涂铁,铁赤色如铜”,成为现代湿法治金的先驱。曾青就是胆矾,即五水硫酸铜。将铁放在胆矾溶液(古人称为胆水)中,可以得到金属铜,请写出该反应的化学方程式:____________ 。
(2)工业上,向500~600℃的铁屑中通入 生产
生产 ,每生产1 kg
,每生产1 kg ,消耗
,消耗 的物质的量为
的物质的量为_____ (计算结果保留2位小数)。
(3)实现Fe转化为 ,可选用
,可选用______ (填化学式)溶液。
(4)高温下,Fe粉与水蒸气反应的化学方程式为_______________ 。
(5)请写出 溶于稀盐酸的离子方程式:
溶于稀盐酸的离子方程式:_____________ 。

(1)晋代的《抱朴子》中有记载“以曾青涂铁,铁赤色如铜”,成为现代湿法治金的先驱。曾青就是胆矾,即五水硫酸铜。将铁放在胆矾溶液(古人称为胆水)中,可以得到金属铜,请写出该反应的化学方程式:
(2)工业上,向500~600℃的铁屑中通入
 生产
生产 ,每生产1 kg
,每生产1 kg ,消耗
,消耗 的物质的量为
的物质的量为(3)实现Fe转化为
 ,可选用
,可选用(4)高温下,Fe粉与水蒸气反应的化学方程式为
(5)请写出
 溶于稀盐酸的离子方程式:
溶于稀盐酸的离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】铁是人类较早使用的金属之一,根据铁及其化合物之间的相互转化,回答下列问题:
(1)Fe2+易被人体吸收,医生建议在服用补铁剂时,同时服用维生素C.维生素C的作用是______ 。
(2)印刷电路板的制作原理是用足量的FeCl3溶液腐蚀覆铜板上不需要的铜箔。写出上述反应的离子方程式:______ 。
(3)某废料铁泥的主要成分为Fe2O3、FeO、Fe和杂质(杂质不与硫酸反应)。现取wg废料铁泥提取Fe2O3,设计实验流程如下:

①分离溶液A和沉淀C的实验操作为______ 。
②能检验溶液A中含有Fe2+的试剂是______ (填字母)。
A.铁粉 B.酸性KMnO4溶液 C.KSCN溶液
③步骤Ⅱ中发生反应的离子方程式为______ 。
④若最终获得ngFe2O3,则废料铁泥中铁元素的质量分数为______ 。
(1)Fe2+易被人体吸收,医生建议在服用补铁剂时,同时服用维生素C.维生素C的作用是
(2)印刷电路板的制作原理是用足量的FeCl3溶液腐蚀覆铜板上不需要的铜箔。写出上述反应的离子方程式:
(3)某废料铁泥的主要成分为Fe2O3、FeO、Fe和杂质(杂质不与硫酸反应)。现取wg废料铁泥提取Fe2O3,设计实验流程如下:

①分离溶液A和沉淀C的实验操作为
②能检验溶液A中含有Fe2+的试剂是
A.铁粉 B.酸性KMnO4溶液 C.KSCN溶液
③步骤Ⅱ中发生反应的离子方程式为
④若最终获得ngFe2O3,则废料铁泥中铁元素的质量分数为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】一方面,磷矿藏在地球上分布不均匀且储量有限;另一方面,污水中含有较多的磷元素。因此在污水处理生物污泥中的蓝铁矿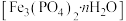 因其潜在的特殊用途以及经济价值而备受关注。蓝铁矿在自然水体中形成的过程如图。
因其潜在的特殊用途以及经济价值而备受关注。蓝铁矿在自然水体中形成的过程如图。
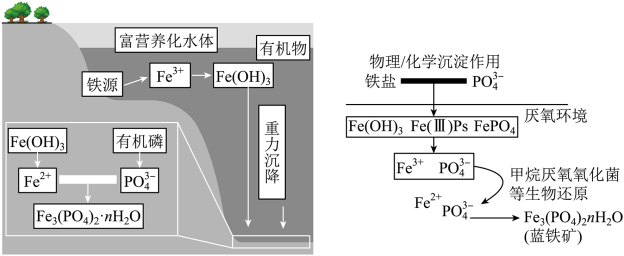
(1)水处理时,加入的高铁酸钾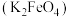 作为净水消毒剂,发生反应的化学方程式为
作为净水消毒剂,发生反应的化学方程式为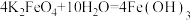 (胶体)
(胶体)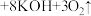 。
。
① 中
中 的化合价为
的化合价为_______ 价,上述反应涉及的物质中属于盐的是_______ 。
②高铁酸钾可用于净水消毒的原因是_______ 。
(2)在甲烷厌氧氧化菌的作用下,氢氧化铁和甲烷发生如下反应,配平该离子方程式:_______ 。

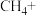

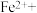
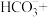

(3)无氧条件下加热,蓝铁矿(无杂质)发生分解: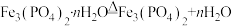 ,蓝铁矿的质量由5.02g减小为3.58g,则n=
,蓝铁矿的质量由5.02g减小为3.58g,则n=_______ ,蓝铁矿的相对分子质量为_______ 。
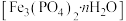 因其潜在的特殊用途以及经济价值而备受关注。蓝铁矿在自然水体中形成的过程如图。
因其潜在的特殊用途以及经济价值而备受关注。蓝铁矿在自然水体中形成的过程如图。
(1)水处理时,加入的高铁酸钾
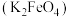 作为净水消毒剂,发生反应的化学方程式为
作为净水消毒剂,发生反应的化学方程式为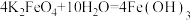 (胶体)
(胶体)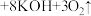 。
。①
 中
中 的化合价为
的化合价为②高铁酸钾可用于净水消毒的原因是
(2)在甲烷厌氧氧化菌的作用下,氢氧化铁和甲烷发生如下反应,配平该离子方程式:

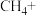

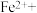
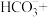

(3)无氧条件下加热,蓝铁矿(无杂质)发生分解:
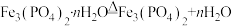 ,蓝铁矿的质量由5.02g减小为3.58g,则n=
,蓝铁矿的质量由5.02g减小为3.58g,则n=
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】高铁酸钾(K2FeO4)是一种新型、高效、多功能绿色水处理剂,比Cl2、O2、ClO2、KMnO4氧化性更强,无二次污染,工业上先制得高铁酸钠,然后在低温下,向高铁酸钠溶液中加入KOH至饱和,使高铁酸钾析出。
(1)干法制备高铁酸钠的主要反应为:2FeSO4+6Na2O2=2Na2FeO4+2Na2O+2Na2SO4+O2↑。
①该反应中的氧化剂是_____ ,还原剂是____ ,每生成1molNa2FeO4转移_______ mol电子。
②简要说明K2FeO4作为水处理剂时所起的作用:_________ 。
(2)湿法制备高铁酸钾(K2FeO4)的反应体系中有六种微粒:Fe(OH)3、ClO-、OH-、FeO42—、Cl-、H2O。写出并配平湿法制备高铁酸钾的离子反应方程式:______________ 。
(1)干法制备高铁酸钠的主要反应为:2FeSO4+6Na2O2=2Na2FeO4+2Na2O+2Na2SO4+O2↑。
①该反应中的氧化剂是
②简要说明K2FeO4作为水处理剂时所起的作用:
(2)湿法制备高铁酸钾(K2FeO4)的反应体系中有六种微粒:Fe(OH)3、ClO-、OH-、FeO42—、Cl-、H2O。写出并配平湿法制备高铁酸钾的离子反应方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】HNO2是一种弱酸,且不稳定,易分解生成NO和NO2;它能被常见的强氧化剂氧化;在酸性溶液中它也是一种氧化剂,如能把Fe2+氧化成Fe3+。AgNO2是一种难溶于水、易溶于酸的化合物,试回答下列问题:
(1)人体正常的血红蛋白含有Fe2+,若误食亚硝酸盐(如NaNO2),则导致血红蛋白中的Fe2+转化为Fe3+而中毒,服用维生素C可解毒。下列叙述不正确的是( ) (填字母)。
A.亚硝酸盐被还原 B.维生素C是还原剂
C.维生素C将Fe3+还原为Fe2+ D.亚硝酸盐是还原剂
(2)某同学把新制的氯水加到NaNO2溶液中,观察到氯水褪色,同时生成NaNO3和HCl,请写出反应的离子方程式:________________________ 。
(3)Fe与过量稀硫酸反应可以制取FeSO4,若用反应所得的酸性溶液,将Fe2+转化为Fe3+,要求产物纯净,可选用的最佳试剂是( ) (填字母)
A.Cl2 B.Fe C.H2O2 D.HNO3
请写离子方程式________________________ 。
(4)FeSO4可用于制备高铁酸钾(K2FeO4),写出在碱性条件下用FeSO4与NaClO反应制高铁酸钾的离子方程式:___________________ 。
①该反应中的还原剂是___________________ ,
②当有38g的FeSO4反应转移的电子数目为___________________ 。
(1)人体正常的血红蛋白含有Fe2+,若误食亚硝酸盐(如NaNO2),则导致血红蛋白中的Fe2+转化为Fe3+而中毒,服用维生素C可解毒。下列叙述不正确的是
A.亚硝酸盐被还原 B.维生素C是还原剂
C.维生素C将Fe3+还原为Fe2+ D.亚硝酸盐是还原剂
(2)某同学把新制的氯水加到NaNO2溶液中,观察到氯水褪色,同时生成NaNO3和HCl,请写出反应的离子方程式:
(3)Fe与过量稀硫酸反应可以制取FeSO4,若用反应所得的酸性溶液,将Fe2+转化为Fe3+,要求产物纯净,可选用的最佳试剂是
A.Cl2 B.Fe C.H2O2 D.HNO3
请写离子方程式
(4)FeSO4可用于制备高铁酸钾(K2FeO4),写出在碱性条件下用FeSO4与NaClO反应制高铁酸钾的离子方程式:
①该反应中的还原剂是
②当有38g的FeSO4反应转移的电子数目为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】消毒剂在生产、生活中有重要的作用,常见的含氯消毒剂有NaClO2、NaClO、ClO2 和Cl2
回答下列问题:
(1)NaClO2所含的化学键类型有________________ 。
(2)消毒剂投入水中,一段时间后与氨结合得到一种结合性氯胺(NH2Cl)。NH2Cl 在中性或酸性条件下也是一种强杀菌消毒剂,常用于城市自来水消毒。其理由是________________ (用化学方程式表示)。
(3) “有效氯含量”可用来衡量含氯消毒剂的消毒能力,其定义是每克含氯消毒剂的氧化能力相当于多少克Cl2 的氧化能力。上述四种含氯消毒剂中消毒能力最强的是________________ 。
(4)自来水厂用ClO2 处理后的水中,要求ClO2 的浓度在0.1~0.8 mg·L-1之间。用碘量法检测ClO2 处理后的自来水中ClO2 浓度的实验步骤如下:
步骤Ⅰ.取一定体积的水样,加入足量碘化钾,再用氢氧化钠溶液调至中性,并加入淀粉溶液。
步骤Ⅱ.用Na2S2O3 溶液滴定步骤Ⅰ中所得的溶液。
已知:a. 操作时,不同pH 环境中粒子种类如下表所示。
b. 2S2O32-+I2==S4O62-+2I-。
①步骤Ⅱ中反应结束时溶液呈___________ (填“蓝色”或“无色”)
②若水样的体积为1.0L,在步骤Ⅱ中消耗10mL1.0×10-3mol·L-1Na2S2O3 溶液,则该水样中c(ClO2)=___________ mg·L-1
回答下列问题:
(1)NaClO2所含的化学键类型有
(2)消毒剂投入水中,一段时间后与氨结合得到一种结合性氯胺(NH2Cl)。NH2Cl 在中性或酸性条件下也是一种强杀菌消毒剂,常用于城市自来水消毒。其理由是
(3) “有效氯含量”可用来衡量含氯消毒剂的消毒能力,其定义是每克含氯消毒剂的氧化能力相当于多少克Cl2 的氧化能力。上述四种含氯消毒剂中消毒能力最强的是
(4)自来水厂用ClO2 处理后的水中,要求ClO2 的浓度在0.1~0.8 mg·L-1之间。用碘量法检测ClO2 处理后的自来水中ClO2 浓度的实验步骤如下:
步骤Ⅰ.取一定体积的水样,加入足量碘化钾,再用氢氧化钠溶液调至中性,并加入淀粉溶液。
步骤Ⅱ.用Na2S2O3 溶液滴定步骤Ⅰ中所得的溶液。
已知:a. 操作时,不同pH 环境中粒子种类如下表所示。
| pH | 2 | 7 |
| 粒子种类 | Cl- | ClO2- |
b. 2S2O32-+I2==S4O62-+2I-。
①步骤Ⅱ中反应结束时溶液呈
②若水样的体积为1.0L,在步骤Ⅱ中消耗10mL1.0×10-3mol·L-1Na2S2O3 溶液,则该水样中c(ClO2)=
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】三水乳酸亚铁晶体[(CH3CHOHCOO)2Fe•3H2O,Mr=288]是一种很好的补铁剂,易溶于水,吸收效果比无机铁好。可由绿矾(FeSO4·7H2O)通过下列反应制备:
FeSO4+Na2CO3== FeCO3↓+Na2SO4
FeCO3+ 2CH3CHOHCOOH ==(CH3CHOHCOO)2Fe+CO2↑+H2O
(1)制备FeCO3时,选用的加料方式是______ (填字母),原因是_______________________ 。
a.将FeSO4溶液与Na2CO3溶液同时加入到反应容器中
b.将FeSO4溶液缓慢加入到盛有Na2CO3溶液的反应容器中
c.将Na2CO3溶液缓慢加入到盛有FeSO4溶液的反应容器中
(2)生成的FeCO3沉淀需经充分洗涤,检验洗涤是否完全的方法是__________________ 。
(3)将制得的FeCO3加入到足量乳酸溶液中,再加入少量铁粉,75℃下搅拌反应。
①铁粉的作用是_____________________ 。
②反应结束后,无需过滤,除去过量铁粉的方法及反应方程式是______________________________________ 。
(4)最后溶液经浓缩、加入适量无水乙醇、静置、过滤、洗涤、干燥,获得三水乳酸亚铁晶体。分离过程中加入无水乙醇的目的是_______________ 。
(5)某研究性学习小组从硫铁矿烧渣(主要成分为Fe2O3、SiO2、Al2O3 ) 出发,经过一系列的实验步骤,最后制得到了硫酸亚铁溶液。请结合如图的绿矾溶解度曲线,将FeSO4溶液____________ ,得到FeSO4·7H2O晶体。
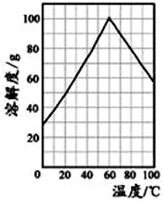
(6)该兴趣小组用标准KMnO4溶液测定产品中亚铁含量进而计算乳酸亚铁晶体的质量分数,发现产品的质量分数总是大于100%,其原因可能是____________________ 。经查阅文献后,该兴趣小组改用铈(Ce)量法测定产品中Fe2+的含量。取2.880g产品配成100mL溶液,每次取20.00mL,进行必要处理,用0.1000mol•L-1Ce(SO4)2标准溶液滴定至终点,平均消耗Ce(SO4)219.7mL。滴定反应为Ce4++Fe2+═Ce3++Fe3+,则产品中乳酸亚铁晶体的质量分数为__________ 。
FeSO4+Na2CO3== FeCO3↓+Na2SO4
FeCO3+ 2CH3CHOHCOOH ==(CH3CHOHCOO)2Fe+CO2↑+H2O
(1)制备FeCO3时,选用的加料方式是
a.将FeSO4溶液与Na2CO3溶液同时加入到反应容器中
b.将FeSO4溶液缓慢加入到盛有Na2CO3溶液的反应容器中
c.将Na2CO3溶液缓慢加入到盛有FeSO4溶液的反应容器中
(2)生成的FeCO3沉淀需经充分洗涤,检验洗涤是否完全的方法是
(3)将制得的FeCO3加入到足量乳酸溶液中,再加入少量铁粉,75℃下搅拌反应。
①铁粉的作用是
②反应结束后,无需过滤,除去过量铁粉的方法及反应方程式是
(4)最后溶液经浓缩、加入适量无水乙醇、静置、过滤、洗涤、干燥,获得三水乳酸亚铁晶体。分离过程中加入无水乙醇的目的是
(5)某研究性学习小组从硫铁矿烧渣(主要成分为Fe2O3、SiO2、Al2O3 ) 出发,经过一系列的实验步骤,最后制得到了硫酸亚铁溶液。请结合如图的绿矾溶解度曲线,将FeSO4溶液

(6)该兴趣小组用标准KMnO4溶液测定产品中亚铁含量进而计算乳酸亚铁晶体的质量分数,发现产品的质量分数总是大于100%,其原因可能是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】氯碱工业的原料饱和食盐水中含有一定量的铵根离子,在电解时会生成性质极不稳定的三氯化氮,容易引起爆炸。
(1)三氯化氮易水解,其水解的最初产物除生成氨气外,另一产物为_________ 。
(2)为除去饱和食盐水中的铵根离子,可在碱性条件下通入氯气,反应生成氮气。该反应的离子方程式为________ 。该工艺选择氯气的优点是__________ 。(答一点即可)
(3)过量氯气用Na2S2O3除去,反应中S2O32-被氧化为SO42-。若过量的氯气为10-3 mol/L,则理论上生成的SO42-为___________ mol/L。
(4)生产和实验中广泛采用甲醛法测定样品的含氮量。甲醛和铵根离子的反应如下:
4NH4++ 6HCHO =(CH2)6N4H+(一元酸)+ 3H+ + 6H2O
实验步骤如下:
①甲醛中常含有微量甲酸,应先除去。可取甲醛bmL于锥形瓶,加入1滴酚酞,用浓度为Cmol/L的NaOH溶液中和,滴定管的初始读数V1mL,当溶液呈微红色时,滴定管的读数V2mL。
②向其中加入饱和食盐水试样amL,静置1分钟。
③再加1~2滴酚酞,再用上述NaOH溶液滴定至微红色,滴定管的读数V3mL。
则饱和食盐水中的含氮量为__________ mg/L。
(1)三氯化氮易水解,其水解的最初产物除生成氨气外,另一产物为
(2)为除去饱和食盐水中的铵根离子,可在碱性条件下通入氯气,反应生成氮气。该反应的离子方程式为
(3)过量氯气用Na2S2O3除去,反应中S2O32-被氧化为SO42-。若过量的氯气为10-3 mol/L,则理论上生成的SO42-为
(4)生产和实验中广泛采用甲醛法测定样品的含氮量。甲醛和铵根离子的反应如下:
4NH4++ 6HCHO =(CH2)6N4H+(一元酸)+ 3H+ + 6H2O
实验步骤如下:
①甲醛中常含有微量甲酸,应先除去。可取甲醛bmL于锥形瓶,加入1滴酚酞,用浓度为Cmol/L的NaOH溶液中和,滴定管的初始读数V1mL,当溶液呈微红色时,滴定管的读数V2mL。
②向其中加入饱和食盐水试样amL,静置1分钟。
③再加1~2滴酚酞,再用上述NaOH溶液滴定至微红色,滴定管的读数V3mL。
则饱和食盐水中的含氮量为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】某研究性学习小组为了测定某品牌合金中铝的含量,现设计了如下实验:

已知:(1)该铝合金的主要成分为铝、镁、铜、硅。
(2)常温下,硅能和NaOH发生反应:Si+2NaOH+H2O===Na2SiO3+2H2↑。
(3)硅酸不溶于水
(4)固体C为Al2O3
请回答下列问题:
(1)固体A在潮湿的空气中久置可能会发生一个明显的变化,这个变化是________________ ;发生反应的化学方程式为_______________________ ;
(2)步骤③中洗涤沉淀的实验操作为_________________ ;
(3)该样品中铝的质量分数是_________________________ (用a、b表示);
(4)下列因操作不当,会使测定结果偏大的是_____________________ ;
A.第③步中沉淀未用蒸馏水洗涤
B.第①步中加入NaOH溶液不足
C.第④步对沉淀灼烧不充分

已知:(1)该铝合金的主要成分为铝、镁、铜、硅。
(2)常温下,硅能和NaOH发生反应:Si+2NaOH+H2O===Na2SiO3+2H2↑。
(3)硅酸不溶于水
(4)固体C为Al2O3
请回答下列问题:
(1)固体A在潮湿的空气中久置可能会发生一个明显的变化,这个变化是
(2)步骤③中洗涤沉淀的实验操作为
(3)该样品中铝的质量分数是
(4)下列因操作不当,会使测定结果偏大的是
A.第③步中沉淀未用蒸馏水洗涤
B.第①步中加入NaOH溶液不足
C.第④步对沉淀灼烧不充分
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
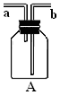
【推荐2】已知气体X是一种难溶于水的无色气体,常温时易与空气中的氧气迅速化合生成红棕色的气体Y。实验室常用以下反应制取X:3Cu+8HNO3=3Cu(NO3)2+2X↑+4H2O,则X为_____________ ;用装置A来收集NO气体,正确的操作步骤是:_________________

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】工业制备氯化铜时,将浓盐酸用蒸气加热至80℃左右,慢慢加入粗CuO粉末(含杂质Fe2O3、FeO),充分搅拌,使之溶解,得一强酸性的混合溶液,现欲从该混合溶液中制备纯净的CuCl2溶液,采用以下步骤:
参考数据:pH≥9.6时,Fe2+完全水解成Fe(OH)2;pH≥6.4时,Cu2+完全水解成Cu(OH)2;pH≥3.7时,Fe3+完全水解成Fe(OH)3。
请回答以下问题:
(1)第一步除去Fe2+,能否直接调整pH=9.6,将Fe2+沉淀除去?___ ,理由是___ 。
(2)有人用强氧化剂NaClO将Fe2+氧化为Fe3+:
①加入NaClO后,溶液的pH变化是____ 。(填序号)
A.一定增大 B.一定减小 C.可能增大 D.可能减小
②你认为用NaClO作氧化剂是否妥当?___ ,理由是___ 。
③现有下列几种常用的氧化剂,可用于除去混合溶液中Fe2+的有___ (多选)。
A.浓HNO3 B.KMnO4 C.Cl2 D.O2 E.H2O2
(3)除去溶液中的Fe3+的方法是调整溶液的pH=3.7,现有下列试剂均可以使强酸性溶液的pH调整到3.7,可选用的有___ (多选)。
A.NaOH B.氨水 C.Cu2(OH)2CO3 D.Na2CO3 E.CuO F.Cu(OH)2
参考数据:pH≥9.6时,Fe2+完全水解成Fe(OH)2;pH≥6.4时,Cu2+完全水解成Cu(OH)2;pH≥3.7时,Fe3+完全水解成Fe(OH)3。
请回答以下问题:
(1)第一步除去Fe2+,能否直接调整pH=9.6,将Fe2+沉淀除去?
(2)有人用强氧化剂NaClO将Fe2+氧化为Fe3+:
①加入NaClO后,溶液的pH变化是
A.一定增大 B.一定减小 C.可能增大 D.可能减小
②你认为用NaClO作氧化剂是否妥当?
③现有下列几种常用的氧化剂,可用于除去混合溶液中Fe2+的有
A.浓HNO3 B.KMnO4 C.Cl2 D.O2 E.H2O2
(3)除去溶液中的Fe3+的方法是调整溶液的pH=3.7,现有下列试剂均可以使强酸性溶液的pH调整到3.7,可选用的有
A.NaOH B.氨水 C.Cu2(OH)2CO3 D.Na2CO3 E.CuO F.Cu(OH)2
您最近一年使用:0次



