下列物质A~F是我们熟悉的单质或化合物,其中A、B均是常见的金属;E在常温下是黄绿色气体;在适当的条件下,它们之间可以发生如下图所示的转化。

试回答下列问题:
(1)写出无色溶液中溶质的化学式:___________ ;写出E的电子式_________________ 。
(2)写出C到白色沉淀的化学方程式是_________________________ 。
(3)反应F→D的离子方程式是________________________________ 。

试回答下列问题:
(1)写出无色溶液中溶质的化学式:
(2)写出C到白色沉淀的化学方程式是
(3)反应F→D的离子方程式是
更新时间:2016-12-09 09:21:33
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】X、Y、Z、W是元素周期表前四周期中的四种常见元素,其相关信息如表:
(1)X简单氢化物的电子式是______ 。
(2)元素Y的基态原子的价层电子排布式为______ 。
(3)元素Z的原子最外层共有______ 种不同运动状态的电子。
(4)元素Y与元素Z相比,非金属性较强的是______ (用元素符号表示),下列表述中能证明这一事实的是______ (填字母)。
A.Y的单质常温下呈固态,Z的单质常温下呈气态
B.等物质的量浓度的氢化物水溶液的酸性不同
C.Z的电负性大于Y
D.Z的气态氢化物比Y的气态氢化物稳定
E.在反应中,Y原子得电子数比Z原子得电子数多
F.Z元素最高价氧化物对应水化物的酸性比Y元素最高价氧化物对应水化物的酸性强
| 元素 | 相关信息 |
| X | X的基态原子核外3个能级上有电子,且最高能级是半充满状态 |
| Y | 第三周期元素,它的单质是良好的半导体材料 |
| Z | Z和Y同周期,Z是该周期中原子半径最小的主族元素 |
| W | W的一种核素的质量数为63,中子数为34 |
(2)元素Y的基态原子的价层电子排布式为
(3)元素Z的原子最外层共有
(4)元素Y与元素Z相比,非金属性较强的是
A.Y的单质常温下呈固态,Z的单质常温下呈气态
B.等物质的量浓度的氢化物水溶液的酸性不同
C.Z的电负性大于Y
D.Z的气态氢化物比Y的气态氢化物稳定
E.在反应中,Y原子得电子数比Z原子得电子数多
F.Z元素最高价氧化物对应水化物的酸性比Y元素最高价氧化物对应水化物的酸性强
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】Ⅰ.使用正确的化学用语填空。
(1)写出下列物质的电子式:
氮气___________ ;过氧化钠___________ ;四氯化碳___________ 。
(2)写出下列物质的结构式:
二氧化碳___________ ;过氧化氢___________ ;次氯酸___________ 。
Ⅱ.正确比较下列各组对应关系。
(3)已知短周期元素的四种离子A2+、B+、C3-、D-具有相同的电子层结构,则这四种元素:
①原子序数由大到小的顺序:___________ 。
②原子半径由大到小的顺序:___________ 。
③离子半径由大到小的顺序:___________ 。
(4)比较下列微粒半径大小,用“>”或“<”填空。
①F___________ Cl- ②Fe2+___________ Fe3+ ③O2-___________ Mg2+。
(1)写出下列物质的电子式:
氮气
(2)写出下列物质的结构式:
二氧化碳
Ⅱ.正确比较下列各组对应关系。
(3)已知短周期元素的四种离子A2+、B+、C3-、D-具有相同的电子层结构,则这四种元素:
①原子序数由大到小的顺序:
②原子半径由大到小的顺序:
③离子半径由大到小的顺序:
(4)比较下列微粒半径大小,用“>”或“<”填空。
①F
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】有A、B、C、D四种元素,已知A元素原子的K层和M层电子数相同;B元素原子的L层比K层电子数多5个;C元素的+3价阳离子和氖原子具有相同的电子数;D元素的最外层电子数是次外层电子数的3倍。
(1)写出元素符号:A_______ ,D_______ 。
(2)A的原子结构示意图_______ ,B的离子结构示意图_______ ,C的离子结构示意图_______ 。
(3)C原子的电子式_______ 。
(4)A和B元素组成的物质的化学式为_______ ,它是由_______ (选填“原子”、“离子”或“分子”)构成的物质。
(5)由C和D可组成CD 离子,一个CD
离子,一个CD 离子所带电子数为
离子所带电子数为_______ 。
(1)写出元素符号:A
(2)A的原子结构示意图
(3)C原子的电子式
(4)A和B元素组成的物质的化学式为
(5)由C和D可组成CD
 离子,一个CD
离子,一个CD 离子所带电子数为
离子所带电子数为
您最近一年使用:0次
【推荐1】电子工业常用过量的 FeCl3 溶液腐蚀绝缘板上的铜箔来制造电路板。利用腐蚀废液 可制铁红,过程如图:
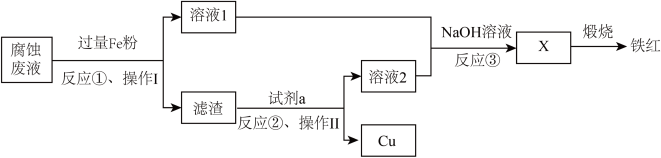
(1)反应①的离子方程式有___________ 。
(2)试剂 a 可以是___________。
(3)操作Ⅱ为___________ 。
(4)检验溶液 1 中是否含有 Fe3+ 的试剂是___________ 。
(5)经检验铁红中有 Fe3O4,取 100 g 产品,用足量稀硫酸溶解,逐滴加入 0.100 mol·L-1高锰酸钾溶液 40.0 mL 至恰好反应完全,反应的离子方程式为___________ , 则 Fe3O4 的物质的量为___________ mol。

(1)反应①的离子方程式有
(2)试剂 a 可以是___________。
| A.HCl | B.H2SO4 | C.KOH 溶液 | D.Na2CO3 溶液 |
(3)操作Ⅱ为
(4)检验溶液 1 中是否含有 Fe3+ 的试剂是
(5)经检验铁红中有 Fe3O4,取 100 g 产品,用足量稀硫酸溶解,逐滴加入 0.100 mol·L-1高锰酸钾溶液 40.0 mL 至恰好反应完全,反应的离子方程式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】铜和三氧化二铁在工农业生产中用途广泛,用黄铜矿(主要成分为CuFeS2,其中Cu为+2价、Fe为+2价)制取铜和三氧化二铁的工艺流程如图所示

(1)将黄铜矿粉碎的目的是___________ 。
(2)高温焙烧时发生的反应是CuFeS2+O2 SO2+FeS+Cu,该反应中,还原产物是
SO2+FeS+Cu,该反应中,还原产物是___________ ;1molO2参加反应时,反应中转移电子___________ mol。
(3)滤液A中含有FeCl2,向滤液A通入Cl2的离子方程式为___________ 。
(4)向溶液B中通入NH3后发生反应的离子方程式为___________ 。
(5)操作b后检验滤渣已经洗涤干净的实验操作为___________ 。
(6)工业上用生物法处理H2S的原理为(硫杆菌有较强的活性作催化剂):H2S+Fe2(SO4)3=S↓+2FeSO4+H2SO4;4FeSO4+O2+2H2SO4=2Fe2(SO4)3+2H2O,由图甲和图乙判断使用硫杆菌的最佳条件为___________ ,若反应温度过高,反应速率下降,其原因是___________ 。


(1)将黄铜矿粉碎的目的是
(2)高温焙烧时发生的反应是CuFeS2+O2
 SO2+FeS+Cu,该反应中,还原产物是
SO2+FeS+Cu,该反应中,还原产物是(3)滤液A中含有FeCl2,向滤液A通入Cl2的离子方程式为
(4)向溶液B中通入NH3后发生反应的离子方程式为
(5)操作b后检验滤渣已经洗涤干净的实验操作为
(6)工业上用生物法处理H2S的原理为(硫杆菌有较强的活性作催化剂):H2S+Fe2(SO4)3=S↓+2FeSO4+H2SO4;4FeSO4+O2+2H2SO4=2Fe2(SO4)3+2H2O,由图甲和图乙判断使用硫杆菌的最佳条件为

您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】综合利用粉煤灰既有利于环境保护,又有利于资源节约。某种粉煤灰(主要Al2O3、Fe2O3、CaCO3等)的铝、铁分离工艺流程如下:
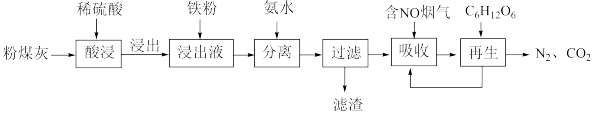
(1)①“酸浸”时Fe2O3发生反应的化学方程式_______ 。
②提高浸出率的措施有_______ (写出一点)。
③当硫酸浓度大于9.2 mol·L-1时,铝铁的浸出率下降。可能原因是_______ 。
(2)“分离”过程中加入氨水调pH的范围是_______ 。(已知:部分氢氧化物开始沉淀和沉淀完全的pH如下表所示)
若浸出液不加铁粉直接与氨水混合,铝、铁元素分离效果较差的原因是_______ 。
(3)①“分离”后所得FeSO4溶液可用于烟气中NO的吸收,生成[Fe(NO)2]2+,其反应的离子方程式为_______ 。
②“再生”过程中,[Fe(NO)2]2+在微生物的作用下与C6H12O6发生反应,得到CO2与N2的质量之比为_______ 。

(1)①“酸浸”时Fe2O3发生反应的化学方程式
②提高浸出率的措施有
③当硫酸浓度大于9.2 mol·L-1时,铝铁的浸出率下降。可能原因是
(2)“分离”过程中加入氨水调pH的范围是
| 氢氧化物 | 氢氧化铁 | 氢氧化铝 | 氢氧化亚铁 |
| 开始沉淀的pH | 1.5 | 3.2 | 7.1 |
| 沉淀完全的pH | 3.1 | 4.9 | 8.9 |
(3)①“分离”后所得FeSO4溶液可用于烟气中NO的吸收,生成[Fe(NO)2]2+,其反应的离子方程式为
②“再生”过程中,[Fe(NO)2]2+在微生物的作用下与C6H12O6发生反应,得到CO2与N2的质量之比为
您最近一年使用:0次
【推荐1】某混合物A含有KAl(SO4)2、Al2O3和Fe2O3,在一定条件下可实现如图所示的物质间的变化:

据此回答下列问题:
(1)I、Ⅱ、Ⅲ、Ⅳ四步中对于溶液和沉淀的分离采取的方法是_______ 。
(2)根据上述框图反应关系,写出溶液E主要溶质的化学式_______ ,固体D的化学式_______ 。
(3)写出④的化学方程式_______ 。
(4)写出③的离子方程式_______ 。
(5)向沉淀D中加入适量盐酸,设计实验检验所得溶液中的溶质:_______ 。
(6)写出Al2O3在工业上的一种主要用途:_______ 。

据此回答下列问题:
(1)I、Ⅱ、Ⅲ、Ⅳ四步中对于溶液和沉淀的分离采取的方法是
(2)根据上述框图反应关系,写出溶液E主要溶质的化学式
(3)写出④的化学方程式
(4)写出③的离子方程式
(5)向沉淀D中加入适量盐酸,设计实验检验所得溶液中的溶质:
(6)写出Al2O3在工业上的一种主要用途:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】A、B、C、D表示中学化学中的四种常见物质,其中A、B、C均含有同一种元素,在一定条件下相互转化关系如图(部分反应中的水已略去)。

(1)若A为强碱溶液,其焰色反应显黄色,C为厨房中用品,请回答下列问题:
①D的化学式是_________ 。
②反应III的离子方程式是______________________ 。
③现有B和C的固体混合物a g,加热至质量不再改变时剩余固体b g,则B的质量分数为_______________ 。
(2)若A、D均为单质,且A为黄绿色气体,D的一种红棕色氧化物常用作颜料,则:
①反应III的离子方程式是___________________________ 。
②取少许C溶液于试管中,滴入NaOH溶液并振荡,发生反应的化学方程式为:______________________________ ,________________________________ 。
③检验C溶液中金属阳离子的操作是________________________________________ 。

(1)若A为强碱溶液,其焰色反应显黄色,C为厨房中用品,请回答下列问题:
①D的化学式是
②反应III的离子方程式是
③现有B和C的固体混合物a g,加热至质量不再改变时剩余固体b g,则B的质量分数为
(2)若A、D均为单质,且A为黄绿色气体,D的一种红棕色氧化物常用作颜料,则:
①反应III的离子方程式是
②取少许C溶液于试管中,滴入NaOH溶液并振荡,发生反应的化学方程式为:
③检验C溶液中金属阳离子的操作是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】以硫铁矿(FeS2的质量分数为60%)为原料制备氯化铁晶体(FeCl3·6H2O,270.5g·moˉ1)的工艺流程如图所示。

请回答下列问题:
(1)为加快焙烧反应的化学反应速率,可采取的措施为_____ 、_____ 。(任写两条)
(2)焙烧后得到的Fe2O3在酸溶过程中发生反应的离子方程式为________ 。
(3)过滤操作用到的玻璃仪器有烧杯、_______ 、______ 。
(4)焙烧过程中产生的SO2可用过量的氨水进行吸收,所得溶液中溶质的名称为_______ 。
(5)先向氯化铁溶液中加适量盐酸的目的是______ ,再______ 、______ 、过滤、洗涤,最终得到氯化铁晶体。
(6)若取1kg硫铁矿经过上述流程(铁元素在整个流程中损失率为4%),则可得氯化铁晶体的质量为_______ (保留一位小数)kg。

请回答下列问题:
(1)为加快焙烧反应的化学反应速率,可采取的措施为
(2)焙烧后得到的Fe2O3在酸溶过程中发生反应的离子方程式为
(3)过滤操作用到的玻璃仪器有烧杯、
(4)焙烧过程中产生的SO2可用过量的氨水进行吸收,所得溶液中溶质的名称为
(5)先向氯化铁溶液中加适量盐酸的目的是
(6)若取1kg硫铁矿经过上述流程(铁元素在整个流程中损失率为4%),则可得氯化铁晶体的质量为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】由单质A与化合物B两种粉末组成的混合物, 在一定条件下可按下图所示发生转化:

请回答:
(1)A的化学式_______ ;B的俗称_______ ;J的化学式_______
(2)反应③的离子方程式__________________________________
(3)反应②的离子方程式_______________________________________________
(4)沉淀H变沉淀I的化学方程式______________________________________
(5)如何检验溶液F中的阳离子________________________________

请回答:
(1)A的化学式
(2)反应③的离子方程式
(3)反应②的离子方程式
(4)沉淀H变沉淀I的化学方程式
(5)如何检验溶液F中的阳离子
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】两种常见的金属单质A、B有如图所示的转化关系(部分产物省略)。
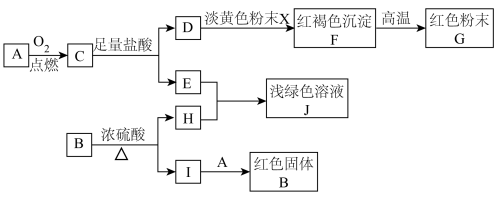
回答下列问题:
(1)淡黄色粉末X是_______ (填化学式,下同);H是_______ 。
(2)写出C和盐酸反应的离子方程式:_______ 。
(3)G的用途有_______ (答一条);写出E和H反应的离子方程式:_______ 。
(4)将E饱和溶液滴入沸水中得到红褐色液体,当________ (填实验操作和现象)时,说明该红褐色液体的分散质颗粒直径在1~100nm。
(5)B和浓硫酸反应一段时间后停止,添加某物质Y,导致B继续溶解。Y可能是_______ (填化学式)。
(6)工业上,利用B制备I除本题方法外,还有多种方法。写一种环保方法:________ 。

回答下列问题:
(1)淡黄色粉末X是
(2)写出C和盐酸反应的离子方程式:
(3)G的用途有
(4)将E饱和溶液滴入沸水中得到红褐色液体,当
(5)B和浓硫酸反应一段时间后停止,添加某物质Y,导致B继续溶解。Y可能是
(6)工业上,利用B制备I除本题方法外,还有多种方法。写一种环保方法:
您最近一年使用:0次




