某酸性工业废水中含有K2Cr2O7。光照下,草酸(H2C2O4)能将其中的Cr2O72-转化为Cr3+。某课题组研究发现,少量铁明矾[Al2Fe(SO4)4·24H2O]即可对该反应起催化作用。为进一步研究有关因素对该反应速率的影响,探究如下:
(1)在25 ℃下,控制光照强度、废水样品初始浓度和催化剂用量相同,调节不同的初始pH和一定浓度草酸溶液用量,做对比实验,完成以下实验设计表(表中不要留空格)。
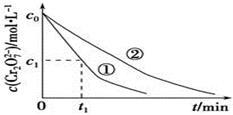
测得实验①和②溶液中的Cr2O72—浓度随时间变化关系如图所示。
(2)上述反应后草酸被氧化的离子方程式为____________________
(3)实验①和②的结果表明________________ ;实验①中0~t1时间段反应速率v(Cr3+)=________________ mol·L-1·min-1(用代数式表示)。
(4)该课题组对铁明矾[Al2Fe(SO4)4·24H2O]中起催化作用的成分提出如下假设,请你完成假设二和假设三:
假设一:Fe2+起催化作用:
假设二:____________________ ;
假设三:____________________ ;
……
(5)请你设计实验验证上述假设一,完成下表中内容。
(除了上述实验提供的试剂外,可供选择的药品有K2SO4、FeSO4、K2SO4·Al2(SO4)3·24H2O、Al2(SO4)3等。溶液中Cr2O72—的浓度可用仪器测定)
________________________ 。
(1)在25 ℃下,控制光照强度、废水样品初始浓度和催化剂用量相同,调节不同的初始pH和一定浓度草酸溶液用量,做对比实验,完成以下实验设计表(表中不要留空格)。
| 实验编号 | 初始pH | 废水样品体积/mL | 草酸溶液体积/mL | 蒸馏水体积/mL |
| ① | 4 | 60 | 10 | 30 |
| ② | 5 | 60 | 10 | 30 |
| ③ | 5 | 60 |

测得实验①和②溶液中的Cr2O72—浓度随时间变化关系如图所示。
(2)上述反应后草酸被氧化的离子方程式为
(3)实验①和②的结果表明
(4)该课题组对铁明矾[Al2Fe(SO4)4·24H2O]中起催化作用的成分提出如下假设,请你完成假设二和假设三:
假设一:Fe2+起催化作用:
假设二:
假设三:
……
(5)请你设计实验验证上述假设一,完成下表中内容。
(除了上述实验提供的试剂外,可供选择的药品有K2SO4、FeSO4、K2SO4·Al2(SO4)3·24H2O、Al2(SO4)3等。溶液中Cr2O72—的浓度可用仪器测定)
| 实验方案(不要求写具体操作过程) | 预期实验结果和结论 |
更新时间:2016-12-09 09:25:13
|
相似题推荐
解答题-实验探究题
|
较难
(0.4)
【推荐1】化学实验是化学学科学习、探究的基础.
(1)下列描述错误的是___________
a.为了防止试剂瓶内的试剂被污染,取用后多余的试剂一定都不能放回原试剂瓶
b.滴定管、容量瓶、分液漏斗在使用时都需要检漏
c.海带中碘的提取时需要对干海带进行灼烧,此时需要用到的仪器有玻璃棒、燃烧匙、泥三角、三脚架、酒精灯
d.检验Na2SO3固体是否被氧化:取少量固体溶于水,加入Ba(NO3)2溶液,产生白色沉淀,滴加稀盐酸,观察白色沉淀是否溶解
e.海带中碘的提取时,对碘水中的碘进行萃取可采用裂化汽油、苯、四氯化碳、无水酒精等有机溶剂
(2)某溶液中可能存在Br-、CO32-、SO32-、I-、A13+、Mg2+、Na+等7种离子中的某几种。现取该溶液进行实验,得到如下现象:
①向溶液中滴加足量氯水后,溶液变橙色,且有无色气泡冒出;
②向所得橙色溶液中加入足量BaCl2溶液,有白色沉淀生成,加入稀盐酸沉淀不溶解.
③向所得溶液中继续滴加淀粉溶液,溶液不变蓝色.据此可以推断:该溶液肯定存在的离子是:___________
(3)为了进一步研究硫酸铜的量对氢气生成速率的影响,该同学设计了如下一系列实验.将表中所给的混合溶液分别加入到6个盛有过量Zn粒的反应瓶中,收集产生的气体,记录获得相同体积的气体所需时间。
①请完成此实验设计,其中:V1="___________ " ,V6=" ___________ " ,V9= ___________ ;
②该同学最后得出的结论为:当加入少量CuSO4溶液时,生成氢气的速率会大大提高,但当加入的CuSO4溶液超过一定量时,生成氢气的速率反而会下降.请分析氢气生成速率下降的主要原因:___________ 。
(1)下列描述错误的是
a.为了防止试剂瓶内的试剂被污染,取用后多余的试剂一定都不能放回原试剂瓶
b.滴定管、容量瓶、分液漏斗在使用时都需要检漏
c.海带中碘的提取时需要对干海带进行灼烧,此时需要用到的仪器有玻璃棒、燃烧匙、泥三角、三脚架、酒精灯
d.检验Na2SO3固体是否被氧化:取少量固体溶于水,加入Ba(NO3)2溶液,产生白色沉淀,滴加稀盐酸,观察白色沉淀是否溶解
e.海带中碘的提取时,对碘水中的碘进行萃取可采用裂化汽油、苯、四氯化碳、无水酒精等有机溶剂
(2)某溶液中可能存在Br-、CO32-、SO32-、I-、A13+、Mg2+、Na+等7种离子中的某几种。现取该溶液进行实验,得到如下现象:
①向溶液中滴加足量氯水后,溶液变橙色,且有无色气泡冒出;
②向所得橙色溶液中加入足量BaCl2溶液,有白色沉淀生成,加入稀盐酸沉淀不溶解.
③向所得溶液中继续滴加淀粉溶液,溶液不变蓝色.据此可以推断:该溶液肯定存在的离子是:
(3)为了进一步研究硫酸铜的量对氢气生成速率的影响,该同学设计了如下一系列实验.将表中所给的混合溶液分别加入到6个盛有过量Zn粒的反应瓶中,收集产生的气体,记录获得相同体积的气体所需时间。
| 实验 混合溶液 | A | B | C | D | E | F |
| 4mol•L-1 H2SO4/mL | 30 | V1 | V2 | V3 | V4 | V5 |
| 饱和CuSO4溶液/mL | 0 | 0.5 | 2.5 | 5 | V6 | 20 |
| H2O/mL | V7 | V8 | V9 | V10 | 10 | 0 |
①请完成此实验设计,其中:V1="
②该同学最后得出的结论为:当加入少量CuSO4溶液时,生成氢气的速率会大大提高,但当加入的CuSO4溶液超过一定量时,生成氢气的速率反而会下降.请分析氢气生成速率下降的主要原因:
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
【推荐2】目前世界各国都规划了碳达峰、碳中和的时间节点,以CO2为碳源,将其转化为能源物质。选择性加氢合成CH3OH,合成过程中发生下列反应:
反应i:CO2(g)+H2(g)⇌CO(g)+H2O(g) ∆H1=-akJ‧mol-1
反应ii:CO(g)+2H2(g)⇌CH3OH(g) ∆H2
反应iii:CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g) ∆H3=-bkJ‧mol-1
回答下列问题:
(1)根据盖斯定律,∆H2=。___________ kJ‧mol-1(用含a,b的代数式表示)。
(2)在一绝热、刚性容器中,只发生反应iii。下列说法表明反应已达到平衡状态的是___________(填序号)。
(3)中科院兰州化物所用Fe3(CO)12/ZSM-5催化CO2加氢合成低碳烯烃反应,反应过程如图所示。催化剂中添加助剂Na、K、Cu(也起催化作用)后可改变反应的选择性。

在其他条件相同时,添加不同助剂,经过相同时间后测得CO2转化率和各产物的物质的量分数如下表所示:
欲提高单位时间内乙烯的产量,在Fe3(CO)12/ZSM-5中添加Na助剂是否效果最好?_________ (填“是”或“否”),请叙述原因:___________ 。
(4)合成二甲醚反应:2CO2(g)+6H2(g)⇌CH3OCH3(g)+3H2O(g) ∆H=-74kJ‧mol-1。该反应正反应的活化能___________ (填“>”“<”或“=”) 逆反应的活化能。
(5)在一定条件下,将1molCO和2molH2充入IL恒容密闭容器中:发生反应:CO(g)+2H2(g)⇌CH3OH(g) ∆H2,相同时间(2min)内测得CO的转化率与温度的对应关系如图所示:
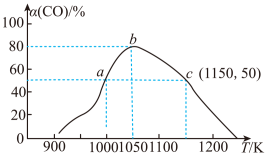
①温度为1000K时,反应开始至2min时,v(H2)=___________ mol‧L-1‧min-1
②CO的转化率随温度的升高先增大后变小的原因是___________ 。
(6)为实现CO2资源化利用,通过光电转化原理以CO2为原料制备甲酸产品(如图所示)。
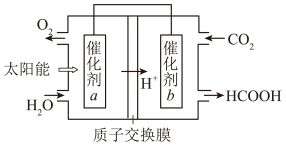
①光电转化过程中,阴极反应式为___________
②催化剂b附近生成lmolHCOOH时,标准状况下催化剂a附近理论上产生______ L气体。
反应i:CO2(g)+H2(g)⇌CO(g)+H2O(g) ∆H1=-akJ‧mol-1
反应ii:CO(g)+2H2(g)⇌CH3OH(g) ∆H2
反应iii:CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g) ∆H3=-bkJ‧mol-1
回答下列问题:
(1)根据盖斯定律,∆H2=。
(2)在一绝热、刚性容器中,只发生反应iii。下列说法表明反应已达到平衡状态的是___________(填序号)。
| A.混合气体的总物质的量不再变化 | B.n(CH3OH):n(H2O)=1:1 |
| C.v正(CH3OH)=3v逆(H2) | D.该反应的K不再变化 |

在其他条件相同时,添加不同助剂,经过相同时间后测得CO2转化率和各产物的物质的量分数如下表所示:
| 助剂 | CO2转化率(%) | 各产物在所有产物中的占比 | ||
| C2H4 | C3H6 | 其他 | ||
| Na | 42.5 | 35.9 | 39.6 | 24.5 |
| K | 27.2 | 75.6 | 22.8 | 1.6 |
| Cu | 9.8 | 80.7 | 12.5 | 6.8 |
(4)合成二甲醚反应:2CO2(g)+6H2(g)⇌CH3OCH3(g)+3H2O(g) ∆H=-74kJ‧mol-1。该反应正反应的活化能
(5)在一定条件下,将1molCO和2molH2充入IL恒容密闭容器中:发生反应:CO(g)+2H2(g)⇌CH3OH(g) ∆H2,相同时间(2min)内测得CO的转化率与温度的对应关系如图所示:

①温度为1000K时,反应开始至2min时,v(H2)=
②CO的转化率随温度的升高先增大后变小的原因是
(6)为实现CO2资源化利用,通过光电转化原理以CO2为原料制备甲酸产品(如图所示)。

①光电转化过程中,阴极反应式为
②催化剂b附近生成lmolHCOOH时,标准状况下催化剂a附近理论上产生
您最近一年使用:0次
【推荐3】将天然气(主要成分为CH4)中的CO2、H2S资源化转化在能源利用、环境保护等方面意义重大。
(1)CO2转化为CO、H2S转化为S的反应如下:
i.2CO2(g)=2CO(g)+O2(g) △H1=+566kJ/mol
ii.2H2S(g)+O2(g)=2H2O(l)+2S(s) △H2=﹣530kJ/mol
iii.CO2、H2S转化生成CO、S等物质的热化学方程式是___________ 。
(2)CO2性质稳定,是一种“惰性”分子。对于反应ⅲ,通过设计合适的催化剂可以降低______ ,提高反应速率。
a.活化能 b.△H c.平衡常数
(3)我国科学家研制新型催化剂,设计协同转化装置实现反应ⅲ,工作原理如下所示。
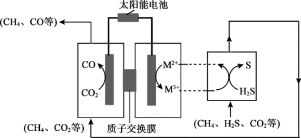
【方案1】若M3+/M2+=Fe3+/Fe2+
①所含Fe3+、Fe2+的溶液需为较强的酸性,原因是___________ 。
②结合反应式说明生成S、CO的原理:___________ 。
【方案2】若M3+/M2+=EDTA-Fe3+/EDTA-Fe2+(配合物)
已知:电解效率η的定义:
③测得η(EDTA-Fe3+)≈100%,η(CO)≈80%。阴极放电的物质有___________ 。
④为进一步确认CO2、H2S能协同转化,对CO的来源分析如下:
来源1:CO2通过电极反应产生CO
来源2:电解质(含碳元素)等物质发生降解,产生CO
设计实验探究,证实来源2不成立。实验方案是___________ 。
结论:方案2明显优于方案1,该研究成果为天然气的净化、资源化转化提供了工业化解决思路。
(1)CO2转化为CO、H2S转化为S的反应如下:
i.2CO2(g)=2CO(g)+O2(g) △H1=+566kJ/mol
ii.2H2S(g)+O2(g)=2H2O(l)+2S(s) △H2=﹣530kJ/mol
iii.CO2、H2S转化生成CO、S等物质的热化学方程式是
(2)CO2性质稳定,是一种“惰性”分子。对于反应ⅲ,通过设计合适的催化剂可以降低
a.活化能 b.△H c.平衡常数
(3)我国科学家研制新型催化剂,设计协同转化装置实现反应ⅲ,工作原理如下所示。

【方案1】若M3+/M2+=Fe3+/Fe2+
①所含Fe3+、Fe2+的溶液需为较强的酸性,原因是
②结合反应式说明生成S、CO的原理:
【方案2】若M3+/M2+=EDTA-Fe3+/EDTA-Fe2+(配合物)
已知:电解效率η的定义:

③测得η(EDTA-Fe3+)≈100%,η(CO)≈80%。阴极放电的物质有
④为进一步确认CO2、H2S能协同转化,对CO的来源分析如下:
来源1:CO2通过电极反应产生CO
来源2:电解质(含碳元素)等物质发生降解,产生CO
设计实验探究,证实来源2不成立。实验方案是
结论:方案2明显优于方案1,该研究成果为天然气的净化、资源化转化提供了工业化解决思路。
您最近一年使用:0次
【推荐1】我国对世界郑重承诺:2030年前实现碳达峰,2060年前实现碳中和,而研发CO2的碳捕捉和碳利用技术则是关键。
(1)大气中的CO2主要来自于煤、石油及其他含碳化合物的燃烧,CH4与CO2重整是CO2利用的研究热点之一。该重整反应体系主要涉及以下反应:
①CH4(g) C(s)+2H2(g) ΔH1=akJ•mol-1
C(s)+2H2(g) ΔH1=akJ•mol-1
②CO2(g)+H2(g) CO(g)+H2O(g) ΔH2=bkJ•mol-1
CO(g)+H2O(g) ΔH2=bkJ•mol-1
③2CO(g) CO2(g)+C(s) ΔH3=ckJ•mol-1
CO2(g)+C(s) ΔH3=ckJ•mol-1
反应CH4(g)+CO2(g) 2CO(g)+2H2(g)的ΔH=
2CO(g)+2H2(g)的ΔH=_____ kJ•mol-1。
(2)多晶Cu是目前唯一被实验证实能高效催化CO2还原为烃类(如C2H4)的金属。如图所示,电解装置中分别以多晶Cu和Pt为电极材料,用阴离子交换膜分隔开阴、阳极室,反应前后KHCO3浓度基本保持不变,温度控制在10℃左右。生成C2H4的电极反应式为_____ 。

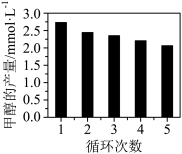
(3)CO2与H2反应如果用Co/C作为催化剂,可以得到含有少量甲酸的甲醇。为了研究催化剂的催化效率,将Co/C催化剂循环使用,相同条件下,随着循环使用次数的增加,甲醇的产量如图所示,试推测甲醇产量变化的可能原因_____ 。
(4)常温下,以NaOH溶液作CO2捕捉剂不仅可以降低碳排放,而且可得到重要的化工产品Na2CO3。用1LNa2CO3溶液将2.33gBaSO4固体全都转化为BaCO3,再过滤,所用的Na2CO3溶液的物质的量浓度至少为_____ mol•L-1。[已知:常温下Ksp(BaSO4)=1×10-11,Ksp(BaCO3)=1×10-10;忽略溶液体积变化]
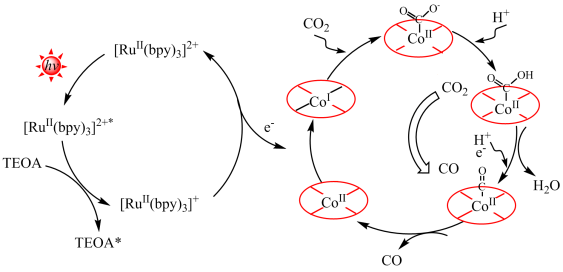
(5)某课题组通过温和的自光刻技术制备出富含氧空位的Co(CO3)0.5(OH)•0.11H2O纳米线(用CoII表示),测试结果表明,该CoII在可见光下具有优异的光催化CO2还原活性。分析表明,该CO2还原催化机理为典型的CoII/CoI反应路径(如图)。首先,光敏剂([Ru(bpy)3]2+)通过可见光照射被激发到激发态([Ru(bpy)3]2+*),随后([Ru(bpy)3]2+*)被TEOA淬灭得到([Ru(bpy)3]+)还原物种,该还原物种将向CoII供激发电子将CoII还原为CoI,_____ 。(结合图示,描述CO2还原为CO的过程)
(1)大气中的CO2主要来自于煤、石油及其他含碳化合物的燃烧,CH4与CO2重整是CO2利用的研究热点之一。该重整反应体系主要涉及以下反应:
①CH4(g)
 C(s)+2H2(g) ΔH1=akJ•mol-1
C(s)+2H2(g) ΔH1=akJ•mol-1②CO2(g)+H2(g)
 CO(g)+H2O(g) ΔH2=bkJ•mol-1
CO(g)+H2O(g) ΔH2=bkJ•mol-1③2CO(g)
 CO2(g)+C(s) ΔH3=ckJ•mol-1
CO2(g)+C(s) ΔH3=ckJ•mol-1反应CH4(g)+CO2(g)
 2CO(g)+2H2(g)的ΔH=
2CO(g)+2H2(g)的ΔH=(2)多晶Cu是目前唯一被实验证实能高效催化CO2还原为烃类(如C2H4)的金属。如图所示,电解装置中分别以多晶Cu和Pt为电极材料,用阴离子交换膜分隔开阴、阳极室,反应前后KHCO3浓度基本保持不变,温度控制在10℃左右。生成C2H4的电极反应式为

(3)CO2与H2反应如果用Co/C作为催化剂,可以得到含有少量甲酸的甲醇。为了研究催化剂的催化效率,将Co/C催化剂循环使用,相同条件下,随着循环使用次数的增加,甲醇的产量如图所示,试推测甲醇产量变化的可能原因

(4)常温下,以NaOH溶液作CO2捕捉剂不仅可以降低碳排放,而且可得到重要的化工产品Na2CO3。用1LNa2CO3溶液将2.33gBaSO4固体全都转化为BaCO3,再过滤,所用的Na2CO3溶液的物质的量浓度至少为
(5)某课题组通过温和的自光刻技术制备出富含氧空位的Co(CO3)0.5(OH)•0.11H2O纳米线(用CoII表示),测试结果表明,该CoII在可见光下具有优异的光催化CO2还原活性。分析表明,该CO2还原催化机理为典型的CoII/CoI反应路径(如图)。首先,光敏剂([Ru(bpy)3]2+)通过可见光照射被激发到激发态([Ru(bpy)3]2+*),随后([Ru(bpy)3]2+*)被TEOA淬灭得到([Ru(bpy)3]+)还原物种,该还原物种将向CoII供激发电子将CoII还原为CoI,

您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
解题方法
【推荐2】研究化学反应机理,就是研究化学反应的本质,是目前化学研究的重要方向。
把 转化为HCOOH是降碳并生产化工原料的常用方法,有关反应如下:
转化为HCOOH是降碳并生产化工原料的常用方法,有关反应如下:
①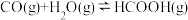

②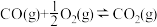
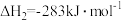
③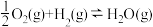
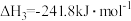
(1)反应: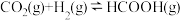 中
中
___________ 
(2)温度为T1℃时,将等物质的量的 和
和 充入体积为1L的密闭容器中发生反应:
充入体积为1L的密闭容器中发生反应: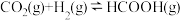 K=2。实验测得:
K=2。实验测得: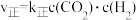 ,
, ,k正、k逆为速率常数。T1℃时,k逆=
,k正、k逆为速率常数。T1℃时,k逆=___________ (以k正表示)。
(3)当温度改变为T2℃时,k正=2.1k逆,则T2℃___________ T1℃(填“ ”或“
”或“ ”或“
”或“ ”),理由是
”),理由是___________ 。
(4)硫一碘循环分解水制氢主要涉及下列反应:
①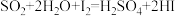
②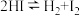
③
下列判断正确的是___________(填标号,下同)
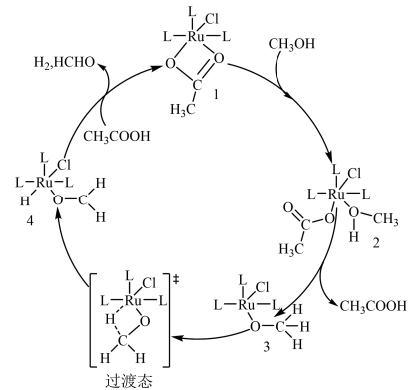
(5)钌(Ru)的配合物[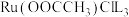 ](L是一个基团)可催化甲醇脱氢,反应过程如图所示。下列叙述错误的是___________。
](L是一个基团)可催化甲醇脱氢,反应过程如图所示。下列叙述错误的是___________。
把
 转化为HCOOH是降碳并生产化工原料的常用方法,有关反应如下:
转化为HCOOH是降碳并生产化工原料的常用方法,有关反应如下:①
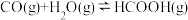

②
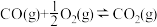
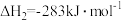
③
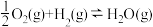
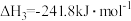
(1)反应:
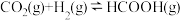 中
中

(2)温度为T1℃时,将等物质的量的
 和
和 充入体积为1L的密闭容器中发生反应:
充入体积为1L的密闭容器中发生反应: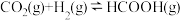 K=2。实验测得:
K=2。实验测得: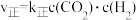 ,
, ,k正、k逆为速率常数。T1℃时,k逆=
,k正、k逆为速率常数。T1℃时,k逆=(3)当温度改变为T2℃时,k正=2.1k逆,则T2℃
 ”或“
”或“ ”或“
”或“ ”),理由是
”),理由是(4)硫一碘循环分解水制氢主要涉及下列反应:
①
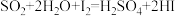
②
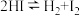
③

下列判断正确的是___________(填标号,下同)
| A.反应③易在常温下进行 | B.反应①中 氧化性比HI强 氧化性比HI强 |
C.循环过程中需补充 | D.循环过程中产生 的同时产生 的同时产生 |
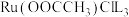 ](L是一个基团)可催化甲醇脱氢,反应过程如图所示。下列叙述错误的是___________。
](L是一个基团)可催化甲醇脱氢,反应过程如图所示。下列叙述错误的是___________。
A.2和4及 均是反应的中间产物 均是反应的中间产物 |
B.甲醇脱氢反应为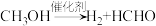 |
| C.反应过程中有极性键与非极性键的断裂与形成 |
D.增加 的量可以增加化学反应速率并提高产物产率 的量可以增加化学反应速率并提高产物产率 |
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
【推荐3】CO是一种重要的化工原料,主要用于制氢、甲醇等工业领域中。回答下列问题:
I.制氢气
450°C时,在10L体积不变的容器中投入2mol CO和2mol H2O, 发生如下反应:CO(g)+ H2O(g)⇌CO2(g)+H2(g) △H,当反应达平衡时,测得平衡常数为9.0。
已知:①2H2(g) + O2(g) = 2H2O(g) △H1= -483.6kJ·mol -1
②2CO(g) + O2(g) = 2CO2(g) △H2=-566.0kJ· mol-1
(1)△H=_______ kJ·mol-1。
(2)在450°C下反应达平衡时, CO的转化率为_______
(3)下列情况能说明该反应一定达平衡的是_______ (填标号)。
A.单位时间内断裂2NA个O—H键同时断裂NA个H—H键
B.c(CO):c(CO2)=1:1
C.CO的体积分数不再随时间改变
D.气体的平均摩尔质量不再随时间改变
(4)该反应的v-t图象如图1所示,若其他条件不变,只是在反应前加入催化剂,则其v-t图象如图2所示。

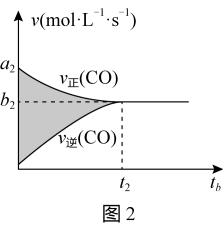
下列说法正确的是_______ (填正确答案标号),
①a1>a2②a1<a2③b1>b2④b1<b 2.⑤t1>t2⑥tl<t2⑦t1=t2
A.①③⑤ B.①③⑥ C.②④⑦ D.②④⑤
两图中阴影部分面积,图1_______ 图2(填“大于”“小于”或“等于”)。
II.制甲醇
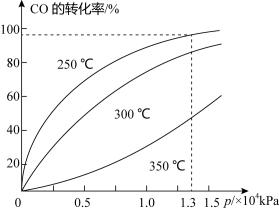
(5)合成甲醇的反应为:CO(g)+2H2(g)⇌CH3OH(g) △H ;在催化剂作用下,测得CO的平衡转化率与反应温度、压强关系如图所示,由图中数据可知,△H_______ 0(填“>"“<”或“=”),甲醇产率随着压强变化呈现图示规律的原因是_______ 。
I.制氢气
450°C时,在10L体积不变的容器中投入2mol CO和2mol H2O, 发生如下反应:CO(g)+ H2O(g)⇌CO2(g)+H2(g) △H,当反应达平衡时,测得平衡常数为9.0。
已知:①2H2(g) + O2(g) = 2H2O(g) △H1= -483.6kJ·mol -1
②2CO(g) + O2(g) = 2CO2(g) △H2=-566.0kJ· mol-1
(1)△H=
(2)在450°C下反应达平衡时, CO的转化率为
(3)下列情况能说明该反应一定达平衡的是
A.单位时间内断裂2NA个O—H键同时断裂NA个H—H键
B.c(CO):c(CO2)=1:1
C.CO的体积分数不再随时间改变
D.气体的平均摩尔质量不再随时间改变
(4)该反应的v-t图象如图1所示,若其他条件不变,只是在反应前加入催化剂,则其v-t图象如图2所示。


下列说法正确的是
①a1>a2②a1<a2③b1>b2④b1<b 2.⑤t1>t2⑥tl<t2⑦t1=t2
A.①③⑤ B.①③⑥ C.②④⑦ D.②④⑤
两图中阴影部分面积,图1
II.制甲醇
(5)合成甲醇的反应为:CO(g)+2H2(g)⇌CH3OH(g) △H ;在催化剂作用下,测得CO的平衡转化率与反应温度、压强关系如图所示,由图中数据可知,△H

您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
解题方法
【推荐1】利用废铝箔(主要成分为Al、少量的Fe、Si等)既可制取有机合成催化剂AlBr3又可制取净水剂硫酸铝晶体[A12(SO4)3•18H2O]。
I.实验室制取无色的无水AlBr3(熔点:97.5℃,沸点:263.3~265℃)可用如图所示装置,
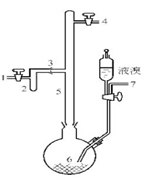
主要实验步骤如下:
步骤l.将铝箔剪碎,用CCl4浸泡片刻,干燥,然后投入到烧瓶6中。
步骤2.从导管口7导入氮气,同时打开导管口l和4放空,一段时间后关闭导管口7和1;导管口4接装有五氧化二磷的干燥管。
步骤3.从滴液漏斗滴入一定量的液溴于烧瓶6中,并保证烧瓶6中铝过剩。
步骤4.加热烧瓶6,回流一定时间。
步骤5.将氮气的流动方向改为从导管口4到导管口l。将装有五氧化二磷的干燥管与导管口1连接,将烧瓶6加热至270℃左右,使溴化铝蒸馏进入收集器2。
步骤6.蒸馏完毕时,在继续通入氮气的情况下,将收集器2从3处拆下,并立即封闭3处。
(1)步骤l中,铝箔用CCl4浸泡的目的是__ 。
(2)步骤2操作中,通氮气的目的是___ 。
(3)步骤3中,该实验要保证烧瓶中铝箔过剩,其目的是___ 。
(4)铝与液溴反应的化学方程式为___ 。
(5)步骤4依据何种现象判断可以停止回流操作___ 。
(6)步骤5需打开导管口l和4,并从4通入N2的目的是___ 。
II.某课外小组的同学拟用废铝箔制取硫酸铝晶体,已知铝的物种类别与溶液pH关系如图所示,实验中可选用的试剂:处理过的铝箔;2.0mol•L-1NaOH溶液:2.0 mol•L-1硫酸
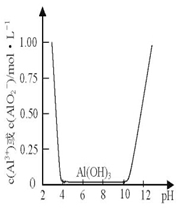
(7)由铝箔制备硫酸铝晶体的实验步骤依次为:
①称取一定质量的铝箔于烧杯中,分次加入2.0 mol•L-1NaOH溶液,加热至不再产生气泡为止。
②过滤 ③___ ;
④过滤、洗涤 ⑤___ ;⑥___ ;
⑦冷却结晶; ⑧过滤、洗涤、干燥。
I.实验室制取无色的无水AlBr3(熔点:97.5℃,沸点:263.3~265℃)可用如图所示装置,

主要实验步骤如下:
步骤l.将铝箔剪碎,用CCl4浸泡片刻,干燥,然后投入到烧瓶6中。
步骤2.从导管口7导入氮气,同时打开导管口l和4放空,一段时间后关闭导管口7和1;导管口4接装有五氧化二磷的干燥管。
步骤3.从滴液漏斗滴入一定量的液溴于烧瓶6中,并保证烧瓶6中铝过剩。
步骤4.加热烧瓶6,回流一定时间。
步骤5.将氮气的流动方向改为从导管口4到导管口l。将装有五氧化二磷的干燥管与导管口1连接,将烧瓶6加热至270℃左右,使溴化铝蒸馏进入收集器2。
步骤6.蒸馏完毕时,在继续通入氮气的情况下,将收集器2从3处拆下,并立即封闭3处。
(1)步骤l中,铝箔用CCl4浸泡的目的是
(2)步骤2操作中,通氮气的目的是
(3)步骤3中,该实验要保证烧瓶中铝箔过剩,其目的是
(4)铝与液溴反应的化学方程式为
(5)步骤4依据何种现象判断可以停止回流操作
(6)步骤5需打开导管口l和4,并从4通入N2的目的是
II.某课外小组的同学拟用废铝箔制取硫酸铝晶体,已知铝的物种类别与溶液pH关系如图所示,实验中可选用的试剂:处理过的铝箔;2.0mol•L-1NaOH溶液:2.0 mol•L-1硫酸

(7)由铝箔制备硫酸铝晶体的实验步骤依次为:
①称取一定质量的铝箔于烧杯中,分次加入2.0 mol•L-1NaOH溶液,加热至不再产生气泡为止。
②过滤 ③
④过滤、洗涤 ⑤
⑦冷却结晶; ⑧过滤、洗涤、干燥。
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
【推荐2】碳酸镧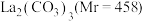 为白色粉末、难溶于水、分解温度900℃,可用于治疗高磷酸盐血症.在溶液中制备时,形成水合碳酸镧
为白色粉末、难溶于水、分解温度900℃,可用于治疗高磷酸盐血症.在溶液中制备时,形成水合碳酸镧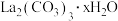 ,如果溶液碱性太强,易生成受热分解的碱式碳酸镧
,如果溶液碱性太强,易生成受热分解的碱式碳酸镧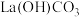 .已知酒精喷灯温度可达1000℃。回答下列问题:
.已知酒精喷灯温度可达1000℃。回答下列问题:
(1)用如图装置模拟制备水合碳酸镧:

①仪器B的名称为_______ 。
②装置接口的连接顺序为f→_______ 。
③Z中应先通入:_______ (化学式),后通入过量的另一种气体,该气体需要过量的原因是_______ 。
④该反应中生成副产物氯化铵,请写出生成水合碳酸镧的化学方程式:_______ 。
(2)甲小组通过以下实验验证制得的样品中不含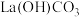 ,并测定水合碳酸铜
,并测定水合碳酸铜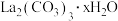 中结晶水的含量,将石英玻璃A管称重,记为
中结晶水的含量,将石英玻璃A管称重,记为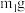 ,将样品装入石英玻璃管中,再次将装置A称重,记为
,将样品装入石英玻璃管中,再次将装置A称重,记为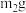 ,将装有试剂的装置C称重,记为
,将装有试剂的装置C称重,记为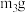 .按图示连接好装置进行实验。
.按图示连接好装置进行实验。
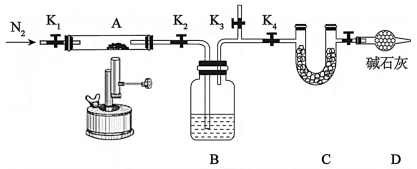
实验步骤:
①打开 、
、 和
和 ,缓缓通入
,缓缓通入 ;
;
②数分钟后关闭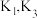 ,打开
,打开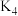 ,点燃酒精喷灯,加热A中样品:
,点燃酒精喷灯,加热A中样品:
③一段时间后,熄灭酒精灯,打开 ,通入
,通入 数分钟后关闭
数分钟后关闭 和
和 ,冷却到室温,称量A.重复上述操作步骤,直至A恒重,记为
,冷却到室温,称量A.重复上述操作步骤,直至A恒重,记为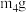 (此时装置A中为
(此时装置A中为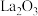 ).称重装置C,记为
).称重装置C,记为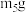 。
。
①实验中第二次通入 的目的为
的目的为_______ 。
②根据实验记录,当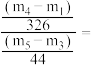
_______ ,说明制得的样品中不含有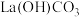 ;计算水合碳酸镧化学式中结晶水数目
;计算水合碳酸镧化学式中结晶水数目
_______ (列式表示).(用含 、
、 、
、 的式子表示)
的式子表示)
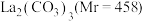 为白色粉末、难溶于水、分解温度900℃,可用于治疗高磷酸盐血症.在溶液中制备时,形成水合碳酸镧
为白色粉末、难溶于水、分解温度900℃,可用于治疗高磷酸盐血症.在溶液中制备时,形成水合碳酸镧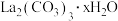 ,如果溶液碱性太强,易生成受热分解的碱式碳酸镧
,如果溶液碱性太强,易生成受热分解的碱式碳酸镧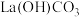 .已知酒精喷灯温度可达1000℃。回答下列问题:
.已知酒精喷灯温度可达1000℃。回答下列问题:(1)用如图装置模拟制备水合碳酸镧:

①仪器B的名称为
②装置接口的连接顺序为f→
③Z中应先通入:
④该反应中生成副产物氯化铵,请写出生成水合碳酸镧的化学方程式:
(2)甲小组通过以下实验验证制得的样品中不含
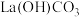 ,并测定水合碳酸铜
,并测定水合碳酸铜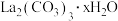 中结晶水的含量,将石英玻璃A管称重,记为
中结晶水的含量,将石英玻璃A管称重,记为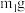 ,将样品装入石英玻璃管中,再次将装置A称重,记为
,将样品装入石英玻璃管中,再次将装置A称重,记为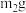 ,将装有试剂的装置C称重,记为
,将装有试剂的装置C称重,记为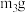 .按图示连接好装置进行实验。
.按图示连接好装置进行实验。
实验步骤:
①打开
 、
、 和
和 ,缓缓通入
,缓缓通入 ;
;②数分钟后关闭
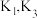 ,打开
,打开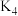 ,点燃酒精喷灯,加热A中样品:
,点燃酒精喷灯,加热A中样品:③一段时间后,熄灭酒精灯,打开
 ,通入
,通入 数分钟后关闭
数分钟后关闭 和
和 ,冷却到室温,称量A.重复上述操作步骤,直至A恒重,记为
,冷却到室温,称量A.重复上述操作步骤,直至A恒重,记为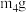 (此时装置A中为
(此时装置A中为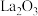 ).称重装置C,记为
).称重装置C,记为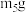 。
。①实验中第二次通入
 的目的为
的目的为②根据实验记录,当
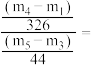
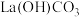 ;计算水合碳酸镧化学式中结晶水数目
;计算水合碳酸镧化学式中结晶水数目
 、
、 、
、 的式子表示)
的式子表示)
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
【推荐3】一位同学在复习时遇到这样一道习题:某无色溶液中可能含有“H+、OH-、Na+、NO3-”,加入铝粉后,只产生H2,问该无色溶液中能大量存在哪几种离子。
(1)加入铝粉产生H2,说明铝具有__________ (填“氧化性”或“还原性”)。
(2)该同学分析:若H+大量存在,则NO3-就不能大量存在。 设计实验证实如下:
①盐酸溶解Al2O3薄膜的离子方程式是_______________________________ 。
②根据现象ⅱ,推测溶液中产生了NO,为进一步确认,进行如下实验:
a.浅棕色气体是____________ 。
b.实验1的目的是_______________________________ 。
c.实验1、2说明反应生成了NO,将生成NO的离子方程式补充完整:
______Al +______NO3- +_____ _ ==______Al 3++______NO +______ ,_______
(3)再假设:若OH-大量存在,NO3-也可能不能大量存在。重新设计实验证实如下:
为确认“刺激性气味”气体,进行如下实验:用湿润KI—淀粉试纸检验,未变蓝;用湿润红色石蕊试纸检验,试纸变蓝。
①刺激性气味的气体是____________ 。
②产生该气体的离子方程式是____________________________________ 。
(4)在NaOH溶液中加入铝粉,结果只检验出有H2生成,其化学方程式是_________________________________ 。
(5)实验结果证实:NO3-在酸、碱性环境中都有一定的氧化性,能氧化铝单质,产生含氮化合物。试题中的无色溶液一定能大量存在的是_______________ 。
(1)加入铝粉产生H2,说明铝具有
(2)该同学分析:若H+大量存在,则NO3-就不能大量存在。 设计实验证实如下:
| 装 置 | 现 象 |
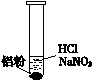 | ⅰ. 实验初始,未见明显现象 ⅱ. 过一会儿,出现气泡,液面上方呈浅棕色 ⅲ. 试管变热,溶液沸腾 |
②根据现象ⅱ,推测溶液中产生了NO,为进一步确认,进行如下实验:
| 实 验 | 内 容 | 现 象 |
| 实验1 | 将湿润KI—淀粉试纸置于空气中 | 未变蓝 |
| 实验2 | 用湿润KI—淀粉试纸检验浅棕色气体 | 试纸变蓝 |
b.实验1的目的是
c.实验1、2说明反应生成了NO,将生成NO的离子方程式补充完整:
______Al +______NO3- +_____ _ ==______Al 3++______NO +______ ,
(3)再假设:若OH-大量存在,NO3-也可能不能大量存在。重新设计实验证实如下:
| 装 置 | 现 象 |
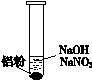 | ⅰ. 实验初始,未见明显现象 ⅱ. 过一会儿,出现气泡,有刺激性气味 |
①刺激性气味的气体是
②产生该气体的离子方程式是
(4)在NaOH溶液中加入铝粉,结果只检验出有H2生成,其化学方程式是
(5)实验结果证实:NO3-在酸、碱性环境中都有一定的氧化性,能氧化铝单质,产生含氮化合物。试题中的无色溶液一定能大量存在的是
您最近一年使用:0次



