在如图所示的一些常见单质,化合物等物质之间的转化关系中(有些反应过程中的水,部分产物和反应条件未全部列出),已知反应①是氯碱工业的最基础的反应,A、B、F、H、J的焰色反应均为黄色,热的F溶液可以去除物品表面的油污,I为地壳中含量最多的金属元素的单质,L是典型的两性氧化物,在常温常压下C、D、G均为气体,D呈黄绿色,G是形成温室效应的主要气体。
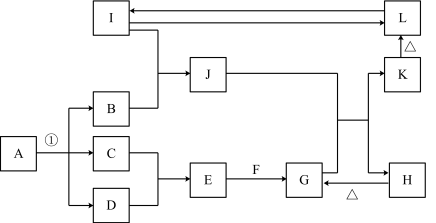
(1)反应①进行的条件为_______ 。
(2)化合物F的化学式为_______ 。
(3)I与氧化铁反应的化学方程式为_______ 。
(4)J的水溶液与G反应生成K和H的离子方程式为_______ .

(1)反应①进行的条件为
(2)化合物F的化学式为
(3)I与氧化铁反应的化学方程式为
(4)J的水溶液与G反应生成K和H的离子方程式为
更新时间:2016-12-09 10:53:57
|
相似题推荐
解答题-工业流程题
|
较易
(0.85)
名校
解题方法
【推荐1】镓( )是非常重要的稀土金属,其化合物广泛应用于诸多领域。
)是非常重要的稀土金属,其化合物广泛应用于诸多领域。
(1)镓元素在元素周期表中的位置是___________ 。
(2)工业上利用炼锌矿渣[主要含可溶性铁酸镓 、铁酸锌
、铁酸锌 ]提取
]提取 。矿渣经“酸浸”后所得酸浸液含有
。矿渣经“酸浸”后所得酸浸液含有 、
、 、
、 等离子,经萃取富集其中的镓元素用于后续反应可制备氮化镓晶体。萃取工艺流程如下图所示。
等离子,经萃取富集其中的镓元素用于后续反应可制备氮化镓晶体。萃取工艺流程如下图所示。
①“酸浸”过程中 发生的反应的离子方程式为
发生的反应的离子方程式为___________ 。
②萃取剂水杨羟肟酸的结构简式如图1所示,萃取时分子中的 、
、 原子能与金属离子形成稳定的配位键。解释
原子能与金属离子形成稳定的配位键。解释 、
、 原子能作为配位原子的原因
原子能作为配位原子的原因___________ 。___________ (填试剂)充分反应后再进行萃取。
④“反萃取”后,溶液中镓元素的存在形式为___________ 。(填离子符号)
(3)氮化镓是非常重要的半导体材料,其立方晶胞如图2所示,与金刚石结构相似。 原子采用
原子采用___________ 杂化轨道成键。
②常压下,该晶体熔点为 ,其晶体类型为
,其晶体类型为___________ 。
③已知 晶体中距离最近的
晶体中距离最近的 原子间的核间距为
原子间的核间距为 ,
, 的摩尔质量为
的摩尔质量为 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,则
,则 晶体的密度为
晶体的密度为___________  。
。
 )是非常重要的稀土金属,其化合物广泛应用于诸多领域。
)是非常重要的稀土金属,其化合物广泛应用于诸多领域。(1)镓元素在元素周期表中的位置是
(2)工业上利用炼锌矿渣[主要含可溶性铁酸镓
 、铁酸锌
、铁酸锌 ]提取
]提取 。矿渣经“酸浸”后所得酸浸液含有
。矿渣经“酸浸”后所得酸浸液含有 、
、 、
、 等离子,经萃取富集其中的镓元素用于后续反应可制备氮化镓晶体。萃取工艺流程如下图所示。
等离子,经萃取富集其中的镓元素用于后续反应可制备氮化镓晶体。萃取工艺流程如下图所示。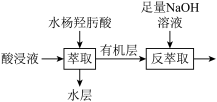
| 金属离子 |  |  |  |  |
| 萃取率/% | 0 | 0 | 99 | 97~98.5 |
 发生的反应的离子方程式为
发生的反应的离子方程式为②萃取剂水杨羟肟酸的结构简式如图1所示,萃取时分子中的
 、
、 原子能与金属离子形成稳定的配位键。解释
原子能与金属离子形成稳定的配位键。解释 、
、 原子能作为配位原子的原因
原子能作为配位原子的原因
④“反萃取”后,溶液中镓元素的存在形式为
(3)氮化镓是非常重要的半导体材料,其立方晶胞如图2所示,与金刚石结构相似。
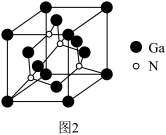
 原子采用
原子采用②常压下,该晶体熔点为
 ,其晶体类型为
,其晶体类型为③已知
 晶体中距离最近的
晶体中距离最近的 原子间的核间距为
原子间的核间距为 ,
, 的摩尔质量为
的摩尔质量为 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,则
,则 晶体的密度为
晶体的密度为 。
。
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐2】某学生欲用下列装置制取纯净的 固体。其中
固体。其中 是
是 发生装置,
发生装置, 为气体净化装置,
为气体净化装置, 硬质玻璃管中装有细铁丝网,
硬质玻璃管中装有细铁丝网, 为干燥的空广口瓶,烧杯
为干燥的空广口瓶,烧杯 为尾气吸收装置。
为尾气吸收装置。

试回答:
(1)该装置中的一处明显错误是___________ 。
(2)D中所装试剂为___________ ,C装置的作用是___________ 。
(3)A中发生反应的化学方程式是___________ 。G中发生反应的离子方程式是___________ 。
(4)若用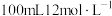 盐酸跟足量
盐酸跟足量 充分反应,生成的
充分反应,生成的 体积(标准状况)
体积(标准状况)___________ (填“大于”“小于”或“等于”) 。
。
(5)若用所制取的 固体制成
固体制成 胶体,
胶体, 胶体分散质粒子
胶体分散质粒子___________ (填“能”或“不能”)通过滤纸孔隙;在 胶体中逐滴加入稀盐酸,现象是
胶体中逐滴加入稀盐酸,现象是___________ 。
 固体。其中
固体。其中 是
是 发生装置,
发生装置, 为气体净化装置,
为气体净化装置, 硬质玻璃管中装有细铁丝网,
硬质玻璃管中装有细铁丝网, 为干燥的空广口瓶,烧杯
为干燥的空广口瓶,烧杯 为尾气吸收装置。
为尾气吸收装置。
试回答:
(1)该装置中的一处明显错误是
(2)D中所装试剂为
(3)A中发生反应的化学方程式是
(4)若用
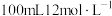 盐酸跟足量
盐酸跟足量 充分反应,生成的
充分反应,生成的 体积(标准状况)
体积(标准状况) 。
。(5)若用所制取的
 固体制成
固体制成 胶体,
胶体, 胶体分散质粒子
胶体分散质粒子 胶体中逐滴加入稀盐酸,现象是
胶体中逐滴加入稀盐酸,现象是
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐3】人体血液里Ca2+离子的浓度一般采用g/cm3来表示。抽取一定体积的血样,加适量的草酸铵[(NH4)2C2O4]溶液,可析出草酸钙(CaC2O4)沉淀,将此草酸钙沉淀洗涤后溶于强酸可得一种弱酸草酸(H2C2O4),再用KMnO4溶液滴定即可测定血液样品中Ca2+的浓度。某研究性学习小组设计如下实验步骤测定血液样品中Ca2+的浓度:
【配制KMnO4标准溶液】下图是配制50mLKMnO4标准溶液的过程示意图。
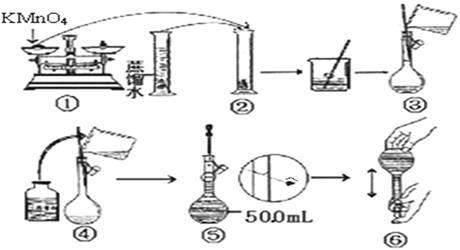
(1)上述过程中有两处错误,请你观察图示判断其中不正确的操作是(填序号)____________ ;
(2)如果按照图示的操作配制溶液,所得的实验结果将____________ (填偏大或偏小)。
【测定血液样品中Ca2+的浓度】抽取血样20.00mL,经过上述处理后得到草酸,再用酸化的0.020mol/L KMnO4溶液滴定,使草酸转化成CO2逸出,这时共消耗12.00mL KMnO4溶液。
(3)滴定时高锰酸钾需要酸化,从括号中选择酸化高锰酸钾溶液所用的酸(硫酸、盐酸、硝酸)________ ,确定反应达到终点的现象_____________________________ 。
(4)写出草酸跟酸性KMnO4溶液反应的离子方程式为:_____________________ ;反应中若转移0.2mol 电子生成标准状况下CO2气体的体积为_______ L。
(5)根据所给数据计算血液样品中Ca2+离子的浓度为________ mg/cm3。
【配制KMnO4标准溶液】下图是配制50mLKMnO4标准溶液的过程示意图。

(1)上述过程中有两处错误,请你观察图示判断其中不正确的操作是(填序号)
(2)如果按照图示的操作配制溶液,所得的实验结果将
【测定血液样品中Ca2+的浓度】抽取血样20.00mL,经过上述处理后得到草酸,再用酸化的0.020mol/L KMnO4溶液滴定,使草酸转化成CO2逸出,这时共消耗12.00mL KMnO4溶液。
(3)滴定时高锰酸钾需要酸化,从括号中选择酸化高锰酸钾溶液所用的酸(硫酸、盐酸、硝酸)
(4)写出草酸跟酸性KMnO4溶液反应的离子方程式为:
(5)根据所给数据计算血液样品中Ca2+离子的浓度为
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐1】A、B、C、D、E五种物质的焰色反应都呈黄色,A、B分别与水反应都有气体放出,同时都生成C溶液,A与水反应放出的气体具有还原性,B与水反应放出的气体具有氧化性,C与适量的F气体反应生成D,D溶液与F气体反应生成E,E加热能够生成D、F气体和水。根据以上叙述回答下列问题:
(1)写出下列物质的化学式:
A__________ B__________ ,C__________ ,D_________
(2)按要求完成方程式:
①E加热生成D和F的化学方程式_______________________________ ;
②C溶液和CO2反应生成D的离子方程式______________________________ 。
(1)写出下列物质的化学式:
A
(2)按要求完成方程式:
①E加热生成D和F的化学方程式
②C溶液和CO2反应生成D的离子方程式
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
解题方法
【推荐2】亚氯酸的 ,常温常压下二氧化氯
,常温常压下二氧化氯 是一种黄绿色气体,它具有漂白性,消毒能力较强,可替代传统的液氯作为饮用水消毒杀菌剂。实验室用以下方式制备
是一种黄绿色气体,它具有漂白性,消毒能力较强,可替代传统的液氯作为饮用水消毒杀菌剂。实验室用以下方式制备 :
:____________ 。
② 在水溶液中很快水解成
在水溶液中很快水解成 和另一种化合物,该化合物名称为:
和另一种化合物,该化合物名称为:______ 。上述流程中在 酸性溶液条件下加入
酸性溶液条件下加入 反应的离子方程式为:
反应的离子方程式为:____________ 。
(2)纯 易分解爆炸,故常与
易分解爆炸,故常与 的烧碱溶液反应生成
的烧碱溶液反应生成 保存,需要时再通过溶于酸溶液反应获得
保存,需要时再通过溶于酸溶液反应获得 ,该反应刚开始十分缓慢,稍后一段时间产生气体急剧加快。下列说法正确的是______。
,该反应刚开始十分缓慢,稍后一段时间产生气体急剧加快。下列说法正确的是______。
(3)设计实验验证溶液 中的金属阳离子与氯离子
中的金属阳离子与氯离子____________ 。
 ,常温常压下二氧化氯
,常温常压下二氧化氯 是一种黄绿色气体,它具有漂白性,消毒能力较强,可替代传统的液氯作为饮用水消毒杀菌剂。实验室用以下方式制备
是一种黄绿色气体,它具有漂白性,消毒能力较强,可替代传统的液氯作为饮用水消毒杀菌剂。实验室用以下方式制备 :
: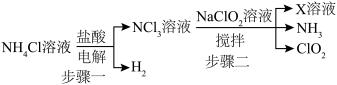
②
 在水溶液中很快水解成
在水溶液中很快水解成 和另一种化合物,该化合物名称为:
和另一种化合物,该化合物名称为: 酸性溶液条件下加入
酸性溶液条件下加入 反应的离子方程式为:
反应的离子方程式为:(2)纯
 易分解爆炸,故常与
易分解爆炸,故常与 的烧碱溶液反应生成
的烧碱溶液反应生成 保存,需要时再通过溶于酸溶液反应获得
保存,需要时再通过溶于酸溶液反应获得 ,该反应刚开始十分缓慢,稍后一段时间产生气体急剧加快。下列说法正确的是______。
,该反应刚开始十分缓慢,稍后一段时间产生气体急剧加快。下列说法正确的是______。| A.亚氯酸钠有强氧化性,在溶液中水解显酸性 |
B. 和 和 在碱性溶液中反应时, 在碱性溶液中反应时, 表现还原性 表现还原性 |
C.将 溶液进行加热浓缩,蒸发结晶,过滤洗涤,得到 溶液进行加热浓缩,蒸发结晶,过滤洗涤,得到 |
D.两份相同 溶液分别与等 溶液分别与等 的盐酸和硫酸反应,与盐酸反应可能快 的盐酸和硫酸反应,与盐酸反应可能快 |
(3)设计实验验证溶液
 中的金属阳离子与氯离子
中的金属阳离子与氯离子
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐3】如图所示,A为化学学习中常见的单质,B、C、D、E是含A元素的常用化合物,它们的焰色均为黄色。请按要求回答下列问题。

(1)写出下列物质的化学式:B________ ;E__________ 。
(2)以上反应中属于氧化还原反应的有________ (填写编号)。
(3)写出A→C反应的离子方程式:____________________ 。
(4)写出B→D反应的化学方程式:____________________ 。
(5)加热5.00 g D和E的固体混合物,使E完全分解,固体混合物的质量减少了0.31 g,则原混合物中D的质量为__________ 。

(1)写出下列物质的化学式:B
(2)以上反应中属于氧化还原反应的有
(3)写出A→C反应的离子方程式:
(4)写出B→D反应的化学方程式:
(5)加热5.00 g D和E的固体混合物,使E完全分解,固体混合物的质量减少了0.31 g,则原混合物中D的质量为
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐1】下图是元素周期表的一部分:
回答下列问题:
(1)元素⑤的符号为_______ ;元素⑧所在的主族为_______ 。
(2)元素①和②能形成多种化合物,其中相对分子质量最小的是_______ (填化学式);元素⑦的原子结构示意图为_______ 。
(3)元素①与③组成的化合物是_______ (填两种化学式);元素⑥与①③④组成的化合物反应的离子方程式为_______ 。
| ① | |||||||||||||||||
| ② | ③ | ||||||||||||||||
| ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ |
(1)元素⑤的符号为
(2)元素①和②能形成多种化合物,其中相对分子质量最小的是
(3)元素①与③组成的化合物是
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
【推荐2】现有金属单质A、B、C和气体甲、乙、丙以及物质D、E、F、G、H,它们之间的相互转化关系如图所示(图中有些反应的生成物和反应的条件没有标出)。

请根据以上信息完成下列各题:
(1)写出下列物质的化学式:C_______ ,丙_______ ;
(2)写出过程①涉及的离子方程式_______ ;
(3)写出过程⑦涉及的化学方程式_______ ,_______ ;
(4)反应⑦中如果想白色沉淀保持时间长,可采用如下装置:
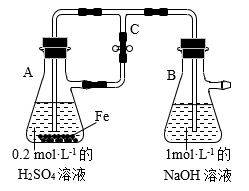
其操作是检验装置的气密性,装好药品,打开C处开关,反应一段时间后。关闭C处开关,A处的溶液沿导管流入B处。生成的白色沉淀可以保存较长时间,原因是:_______ 。
(5) 常见检验的方法:
常见检验的方法:_______ 。

请根据以上信息完成下列各题:
(1)写出下列物质的化学式:C
(2)写出过程①涉及的离子方程式
(3)写出过程⑦涉及的化学方程式
(4)反应⑦中如果想白色沉淀保持时间长,可采用如下装置:

其操作是检验装置的气密性,装好药品,打开C处开关,反应一段时间后。关闭C处开关,A处的溶液沿导管流入B处。生成的白色沉淀可以保存较长时间,原因是:
(5)
 常见检验的方法:
常见检验的方法:
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐3】下图表示的反应关系中,部分产物被略去。已知2 mol白色固体粉末X受热分解,恢复到室温生成白色固体A、无色液体B、无色气体C各1 mol。X、E、G的焰色反应均为黄色。
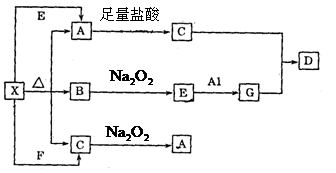
回答下列问题:
(1)写出下列物质的化学式:X_____________ G_____________ D_____________ ;
(2)写出G与过量的C反应生成D的离子方程式:_____________________________ ;
(3)写出X+E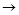 A的离子方程式:
A的离子方程式:_____________________________________ ;
(4)C与Na2O2反应时,若消耗0.2 mol Na2O2则转移的电子数为_____________ 个。

回答下列问题:
(1)写出下列物质的化学式:X
(2)写出G与过量的C反应生成D的离子方程式:
(3)写出X+E
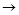 A的离子方程式:
A的离子方程式:(4)C与Na2O2反应时,若消耗0.2 mol Na2O2则转移的电子数为
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
【推荐1】某金属A及其化合物之间有如下的转化关系:
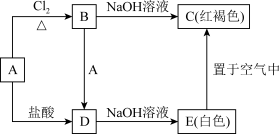
(1)请写出A、B、C的化学式:A_______ ;B_______ ;C_______ 。
(2)写出E转化为C的化学方程式:_______ 。
(3)写出A转化为D的离子方程式:_______ 。

(1)请写出A、B、C的化学式:A
(2)写出E转化为C的化学方程式:
(3)写出A转化为D的离子方程式:
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐2】室温下,A是常见的金属单质、单质B是黄绿色气体、单质C是无色气体。在合适反应条件下,它们可以按下面框图进行反应;E是无色溶液,F是淡绿色溶液。B和C反应发出苍白色火焰。请回答:
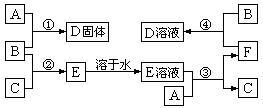
(1)A是__________ ,B是__________ ,C是__________ (请填写化学式);
(2)反应①的化学方程式______________________________ ;
(3)反应③的离子方程式______________________________ ;
(4)反应④的离子方程式______________________________ 。

(1)A是
(2)反应①的化学方程式
(3)反应③的离子方程式
(4)反应④的离子方程式
您最近一年使用:0次




