正盐A能发生下图所示的反应,图中①~⑧分别代表有关反应中的一种物质(某些物质已略去),其中①、②、④、⑤为无色气体,⑥为红棕色气体。
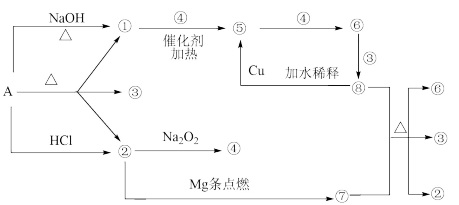
请完成下列各题:
(1)写出化学式A___________ ⑥___________ ⑦___________
(2)写出下列反应方程式:
⑧+⑦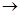 ②+③+⑥:
②+③+⑥:___________
①+④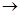 ⑤:
⑤:___________
(3)⑧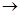 ⑤的离子方程式为:
⑤的离子方程式为:___________

请完成下列各题:
(1)写出化学式A
(2)写出下列反应方程式:
⑧+⑦
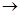 ②+③+⑥:
②+③+⑥:①+④
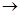 ⑤:
⑤:(3)⑧
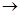 ⑤的离子方程式为:
⑤的离子方程式为:
更新时间:2016-12-09 11:04:14
|
相似题推荐
解答题-原理综合题
|
适中
(0.65)
【推荐1】2020年9月中国明确提出“双碳”目标。因此,研发 资源化利用技术、降低空气中
资源化利用技术、降低空气中 含量成为科学家的研究热点。图1为我国科学家利用
含量成为科学家的研究热点。图1为我国科学家利用 和金属
和金属 成功发明的
成功发明的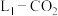 电池的工作示意图。通入
电池的工作示意图。通入 一极的反应产物为
一极的反应产物为 和单质碳;图2为采用“两室”膜电解法将
和单质碳;图2为采用“两室”膜电解法将 转化为
转化为 的示意图。请回答下列问题:
的示意图。请回答下列问题: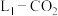 电池中:
电池中:
(1) Li为______ (填“正”或“负”)极,正极的电极反应为____________ 。
(2)研究表明, 电还原后与
电还原后与 结合形成
结合形成 的反应历程如下,反应II的离子方程式为
的反应历程如下,反应II的离子方程式为____________
I.
II._________________
III.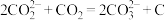
IV.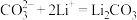
II、利用 电池作为图2装置的中源。
电池作为图2装置的中源。
(3) 片连接
片连接 电池的
电池的_______ (填“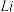 ”或“
”或“ ”)电极,电解过程中,
”)电极,电解过程中,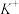 通过阳离子交换膜由
通过阳离子交换膜由_______ (填“左室移向右室”或“右室移向左室”),阴极发生的电极反应为_______ 。
(4)电解一段时间后, 电池中生成
电池中生成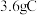 时,图2中阳极区产生气体的体积(标准状况)为
时,图2中阳极区产生气体的体积(标准状况)为_______ L。
 资源化利用技术、降低空气中
资源化利用技术、降低空气中 含量成为科学家的研究热点。图1为我国科学家利用
含量成为科学家的研究热点。图1为我国科学家利用 和金属
和金属 成功发明的
成功发明的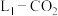 电池的工作示意图。通入
电池的工作示意图。通入 一极的反应产物为
一极的反应产物为 和单质碳;图2为采用“两室”膜电解法将
和单质碳;图2为采用“两室”膜电解法将 转化为
转化为 的示意图。请回答下列问题:
的示意图。请回答下列问题: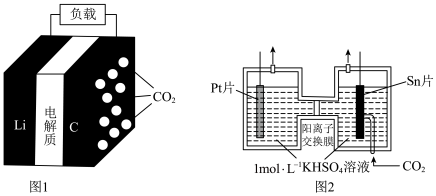
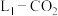 电池中:
电池中:(1) Li为
(2)研究表明,
 电还原后与
电还原后与 结合形成
结合形成 的反应历程如下,反应II的离子方程式为
的反应历程如下,反应II的离子方程式为I.

II._________________
III.
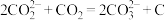
IV.
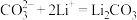
II、利用
 电池作为图2装置的中源。
电池作为图2装置的中源。(3)
 片连接
片连接 电池的
电池的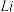 ”或“
”或“ ”)电极,电解过程中,
”)电极,电解过程中,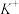 通过阳离子交换膜由
通过阳离子交换膜由(4)电解一段时间后,
 电池中生成
电池中生成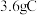 时,图2中阳极区产生气体的体积(标准状况)为
时,图2中阳极区产生气体的体积(标准状况)为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
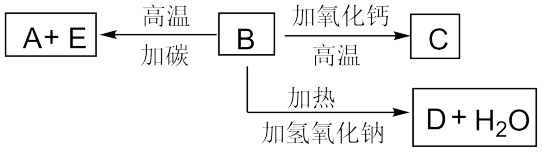
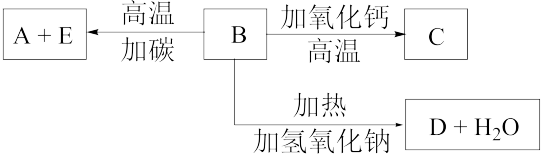
【推荐2】Ⅰ、有4种钠的化合物W、X、Y、Z,它们之间存在如下关系:
①W X+H2O+CO2↑②Z+CO2→X+O2③Z+H2O→Y+O2↑④X+Ca(OH)2→Y+CaCO3↓
X+H2O+CO2↑②Z+CO2→X+O2③Z+H2O→Y+O2↑④X+Ca(OH)2→Y+CaCO3↓
(1)W、X、Y、Z的化学式分别是:W:___________ 、X:___________ 、Y:___________ 、Z:___________ 。
(2)以上4个化学反应,属于氧化还原反应的是___________ (填序号),反应中氧化剂是___________ (写化学式),还原剂是___________ (写化学式)。
(3)W与盐酸反应的离子方程式为:___________ 。
Ⅱ、某化学兴趣小组同学将金属钠加热至熔化后,误通入了干燥的CO2进行反应,将反应后固体产物溶于稀盐酸,产生气泡,观察到难溶于水的黑色固体。
(4)产物中与盐酸反应的物质可能为___________ (填化学式)。
(5)经检验,黑色固体为单质碳。写出CO2与Na反应的化学方程式___________ 。
①W
 X+H2O+CO2↑②Z+CO2→X+O2③Z+H2O→Y+O2↑④X+Ca(OH)2→Y+CaCO3↓
X+H2O+CO2↑②Z+CO2→X+O2③Z+H2O→Y+O2↑④X+Ca(OH)2→Y+CaCO3↓(1)W、X、Y、Z的化学式分别是:W:
(2)以上4个化学反应,属于氧化还原反应的是
(3)W与盐酸反应的离子方程式为:
Ⅱ、某化学兴趣小组同学将金属钠加热至熔化后,误通入了干燥的CO2进行反应,将反应后固体产物溶于稀盐酸,产生气泡,观察到难溶于水的黑色固体。
(4)产物中与盐酸反应的物质可能为
(5)经检验,黑色固体为单质碳。写出CO2与Na反应的化学方程式
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】金属钛(Ti)的机械强度高,抗蚀能力强,有“未来金属”之称。工业上常用硫酸浸钛铁矿[主要成分为钛酸亚铁( 难溶于水,能与酸反应)]的方法制取二氧化钛,再由二氧化钛制取金属钛。工艺流程如下:
难溶于水,能与酸反应)]的方法制取二氧化钛,再由二氧化钛制取金属钛。工艺流程如下:
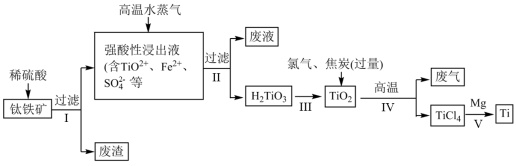
回答下列问题:
(1) 中钛元素的化合价为
中钛元素的化合价为______ 。
(2)稀硫酸与 反应的离子方程式为
反应的离子方程式为______ 。
(3)过程Ⅴ表现了金属镁的还原性比金属钛的还原性______ (填“强”或“弱”)。
(4)过程Ⅳ的化学方程式______ 。转移8个电子生成______ 个 。
。
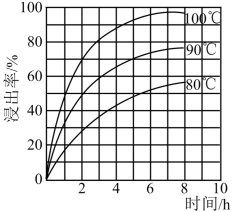
(5)酸浸中,铁的浸出率与时间、温度的关系如图所示,如图可知,当铁的浸出率为70%时,可采用的实验条件为______ 。
 难溶于水,能与酸反应)]的方法制取二氧化钛,再由二氧化钛制取金属钛。工艺流程如下:
难溶于水,能与酸反应)]的方法制取二氧化钛,再由二氧化钛制取金属钛。工艺流程如下:
回答下列问题:
(1)
 中钛元素的化合价为
中钛元素的化合价为(2)稀硫酸与
 反应的离子方程式为
反应的离子方程式为(3)过程Ⅴ表现了金属镁的还原性比金属钛的还原性
(4)过程Ⅳ的化学方程式
 。
。(5)酸浸中,铁的浸出率与时间、温度的关系如图所示,如图可知,当铁的浸出率为70%时,可采用的实验条件为

您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】已知A、B、C为中学化学中常见的单质。室温下,A为固体,B和C均为气体。在适宜的条件下,它们可以按下面框图进行反应。
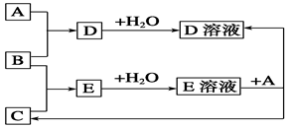
回答下列问题:
(1)A、B、C三种元素中的任意两种元素形成的化合物所属物质类别一定不是_________ 。
①氢化物 ②酸 ③碱 ④盐 ⑤氧化物
(2)A、B、C三种元素中有一种是金属,则这种元素是A、B、C中的_______ ,理由是_________________________ 。
(3)如果E溶液是一种强酸,则E的化学式为_________ 。

回答下列问题:
(1)A、B、C三种元素中的任意两种元素形成的化合物所属物质类别一定不是
①氢化物 ②酸 ③碱 ④盐 ⑤氧化物
(2)A、B、C三种元素中有一种是金属,则这种元素是A、B、C中的
(3)如果E溶液是一种强酸,则E的化学式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】金属铝在酸性或碱性溶液中均可与NO 发生氧化还原反应,转化关系如图:
发生氧化还原反应,转化关系如图:
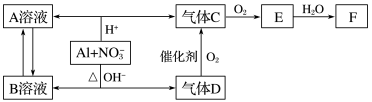
已知:气体D和F反应可生成盐。A和B两溶液混合会产生白色沉淀,请回答下列问题:
(1)将气体D的水溶液逐滴加入A溶液会生成白色沉淀,其反应的离子方程式为____ 。
(2)C、E排入大气中会造成大气污染,在催化剂存在下,D可以将C或E都转化为无毒的气态单质,写出D与E反应的化学方程式:____ 。
(3)写出铝在碱性条件下与NO 反应的离子方程式:
反应的离子方程式:____ 。
(4)除去气体C中的杂质气体E的化学方法:____ (用化学方程式表示)。
(5)Al与NO 在酸性条件下反应,Al与被还原的NO
在酸性条件下反应,Al与被还原的NO 的物质的量之比是
的物质的量之比是____ 。
 发生氧化还原反应,转化关系如图:
发生氧化还原反应,转化关系如图:
已知:气体D和F反应可生成盐。A和B两溶液混合会产生白色沉淀,请回答下列问题:
(1)将气体D的水溶液逐滴加入A溶液会生成白色沉淀,其反应的离子方程式为
(2)C、E排入大气中会造成大气污染,在催化剂存在下,D可以将C或E都转化为无毒的气态单质,写出D与E反应的化学方程式:
(3)写出铝在碱性条件下与NO
 反应的离子方程式:
反应的离子方程式:(4)除去气体C中的杂质气体E的化学方法:
(5)Al与NO
 在酸性条件下反应,Al与被还原的NO
在酸性条件下反应,Al与被还原的NO 的物质的量之比是
的物质的量之比是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】某化学小组模拟工业生产制取HNO3,设计了如图所示装置,其中a为一个可持续鼓入空气的橡皮球。
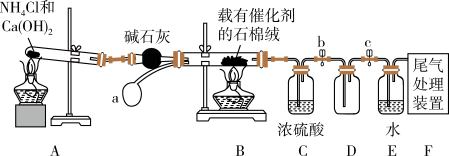
(1)写出装置A中主要反应的化学方程式____ 。
(2)写出装置B中发生反应的化学方程式____ 。
(3)装置C中浓硫酸的主要作用是___ 。
(4)请你帮助该化学小组设计实验室制取NH3的另一个方案:___ ,并写出NH3的两种用途:___ ,___ 。

(1)写出装置A中主要反应的化学方程式
(2)写出装置B中发生反应的化学方程式
(3)装置C中浓硫酸的主要作用是
(4)请你帮助该化学小组设计实验室制取NH3的另一个方案:
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】氨既是一种重要的化工产品,又是一种重要的化工原料。下图为合成氨以及氨氧化制硝酸的流程示意图。回答下列问题
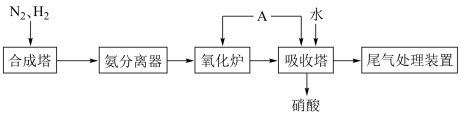
(1)已知断开 键、
键、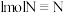 键和
键和 键分别需要吸收的能量为
键分别需要吸收的能量为 和
和 ,则每生成
,则每生成 需要
需要___________ (填“吸收”或“放出”)热量___________  。
。
(2)在相同条件下向密闭容器中充入 和足量
和足量 ,完全反应后吸收或放出的热量
,完全反应后吸收或放出的热量_______ (填“大于”、“等于”或“小于”)(1)中计算值。
(3)合成氨技术中采取高温的原因是___________ 。
(4)A物质是___________ ,在吸收塔中水参与了反应,所起的作用是___________ 。
A.作氧化剂
B.作还原剂
C.既作氧化剂又作还原剂
D.既不作氧化剂又不作还原剂,仅作反应物
(5)为避免硝酸生产尾气中的氮氧化物污染环境,人们开发了溶液吸收、催化还原等尾气处理方法。前者使用具有碱性的NaOH溶液等吸收尾气,后者使用NH3或其他物质将氮氧化物还原为N2.请以尾气中的NO2处理为例,写出相关反应的化学方程式:前者___________ ,后者___________ 。(提示:前者生成物之一为NaNO2 )

(1)已知断开
 键、
键、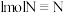 键和
键和 键分别需要吸收的能量为
键分别需要吸收的能量为 和
和 ,则每生成
,则每生成 需要
需要 。
。(2)在相同条件下向密闭容器中充入
 和足量
和足量 ,完全反应后吸收或放出的热量
,完全反应后吸收或放出的热量(3)合成氨技术中采取高温的原因是
(4)A物质是
A.作氧化剂
B.作还原剂
C.既作氧化剂又作还原剂
D.既不作氧化剂又不作还原剂,仅作反应物
(5)为避免硝酸生产尾气中的氮氧化物污染环境,人们开发了溶液吸收、催化还原等尾气处理方法。前者使用具有碱性的NaOH溶液等吸收尾气,后者使用NH3或其他物质将氮氧化物还原为N2.请以尾气中的NO2处理为例,写出相关反应的化学方程式:前者
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐3】(1)X、Y、Z、W是中学化学中常见的四种气体。已知:X、Y、Z三种气体都能对大气造成污染,在工业上都可以用碱液吸收;X是化石燃料燃烧的产物之一,是形成酸雨的物质;Y是一种单质,它的水溶液具有漂白作用;Z是硝酸工业的汽车尾气中的有害物质之一,能与水反应;W气体的水溶液滴入酚酞变红色。请回答下列问题:
①X、Y两种气体按物质的量之比1:1在水溶液中能发生反应,化学方程式为_______________ 。
②科学家发现,Z在催化剂条件下能与W反应,写出该反应的化学方程式_________________ 。其产物中的单质的结构式为:______________ 。
③检验W气体的方法是_________________________________________________ 。
(2)SiO2在自然界中广泛存在,它是制备现代通讯材料_________ (写该材料名称)的主要原料;以SiO2为原料,在工业上制备单质硅的化学方程式为____________________________________ ;在常温下,SiO2可与一种酸发生反应,该反应的化学方程式为____________________________ 。
①X、Y两种气体按物质的量之比1:1在水溶液中能发生反应,化学方程式为
②科学家发现,Z在催化剂条件下能与W反应,写出该反应的化学方程式
③检验W气体的方法是
(2)SiO2在自然界中广泛存在,它是制备现代通讯材料
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】I.A经如图所示的过程转化为D。已知D为强酸或强碱,回答:


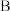

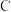 →
→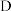
(1)若常温下C是红棕色的气体,A是碱性气体。则:
①A的化学式是:A____ ,C转化D的过程中,氧化剂和还原剂的质量之比为____ 。
②D的稀溶液在常温下可与铜反应,请写出该反应的离子方程式____ 。
(2)若A是一种黄色单质固体,则:向含2molD浓溶液中加入足量的Cu加热,标准状况下产生气体体积____ 22.4L(“大于”“等于”或“小于”);
(3)若A为金属单质,C为淡黄色固体,则C的化学式为____ 。
II.根据如图所示装置回答以下问题:
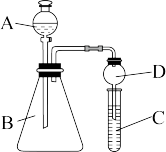
(4)若要用此装置证明非金属性:C>Si,从以下所给物质中选出甲同学设计的实验所用到的物质:
①稀盐酸 ②稀硫酸 ③碳酸钙 ④Na2SiO3溶液 ⑤碳酸钠
试剂A为____ ,试剂C为____ (填序号)。


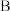

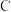 →
→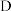
(1)若常温下C是红棕色的气体,A是碱性气体。则:
①A的化学式是:A
②D的稀溶液在常温下可与铜反应,请写出该反应的离子方程式
(2)若A是一种黄色单质固体,则:向含2molD浓溶液中加入足量的Cu加热,标准状况下产生气体体积
(3)若A为金属单质,C为淡黄色固体,则C的化学式为
II.根据如图所示装置回答以下问题:

(4)若要用此装置证明非金属性:C>Si,从以下所给物质中选出甲同学设计的实验所用到的物质:
①稀盐酸 ②稀硫酸 ③碳酸钙 ④Na2SiO3溶液 ⑤碳酸钠
试剂A为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】SO2是有毒气体,任意排放会造成环境污染。若加以利用,可以变废为宝。如图为SO2的无害化处理流程图,回答下列问题:_______ 。
(2)X可能为_______ (填化学式),该反应说明SO2具有 _______ (填“氧化性”或“还原性”)。
(3)“蒸发浓缩、冷却结晶”后获得(NH4)2SO3•H2O固体的操作是_______ 。
(4)(NH4)2SO3•H2O暴露在空气中易被氧化而变质,可以选用哪组试剂进行验证:_______ 。
A.稀硝酸,BaCl2 B.稀盐酸,BaCl2 C.稀盐酸,硝酸钡
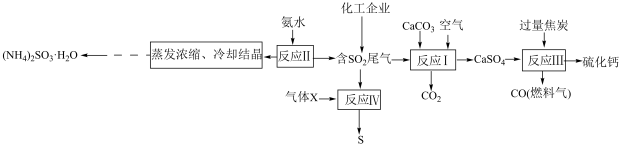
(2)X可能为
(3)“蒸发浓缩、冷却结晶”后获得(NH4)2SO3•H2O固体的操作是
(4)(NH4)2SO3•H2O暴露在空气中易被氧化而变质,可以选用哪组试剂进行验证:
A.稀硝酸,BaCl2 B.稀盐酸,BaCl2 C.稀盐酸,硝酸钡
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】图中A~X分别代表一种反应物或生成物,其中F、G、X为单质,短周期元素X原子的核电荷数是其最外层和最内层电子数之和的3倍。已知A受热分解得到等物质的量的B、C、D三种气态物质,D气体能使湿润的红色石蕊试纸变蓝色,其它为化合物,图中部分生成物未列出。
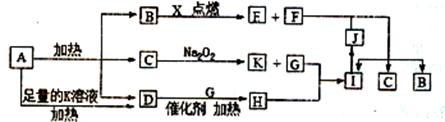
请回答:
(1)B的电子式______ ,写出F的一种同素异形体____ ;
(2)写出反应B与X反应的化学方程式_____________________ ;
(3)写出A与足量K溶液加热时反应的离子方程式__________________ ;
(4)在一定条件下,2 L的H气体与0.5 L的G气体相混合,若该混合气体被NaOH溶液恰好完全吸收,只生成一种盐。请写出该反应过程中总的化学反应方程式:________ ;
(5)在F与J的反应中当转移了1.5 mol电子时,产生标准状况下的I气体的体积为_______ L。

请回答:
(1)B的电子式
(2)写出反应B与X反应的化学方程式
(3)写出A与足量K溶液加热时反应的离子方程式
(4)在一定条件下,2 L的H气体与0.5 L的G气体相混合,若该混合气体被NaOH溶液恰好完全吸收,只生成一种盐。请写出该反应过程中总的化学反应方程式:
(5)在F与J的反应中当转移了1.5 mol电子时,产生标准状况下的I气体的体积为
您最近一年使用:0次