在热的稀硫酸中溶解了7.6gFeSO4固体,当加入50mL 0.5mol•L﹣1 KNO2溶液时,其中的Fe2+全部转化成Fe3+,KNO2也完全反应并放出NxOy气体。
(1)推算出x=____ ;y=____ 。(其中x、y均为正整数,且没有公约数)
(2)配平该反应的方程式:(配平系数若为“1”,也必须写出)____ 。
___FeSO4+__KNO2+___H2SO4=___K2SO4+__Fe2(SO4)3+___↑+___H2O(配平时x、y用(1)中求解的具体数值表示,物质填在□中)。
(3)反应中还原产物是_____ (填物质名称)。
(4)标准状况下,NxOy气体的体积为_____ L。
(1)推算出x=
(2)配平该反应的方程式:(配平系数若为“1”,也必须写出)
___FeSO4+__KNO2+___H2SO4=___K2SO4+__Fe2(SO4)3+___↑+___H2O(配平时x、y用(1)中求解的具体数值表示,物质填在□中)。
(3)反应中还原产物是
(4)标准状况下,NxOy气体的体积为
更新时间:2016/12/09 11:05:35
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】根据所学知识填写下列空白。
(1)在标准状况下,6.72 L CO2质量为___________ g,其中含有氧原子数目为___________ 。
(2)在标准状况下,3.4 g氨气所占的体积约为___________ L,它与同条件下___________ mol H2S含有相同的氢原子数。
(3)V L Fe2(SO4)3溶液中含有a g SO ,取此溶液0.5 VL,用水稀释至2 VL,则稀释后溶液中SO
,取此溶液0.5 VL,用水稀释至2 VL,则稀释后溶液中SO 的物质的量浓度为
的物质的量浓度为___________ 。
(4)下列数量的各物质,所含原子个数由大到小的顺序是___________ (填序号)。
①0.5 mol SO3 ②标准状况下22.4 L He
③4℃时9 mL水(水的密度为1 g/mL) ④0.2 mol CH3COONH4
(5)在一密闭容器中充入a mol NO和b mol O2,可发生如下反应:2NO+O2=2NO2,充分反应后容器中氮原子和氧原子的个数之比为___________ 。
(1)在标准状况下,6.72 L CO2质量为
(2)在标准状况下,3.4 g氨气所占的体积约为
(3)V L Fe2(SO4)3溶液中含有a g SO
 ,取此溶液0.5 VL,用水稀释至2 VL,则稀释后溶液中SO
,取此溶液0.5 VL,用水稀释至2 VL,则稀释后溶液中SO 的物质的量浓度为
的物质的量浓度为(4)下列数量的各物质,所含原子个数由大到小的顺序是
①0.5 mol SO3 ②标准状况下22.4 L He
③4℃时9 mL水(水的密度为1 g/mL) ④0.2 mol CH3COONH4
(5)在一密闭容器中充入a mol NO和b mol O2,可发生如下反应:2NO+O2=2NO2,充分反应后容器中氮原子和氧原子的个数之比为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】NA为阿伏加德罗常数的值。下列说法正确的是___________ 。
A.22.4LCl2(标准状况)与水充分反应转移1mol电子
B.1L0.1mol·L-1的Na2CO3溶液含 的数目为0.1NA
的数目为0.1NA
C.0.1molCH4与足量Cl2反应生成CH3Cl的分子数为0.1NA
D.1LpH=4的0.1mol·L-1K2Cr2O7溶液中Cr2O 离子数为0.1NA
离子数为0.1NA
E.2molNO与1molO2在密闭容器中充分反应后的分子数为2NA
F.11.2LCH4和22.4LCl2(均为标准状况)在光照下充分反应后的分子数为1.5NA
G.1mol碘蒸气和1mol氢气在密闭容器中充分反应,生成的碘化氢分子数小于2NA
H.2.0L1.0mol·L-1AlCl3溶液中,Al3+的数目为2.0NA
I.0.1molH2和0.1molI2于密闭容器中充分反应后,其分子总数为0.2NA
A.22.4LCl2(标准状况)与水充分反应转移1mol电子
B.1L0.1mol·L-1的Na2CO3溶液含
 的数目为0.1NA
的数目为0.1NAC.0.1molCH4与足量Cl2反应生成CH3Cl的分子数为0.1NA
D.1LpH=4的0.1mol·L-1K2Cr2O7溶液中Cr2O
 离子数为0.1NA
离子数为0.1NAE.2molNO与1molO2在密闭容器中充分反应后的分子数为2NA
F.11.2LCH4和22.4LCl2(均为标准状况)在光照下充分反应后的分子数为1.5NA
G.1mol碘蒸气和1mol氢气在密闭容器中充分反应,生成的碘化氢分子数小于2NA
H.2.0L1.0mol·L-1AlCl3溶液中,Al3+的数目为2.0NA
I.0.1molH2和0.1molI2于密闭容器中充分反应后,其分子总数为0.2NA
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】近年来,我国储氢碳管研究获得重大进展,电弧法合成碳纳米管,常伴有大量物质-碳纳米颗粒,这种碳纳米颗粒可用氧化气化法提纯,其反应的化学方程式为:3C+2K2Cr2O7+8H2SO4(稀)=3CO2↑+2K2SO4+2Cr2(SO4)3 + 8 H2O
请回答下列问题。
(1)H2O的摩尔质量为_______ ,0.18g H2O的物质的量为_______ mol
(2)配制0.1mol/L H2SO4溶液500mL,则需要H2SO4的质量为_______ g
(3)在上述的反应中,若生成22g CO2,标准状况下,CO2的体积为_______ L
(4)标准状况下,由CO和CO2 组成的混合气体为6.72 L,质量为12 g,则该混合气体的平均相对分子质量是_______ 。CO与CO2的物质的量之比_______
请回答下列问题。
(1)H2O的摩尔质量为
(2)配制0.1mol/L H2SO4溶液500mL,则需要H2SO4的质量为
(3)在上述的反应中,若生成22g CO2,标准状况下,CO2的体积为
(4)标准状况下,由CO和CO2 组成的混合气体为6.72 L,质量为12 g,则该混合气体的平均相对分子质量是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】双氧水和84消毒液是生活中常用的两种消毒剂,了解物质的性质是科学合理使用化学品的基础和前提,请回答下列问题:
(1)某同学设计如下实验研究H2O2的性质
①从化合价上看H2O2既有氧化性又有还原性,理由是_______ ;
②上述实验能证明H2O2具有还原性的是_______ (填序号);
(2)84消毒液的有效成分为NaClO,某游泳馆的工作人员将84消毒液与双氧水混用,导致游泳池藻类快速生长,池水变绿。化学兴趣小组的同学猜测可能是NaClO与H2O2反应产生O2促进藻类快速生长,由此推断该反应中H2O2是_______ (填“氧化剂”或“还原剂”)。
(1)某同学设计如下实验研究H2O2的性质
| 序号 | 实验 | 实验现象 |
| ⅰ | 向5%H2O2溶液中滴加酸性KMnO4溶液 | a.溶液紫色褪去 b.有大量气泡产生 |
| ⅱ | 向5%H2O2溶液中滴加淀粉碘化钾溶液 | c.溶液变蓝 |
②上述实验能证明H2O2具有还原性的是
(2)84消毒液的有效成分为NaClO,某游泳馆的工作人员将84消毒液与双氧水混用,导致游泳池藻类快速生长,池水变绿。化学兴趣小组的同学猜测可能是NaClO与H2O2反应产生O2促进藻类快速生长,由此推断该反应中H2O2是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】有以下反应方程式:
①SO3 + H2O=H2SO4; ②2Na2O2+2H2O=4NaOH+ O2↑;
③2Na+2H2O=2NaOH+ H2↑; ④SiO2+2NaOH=Na2SiO3+ H2O;
Ⅰ.按要求将上述化学方程式字母填入相应空格内:
上述反应中不属于氧化还原反应的有_________ (填序号,下同);H2O做氧化剂的是_________ 。属于氧化还原反应,但其中的H2O既不被氧化,又不被还原的是______ 。
Ⅱ.已知方程式F:KClO3+6HCl(浓)=KCl+3H2O+3Cl2↑。
(1)请用双线桥法标出电子转移的方向和数目___________________________________ 。
(2)标准状况下当有33.6 L的氯气放出时,转移电子的数目是__________ 。
(3)上述反应中氧化产物和还原产物的质量比为___________ 。
Ⅲ.酸性条件下,K2Cr2O7溶液和FeCl2溶液混合后生成Cr3+,请写出离子方程式__________________________________________________________________ 。
①SO3 + H2O=H2SO4; ②2Na2O2+2H2O=4NaOH+ O2↑;
③2Na+2H2O=2NaOH+ H2↑; ④SiO2+2NaOH=Na2SiO3+ H2O;
Ⅰ.按要求将上述化学方程式字母填入相应空格内:
上述反应中不属于氧化还原反应的有
Ⅱ.已知方程式F:KClO3+6HCl(浓)=KCl+3H2O+3Cl2↑。
(1)请用双线桥法标出电子转移的方向和数目
(2)标准状况下当有33.6 L的氯气放出时,转移电子的数目是
(3)上述反应中氧化产物和还原产物的质量比为
Ⅲ.酸性条件下,K2Cr2O7溶液和FeCl2溶液混合后生成Cr3+,请写出离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
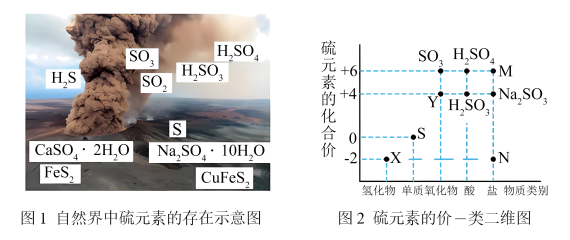
【推荐1】硫元素是动植物生长不可缺少的元素,图1是自然界中硫元素的存在示意图。图2是硫元素的常见化合价与部分物质类别的对应关系,回答下列问题。______ 、______ 。
(2)X与Y反应中氧化剂与还原剂的物质的量之比为______ 。
(3) 溶液易变质,实验室检验
溶液易变质,实验室检验 溶液是否变质的基本操作是
溶液是否变质的基本操作是______ 。
(4)已知 能被酸性
能被酸性 氧化为
氧化为 ,则
,则 的
的 溶液与
溶液与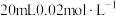 的
的 溶液恰好反应时,发生的离子方程式为:
溶液恰好反应时,发生的离子方程式为:______ 。
(5)过二硫酸钠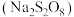 有强氧化性,在碱性条件下
有强氧化性,在碱性条件下 溶液能将
溶液能将 氧化成
氧化成 ,且反应后的溶液滴入
,且反应后的溶液滴入 溶液生成不溶于稀盐酸的白色沉淀,该反应的离子方程式为
溶液生成不溶于稀盐酸的白色沉淀,该反应的离子方程式为______ 。
(6)雌黄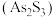 和雄黄
和雄黄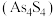 在自然界中共生且可以相互转化(两者的硫元素价态均为-2价)。
在自然界中共生且可以相互转化(两者的硫元素价态均为-2价)。
① 和
和 在盐酸中恰好完全反应转化为
在盐酸中恰好完全反应转化为 和
和 并放出
并放出 气体。则参加反应的
气体。则参加反应的 和
和 的物质的量之比为
的物质的量之比为______ 。
② 和
和 可以相互转化,转化过程中存在如图所示的步骤。若
可以相互转化,转化过程中存在如图所示的步骤。若 参加反应时,转移
参加反应时,转移 电子,则物质
电子,则物质 为
为______ ,消耗氧气______ mol。
(2)X与Y反应中氧化剂与还原剂的物质的量之比为
(3)
 溶液易变质,实验室检验
溶液易变质,实验室检验 溶液是否变质的基本操作是
溶液是否变质的基本操作是(4)已知
 能被酸性
能被酸性 氧化为
氧化为 ,则
,则 的
的 溶液与
溶液与 的
的 溶液恰好反应时,发生的离子方程式为:
溶液恰好反应时,发生的离子方程式为:(5)过二硫酸钠
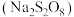 有强氧化性,在碱性条件下
有强氧化性,在碱性条件下 溶液能将
溶液能将 氧化成
氧化成 ,且反应后的溶液滴入
,且反应后的溶液滴入 溶液生成不溶于稀盐酸的白色沉淀,该反应的离子方程式为
溶液生成不溶于稀盐酸的白色沉淀,该反应的离子方程式为(6)雌黄
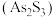 和雄黄
和雄黄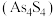 在自然界中共生且可以相互转化(两者的硫元素价态均为-2价)。
在自然界中共生且可以相互转化(两者的硫元素价态均为-2价)。①
 和
和 在盐酸中恰好完全反应转化为
在盐酸中恰好完全反应转化为 和
和 并放出
并放出 气体。则参加反应的
气体。则参加反应的 和
和 的物质的量之比为
的物质的量之比为②
 和
和 可以相互转化,转化过程中存在如图所示的步骤。若
可以相互转化,转化过程中存在如图所示的步骤。若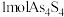 参加反应时,转移
参加反应时,转移 电子,则物质
电子,则物质 为
为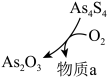
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】工业甲醇的质量分数可以用下列方法测定:
①在稀H2SO4中甲醇被Cr2O72-氧化成CO2和H2O,反应式为:CH3OH+Cr2O72-+8H+=CO2↑+2Cr3++6H2O;
②过量的Cr2O72-可用Fe2+与之完全反应:
Cr2O72﹣+ Fe2++ H+- Cr3++ Fe3++ H2O
现有0.12g工业甲醇,在H2SO4溶液中与25mL0.2mol•L-1K2Cr2O7溶液反应,多余的K2Cr2O7再用1mol•L-1FeSO4与其反应,结果用去FeSO4溶液9.6mL。
(1)配平第②步中离子方程式___ 。
(2)计算工业甲醇的质量分数___ 。
①在稀H2SO4中甲醇被Cr2O72-氧化成CO2和H2O,反应式为:CH3OH+Cr2O72-+8H+=CO2↑+2Cr3++6H2O;
②过量的Cr2O72-可用Fe2+与之完全反应:
Cr2O72﹣+ Fe2++ H+- Cr3++ Fe3++ H2O
现有0.12g工业甲醇,在H2SO4溶液中与25mL0.2mol•L-1K2Cr2O7溶液反应,多余的K2Cr2O7再用1mol•L-1FeSO4与其反应,结果用去FeSO4溶液9.6mL。
(1)配平第②步中离子方程式
(2)计算工业甲醇的质量分数
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】世界环保联盟将全面禁止在自来水中加氯,取而代之的是安全高效的杀菌消毒剂ClO2。ClO2是一种黄绿色,有刺激性气味的气体,熔点:-59℃,沸点:11.0℃。浓度>10%遇热、光照都会引起爆炸。遇到有机物也会爆炸。
(1)ClO2为高效低毒的消毒剂,其消毒的效率是等物质的量的Cl2的____ 倍。
(2)欧洲一些国家用NaClO3氧化浓盐酸来制取ClO2,同时有Cl2生成,且Cl2的体积为ClO2的1/4。写出化学反应方程式___________ 。
(3)我国广泛采用将经干燥空气稀释的氯气通入填有固体亚氯酸钠(NaClO2)的柱内制得ClO2。写出化学反应方程式___________ 。和欧洲的方法相比,我国这一方法的主要优点是什么?___________ 。
(4)在25℃时,选择 与ClO2体积比为8:1可以使ClO2较平缓、彻底的分解,CO不会参与反应,以分解后的混合气体为研究对象,设计简单合理的实验,验证ClO2分解的产物是Cl2和O2,而不是Cl2O和O2
与ClO2体积比为8:1可以使ClO2较平缓、彻底的分解,CO不会参与反应,以分解后的混合气体为研究对象,设计简单合理的实验,验证ClO2分解的产物是Cl2和O2,而不是Cl2O和O2___________ 。
(1)ClO2为高效低毒的消毒剂,其消毒的效率是等物质的量的Cl2的
(2)欧洲一些国家用NaClO3氧化浓盐酸来制取ClO2,同时有Cl2生成,且Cl2的体积为ClO2的1/4。写出化学反应方程式
(3)我国广泛采用将经干燥空气稀释的氯气通入填有固体亚氯酸钠(NaClO2)的柱内制得ClO2。写出化学反应方程式
(4)在25℃时,选择
 与ClO2体积比为8:1可以使ClO2较平缓、彻底的分解,CO不会参与反应,以分解后的混合气体为研究对象,设计简单合理的实验,验证ClO2分解的产物是Cl2和O2,而不是Cl2O和O2
与ClO2体积比为8:1可以使ClO2较平缓、彻底的分解,CO不会参与反应,以分解后的混合气体为研究对象,设计简单合理的实验,验证ClO2分解的产物是Cl2和O2,而不是Cl2O和O2
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】氧化还原反应在日常生活和生产中应用广泛,结合相关知识回答下列问题:
I.根据反应①~③,回答下列问题:
①Cl2+2KI=2KCl+I2 ②2FeCl2+Cl2=2FeCl3 ③2FeCl3+2HI=2FeCl2+2HCl+I2
(1)反应②的反应类型为___ (填字母)。
A.置换反应 B.复分解反应 C.分解反应 D.氧化还原反应
(2)对于反应③,氧化产物是___ ,还原产物是___ 。
(3)根据上述三个反应可判断出Cl-、I-、Fe2+三种物质的还原性由强到弱顺序为___ 。
II.实验室可以用 KMnO4固体和浓盐酸反应制取少量Cl2,反应的化学方程式为:__KMnO4+__HCl(浓)-__KCl+__MnCl2+__Cl2↑+__H2O,回答下列问题:
(1)请配平上述化学方程式。___
(2)浓盐酸在反应中表现的性质是___ 。
(3)该反应中氧化剂和还原剂的物质的量之比为___ 。
III.饮用水中NO3-对人类健康会产生危害,为了降低饮用水中NO3-的浓度,某饮用水研究人员提出,在碱性条件下用铝粉将NO3-还原为N2,其化学方程式为:10Al+6NaNO3+4NaOH=10NaAlO2+3N2↑+2H2O,请回答下列问题:
(1)上述反应中,被还原的物质是___ 。
(2)用双线桥标出反应中电子转移的方向和数目。___
(3)上述反应中若标准状况下产生11.2L气体,则转移电子的数目为___ 。
I.根据反应①~③,回答下列问题:
①Cl2+2KI=2KCl+I2 ②2FeCl2+Cl2=2FeCl3 ③2FeCl3+2HI=2FeCl2+2HCl+I2
(1)反应②的反应类型为
A.置换反应 B.复分解反应 C.分解反应 D.氧化还原反应
(2)对于反应③,氧化产物是
(3)根据上述三个反应可判断出Cl-、I-、Fe2+三种物质的还原性由强到弱顺序为
II.实验室可以用 KMnO4固体和浓盐酸反应制取少量Cl2,反应的化学方程式为:__KMnO4+__HCl(浓)-__KCl+__MnCl2+__Cl2↑+__H2O,回答下列问题:
(1)请配平上述化学方程式。
(2)浓盐酸在反应中表现的性质是
(3)该反应中氧化剂和还原剂的物质的量之比为
III.饮用水中NO3-对人类健康会产生危害,为了降低饮用水中NO3-的浓度,某饮用水研究人员提出,在碱性条件下用铝粉将NO3-还原为N2,其化学方程式为:10Al+6NaNO3+4NaOH=10NaAlO2+3N2↑+2H2O,请回答下列问题:
(1)上述反应中,被还原的物质是
(2)用双线桥标出反应中电子转移的方向和数目。
(3)上述反应中若标准状况下产生11.2L气体,则转移电子的数目为
您最近一年使用:0次
【推荐2】根据所学知识回答下列问题:
(1)关于物质的分类,下列组合中正确的是___________(填标号)。
(2)火法炼锌反应的化学方程式为 ,下列说法正确的是___________(填标号)。
,下列说法正确的是___________(填标号)。
(3)铜器在空气中久置会和空气中的水蒸气、CO2、O2作用产生绿锈,该绿锈俗称铜绿,又称孔雀石[主要成分为Cu2(OH)2CO3],铜绿能与酸反应生成铜盐、CO2和H2O。
①上述描述中生成铜绿反应的化学方程式为___________ ,该反应的反应类型为___________ 。
②将少量的铜绿粉末加入足量的稀盐酸中,可观察到的现象为___________ 。
(4)现有KOH、NaHCO3和BaCl2三种无色溶液,仅选用一种试剂把它们鉴别出来,该试剂可能为___________ (填化学式)。
(5)已知:硝酸具有强氧化性,其溶液的质量分数越大,氧化性越强,质量分数越小,氧化性越弱。现将少量铁粉加入质量分数很小的硝酸中,发生的反应为Fe+HNO3→Fe(NO3)3+NH4NO3+H2O,则该反应配平后的化学方程式为___________ 。
(1)关于物质的分类,下列组合中正确的是___________(填标号)。
| 选项 | 酸 | 盐 | 氧化物 | 纯净物 |
| A | HCl | CaSO4 | SO2 | O3 |
| B | HNO3 | FeCl2 | KMnO4 | He |
| C | H3PO4 | CuSO4 | Al2O3 | 纯净的空气 |
| D | H2S | KAl(SO4)2∙12H2O | Fe2O3 | 氢氧化钠溶液 |
| A.A | B.B | C.C | D.D |
 ,下列说法正确的是___________(填标号)。
,下列说法正确的是___________(填标号)。| A.常温下,碳的化学性质很活泼 | B.CO用作还原剂时,失去电子 |
| C.ZnCO3中氧元素的质量分数为38.4% | D.该反应中,还原性:C<Zn |
①上述描述中生成铜绿反应的化学方程式为
②将少量的铜绿粉末加入足量的稀盐酸中,可观察到的现象为
(4)现有KOH、NaHCO3和BaCl2三种无色溶液,仅选用一种试剂把它们鉴别出来,该试剂可能为
(5)已知:硝酸具有强氧化性,其溶液的质量分数越大,氧化性越强,质量分数越小,氧化性越弱。现将少量铁粉加入质量分数很小的硝酸中,发生的反应为Fe+HNO3→Fe(NO3)3+NH4NO3+H2O,则该反应配平后的化学方程式为
您最近一年使用:0次
【推荐3】在工业上次磷酸(H3PO2)常用于化学镀银,发生的反应如下:____Ag++___H3PO2+___H2O→____Ag↓+____H3PO4+___H+
请回答下列问题:
(1)H3PO2中,P元素的化合价为___ ;该反应中,H3PO2被___ (填“氧化”或“还原”)。
(2)配平该离子方程式:__ Ag++__ H3PO2+__ H2O→__ Ag↓+__ H3PO4+__ H+。
(3)若反应中生成1.08gAg,则转移的电子数为___ 。
(4)H3PO2是一元弱酸,写出其与足量NaOH溶液反应的离子方程式:__ 。
请回答下列问题:
(1)H3PO2中,P元素的化合价为
(2)配平该离子方程式:
(3)若反应中生成1.08gAg,则转移的电子数为
(4)H3PO2是一元弱酸,写出其与足量NaOH溶液反应的离子方程式:
您最近一年使用:0次



