某化工厂将钛、氯碱工业和甲醇制备联合生产,大大提高原料利用率,并减少环境污染。流程如下:
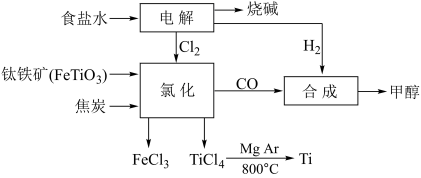
回答下列问题:
(1)写出以石墨为电极电解饱和食盐水的化学方程式___________________ 。
(2)写出钛铁矿在高温下与焦炭经氯化得四氯化钛的化学方程式__________________ ,生成1mol四氯化钛时转移电子的物质的量为________ mol。
(3)利用四氯化钛制备TiO2.xH2O时,需加入大量的水并加热的目的是____________ 。
(4)钛广泛用于航天领域。氩气在冶炼钛的流程中的作用是______________________ 。
(5)利用CO和H2制备甲醇。
①已知H2(g)、CO(g)和CH3OH(l)的燃烧热△H分别为-285.8kJ/mol、-283.0kJ/mol和-726.5kJ/mol。写出CO和H2制备甲醇的热化学方程式___________________________ 。
②假设联合生产中各原料利用率为100%,若得到6mol甲醇,则只需再补充标准状况下的H2________ L。

回答下列问题:
(1)写出以石墨为电极电解饱和食盐水的化学方程式
(2)写出钛铁矿在高温下与焦炭经氯化得四氯化钛的化学方程式
(3)利用四氯化钛制备TiO2.xH2O时,需加入大量的水并加热的目的是
(4)钛广泛用于航天领域。氩气在冶炼钛的流程中的作用是
(5)利用CO和H2制备甲醇。
①已知H2(g)、CO(g)和CH3OH(l)的燃烧热△H分别为-285.8kJ/mol、-283.0kJ/mol和-726.5kJ/mol。写出CO和H2制备甲醇的热化学方程式
②假设联合生产中各原料利用率为100%,若得到6mol甲醇,则只需再补充标准状况下的H2
15-16高三·甘肃武威·阶段练习 查看更多[2]
更新时间:2016-12-09 11:22:12
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】磷酸二氢钾在工农业和医学领域具有广泛的应用。工业上制备磷酸二氢钾的工业流程如下:
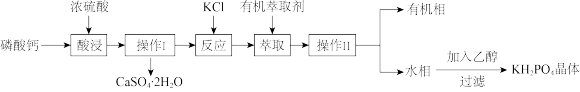
已知:① 能溶于水,
能溶于水, 和
和 均难溶于水。
均难溶于水。
②萃取原理: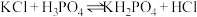 ,HCl易溶于有机萃取剂。
,HCl易溶于有机萃取剂。
回答下列问题:
(1)为提高酸浸效率,可以采取的措施有_______ 、_______ 。
(2)“酸浸”发生反应的化学方程式为_______ 。
(3)“操作II”需要用到的玻璃仪器有_______ 。
(4)“水相”中加入乙醇的作用是_______ 。
(5)常温下,已知 的电离平衡常数:
的电离平衡常数: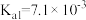 ,
,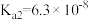 ,
,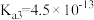 。常温下,
。常温下, 水溶液显
水溶液显_______ 性,请通过计算说明其原因_______ 。

已知:①
 能溶于水,
能溶于水, 和
和 均难溶于水。
均难溶于水。②萃取原理:
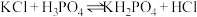 ,HCl易溶于有机萃取剂。
,HCl易溶于有机萃取剂。回答下列问题:
(1)为提高酸浸效率,可以采取的措施有
(2)“酸浸”发生反应的化学方程式为
(3)“操作II”需要用到的玻璃仪器有
(4)“水相”中加入乙醇的作用是
(5)常温下,已知
 的电离平衡常数:
的电离平衡常数: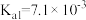 ,
,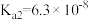 ,
,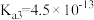 。常温下,
。常温下, 水溶液显
水溶液显
您最近半年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐2】海水是巨大的资源宝库,海水淡化及其综合利用具有重要意义。
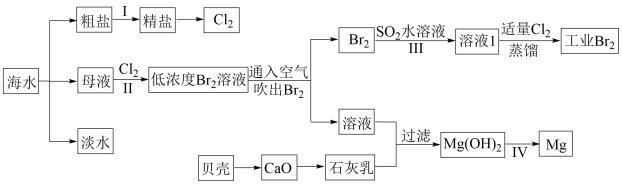
回答下列问题:
(1)请列举除蒸馏法外海水淡化的一种方法:___________________ 。
(2)步骤I中,粗盐中含有Ca2+、Mg2+、SO 等杂质离子,精制时常用的试剂有①稀盐酸;②氯化钡溶液;③氢氧化钠溶液;④碳酸钠溶液。下列加入试剂的顺序正确的是____(填字母)。
等杂质离子,精制时常用的试剂有①稀盐酸;②氯化钡溶液;③氢氧化钠溶液;④碳酸钠溶液。下列加入试剂的顺序正确的是____(填字母)。
(3)步骤II已经获得Br2,步骤III又将Br2还原为Br-,其目的是___________________ 。
(4)写出步骤III反应的离子方程式:______________________ 。工业上也可用Na2CO3溶液代替二氧化硫水溶液吸收Br2,完成下列化学方程式:__________ 。________Br2+ _______Na2CO3 ________NaBrO3+ ________CO2+ ____________
________NaBrO3+ ________CO2+ ____________
(5)海带灰中富含以I-形式存在的碘元素。实验室提取I2的途径如图所示:
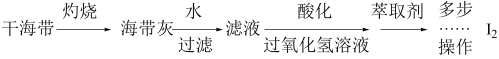
向酸化的滤液中加入过氧化氢溶液,可将I-氧化为I2,请写出该反应的离子方程式:_______________ 。

回答下列问题:
(1)请列举除蒸馏法外海水淡化的一种方法:
(2)步骤I中,粗盐中含有Ca2+、Mg2+、SO
 等杂质离子,精制时常用的试剂有①稀盐酸;②氯化钡溶液;③氢氧化钠溶液;④碳酸钠溶液。下列加入试剂的顺序正确的是____(填字母)。
等杂质离子,精制时常用的试剂有①稀盐酸;②氯化钡溶液;③氢氧化钠溶液;④碳酸钠溶液。下列加入试剂的顺序正确的是____(填字母)。| A.①②③④ | B.②③④① | C.②④③① | D.③④②① |
(4)写出步骤III反应的离子方程式:
 ________NaBrO3+ ________CO2+ ____________
________NaBrO3+ ________CO2+ ____________(5)海带灰中富含以I-形式存在的碘元素。实验室提取I2的途径如图所示:
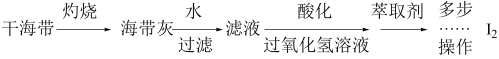
向酸化的滤液中加入过氧化氢溶液,可将I-氧化为I2,请写出该反应的离子方程式:
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】锌钡白ZnS·BaSO4是一种常用白色颜料,以重晶石(BaSO4)和焦炭粉为原料,在回转炉中强热制取可溶性硫化钡。硫化钡在净化后形成溶液,再与硫酸锌经过一系列过程最终制得锌钡白成品。
(1)回转炉中发生反应的化学方程式为___________________________ 。
(2)回转炉尾气中含有有毒气体,生产上通入一定量的水蒸气进行处理,水蒸气的作用是_____________________________ 。
(3)成品中S2-的含量可以用“碘量法”测得。称取m g样品,置于碘量瓶中,移取25.00 mL 0.1000 mol·L-1的I2-KI溶液于其中,并加入乙酸溶液,密闭,置暗处反应5 min,有单质硫析出。以淀粉溶液为指示剂,过量的I2用0.1000 mol·L-1Na2S2O3溶液滴定,反应式为I2+2S2O32-=2I-+S4O62-。测定时消耗Na2S2O3溶液体积V mL,滴定终点现象为__________ ,样品中S2-的含量为____________ (写出表达式与计算过程)。
(1)回转炉中发生反应的化学方程式为
(2)回转炉尾气中含有有毒气体,生产上通入一定量的水蒸气进行处理,水蒸气的作用是
(3)成品中S2-的含量可以用“碘量法”测得。称取m g样品,置于碘量瓶中,移取25.00 mL 0.1000 mol·L-1的I2-KI溶液于其中,并加入乙酸溶液,密闭,置暗处反应5 min,有单质硫析出。以淀粉溶液为指示剂,过量的I2用0.1000 mol·L-1Na2S2O3溶液滴定,反应式为I2+2S2O32-=2I-+S4O62-。测定时消耗Na2S2O3溶液体积V mL,滴定终点现象为
您最近半年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐1】综合利用炼锌矿渣(主要含铁酸镓Ga2(Fe2O4)3、铁酸锌ZnFe2O4)获得3种金属盐,并进一步利用镓盐制备具有优异光电性能的氮化镓(GaN),部分工艺流程如图。
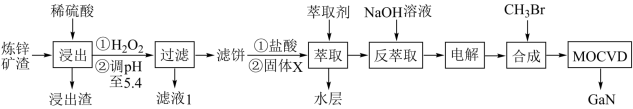
已知:①常温下,浸出液中各离子的浓度及其开始形成氢氧化物沉淀的pH如表1。
②金属离子在工艺条件下的萃取率(进入有机层中金属离子的百分数)如表2。
表1金属离子浓度及开始沉淀的pH
表2金属离子的萃取率
(1)Ga2(Fe2O4)3中Ga的化合价为_____ ,“浸出”后的①中加入H2O2时发生的离子方程式为_____ 。
(2)滤液1中可回收利用的物质是_____ ,滤饼的主要成分是_____ ;萃取前加入的固体X为_____ 。
(3)Ga与Al同主族,化学性质相似。反萃取后,镓的存在形式为_____ 。(填化学式)
(4)电解过程包括电解反萃取液制粗镓和粗镓精炼两个步骤。精炼时,以粗镓为阳极,以NaOH溶液为电解液,阴极的电极反应为_____ 。
(5)GaN可采用MOCVD(金属有机物化学气相淀积)技术制得:以合成的三甲基镓为原料,使其与NH3发生系列反应得到GaN和另一种产物,该过程的化学方程式为______ 。
(6)滤液1中残余的Ga3+的浓度为_____ mol•L-1。

已知:①常温下,浸出液中各离子的浓度及其开始形成氢氧化物沉淀的pH如表1。
②金属离子在工艺条件下的萃取率(进入有机层中金属离子的百分数)如表2。
表1金属离子浓度及开始沉淀的pH
| 金属离子 | 浓度(mol•L-1) | 开始沉淀pH |
| Fe2+ | 1.0×10-3 | 8.0 |
| Fe3+ | 4.0×10-2 | 1.7 |
| Zn2+ | 1.5 | 5.5 |
| Ga3+ | 3.0×10-3 | 3.0 |
| 金属离子 | 萃取率(%) |
| Fe2+ | 0 |
| Fe3+ | 99 |
| Zn2+ | 0 |
| Ga3+ | 97~98.5 |
(2)滤液1中可回收利用的物质是
(3)Ga与Al同主族,化学性质相似。反萃取后,镓的存在形式为
(4)电解过程包括电解反萃取液制粗镓和粗镓精炼两个步骤。精炼时,以粗镓为阳极,以NaOH溶液为电解液,阴极的电极反应为
(5)GaN可采用MOCVD(金属有机物化学气相淀积)技术制得:以合成的三甲基镓为原料,使其与NH3发生系列反应得到GaN和另一种产物,该过程的化学方程式为
(6)滤液1中残余的Ga3+的浓度为
您最近半年使用:0次
【推荐2】硒和碲在工业上有重要用途。在铜、镍、铅等电解工艺的阳极泥中硒、碲主要以硒化物、碲化物及金属状态存在。一种从阳极泥中提取Se和Te的工艺流程见下:

已知:碲酸钠(Na2H4TeO6)难溶,碲酸(H6TeO6)可溶。
回答下列问题:
(1)阳极泥在600 K左右加入一定浓度H2SO4“焙烧”时,单质Te转化为TeO2的化学方程式为___________________________________________ 。
(2) “焙砂”与碳酸钠充分混合,干燥后通空气氧化物料,每生成1 mol碲酸钠,则需要的氧化剂O2至少为_______ mol;生成的碲酸钠不水浸,而采取“酸浸”的原因是______________________________________ 。
(3) “反应”时的化学方程式为_________________________________________________ 。
(4)“还原”中的反应生成物为TeO2,检验反应后是否有反应物Na2SO3过量的实验操作方法为________________________________________________________ 。
(5)已知“电解”时使用石墨电极,阳极产物与阴极产物的物质的量之比为______________ 。
(6)工艺路线中可以循环利用的物质有_____________________ 、_____________________ 。

已知:碲酸钠(Na2H4TeO6)难溶,碲酸(H6TeO6)可溶。
回答下列问题:
(1)阳极泥在600 K左右加入一定浓度H2SO4“焙烧”时,单质Te转化为TeO2的化学方程式为
(2) “焙砂”与碳酸钠充分混合,干燥后通空气氧化物料,每生成1 mol碲酸钠,则需要的氧化剂O2至少为
(3) “反应”时的化学方程式为
(4)“还原”中的反应生成物为TeO2,检验反应后是否有反应物Na2SO3过量的实验操作方法为
(5)已知“电解”时使用石墨电极,阳极产物与阴极产物的物质的量之比为
(6)工艺路线中可以循环利用的物质有
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】氯化亚砜(SOCl2)是一种液态化合物,沸点为77℃,在农药、制药行业中用途广泛。SOCl2遇水剧烈反应,液面上产生白雾,并带有刺激性气味的气体产生。实验室合成原理:SO2+Cl2+SCl2=2SOCl2,部分装置如图所示,回答以下问题:
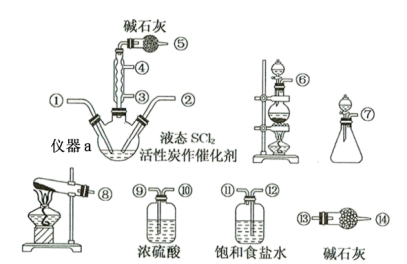
(1)仪器a的名称为_______ 。
(2)实验室制取SOCl2在仪器a中合成,整个装置所选仪器的连接顺序是:⑥→⑫→⑪→⑨→⑩→①②←_______ (用“←”连接各接口,箭头表示气体流向,装置可重复使用)。
(3)冷凝管上连接的干燥管的作用是_______ 。
(4)该实验制取氯气的离子方程式为_______ 。
(5) SOCl2与水反应的化学方程式为_______ 。
(6)若反应中消耗的Cl2的体积为896mL (已转化为标准状况,SO2足量),最后得到纯净的SOCl26.76g,则SOCl2的产率为_______ (保留二位有效数字)

(1)仪器a的名称为
(2)实验室制取SOCl2在仪器a中合成,整个装置所选仪器的连接顺序是:⑥→⑫→⑪→⑨→⑩→①②←
(3)冷凝管上连接的干燥管的作用是
(4)该实验制取氯气的离子方程式为
(5) SOCl2与水反应的化学方程式为
(6)若反应中消耗的Cl2的体积为896mL (已转化为标准状况,SO2足量),最后得到纯净的SOCl26.76g,则SOCl2的产率为
您最近半年使用:0次



