温度为T0时,在容积固定的容器中发生反应,各物质的浓度随时间变化的关系如图a所示.其他条件相同,温度分别为T1、T2时发生反应,Z的浓度随时间变化的关系如图b所示。
图a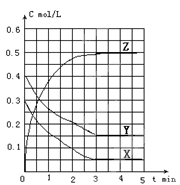 图b
图b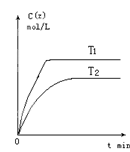
下列叙述正确的是
图a
 图b
图b
下列叙述正确的是
| A.该反应的正反应是放热反应 |
| B.T0时,该反应的平衡常数为1/3 |
| C.图a中反应达到平衡时,Y的转化率为37.5% |
| D.反应时各物质的反应速率关系为:2v(X)=2v(Y)=v(Z) |
2010·北京东城·二模 查看更多[1]
(已下线)2010年北京市东城区高三第二次模拟考试(理综)化学部分
更新时间:2016-12-09 00:28:08
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】反应4A(s)+3B(g) 2C(g)+D(g)经2 min B的浓度减少0.6 mol·L-1。下列说法正确的是
2C(g)+D(g)经2 min B的浓度减少0.6 mol·L-1。下列说法正确的是
①用A表示的反应速率是0.4mol·L-1·min-1
②在2min末时,反应物B的反应速率是0.3mol·L-1·min-1
③在这2min内用C表示的平均速率为0.2mol·L-1·min-1
④在2min时,B、C、D的浓度比一定为3∶2∶1
⑤若D的起始浓度为0.1mol·L-1,则2 min时D的浓度为0.3mol·L-1
 2C(g)+D(g)经2 min B的浓度减少0.6 mol·L-1。下列说法正确的是
2C(g)+D(g)经2 min B的浓度减少0.6 mol·L-1。下列说法正确的是①用A表示的反应速率是0.4mol·L-1·min-1
②在2min末时,反应物B的反应速率是0.3mol·L-1·min-1
③在这2min内用C表示的平均速率为0.2mol·L-1·min-1
④在2min时,B、C、D的浓度比一定为3∶2∶1
⑤若D的起始浓度为0.1mol·L-1,则2 min时D的浓度为0.3mol·L-1
| A.①②③ | B.②③⑤ | C.④⑤ | D.③⑤ |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】t℃时,在2L的恒容密闭容器中充入4molN2O3,发生反应①和②:①N2O3(g) N2O(g)+O2(g),②N2O3(g)+O2(g)
N2O(g)+O2(g),②N2O3(g)+O2(g) N2O5(g),5分钟时达平衡。测得N2O5为0.7mol•L-1,O2为0.5mol•L-1,则下列说法正确的是
N2O5(g),5分钟时达平衡。测得N2O5为0.7mol•L-1,O2为0.5mol•L-1,则下列说法正确的是
 N2O(g)+O2(g),②N2O3(g)+O2(g)
N2O(g)+O2(g),②N2O3(g)+O2(g) N2O5(g),5分钟时达平衡。测得N2O5为0.7mol•L-1,O2为0.5mol•L-1,则下列说法正确的是
N2O5(g),5分钟时达平衡。测得N2O5为0.7mol•L-1,O2为0.5mol•L-1,则下列说法正确的是| A.达到平衡时:c(N2O3)=0.2mol•L-1 |
| B.0~5min的平均反应速率:v(N2O3)=7.6mol•L-1•min-1 |
| C.0~5min的平均反应速率:①<② |
| D.t℃时,反应平衡常数:①<② |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】如图为一定温度下容积不变的密闭容器中,氨的催化氧化4NH3(g)+5O2(g) ⇌4NO(g)+6H2O(g) ΔH=-905 kJ·mol-1平衡体系中NO的体积分数随O2物质的量增加的变化曲线,下列说法正确的是( )
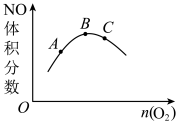

| A.平衡常数KA<KB |
| B.A点反应速率v(正)>v(逆) |
| C.NH3的转化率B>C>A |
| D.B点时n(NH3)∶n(O2)=4∶5 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】 分解的热化学方程式为
分解的热化学方程式为
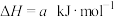 。向体积为1L恒容密闭容器中加入
。向体积为1L恒容密闭容器中加入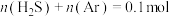 的混合气体(Ar不参与反应),测得不同温度(
的混合气体(Ar不参与反应),测得不同温度( )的平衡转化率随
)的平衡转化率随 比值的变化如图所示。下列说法正确的是
比值的变化如图所示。下列说法正确的是
 分解的热化学方程式为
分解的热化学方程式为
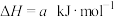 。向体积为1L恒容密闭容器中加入
。向体积为1L恒容密闭容器中加入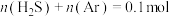 的混合气体(Ar不参与反应),测得不同温度(
的混合气体(Ar不参与反应),测得不同温度( )的平衡转化率随
)的平衡转化率随 比值的变化如图所示。下列说法正确的是
比值的变化如图所示。下列说法正确的是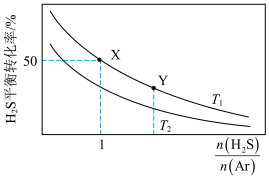
| A.该反应的a<0 |
B.平衡常数 |
C. ,到达平衡时, ,到达平衡时, 的体积分数为 的体积分数为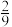 |
D.维持Y点时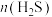 不变,向容器中充入Ar, 不变,向容器中充入Ar, 的平衡转化率减小 的平衡转化率减小 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】反应:L(s)+aG(g) bR(g)达到平衡时,温度和压强对该反应的影响如图所示:图中压强p1>p2,x轴表示温度,y轴表示平衡混合气中G的体积分数。据此可判断( )
bR(g)达到平衡时,温度和压强对该反应的影响如图所示:图中压强p1>p2,x轴表示温度,y轴表示平衡混合气中G的体积分数。据此可判断( )

 bR(g)达到平衡时,温度和压强对该反应的影响如图所示:图中压强p1>p2,x轴表示温度,y轴表示平衡混合气中G的体积分数。据此可判断( )
bR(g)达到平衡时,温度和压强对该反应的影响如图所示:图中压强p1>p2,x轴表示温度,y轴表示平衡混合气中G的体积分数。据此可判断( )
| A.上述反应是放热反应 | B.上述反应是吸热反应 |
| C.a+1>b | D.a+1<b |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】可逆反应aA(g)+bB(s) cC(g)+dD(g),在反应过程中,其他条件不变,C的物质的量分数和T或P关系如图所示,下列叙述中正确的是
cC(g)+dD(g),在反应过程中,其他条件不变,C的物质的量分数和T或P关系如图所示,下列叙述中正确的是

 cC(g)+dD(g),在反应过程中,其他条件不变,C的物质的量分数和T或P关系如图所示,下列叙述中正确的是
cC(g)+dD(g),在反应过程中,其他条件不变,C的物质的量分数和T或P关系如图所示,下列叙述中正确的是 
| A.温度降低,化学平衡向逆反应方向移动 |
| B.使用催化剂,C的物质的量分数增加 |
| C.化学方程式系数a<c+d |
| D.平衡时再加入A,平衡向右移动,A的转化率增大 |
您最近一年使用:0次

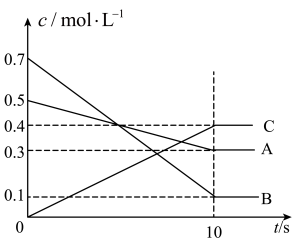
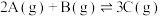
 的正确图像是
的正确图像是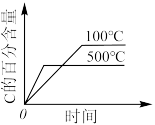
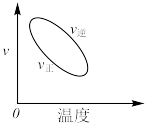
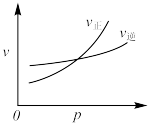

 。在不同温度下反应的过程如图所示。下列说法错误的是
。在不同温度下反应的过程如图所示。下列说法错误的是
 mol⋅L
mol⋅L ⋅min
⋅min

